一种具有负泊松比结构的骨仿生复合材料及其制备方法与流程
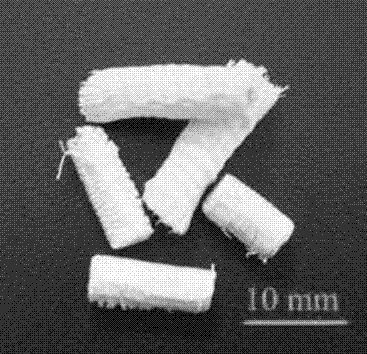
本发明属于生物医用材料技术领域,涉及一种具有负泊松比效应的纳米纤维骨替代材料及其制备方法,应用于骨修复或骨替代材料。
背景技术:
我国每年由于交通和工业事故、肿瘤、骨组织坏死和风湿等疾病引起的骨组织缺损、骨折病患人数达数百万人。随着人口老龄化的日益严重,年老引起的骨组织疏松使骨缺损的病患有增多的趋势,此外,每年需要进行颅颌面和肢体整形、美容的人数也达到千万人。因此,临床治疗对骨组织修复材料有着巨大的市场需求。目前应用于骨组织修复的金属、骨水泥、生物活性玻璃、磷酸钙类生物活性陶瓷以及可吸收性的高分子材料等难以满足临床对骨组织修复和重建的需求。制备能主动诱导和激发组织器官再生并具有良好力学性能的类人骨组织替代、修复材料对于解决临床日益扩大的骨修复需求具有重要意义。
天然骨是一种由约30%的有机基质和70%的羟基磷灰石构成的有机/无机生物复合材料,有机基质主要包括非胶原蛋白、粘多糖等。无机成分的羟基磷灰石纳米晶体有序地嵌在胶原纤维基质中,有机和无机组元间的密切协同作用以及分子水平的独特组装,赋予了天然骨的多级结构和优异的力学性能。能否获得一种从结构和成分上双重仿生并具备优秀的力学性能的骨仿生支架材料是骨组织工程进行的主要难点和关键点。
技术实现要素:
本发明的目的是提供一种设计负泊松比结构的纳米仿生骨复合材料骨仿生复合材料的制备方法。常规材料均表现为正泊松比,即拉伸时材料垂直于拉伸方向变窄,压缩时垂直于拉伸方向变宽;而具有负泊松比效应的材料,其在拉伸时材料垂直于拉伸方向变宽,或压缩时垂直于压缩方向变窄,如图1所示。本发明结合静电纺技术与纺织技术,将负泊松比效应应用于构建具有负泊松比结构的三维多层纳米纤维织物,并以此为模板利用仿生矿化的方法得到类似于天然骨中分级结构的骨替代材料。这种骨仿生材料不仅在成分和结构上实现了对天然骨的仿生,良好的生物相容性、生物可降解性以及良好的骨诱导性能,可激发骨的再生,而且在力学性能方面,由于这种负泊松比结构使其具备足够的强度来承受机体自身的重量,以及自适应性以满足机体可能遭遇的压缩、剪切和撞击等多个外力作用场合。
实现本发明目的技术方案是:
一种具有负泊松比结构的骨仿生复合材料,它是以矿化的纳米纤维为基本单元,沿轴向平行排列形成纳米纤维纱线结构,再进一步交织形成具有负泊松比结构的有机/无机的纳米纤维复合材料,有机的纳米纤维与无机的矿物质的质量比为1:1-10,孔隙率为20%-80%。
所述的纳米纤维复合材料是由纳米纤维经纱、纬纱以及结节纱按照设计的负泊松比结构编织而成,结节点的密度为10-40个/cm2,多层纳米纤维织物的经密为90-240根/5cm,纬密为140-280根/5cm层数至少为4层。
所述的纳米纤维纱线是由矿化的纳米纤维沿纱线轴向平行排列形成的,纳米纤维纱线的直径为100-500μm,所述的矿化纳米纤维是无机矿物在纳米纤维上自组装得到的。
所述的纳米纤维是由聚己内酯和柞蚕丝素构成,纳米纤维的直径为200-1200nm,柞蚕丝素和聚己内酯的质量比为5:95-30:70,聚己内酯分子量大于200000,柞蚕丝素蛋白分子的特性粘度大于或等于0.50。
所述无机的矿物质成分为羟基磷灰石,它是由针状晶粒组成的球状形貌,针状晶粒尺寸为0.5nm-1nm。
所述的具有负泊松比结构的骨仿生复合材料的制备方法,其步骤如下:
(1)将柞蚕丝素和聚己内酯按照质量比为1:1-10放入六氟异丙醇溶液中,在常温下进行磁力搅拌8-36小时得到质量分数为5-15%的静电纺丝溶液;
(2)将去离子水和无水乙醇按照质量比为1:1-4的比例配置混合溶剂,将聚乙烯吡咯烷酮放入混合溶剂中,在室温下磁力搅拌120-360min得到质量分数为15-35%的聚乙烯吡咯烷酮溶液;
(3)以步骤(1)中的混合纺丝溶液作为芯层溶液,以步骤(2)中的聚乙烯吡咯烷酮溶液作为壳层溶液,利用静电纺丝的方法制备具有皮芯结构的纳米纤维构成的纳米纤维纱线,所述的纳米纤维的皮层为聚乙烯吡咯烷酮,所述的纳米纤维的芯层为柞蚕丝素和聚己内酯混合成分,静电纺丝的电压为18-25kv,纺丝溶液总流量为0.1-1.0ml/h,正负喷头溶液流量比1:0.5-2,芯溶液与壳溶液的流量比为1-1:4,喷头内管内径0.2mm,外管内径0.4mm,正负喷头间的距离12-18cm,卷绕速度30-60mm/min;
(4)将步骤(3)中所得的具有皮芯结构的纳米纤维构成的纳米纤维纱线利用纺织编织技术,编织形成具有负泊松比结构的三维多层纳米纤维织物,多层纳米纤维织物的经密为90-240根/5cm,纬密为140-280根/5cm,结节点的密度为10-40个/cm2;
(5)将步骤(4)中的的多层纳米纤维织物浸泡在质量分数为70-95%的乙醇水溶液中处理30-120min,然后放入循环流动的去离子水中,去除纳米纤维皮层的聚乙烯吡咯烷酮;
(6)将步骤(5)中的多层纳米纤维织物浸泡在1-3倍的模拟体液中进行循环流动矿化,模拟体液的循环流动流速为0-50ml/h,在37℃恒温下矿化12-72小时后取出用去离子水清洗,并在真空烘箱中50-70℃下干燥,得到具有负泊松比结构的骨仿生复合材料。
与现有的骨替代材料及其制备方法相比,本发明具有以下优点:
(1)本发明中所设计的纳米仿生骨具有负泊松比结构,相比常规结构的骨仿生材料,具有更加优秀的力学性能,具备足够的强度来承受机体自身的重量,以及自适应性以满足机体可能遭遇的压缩、剪切和撞击等多个外力作用场合。
(2)本发明中以生物相容性较好的柞蚕丝素和聚己内酯为材料,以矿化的纳米纤维纱仿生构建天然骨的结构单元—矿化的胶原纤维束,这种纳米纤维骨仿生复合材料实现了成分和结构上的双重仿生,具有很好的生物相容性和生物活性。
(3)本发明中首先纺制核壳纱线,然后在编织成型后将皮芯结构的纳米纤维皮层的聚乙烯吡咯烷酮成分去除使织物内部的孔隙变大,同时在模拟体液矿化时采用流动矿化的方法促进了羟基磷灰石在织物层中的纳米纤维间生长,能够能够使本发明的骨替代材料具有较好的强度和结构仿真性。
本发明制备的由矿化的纳米纤维构建的仿生天然骨结构的骨替代材料,在成分的选择上选用的是生物材料聚己内酯、柞蚕丝素蛋白和羟基磷灰石,其中柞蚕丝素蛋白富含极性氨基酸和可作为细胞识别信号的arg-gly-asp(精氨酸-甘氨酸-天门冬氨酸,rgd)三肽序列能够使材料有利于细胞的粘附、增殖和分化;在结构上,利用静电纺技术使纳米纤维成纱线并结合纺织编织技术加工成具有负泊松比结构的三维多层纳米纤维织物模板,其中所形成纳米纤维、纳米纤维纱线、负泊松比结构的三维多层纳米纤维织物,可分别仿生骨中的胶原纤维、胶原纤维束、胶原纤维阵列和骨单元,重要的是,这种特殊的结构—负泊松比结构提高了纳米骨复合材料的力学自适应性。由此可见,本发明所制备的这种具有负泊松比结构的纳米仿生骨复合材料具备良好的生物相容性、生物活性和力学性能,在骨组织临床具有广阔的应用前景。
不同于常规的骨修复材料,负泊松比结构材料具有高的能量吸收和断裂韧性,本发明将负泊松比结构效应引入到骨仿生材料的结构设计中,材料能更好的适应外力作用,抵御破坏。
附图说明
图1负泊松比结构受力形变的示意图。
图2负泊松比多管状三维织物实物图。
图3骨仿生材料中不同矿化度的纳米纤维的sem照片形貌。
图4制备的骨替代材料矿化后纳米纤维表面形貌。
具体实施方式
下面结合附图通过实例对本发明进一步详细说明。
实施例1
一种具有负泊松比结构的骨仿生复合材料的制备方法,其步骤如下:
(1)将柞蚕丝素和聚己内酯按照质量比为1:1放入六氟异丙醇溶液中,在常温下进行磁力搅拌12小时得到质量分数为6%的静电纺纺丝溶液;
(2)将去离子水和无水乙醇按照质量比为1:1的比例配置混合溶剂,将28g聚乙烯吡咯烷酮放入混合溶剂中,在室温下磁力搅拌150min得到质量分数为6%的聚乙烯吡咯烷酮溶液;
(3)以步骤(1)中的混合纺丝溶液作为芯层溶液,以步骤(2)中的聚乙烯吡咯烷酮溶液作为壳层溶液,利用静电纺丝的方法制备由皮芯结构的纳米纤维构成的纳米纤维纱线。所述的纳米纤维的皮层为聚乙烯吡咯烷酮,所述的纳米纤维的芯层为柞蚕丝素和聚己内酯混合成分,静电纺丝的电压为18kv,纺丝溶液总流量为0.2ml/h,正负喷头溶液流量比1:0.5,芯溶液与壳溶液的流量比为1:1,喷头内管内径0.2mm,外管内径0.4mm,正负喷头间的距离12cm,卷绕速度30mm/min;
(4)将步骤(3)中所得的由皮芯结构的纳米纤维构成的纳米纤维纱线利用机织技术,编织形成具有负泊松比结构的三维多层纳米纤维织物,纳米纤维织物的经密为100根/5cm,纬密为120根/5cm,结节点的密度为18个/cm2的;
(5)将步骤(4)中的多层纳米纤维织物浸泡在质量分数为75%的乙醇水溶液中处理60min,然后放入循环流动的去离子水中,去除多层纳米纤维织物中皮芯结构的纳米纤维皮层的聚乙烯吡咯烷酮;
(6)将步骤(5)中的多层纳米纤维织物浸泡在1倍的模拟体液中进行循环流动矿化,模拟体液的循环流动流速为10ml/h,在37℃恒温下矿化36h后取出用去离子水清洗,并在真空烘箱中60℃下干燥,得到由矿化的纳米纤维构建的仿生天然骨结构的骨替代材料。
矿化的纳米纤维仿生骨的光学显微镜照片如图2所示。矿化的纳米纤维仿生骨的扫描电镜照片如图3所示。表1显示了具有负泊松比结构的骨替代材料的力学性能、密度和孔隙率。
实施例2
一种具有负泊松比结构的骨仿生复合材料的制备方法,其步骤如下:
(1)将柞蚕丝素和聚己内酯按照质量比为1:5放入六氟异丙醇溶液中,在常温下进行磁力搅拌24小时得到质量分数为8%的静电纺纺丝溶液;
(2)将去离子水和无水乙醇按照质量比为1:3的比例配置混合溶剂,将26.0g聚乙烯吡咯烷酮放入混合溶剂中,在室温下磁力搅拌240min得到质量分数为30%的聚乙烯吡咯烷酮溶液;
(3)以步骤(1)中的混合纺丝溶液作为芯层溶液,以步骤(2)中的聚乙烯吡咯烷酮溶液作为壳层溶液,利用静电纺丝的方法制备由皮芯结构的纳米纤维构成的纳米纤维纱线,所述的纳米纤维的皮层为聚乙烯吡咯烷酮,所述的纳米纤维的芯层为柞蚕丝素和聚己内酯混合成分;静电纺丝的电压为22kv,纺丝溶液总流量为0.5ml/h,正负喷头溶液流量比2:3,芯溶液与壳溶液的流量比为1:3,喷头内管内径0.2mm,外管内径0.4mm,正负喷头间的距离14cm,卷绕速度50mm/min;
(4)将步骤(3)中所得的由皮芯结构的纳米纤维构成的纳米纤维纱线利用机织技术,编织形成具有负泊松比结构的三维多层纳米纤维织物,多层纳米纤维织物的经密为140根/5cm,纬密为160根/5cm,结节点的密度为23个/cm2的;
(5)将步骤(4)中的多层纳米纤维织物浸泡在质量分数为85%的乙醇水溶液中处理70min,然后放入循环流动的去离子水中,去除多层纳米纤维织物中皮芯结构的纳米纤维皮层的聚乙烯吡咯烷酮;
(6)将步骤(5)中的多层纳米纤维织物浸泡在1.5倍的模拟体液中进行循环流动矿化,模拟体液的循环流动流速为14ml/h,在37℃恒温下矿化60h后取出用去离子水清洗,并在真空烘箱中70℃下干燥,得到具有负泊松比结构的骨仿生纳米纤维复合材料。制备的骨替代材料的力学性能、密度和孔隙率如表1所示。
实施例3
一种具有负泊松比结构的骨仿生复合材料的制备方法,其步骤如下:
(1)将柞蚕丝素和聚己内酯按照质量比为1:7放入六氟异丙醇溶液中,在常温下进行磁力搅拌36小时得到质量分数为9%的静电纺纺丝溶液;
(2)将去离子水和无水乙醇按照质量比为1:4的比例配置混合溶剂,将28g聚乙烯吡咯烷酮放入混合溶剂中,在室温下磁力搅拌360min得到质量分数为32%的聚乙烯吡咯烷酮溶液;
(3)以步骤(1)中的混合纺丝溶液作为芯层溶液,以步骤(2)中的聚乙烯吡咯烷酮溶液作为壳层溶液,利用静电纺丝的方法制备由皮芯结构的纳米纤维构成的纳米纤维纱线,所述的纳米纤维的皮层为聚乙烯吡咯烷酮,所述的纳米纤维的芯层为柞蚕丝素和聚己内酯混合成分,静电纺丝的电压为24kv,纺丝溶液总流量为0.6ml/h,正负喷头溶液流量比1:2,芯溶液与壳溶液的流量比为1:4,喷头内管内径0.2mm,外管内径0.4mm,正负喷头间的距离16cm,卷绕速度60mm/min;
(4)将步骤(3)中所得的由皮芯结构的纳米纤维构成的纳米纤维纱线利用机织技术,编织形成具有负泊松比结构的三维多层纳米纤维织物,纳米纤维织物的经密为160根/5cm,纬密为180根/5cm,结节点的密度为25个/cm2的;
(5)将步骤(4)中的的多层纳米纤维织物浸泡在质量分数为90%的乙醇水溶液中处理80min,然后放入循环流动的去离子水中,去除多层纳米纤维织物中皮芯结构的纳米纤维皮层的聚乙烯吡咯烷酮;
(6)将步骤(5)中的多层纳米纤维织物浸泡在2倍的模拟体液中进行循环流动矿化,模拟体液的循环流动流速为16ml/h,在37℃恒温下矿化72h后取出用去离子水清洗,并在真空烘箱中75℃下干燥,得到具有负泊松比结构的骨仿生纳米纤维复合材料,制备的骨替代材料的力学性能、密度和孔隙率如表1所示,矿化后纳米纤维表面形貌如图4所示。
实施例4
一种具有负泊松比结构的骨仿生复合材料的制备方法,其步骤如下:
(1)将柞蚕丝素和聚己内酯按照质量比为1:10放入六氟异丙醇溶液中,在常温下进行磁力搅拌5天得到质量分数为9%的静电纺纺丝溶液;
(2)将去离子水和无水乙醇按照质量比为1:4的比例配置混合溶剂,将28g聚乙烯吡咯烷酮放入混合溶剂中,在室温下磁力搅360min得到质量分数为32%的聚乙烯吡咯烷酮溶液;
(3)以步骤(1)中的混合纺丝溶液作为芯层溶液,以步骤(2)中的聚乙烯吡咯烷酮溶液作为壳层溶液,利用静电纺丝的方法制备由皮芯结构的纳米纤维构成的纳米纤维纱线,所述的纳米纤维的皮层为聚乙烯吡咯烷酮,所述的纳米纤维的芯层为柞蚕丝素和聚己内酯混合成分,静电纺丝的电压为24kv,纺丝溶液总流量为0.6ml/h,正负喷头溶液流量比1:2,芯溶液与壳溶液的流量比为1:4,喷头内管内径0.2mm,外管内径0.4mm,正负喷头间的距离16cm,卷绕速度60mm/min;
(4)将步骤(3)中所得的由皮芯结构的纳米纤维构成的纳米纤维纱线利用机织技术,编织形成不同层数的纳米纤维织物,纱线编织成不同层数的管状或片状的纳米纤维织物,纳米纤维织物的经密为160根/5cm,纬密为180根/5cm,结节点的密度为25个/cm2的;
(5)将步骤(4)中的的多层纳米纤维织物浸泡在质量分数为90%的乙醇水溶液中处理80min,然后放入循环流动的去离子水中,去除多层纳米纤维织物中皮芯结构的纳米纤维皮层的聚乙烯吡咯烷酮;
(6)将步骤(5)中的多层纳米纤维织物浸泡在2.5倍的模拟体液中进行循环流动矿化,模拟体液的循环流动流速为16ml/h,在37℃恒温下矿化72h后取出用去离子水清洗,并在真空烘箱中75℃下干燥,得到具有负泊松比结构的骨仿生纳米纤维复合材料,制备的骨替代材料的力学性能、密度和孔隙率如表1所示。
表1一种由矿化的纳米纤维构建的仿生天然骨结构的骨替代材料的性能
因此,本发明设计了一种具有负泊松比结构的纳米纤维骨仿生复合材料,结合静电纺技术与纺织编织技术,制备出具有负泊松比结构的柞蚕丝素和聚己内酯复合米纤维织物模板,并利用模拟体液仿生矿化的方法在纳米纤维纤维表面沉积羟基磷灰石得到纳米骨仿生复合材料。相比常规骨仿生复合材料,这种骨仿生材料由于其具备负泊松比结构显示了更优秀的力学性能,包括压缩模量,压缩强度、弯曲强度等。此外,这种纳米纤维骨仿生复合材料不仅在成分上模拟了天然骨,而且在结构上实现了对天然骨的仿生。成分中的柞蚕丝素含有的极性基团能够使羟基磷灰石在织物中定点生长并且与织物紧密结合,同时柞蚕丝素中的arg-gly-asp(rgd)三肽序列可作为生物识别信号促进细胞粘附;纳米纤维纱线在空间上的三维编织实现了在结构上对骨材料的分级仿生。根据本发明的方法制备的具有负泊松比结构的纳米仿生复合材料具有优异的力学性能、良好的成形性和生物学性能,可以作为植入型的骨修复材料。
- 还没有人留言评论。精彩留言会获得点赞!