一种他莫昔芬柔性纳米脂质体凝胶剂及其制备方法与流程
本发明涉及药物制剂技术领域,具体涉及一种他莫昔芬柔性纳米脂质体凝胶剂及其制备方法。
背景技术:
他莫昔芬(tam)是一种选择性雌激素受体调节剂(serm),它能干扰雌激素(estrogen)的某些活动,模拟其它雌激素作用,上调转化生长因子β生成,此因子减少与恶性肿瘤的发展有关,还对蛋白激酶c有特异性抑制作用。这些作用都对依赖雌激素才能继续生长的肿瘤细胞有抑制作用。临床上多用于绝经期前雌激素(er+)和孕激素受体(pr+)呈进行性发展的乳癌的治疗。
世界上近百个国家用tam来治疗晚期复发性乳腺癌和卵巢癌,主要用于治疗和预防乳腺癌,近年来国内外对tam的实验和临床研究发展很快,全球每年越有40万例患者因为tam治疗而免于死亡,尽管乳腺癌内分泌治疗新药层出不穷,但是却无法动摇其地位,然而,口服tam存在很多不可避免的副作用,热潮,子宫内膜增厚等,在临床实践中,药物治疗依从性往往不高,如果能在保证乳腺局部剂量的前提下改善不良反应,无疑是一个巨大的突破,从某种意义上来说,打开了化学治疗的一个新窗口。
tam在临床应用的制剂多为片剂。tam在体内分布较广,在杀灭肿瘤细胞的同时也会损害正常细胞,在治疗中可能会引起dna损伤、高甘油三酯血症、骨髓抑制、眼毒性、精神病发作、内分泌紊乱、血管栓塞性疾病、卵巢病变,子宫内膜异位症等,甚至诱发子宫内膜癌,增大了全身不良反应而影响临床应用。为使tam能更多地聚集在肿瘤部位,tam的制剂研究成为了热点,现代研究表明,将tam制备成凝胶,发现tam凝胶剂与口服方案ki67标记指数下降程度相似,而全身效应较小。朱玲等人发现枸橼酸他莫昔芬凝胶制剂经皮给药后在乳腺及其周围的组织形成药物储库,有一定的缓释特性,显著延长他莫昔芬在血浆中的半衰期。刘让如等人制备的tam磁性微球,提高其在肿瘤部位的药物浓度,而增加其药效,张怡等人制备的tam微乳外用制剂具有良好的促透皮作用,这些使得tam的制剂开发成为了研究改善他莫昔芬副作用、提高药效的首选,据报道tam外用制剂有软膏剂和霜剂,但是未见tam传递体凝胶剂的报道,因此有必要对现有的剂型进行改进,制备出释药速度恒定,生物利用度高,毒副作用小的剂型,这需要科研工作者的努力探索。
技术实现要素:
基于上述现有技术,本发明提供了一种他莫昔芬柔性纳米脂质体凝胶剂及其制备方法,该凝胶剂对他莫昔芬有较高的载药量和包封效果,且稳定性和透皮渗透性好。
其制备方法简单,操作方便,制备成本低。
实现本发明上述目的所采取的技术方案为:
一种他莫昔芬柔性纳米脂质体凝胶剂,由以下质量分数的原料制备而成:
一种他莫昔芬柔性纳米脂质体凝胶剂,由以下质量分数的原料制备而成:
进一步,所述的磷脂材料为大豆卵磷脂、氢化大豆卵磷脂和二棕榈酰磷脂酰胆碱中的一种,或者为氢化大豆磷脂和大豆卵磷脂的复合磷脂,或者为氢化大豆卵磷脂和二棕榈酰磷脂酰胆碱的复合磷脂。
进一步,所述的水溶性凝胶基质为纤维素衍生物,所述的纤维素衍生物为甲基纤维素或羧甲基纤维素钠。
进一步,所述的透皮促渗剂为胺、薄荷醇、月桂氮卓酮、泊洛沙姆、月桂醇硫酸钠、脂肪酸或脂肪酸酯。
进一步,所述的胺为尿素;所述的脂肪酸为油酸或月桂酸;所述的脂肪酸酯为月桂醇乳酸酯、肉豆蔻酸异丙酯、丙二醇二壬酸酯或癸二酸二乙酯。
进一步,所述的表面活性剂a为胆酸钠、去氧胆酸钠、脂肪酸甘油酯、蔗糖脂肪酸酯、聚山梨酯或聚氧乙烯脂肪酸酯,所述的表面活性剂b为胆酸钠、去氧胆酸钠或脂肪酸甘油酯。
进一步,所述的防腐剂为苯甲酸、苯甲酸钠、山梨酸或尼泊金酯类,所述的尼泊金酯类为对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯或对羟基苯甲酸丁酯。
进一步,所述的保湿剂为甘油、丙二醇或山梨醇。
一种他莫昔芬柔性纳米脂质体凝胶剂的制备方法,包括如下步骤:
1)将他莫昔芬、胆固醇、磷脂材料、表面活性剂a溶于有机溶剂中,所述的有机溶剂为氯仿、乙醇或乙醚,得到溶液a,将溶液a浓缩去除有机溶剂,加入pbs缓冲液,pbs缓冲液加入的质量为水溶性凝胶基质质量的1-5%,在常温常压下进行水合,得到他莫昔芬柔性纳米脂质体混悬液;
2)将水溶性凝胶基质、表面活性剂b和蒸馏水混合均匀,蒸馏水加入的质量为水溶性凝胶基质质量的0.1-1%,得溶液b,再将透皮促渗剂、防腐剂和保湿剂溶于乙醇中,乙醇加入的质量为水溶性凝胶基质质量的7-12%,得溶液c,搅拌下将溶液c加入溶液b中,溶胀好后,加入氨水调节至中性,氨水加入的质量为水溶性凝胶基质质量的1-5%,得到空白凝胶基质;
3)将空白凝胶基质和他莫昔芬柔性纳米脂质体混悬液混匀,得到他莫昔芬柔性纳米脂质体凝胶剂。
与现有技术相比,本发明的有益效果和优点在于:
1、在载药量和包封率方面,本发明研究发现,他莫昔芬柔性纳米脂质体凝胶剂的载样量0.5~1.2mg/ml,包封率为85.6~96.0%,说明本发明的柔性纳米脂质体凝胶剂对他莫昔芬有较高的载药量和包封效果。
2、在稳定性方面,本发明研究发现,他莫昔芬柔性纳米脂质体凝胶剂的粒径在50.2±0.12~100.8±0.26nm之间,电位为-21.8±0.15~-37.7±0.45mv,多分散系数为0.1±0.05~0.18±0.01,将他莫昔芬柔性纳米脂质体凝胶剂分别放入室温和4℃条件下,于1、5、10、15天内观察外观、粒径、电位和药物含量,发现他莫昔芬柔性纳米脂质体凝胶剂在室温下,粒径稍有增加,电位无明显变化,他莫昔芬含量稍有减少,而4℃下无明显变化,由此表明,本发明的他莫昔芬柔性纳米脂质体凝胶剂在室温和4℃条件下稳定性良好。
3、在体外透皮渗透性方面,本发明研究发现,他莫昔芬柔性纳米脂质体凝胶剂经皮稳态渗透速率和皮内滞留量约为普通他莫昔芬凝胶剂的3-7倍,说明柔性纳米脂质体是一种能有效促进经皮渗透的新型载体。
总之,本发明以他莫昔芬作为药物,以柔性纳米脂质体凝胶剂作为载体,解决了他莫昔芬副作用大,药物依从性的缺陷,本发明的他莫昔芬柔性纳米脂质体凝胶剂能在24h内持续药物释放和透皮,药物通过皮肤进入到给药部位,能够维持局部稳定的血药浓度,同时减少患者的服药次数,增加了患者的依从性。另外,本发明的他莫昔芬柔性纳米脂质体凝胶剂避免了药物口服经胃肠道及肝的首过效应,提高了生物利用度。因此,本发明的他莫昔芬柔性纳米脂质体凝胶剂吸收速率快,透皮量高,具有稳定、高效的特点,在临床应用上具有明显的优势,能有有效的实现药物长时间的持续透皮,从而达到局部给药的靶向作用。
说明书附图
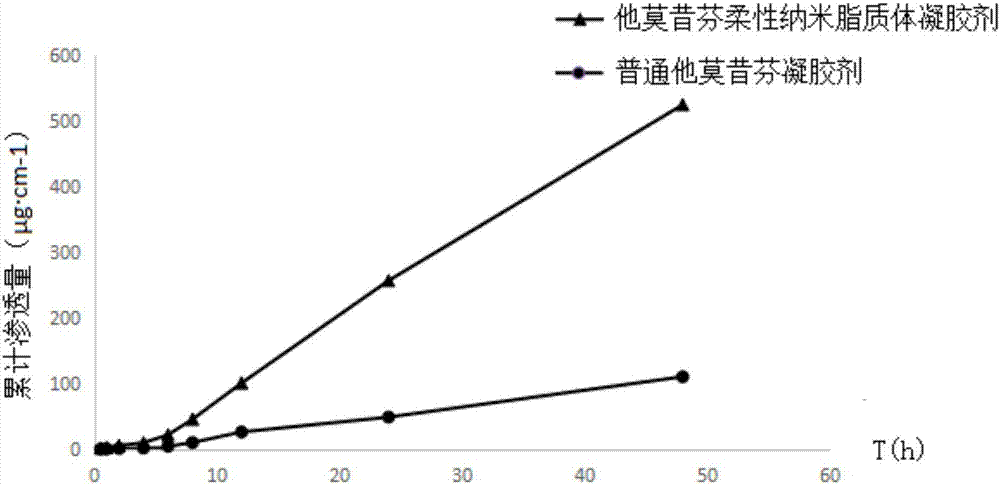
图1为实施例1制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的经皮渗透曲线。
图2为实施例2制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的经皮渗透曲线。
图3为实施例3制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的经皮渗透曲线。
图4为实施例1制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的皮肤药物滞留量对比图。
图5为实施例2制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的皮肤药物滞留量对比图。
图6为实施例3制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的皮肤药物滞留量对比图。
具体实施方式
下面结合具体实施方式对本发明进行详细说明。
实施例1
一种他莫昔芬柔性纳米脂质体凝胶剂,由以下质量分数的原料制备而成:
所述的磷脂材料为氢化大豆磷脂和大豆卵磷脂的复合磷脂,记为spc/hspc(spc和hspc的摩尔比为3:1)。
上述他莫昔芬柔性纳米脂质体凝胶剂的制备方法,其步骤是:
1)将他莫昔芬、胆固醇、spc/hspc、胆酸钠溶于氯仿中,得到溶液a,将溶液a在37℃下减压旋转蒸发除去氯仿,加入pbs缓冲液(ph=7.4),在常温常压下水合15min,得到他莫昔芬柔性纳米脂质体混悬液;
2)将羧甲基纤维素钠、去氧胆酸钠和蒸馏水混合均匀,得溶液b,再将月桂氮卓酮、苯甲酸和丙二醇溶于乙醇中,得溶液c,将溶液c逐渐加入溶液b中,以500rpm的转速搅拌15min,混匀并溶胀好后,加入氨水(25wt%)调节ph值至7.0左右,得到空白凝胶基质;
3)将空白凝胶基质和他莫昔芬柔性纳米脂质体混悬液混合,以500rpm的转速搅拌15min,得到他莫昔芬柔性纳米脂质体凝胶剂。
试验一、本发明的他莫昔芬柔性纳米脂质体凝胶剂的透皮实验
试验方法:
1)将处理好的乳猪皮固定在frank扩散池上,在接受池中加入pbs缓冲液(ph=7.4),供给室中加入他莫昔芬柔性纳米脂质体凝胶剂(实施例1制备),37℃恒温水浴,同时300r·min-1搅拌,在0.5h、1h、2h、4h、6h、8h、12h、24h、48h时取接收液,并补充等量的pbs,将接收液用流动相(乙腈:水=60:40)稀释10倍,高效液相色谱法分析,测定他莫昔芬的含量,计算累计经皮渗透量;以普通他莫昔芬凝胶剂(实验室按照本实施例步骤2方法制备的空白凝胶与他莫昔芬混合搅拌制备而成)为对照,在相同条件下进行实验,测量他莫昔芬的含量,计算累计经皮渗透量。
2)将1)中皮肤渗透试验完成后的乳猪皮取下,去掉乳猪皮表面药物,用pbs缓冲液冲洗角质层和真皮层,擦拭表面水分后,精密称重,再剪碎乳猪皮,置于10ml容量瓶中,甲醇超声提取1h后定容,得到皮肤提取液,将皮肤提取液在12000r·min-1下离心10min,取上清液,将上清液用流动相(乙腈:水=60:40)稀释10倍,高效液相色谱法分析,测定他莫昔芬的含量,计算单位质量皮肤的他莫昔芬滞留量。
试验结果:
1、实施例1制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的经皮渗透曲线如图1所示,该他莫昔芬柔性纳米脂质体凝胶剂经皮渗透曲线的拟合方程为q=8.196t-15.935(r=0.994),普通他莫昔芬凝胶剂的拟合方程为q=2.1717t-4.03(r=0.991)。匀速释药48h,实施例1制备的他莫昔芬柔性纳米脂质体凝胶剂的累计透过量378.26μg·cm-1,经皮稳态渗透速率j为8.196ug·cm-2·h-1。
2、实施例1制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的皮肤药物滞留量如图4所示,从图4可以看出,实施例1制备的他莫昔芬柔性纳米脂质体凝胶剂的皮肤药物滞留量为15.96μg·g-1,普通他莫昔芬凝胶剂的皮肤药物滞留量为5.63μg·g-1。
由此可见,本发明的他莫昔芬柔性纳米脂质体凝胶剂控制释放药物良好,可显著的提高药物皮肤滞留量,从而延长药物作用时间,降低药物毒副作用,实现局部治疗。
实施例2
一种他莫昔芬柔性纳米脂质体凝胶剂,由以下质量分数的原料制备而成:
所述的磷脂材料为二棕榈酰磷脂酰胆碱和大豆卵磷脂的复合磷脂,记为dppc/hspc(dppc和hspc的摩尔比为1:3)。
上述他莫昔芬柔性纳米脂质体凝胶剂的制备方法,其步骤是:
1)将他莫昔芬、胆固醇、dppc/hspc、胆酸钠溶于氯仿中,得到溶液a,将溶液a在37℃下减压旋转蒸发除去氯仿,加入pbs缓冲液(ph=7.4),在常温常压下水合15min,得到他莫昔芬柔性纳米脂质体混悬液;
2)将羧甲基纤维素钠、去氧胆酸钠和蒸馏水混合均匀,得溶液b,再将月桂氮卓酮、苯甲酸和丙二醇溶于乙醇中,得溶液c,将溶液c逐渐加入溶液b中,以500rpm的转速搅拌15min,混匀并溶胀好后,加入氨水调节ph值至7.0左右,得到空白凝胶基质;
3)将空白凝胶基质和他莫昔芬柔性纳米脂质体混悬液混合,以500rpm的转速搅拌15min,得到他莫昔芬柔性纳米脂质体凝胶剂。
试验二、本发明的他莫昔芬柔性纳米脂质体凝胶剂的透皮实验
试验方法:
1)将处理好的乳猪皮固定在frank扩散池上,在接受池中加入pbs缓冲液(ph=7.4),供给室中加入他莫昔芬柔性纳米脂质体凝胶剂(实施例2制备),37℃恒温水浴,同时300r·min-1搅拌,在0.5h、1h、2h、4h、6h、8h、12h、24h、48h时取接收液,并补充等量的pbs,将接收液用流动相(乙腈:水=60:40)稀释10倍,高效液相色谱法分析,测定他莫昔芬的含量,计算累计经皮渗透量;以普通他莫昔芬凝胶剂(实验室按照本实施例步骤2方法制备的空白凝胶与他莫昔芬混合搅拌制备而成)为对照,在相同条件下进行实验,测量他莫昔芬的含量,计算累计经皮渗透量。
2)将1)中皮肤渗透试验完成后的乳猪皮取下,去掉乳猪皮表面药物,用pbs缓冲液冲洗角质层和真皮层,擦拭表面水分后,精密称重,再剪碎乳猪皮,置于10ml容量瓶中,甲醇超声提取1h后定容,得到皮肤提取液,将皮肤提取液在12000r·min-1下离心10min,取上清液,将上清液用流动相(乙腈:水=60:40)稀释10倍,高效液相色谱法分析,测定他莫昔芬的含量,计算单位质量皮肤的他莫昔芬滞留量。
试验结果:
1、实施例2制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的经皮渗透曲线如图2所示,匀速释药48h,实施例2制备的他莫昔芬柔性纳米脂质体凝胶剂的累计透过量523.87μg·cm-1,经皮稳态渗透速率j为11.383ug·cm-2·h-1。
2、实施例2制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的皮肤药物滞留量如图5所示,从图5可以看出,实施例2制备的他莫昔芬柔性纳米脂质体凝胶剂的皮肤药物滞留量为11.47μg·g-1,普通他莫昔芬凝胶剂的皮肤药物滞留量为5.43μg·g-1。
由此可见,本发明的他莫昔芬柔性纳米脂质体凝胶剂控制释放药物良好,可显著的提高药物皮肤滞留量,从而延长药物作用时间,降低药物毒副作用,实现局部治疗。
实施例3
一种他莫昔芬柔性纳米脂质体凝胶剂,由以下质量分数的原料制备而成:
上述他莫昔芬柔性纳米脂质体凝胶剂的制备方法,其步骤是:
1)将他莫昔芬、胆固醇、hspc、胆酸钠溶于氯仿中,得到溶液a,将溶液a在37℃下减压旋转蒸发除去氯仿,加入pbs缓冲液(ph=7.4),在常温常压下水合15min,得到他莫昔芬柔性纳米脂质体混悬液;
2)将羧甲基纤维素钠、去氧胆酸钠和蒸馏水混合均匀,得溶液b,再将月桂氮卓酮、苯甲酸和丙二醇溶于乙醇中,得溶液c,将溶液c逐渐加入溶液b中,以500rpm的转速搅拌15min,混匀并溶胀好后,加入氨水调节ph值至7.0左右,得到空白凝胶基质;
3)将空白凝胶基质和他莫昔芬柔性纳米脂质体混悬液混合,以500rpm的转速搅拌15min,得到他莫昔芬柔性纳米脂质体凝胶剂。
试验三、本发明的他莫昔芬柔性纳米脂质体凝胶剂的透皮实验
试验方法:
1)将处理好的乳猪皮固定在frank扩散池上,在接受池中加入pbs缓冲液(ph=7.4),供给室中加入他莫昔芬柔性纳米脂质体凝胶剂(实施例3制备),37℃恒温水浴,同时300r·min-1搅拌,在0.5h、1h、2h、4h、6h、8h、12h、24h、48h时取接收液,并补充等量的pbs,将接收液用流动相(乙腈:水=60:40)稀释10倍,高效液相色谱法分析,测定他莫昔芬的含量,计算累计经皮渗透量;以普通他莫昔芬凝胶剂(实验室按照本实施例步骤2方法制备的空白凝胶与他莫昔芬混合搅拌制备而成)为对照,在相同条件下进行实验,测量他莫昔芬的含量,计算累计经皮渗透量。
2)将1)中皮肤渗透试验完成后的乳猪皮取下,去掉乳猪皮表面药物,用pbs缓冲液冲洗角质层和真皮层,擦拭表面水分后,精密称重,再剪碎乳猪皮,置于10ml容量瓶中,甲醇超声提取1h后定容,得到皮肤提取液,将皮肤提取液在12000r·min-1下离心10min,取上清液,将上清液用流动相(乙腈:水=60:40)稀释10倍,高效液相色谱法分析,测定他莫昔芬的含量,计算单位质量皮肤的他莫昔芬滞留量。
试验结果:
1、实施例3制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的经皮渗透曲线如图3所示,匀速释药48h,实施例3制备的他莫昔芬柔性纳米脂质体凝胶剂的累计透过量1289.32μg·cm-1,经皮稳态渗透速率j为27.367ug·cm-2·h-1。
2、实施例3制备的他莫昔芬柔性纳米脂质体凝胶剂和普通他莫昔芬凝胶剂的皮肤药物滞留量如图6所示,从图6可以看出,实施例3制备的他莫昔芬柔性纳米脂质体凝胶剂的皮肤药物滞留量为8.27μg·g-1,普通他莫昔芬凝胶剂的皮肤药物滞留量为5.13μg·g-1。
由此可见,本发明的他莫昔芬柔性纳米脂质体凝胶剂控制释放药物良好,可显著的提高药物皮肤滞留量,从而延长药物作用时间,降低药物毒副作用,实现局部治疗。
- 还没有人留言评论。精彩留言会获得点赞!