一种含有ApoG2和AlpcS4的双纳米载药系统及其制备方法和应用与流程
本发明涉及抗肿瘤药物研究领域,特别涉及一种含有apog2和alpcs4的双纳米载药系统及其制备方法和应用。
背景技术:
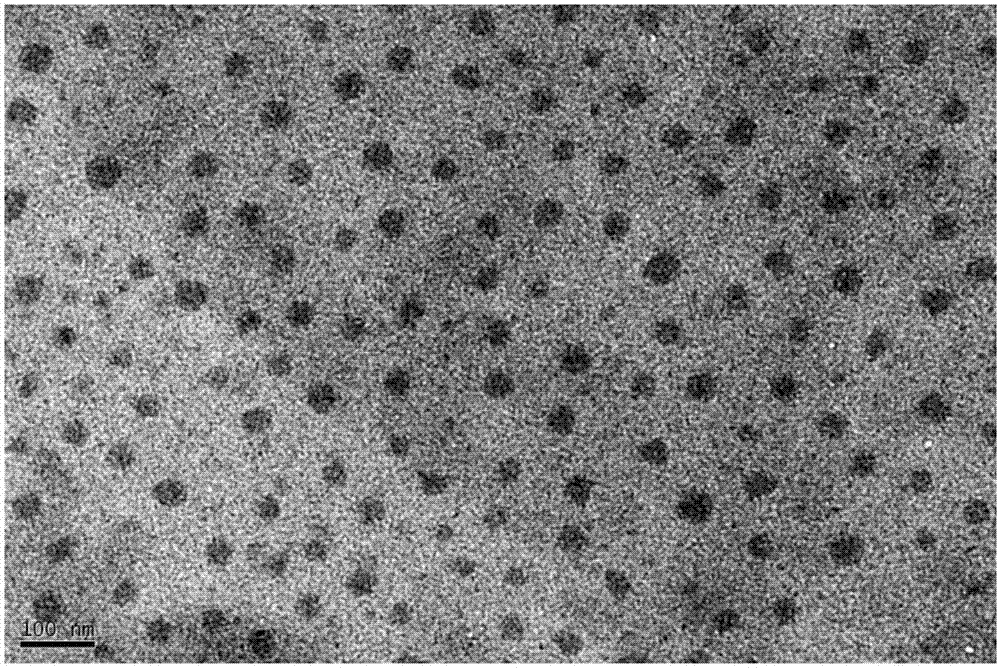
:根据世界卫生组织2014年全球癌症报告,全球每年新增病例1400万,死亡病例800万。因此,恶性肿瘤严重危害着人类生命健康。其中胃癌,是我国第三大常见肿瘤,每年新发率高达40多万人,死亡率高达30多万人,居世界首位。据统计,全球每年新发胃癌有40%以上发生在中国,而其在西方国家发病率较低,从而成为我国必须自主攻克的重大疾病之一。近几年,胃癌的基础研究和临床治疗受到了多个研究学者和医生的广泛关注,各种以期攻克胃癌的基础研究和临床治疗策略取得了很大的进展,各种新型药物和个性化治疗方案层出不穷,尽管治疗效果有所改进但是死亡率及转移复发率仍旧很高。随着癌症研究的不断深入,具有高效、安全、创伤小、副作用少、可协同性、可重复性和相对成本低等优点的光动力疗法,成为最具前景的肿瘤治疗方法之一。光动力疗法主要是利用光照下可产生光敏化作用的光敏剂来破坏病变组织的一种微创疗法,无疑光敏剂是光动力疗法的核心环节。四磺酸酞菁铝(alpcs4)是一种具有近红外荧光特性的第二代光敏剂,由于其具有较深的光组织穿透性、高的荧光量子产量、较强的光稳定性、表面可修饰性以及对目标组织的可视化示踪而成为了光敏剂的研究热点。将其应用于乳腺癌、胰腺癌、卵巢癌、结肠癌等肿瘤光动力治疗已经有所报道,而针对胃癌的治疗研究方面几乎还是空白。而且从目前研究结果看,它对肿瘤组织的选择性和富集能力有限导致其不能完全根治肿瘤进而导致肿瘤复发从而大大阻碍了其向临床应用的推进。光动力疗法与化疗药物协同作用是一种有效的改善光动力治疗效果的途径,但是传统的化疗药物大的毒副作用,反复使用过程中的多药耐药现象导致治疗失败时有发生。项目发明人前期一直致力于一种新型bcl-2/bcl-xl小分子抑制剂apog2化疗药物作用于胃癌的治疗研究,研究结果表明apog2以小的毒副作用可靶向胃癌组织中高表达的bcl-2,bcl-xl蛋白通过激活线粒体凋亡通路以及内质网应激凋亡通路等多途径诱导胃癌细胞凋亡,具有较强的抑瘤效果。现有技术中还不存在以alpcs4和apog2构建的双载药系统。技术实现要素:本发明的目的在于提供一种含有apog2和alpcs4的双纳米载药系统及其制备方法和应用,其能够实现alpcs4光敏剂的光动力治疗和apog2化疗药物协同灭活肿瘤细胞。本发明是通过以下技术方案来实现:一种含有apog2和alpcs4的双纳米载药系统,以质量份数计,包括1~2份apog2,1~2份alpcs4及3~5份泊洛沙姆;其中,apog2和alpcs4包封于泊洛沙姆中。优选地,所述泊洛沙姆包括pluronicf127和pluronicp123。优选地,泊洛沙姆为纳米胶束;apog2和alpcs4包含在泊洛沙姆的聚氧丙烯(ppo)嵌段中。本发明还公开了上述含有apog2和alpcs4的双纳米载药系统的制备方法,包括以下步骤:1)将泊洛沙姆和apog2溶解在第一溶剂中,得第一溶液;将alpcs4溶解在第二溶剂中,得第二溶液;2)在搅拌下,将第一溶液加入到第二溶液中,搅拌12~36小时,得反应混合液;3)将反应混合液用透析袋纯化,纯化产物经过冷冻干燥,制备得含有apog2和alpcs4的双纳米载药系统。优选地,在步骤1)中,将泊洛沙姆溶解在乙醇中,在加入apog2,溶解后得第一溶液。优选地,在步骤1)中,所述第二溶剂为去离子水。优选地,在第一溶液中,泊洛沙姆的浓度为5~15mg/ml。优选地,在第一溶液中,apog2的浓度为2~8mg/ml。优选地,在第二溶液中,alpcs4的浓度为2~8mg/ml。优选地,步骤3)中,透析袋的截留分子量为3000。本发明还公开了上述含有apog2和alpcs4的双纳米载药系统在制备抗肿瘤药物中的应用。优选地,所述肿瘤包括胃癌。与现有技术相比,本发明具有以下有益的技术效果:本发明提供的含有apog2和alpcs4的双纳米载药系统,其包括泊洛沙姆,apog2和alpcs4包封在泊洛沙姆中。波洛沙姆嵌段共聚物在熔融状态和溶液状态下可实现自组装形成胶束,从而成为难溶性、具有不理想药动力学和低稳定药物的理想载体,其内核主要由ppo疏水嵌段构成,但是若干peo亲水嵌段也会存在于内核中;apog2是一种疏水性药物,很容易被波洛沙姆包入胶束的内核中,alpcs4是一类亲水性药物,会包借助peo而含在ppo嵌段中,如此,可以简单快速的制备出含亲水性药物alpcs4和疏水性药物apog2的双纳米载药系统,过程中不需要复杂的设备。而且波洛沙姆纳米胶束可以有效解决apog2难溶性的问题。光敏药物alpcs4进行光动力效应过程中产生有毒的活性氧物质是其发挥作用的关键原因。而活性氧物质是激活内质网应激凋亡通路的关键因素,新型bcl-2/bcl-xl小分子抑制剂apog2化疗药物也可以通过提高细胞内活性氧浓度和钙离子浓度而激活内质网应激凋亡通路刺激细胞发生凋亡进而杀伤细胞。两者在协同过程中,都促进活性氧浓度升高,因此在短时间内就可以有效的杀伤细胞和激活内质网应激凋亡通路,从而有效的杀伤肿瘤细胞。如此,含有apog2和alpcs4的双纳米载药系统能够实现alpcs4光敏剂的光动力治疗和apog2化疗药物协同灭活肿瘤细胞,借助光敏剂alpcs4的光动力治疗效果协同apog2化疗治疗效果有望有效提高肿瘤杀伤效率,解决alpcs4光敏剂的药物传递效率低、光动力治疗效果有限的特点,而且有效解决apog2难溶性的问题,制备方法简单。另外,波洛沙姆具有良好的生物相容性和蛋白抗性,为后期的靶向治疗提供了可靠方案。不仅如此,光敏剂alpcs4的近红外荧光特性为药物监测提供了有效途径:基于alpcs4的荧光特性,可以利用荧光光学成像方式实时有效检测药物在体内外的存留情况,还可以根据alpcs4的可修饰性对其进行靶向修饰实时检测治疗效果。本发明提供的含有apog2和alpcs4的双纳米载药系统的制备方法,其方法简单,无需复杂设备。本发明提供的含有apog2和alpcs4的双纳米载药系统在制备抗肿瘤药物中的应用,其可以制备高效的抗肿瘤药物。附图说明图1为本发明提供的f-127双载药纳米胶束吸收光谱;图2为本发明提供的f-127双载药纳米胶束电镜图;图3为本发明提供的f-127双载药纳米胶束在pbs和水中稳定性结果图;其中,(a)为pbs;(b)为水;图4为本发明提供的f-127双载药纳米胶束对胃癌细胞灭活效果。图5为本发明提供的f-127双载药纳米胶束中alpcs4荧光定位结果图。具体实施方式下面结合具体的实施例对本发明做进一步的详细说明,所述是对本发明的解释而不是限定。1、双纳米载药系统的制备:称取10mgf-127溶于1ml无水乙醇中,再将2.5mg、2.5mg、5mgapog2溶于f-127的无水乙醇溶液中备用。称取2.5mg、2.5mg、5mgalpcs4溶于10ml去离子水中置于磁力搅拌器上搅拌。然后将含有2.5mg、5mg、2.5mgapog2的f-127乙醇溶液缓慢滴加至对应的alpcs4的去离子水中,搅拌24h,具体反应方式见表1。然后将其置于透析袋中进行纯化24h,期间换水8次左右,结束后将其收集于10cm培养板内-20℃冻干,最后冷冻干燥获得载有alpcs4和apog2的f-127双载药纳米胶束。将冷冻干燥后的f-127双载药纳米胶束溶于1mlpbs中,配制合适浓度的纳米胶束滴加至铜网上用透射电镜分析纳米胶束的形貌,结果如图2所示。表1f127alpcs4apog210mg2.5mg2.5mg10mg5mg2.5mg10mg2.5mg5mg2、双纳米载药系统的载药率和包封率的测量参见图1,将配置好的3.125-50um的apog2水溶液在紫外吸收光谱仪上测取od值建立标准曲线备用。将配置好的0.25-8ug/ml的alpcs4水溶液在紫外吸收光谱仪上测取od值建立标准曲线备用。将冷冻干燥后的f-127纳米胶束溶于1mlpbs中,取10ul溶于2ml去离子水中置于紫外吸收光谱仪上测取alpcs4(675nm左右),apog2(281nm)左右od值,根据之前建立的标准曲线,换算药物浓度,然后根据包封率=纳米胶束中药物的浓度/投药量的浓度,载药率=纳米胶束中药物的浓度/载体+所包裹药物的浓度计算包封率和载药率。结果显示2.5mgalpcs4与2.5mgapog2进行包封时包封率分别为35.6%和87.7%,载药率为20.55%,5mgalpcs4与2.5mgapog2进行包封时包封率分别为48.8%和89.6%,载药率为21%,2.5mgalpcs4与5mgapog2进行包封时包封率分别为21.3%和78%,载药率为25.3%。3、双纳米载药系统药物释放分析将10ul的载有alpcs4和apog2的f-127纳米胶束溶液溶于2ml1%trixonx-100溶液中,加入透析袋放置于加热到37℃的盛有100mlpbs的烧杯中,磁力搅拌器上37℃加热搅拌,每隔半小时吸取烧杯内溶液2ml在紫外吸收光谱仪上测量所含药物的od值,参见图3,其中,(a)为pbs;(b)为水。根据之前建立的标准曲线换算药物浓度,制作药物释放曲线,注意每次吸取完待测样后及时补充pbs以防加热导致pbs损失。结果显示apog2和alpcs4在8h内可以有效释放,无突释现象。4、双纳米载药系统对胃癌细胞灭活效应研究将sgc-7901胃癌细胞用含10%的胎牛血清,100u/ml青霉素,100ug/ml链霉素的rpmi1640培养液置37℃,5%的co2的培养箱培养待细胞融合率达80%左右时用0.25%胰蛋白酶消化铺板于96孔板,置于37℃5%的co2的培养箱隔夜培养。然后,将不同浓度的包封的f-127-alpcs4、f-127-apog2、f-127-alpcs4+apog2溶液分别加入96孔板中,每浓度设3个复孔,另外设3个不加细胞只加培养基的空白对照孔。放回培养箱继续培养6h,pbs清洗后换新鲜培养液继续培养24h后,每孔加入10μlcck-8溶液,放回培养箱继续培养1h,最后在酶标仪上490nm处读出各孔的od值,实验重复3次,计算细胞存活率。细胞存活率=(od(实验组值)-od(空白对照组)/od(阴性对照组值)-od(空白对照组))×100%。根据细胞存活率,分析f-127-alpcs4、f-127-apog2、alpcs4浓度相同下apog2不同浓度f-127-alpcs4+apog2溶液以及apog2浓度相同下alpcs4不同浓度f-127-alpcs4+apog2溶液的暗毒性。类似方法对对铺于96孔板的sgc-7901细胞进行药物干预6h,结束后,pbs清洗换新鲜培养液,放置于635nm激光器下以100mw/cm2光照计量光照5min,放回培养箱继续培养24h。利用上述相同的步骤计算f-127-alpcs4、alpcs4浓度相同下apog2不同浓度f-127-alpcs4+apog2溶液以及apog2浓度相同下alpcs4不同浓度f-127-alpcs4+apog2溶液的细胞杀伤作用。参见图4,结果显示,2.5mgalpcs4与2.5mgapog2进行包封,5mgalpcs4与2.5mgapog2进行包封,2.5mgalpcs4与5mgapog2进行包封后基于apog2不变,alpcs4越多杀伤效率越好,含有19.36ug/mlalpcs4和72.4umapog2的细胞活性在24h时可降至20%左右。基于alpcs4不变,apog2越多杀伤效率越好,含有12ug/mlalpcs4和180umapog2的细胞活性在24h时可降至5%左右。5、双纳米载药系统中alpcs4在apog2干预下对胃癌细胞作用差异分析:将sgc-7901胃癌细胞用含10%的胎牛血清,100u/ml青霉素,100ug/ml链霉素的rpmi1640培养液置37℃,5%的co2的培养箱培养待细胞融合率达80%左右时用0.25%胰蛋白酶消化铺板于6孔板,置于37℃5%的co2的培养箱隔夜培养。。待sgc-7901进入对数生长期后,将细胞铺入含有爬片的6孔板,隔夜培养。然后,将不同浓度的f-127-alpcs4、alpcs4浓度相同下apog2不同浓度f-127-alpcs4+apog2溶液以及apog2浓度相同下alpcs4不同浓度f-127-alpcs4+apog2溶液分别加入6孔板中,放回培养箱继续培养6h,然后pbs清洗,加入dapi进行细胞核染色,染色结束后pbs清洗捞出细胞爬片放置于载玻片上用防荧光萃灭甘油封片载入荧光显微镜进行alpcs4在不同浓度药物干预下其在细胞内位置的观察。参见图5,结果显示apog2可以有效促进alpcs4向细胞核内迅速转化。6、双纳米载药系统对胃癌细胞灭活机理研究类似上面的步骤,将sgc-7901细胞置于6孔板最后隔夜培养。第二天,将不同浓度的f-127-alpcs4、alpcs4浓度相同下apog2不同浓度f-127-alpcs4+apog2溶液以及apog2浓度相同下alpcs4不同浓度f-127-alpcs4+apog2溶液分别加入6孔板中,放回培养箱继续培养6h,然后pbs清洗,置换新鲜培养基培养24h后利用hoechst33258观测细胞凋亡形态。将不同浓度的f-127-alpcs4、alpcs4浓度相同下apog2不同浓度f-127-alpcs4+apog2溶液以及apog2浓度相同下alpcs4不同浓度f-127-alpcs4+apog2溶液分别加入6孔板中,放回培养箱继续培养6h,然后pbs清洗,加入sosgr探针,置于635nm激光器进行光照处理然后进行单态氧产量检测,验证apog2可提高alpcs4单态氧产量进而提高光动力治疗效果。相同方法,加入dcfh-da,置于635nm激光器进行光照处理然后进行活性氧产量检测,评价双纳米载药系统中药物对活性氧浓度的影响。参见图5,结果显示双纳米载药系统可以有效改善alpcs4的单态氧产率,可提高至3-5倍。活性氧浓度也在光照后2小时内有效开始提高。综上所述,alpcs4是一类亲水性药物,会包借助peo而含在ppo嵌段中,如此,可以简单快速的制备出含亲水性药物alpcs4和疏水性药物apog2的双纳米载药系统,过程中不需要复杂的设备。而且波洛沙姆纳米胶束可以有效解决apog2难溶性的问题。由于alpcs4经激光照射后产生的有毒的活性氧物质是光动力治疗的关键,而apog2也可以提高细胞内活性氧的浓度和钙离子浓度而激活内质网应激凋亡通路,因此将alpcs4与apog2化疗作用协同作用于胃癌细胞,有望彻底灭活胃癌细胞阻止肿瘤复发的可能。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1