自闭症谱系障碍和精神疾病改善剂的制作方法
本发明涉及催产素和/或加压素的分泌促进剂。本发明还涉及自闭症谱系障碍改善剂或精神疾病改善剂、以及社会性行动改善或社会性促进剂或实现抗焦虑·抗压力效果的补剂或功能性食品。
背景技术:
自闭症谱系障碍(asd)是指精神障碍诊断和统计手册第5版(dsm-5)上的各种各样的神经发育症(neurodevelopmentaldisorder)的分类。其特征在于,社会性交流和相互关系中的持续性障碍、以及限定的反复模式的行动、兴趣、活动这两个核心症状,包括从轻度至重度的谱系。
作为对asd的治疗药,根据症状作为对症疗法将中枢神经刺激药、抗精神病药、抗癫痫药、选择性血清素再摄取抑制药等开具处方,但现状是没有改善核心症状的有效药剂。
催产素是通过脑的下丘脑而产生的肽激素,已知具有用于诱导分娩的子宫收缩刺激、乳汁分泌刺激作用。最近,暗示了催产素对自闭症谱系障碍或asd的患者中观察到的反复行动的发病具有潜在贡献(例如非专利文献1),报告了通过滴鼻给予来改善自闭症患者的社会性行动(例如非专利文献2、3)。
但是,在利用催产素滴鼻给予的治疗中,也报告了非有效例,其效果有限。可能是由于滴鼻是泄露多的给予途径,因此催产素的血中转移变得不稳定。此外,血中催产素的脑屏障通过极其微量,因此推测催产素向脑中的转移不稳定且微量。进一步,自闭症患者本人或家人切实地滴鼻给予也不能称为容易。
加压素与催产素同样,是由脑的下丘脑合成、从垂体后叶向血中分泌的肽激素,已知具有抗利尿、血压上升作用。另一方面,作为脑内的神经传递物质而发挥功能的加压素与催产素同样,已知与精神分裂症、自闭症等精神功能相关联(非专利文献4、5)。
现有技术文献
非专利文献
非专利文献1:erichollander,etal.,"oxytocininfusionreducesrepetitivebehaviorsinadultswithautisticandasperger’sdisorders"neuropsychopharmacology(2003)28,193-198
非专利文献2:yatawara,c.j.,etal.,"theeffectofoxytocinnasalsprayonsocialinteractiondeficitsobservedinyoungchildrenwithautism:arandomizedclinicalcrossovertrial."molecularpsychiatry,(2015)
非专利文献3:watanabe,t.,etal.,"clinicalandneuraleffectsofsix-weekadministrationofoxytocinoncoresymptomsofautism."brain:ajournalofneurology138(11):3400-12,(2015)
非专利文献4:江头伸昭等,日药理志、2009、134、3-7。
非专利文献5:meyer-lindenberga.etal.,“oxytocinandvasopressininthehumanbrain:socialneuropeptidesfortranslationalmedicine.”natrevneurosci.2011,12(9):524-38。
专利文献
专利文献1:日本特表2007-525442号
专利文献2:日本特开2014-171392号。
技术实现要素:
发明要解决的课题
本发明的目的在于,提供具有催产素和/或加压素的分泌促进作用的药剂,进一步在于,提供具有催产素和/或加压素的分泌促进作用、由此能够治疗自闭症谱系障碍的药剂。
本发明的目的还在于,提供对自闭症谱系障碍的治疗有效的新药剂。此外,本发明的目的进一步在于,提供新的精神疾病改善剂。
本发明的进一步的目的在于,提供克服滴鼻催产素那样的不稳定性的自闭症谱系障碍的治疗药。
本发明的进一步的目的在于,提供将中枢催产素和/或加压素神经细胞活化、由此能够治疗自闭症谱系障碍的药剂。
本发明的另一个目的在于,提供实现社会性行动改善或社会性促进或抗焦虑·抗压力效果的补剂或实现这样的效果的功能性食品。
解决课题的手段
本发明人等发现,如果对小鼠经口给予作为稀少糖的d-阿洛酮糖,则发现社会性行动的改善。此外,还发现通过d-阿洛酮糖的经口给予,下丘脑被活化,室旁核(pvn)和视上核(son)和其他新部位的催产素神经元和加压素神经元被活化,进一步下丘脑中的催产素和加压素的mrna的表达亢进。这些的结果显示,通过d-阿洛酮糖的经口给予,产生已知为社会性行动改善、抗焦虑、抗压力、学习促进、抗肥胖作用等的催产素和/或加压素的神经元的功能被活化,或催产素和/或加压素的分泌被促进,从而改善自闭症谱系障碍,实现抗焦虑、抗压力效果。
因此,本发明提供包含d-阿洛酮糖作为有效成分的催产素和/或加压素的分泌促进剂。
上述方式中,前述分泌促进剂优选为经口给予剂。
上述方式中,前述分泌促进剂在给予时,能够不与蔗糖或含蔗糖食品同时摄取而给予,故而优选。
上述方式中,前述分泌促进剂能够活化脑内的催产素和/或加压素神经元,或能够促进催产素和/或加压素的分泌,故而优选。
本发明此外还提供用于催产素和/或加压素的分泌促进的d-阿洛酮糖。
本发明此外还提供以下的实施方式。
<1>自闭症谱系障碍改善剂,其包含d-阿洛酮糖作为有效成分。
<2>精神疾病改善剂,其包含d-阿洛酮糖作为有效成分。
<3>社会性促进或社会性行动改善剂,其包含d-阿洛酮糖作为有效成分。
<4>抗焦虑剂,其包含d-阿洛酮糖作为有效成分。
<5>抗压力剂,其包含d-阿洛酮糖作为有效成分。
<6>焦虑减轻食品,其包含d-阿洛酮糖作为有效成分。
<7>压力减轻食品,其包含d-阿洛酮糖作为有效成分。
<8>催产素和/或加压素的分泌促进剂,其包含d-阿洛酮糖作为有效成分。
<9>根据<1>或<2>所述的药剂,其用于通过经口给予d-阿洛酮糖而促进催产素和/或加压素的脑内分泌,由此改善自闭症谱系障碍、或治疗精神疾病。
此外,本发明提供以下方式。
<10>d-阿洛酮糖,其用于治疗或改善下述疾病或症状:
(i)选自自闭症谱系障碍和精神疾病中的一种或多种疾病;
(ii)选自社会性行动的障碍、焦虑症和压力中的一种或多种症状。
<11>根据<10>所述的d-阿洛酮糖,其被经口给予。
<12>根据<10>或<11>所述的d-阿洛酮糖,其用于通过促进催产素和/或加压素的分泌,从而治疗或改善前述疾病或症状。
进一步,本发明提供以下方式。
<20>下述疾病或症状的治疗或改善方法,其包括将有效量的d-阿洛酮糖对具有下述疾病或症状的患者给予:
(i)选自自闭症谱系障碍和精神疾病中的一种或多种疾病;
(ii)选自社会性行动的障碍、焦虑症和压力中的一种或多种症状。
<21>根据<20>所述的方法,其中,d-阿洛酮糖被经口给予。
<22>通过将催产素和/或加压素分泌促进剂对患者给予,从而治疗或改善下述疾病或症状的方法:
(i)选自自闭症谱系障碍和精神疾病中的一种或多种疾病;
(ii)选自社会性行动的障碍、焦虑症和压力中的一种或多种症状;
前述催产素和加压素分泌促进剂为d-阿洛酮糖。
<23>根据<22>所述的方法,其中,d-阿洛酮糖被经口给予。
发明的效果
通过本发明的药剂,能够促进人或动物的脑内的催产素和/或加压素的分泌。
通过本发明,能够提供对自闭症谱系障碍有效的药剂。此外,本发明进一步提供新的精神疾病改善剂。
本发明的药剂通过经口给予而实现效果,能够提供克服滴鼻催产素那样的给予途径中的不稳定性的自闭症谱系障碍的改善剂。
此外,本发明的药剂能够活化中枢催产素神经细胞,因此能够解决滴鼻催产素中的血脑屏障通过的问题。
本发明的另一个目的在于,提供实现社会性行动改善或社会性促进或抗焦虑·抗压力效果的补剂或实现这样的效果的功能性食品。
此外,通过本发明,由于无安全性、副作用的问题,进一步能够经口给予,具有甜味,因此能够提供容易被儿童摄取的药剂。
附图说明
图1a示出通过本发明的药剂的经口给予,下丘脑的特别是室旁核(pvn)、视上核(son)、和新区域中使c-fos表达量显著亢进。
图1b示出小鼠下丘脑(bregma-1.22mm)的组图谱。除此之外,本发明中不存在醒目的区域名称的新区域在图中用四角框表示。
图1c示出本发明药剂经口给予后的c-fos免疫染色的小鼠下丘脑切片的显微镜照片。图中的表示为新区域的区域中观察到c-fos阳性(黑点)细胞。
图1d是将图1c的新区域部分放大的图。
图2a示出通过本发明的药剂的经口给予,室旁核(pvn)的催产素(oxt)神经元被活化。细胞质整体显示为淡灰色的部分是催产素阳性细胞,核内小而显示为白色的部分表示c-fos蛋白表达。
图2b示出下丘脑室旁核(pvn)催产素神经元中的c-fos阳性神经元的比例(%)。
图2c示出通过本发明的药剂的经口给予,室旁核(pvn)的加压素(avp)神经元被活化。细胞质整体显示为淡灰色的部分是加压素阳性细胞,核内小而显示为白色的部分表示c-fos蛋白表达。
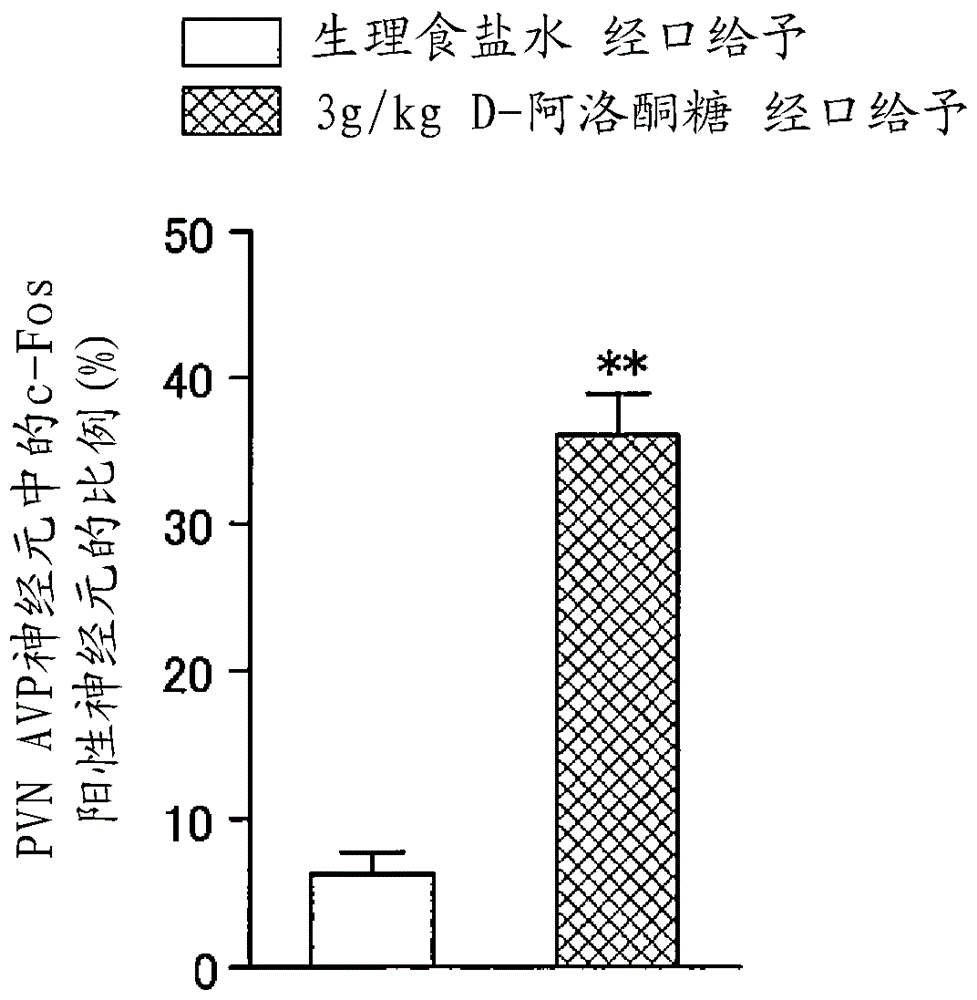
图2d示出下丘脑室旁核(pvn)加压素神经元中的c-fos阳性神经元的比例(%)。
图3a示出下丘脑视上核(son)催产素(oxt)和加压素(avp)神经元被活化。显示为淡灰色的部分是催产素或加压素阳性细胞,显示为白色的部分表示细胞的核中存在的c-fos蛋白表达。
图3b示出下丘脑视上核(son)中的催产素和加压素神经元中的c-fos阳性神经元的比例(%)。
图4a示出下丘脑新区域的催产素(oxt)(a-c)和加压素(avp)(d-f)神经元被活化。显示为淡灰色的部分是催产素或加压素阳性细胞,显示为白色的部分表示细胞的核中存在的c-fos蛋白表达。图a内的b、c的放大图示于图b、图c。此外,图d中的e、f的放大图示于图e、f。
图4b示出下丘脑新区域中的催产素和加压素神经元中的c-fos阳性神经元的比例(%)。
图5示出给予本发明的药剂的小鼠的下丘脑中的催产素和加压素mrna的表达变化量。
图6a示出给予本发明的药剂的小鼠的旷场实验的情况。
图6b示出经口给予本发明的药剂1g/kg和3g/kg的小鼠的旷场实验的结果。
图7a示出给予本发明的药剂的小鼠的社会性测试的情况和结果。
图7b示出经口给予本发明的药剂1g/kg和3g/kg的小鼠的社会性测试的结果(探索行动时间)。
具体实施方式
<d-阿洛酮糖>
本发明的药剂、补剂和功能性食品的有效成分、即d-阿洛酮糖是被分类为六碳单糖和酮糖的单糖的一种。此外,也称为稀少糖。d-阿洛酮糖的甜味度为砂糖的约70%,具有与d-果糖类似的高级且清爽的甜味,但热量几乎为零。
d-阿洛酮糖在以往公知那样的来源或方式的制品中也能够使用。即,无论其精制度如何,有从鼠刺等植物提取的物质;通过碱异构化法以d-葡萄糖、d-果糖为原料异构化得到的物质(例如松谷化学工业(株)制“レアシュガースウィート”);通过利用由微生物或其重组体得到的酶(异构酶、差向异构酶等)的酶法以d-葡萄糖、d-果糖作为原料异构化得到的物质(例如松谷化学工业(株)制“astraeaallulose”)等,能够较为容易地获取。
本发明的药剂为了发挥其效果,特别优选经口摄取d-阿洛酮糖。d-阿洛酮糖可以单独使用,不需要与蔗糖或含蔗糖食品同时摄取,或在摄取后给予。
<药剂·补剂>
本发明的药剂·补剂的剂型没有特别限定,可以为例如液状、片剂状、颗粒状、粉末状、胶囊状、凝胶状、溶胶状中任一者,此外,制剂化按照公知的方法进行即可,可以通过将有效成分的d-阿洛酮糖与淀粉、羧基甲基纤维素等药学可接受的载体混合,进一步根据需要添加稳定剂、赋形剂、结合剂、崩解剂等,从而进行。
此外,不限于经口给予,还可以举出利用注射剂、贴剂、喷雾剂等的非经口给予。此外,这样的医药制剂可以组合制备一般的赋形剂、稳定剂、保存剂、结合剂、崩解剂等适当的添加剂。上述医药品的给予方式之中,优选的方式为经口给予。
<功能性食品>
作为功能性食品的方式,没有特别限定,可以用于例如布丁、果冻、糖果、巧克力、面包、蛋糕、饼干、馒头等点心类、生奶油等蛋制品、功能性饮料、乳酸饮料、果汁饮料、碳酸饮料等饮料、红茶、速溶咖啡等嗜好品、冰淇淋、酸奶、奶酪等乳制品、甘佩斯、果实的糖浆浸渍品等膏类、火腿、香肠、培根等畜肉制品、鱼肉火腿、鱼肉香肠等水产加工制品、酱油、蘸汁、浇汁等调味料等。
此外,还能够用作流动食品、成分营养食品、饮用营养食品、经肠营养食品等功能性食品或营养辅助食品,其方式没有特别限定,例如在运动饮品的情况下为了使营养平衡和风味良好,还可以进一步配合氨基酸、维生素类、矿物质类等营养添加物、组合物、香料、色素等。
<d-阿洛酮糖的摄取量、摄取方法>
本发明的以d-阿洛酮糖作为有效成分的药剂、补剂和功能性食品的摄取量只要得到其效果,则没有特别限定,例如对于小鼠、大鼠,优选每1次每1kg体重以d-阿洛酮糖计摄取0.07g~5.0g\更优选为0.1g~4.0g、进一步优选为0.15g~3.5g的范围、更进一步优选为1.2g~3.5g的范围。
对人而言,可以使用与小鼠、大鼠的摄取量相比更低的摄取量,可以以例如10分之1左右的量使用。例如,优选每1次每1kg体重以d-阿洛酮糖计摄取0.007g~0.5g、更优选为0.01g~0.4g、进一步优选为0.015g~0.35g的范围、更进一步优选为0.12g~0.35g的范围。关于人的摄取量,还考虑对象者的健康状态、体重、年龄其他条件而确定。例如,平均成人(60kg)1人一次摄取的d-阿洛酮糖量可以为10g~12g(0.17g~0.2g/kg)。此外,摄取时机优选为餐前,进一步优选在餐前1小时以内摄取,更优选在餐前15~30分钟以内摄取。
<其他添加物>
特定的实施方式中,第2活性剂为抗精神病药、非典型精神病药、对阿兹海默病的治疗有用的药剂、或胆碱酯酶抑制剂。
特定的实施方式中,第2活性剂是包括snri(血清素·去甲肾上腺素再摄取抑制药)、ssri(选择性血清素再摄取抑制药)、tca(三环系抗抑郁剂)、或maoi(单胺氧化酶抑制药)、但不限于这些的抗抑郁剂。
特定的实施方式中,第2活性剂是卢拉西酮、奥氮平、利培酮、阿立哌唑、阿米舒必利、阿塞那平、布南色林、氯氮平、氯噻平、伊潘立酮、莫沙帕明、帕潘立酮、喹硫平、雷莫昔普、塞地多林、舒必利、齐拉西酮、佐替平、匹马沙林、洛沙平、多奈哌齐、卡巴拉汀、美金刚胺、加兰他敏、他克林、苯丙胺、哌醋甲酯、阿莫西汀、莫达非尼、舍曲林、氟西汀、度洛西汀、文拉法辛、苯乙嗪、司来吉兰、丙米拉明、地昔帕明、氯米帕明、或左旋多巴。
本发明的补剂和功能性食品中,除了d-阿洛酮糖之外,还可以含有水溶性食物纤维作为有效成分。
作为水溶性食物纤维,可以例示出果胶、蒟蒻甘露聚糖、藻酸、瓜尔胶、琼脂等高粘性食物纤维、或难消化性糊精、聚右旋糖、瓜尔胶分解物等低粘性食物纤维。
这些之中,从效果的观点出发,特别优选为难消化性糊精、瓜尔胶水解物、聚右旋糖等。
这些之中,低粘性食物纤维从处理和至大肠的移动时间短的观点出发是优选的。低粘性的水溶性食物纤维是指含有50质量%以上的食物纤维,在常温水中溶解而形成低粘性的溶液、即约5质量%水溶液中示出20mpas以下的粘度的溶液的食物纤维原材料。作为低粘性食物纤维,更具体而言,可以举出难消化性糊精、瓜尔胶水解物、聚右旋糖(例如ライテス等)、半纤维素来源的物质等。
难消化性糊精是将各种淀粉、例如马铃薯淀粉、木薯淀粉、玉米淀粉、小麦粉淀粉等在130℃以上加热分解,将其用淀粉酶进一步水解,按照常规方法,根据需要进行脱色、脱盐而制造的物质。食物纤维的平均分子量为500至3000左右、优选为1400~2500、进一步优选为2000前后。是葡萄糖残基进行α-1,4、α-1,6、β-1,2、β-1,3、β-1,6-葡糖苷键合、还原末端的一部分为左旋葡萄糖(1,6-脱水葡萄糖)的支链结构发达的糊精。以“ニュートリオース”(ロケット公司制)、“パインファイバー”、“ファイバーソル2”(松谷化学工业株式会社制)的商品名市售(”食品新原材料论坛”no.3(1995、食品新原材料协会编))。
瓜尔胶的水解物是将瓜尔胶通过酶水解而得到的物质,因此其性状通常为低粘性且可溶于冷水,水溶液为中性且无色透明。作为瓜尔胶水解物,以“サンファイバー”(太阳化学公司)、“ファイバロン”(大日本制药公司)的商品名市售。
半纤维素来源的物质通常由玉米的外皮用碱提取,精制而制造得到,平均分子量大至约20万,但5%水溶液的粘度低至10cps左右,溶解于水而形成透明液体。半纤维素来源的物质以“セルエース”(日本食品化工公司)的商品名市售。
聚右旋糖(ライテス)是将葡萄糖和山梨糖醇在柠檬酸的存在下液压加热聚合并精制得到的物质,是水溶性且低粘性的。作为“ライテス”(ファイザー公司)而市售。
这些低粘性的水溶性食物纤维之中,难消化性糊精最有效且优选。
<自闭症谱系障碍改善剂>
本发明的1个实施方式是自闭症谱系障碍改善剂,其包含d-阿洛酮糖作为有效成分。
自闭症谱系障碍(asd)是指精神障碍诊断和统计手册第5版(dsm-5)上的各种各样的神经发育症(neurodevelopmentaldisorder)的分类。其特征在于,社会性交流和相互关系中的持续性障碍、以及限定的反复模式的行动、兴趣、活动这两个概念,被定义为轻度至重度的谱系。
本发明的药剂是改善在以前的dsm-iv(diagnosticandstatisticalmanualofmentaldisorders-iv,精神障碍诊断和统计手册iv)中被分类为自闭症、亚斯伯格综合征、无法确定的广泛性发育障碍、儿童期瓦解性障碍等的社会性交流和相互关系中的持续性障碍的药剂。
旷场实验
一直以来,开发了在基因改变小鼠的表型分析中使用的用于评价情绪、记忆学习等高次脑功能的测试,这些测试被用于进行asd的疾病分析、治疗剂的开发。
旷场实验(openfiledtest)是测定在新环境中的移动距离、站立次数、刻板行为、中央区域停留时间等,评价新环境中的自发性活动性、焦虑样行动等的测试。在对于小鼠而言新且明亮的环境、即旷场内,放入小鼠,使其一定时间自由探索。旷场的形状为圆形或正方形,大小在正方形的情况中为一边大于1m至30cm以下的各种各样的大小。一般而言为5分钟左右的实验时间,显著的过量活动、休止状态等能够通过这样的短时间的观察而检测。此外,通过经过长时间进行记录,能够观察在新环境下的动物的行动随时间经过而产生的变化。小鼠被认为用30分钟至2小时左右对旷场的环境驯化,因此大多在30分钟至3小时之间设定实验时间。旷场实验还常用于检查基因改变小鼠的表型分析、对药物的反应性。
社交互动测试
社会性测试(也称为社交互动测试(socialinteractiontest))是为了研究社会性,使用首次遭遇的2个个体的小鼠的旷场实验。作为基本的流程,与1个个体的旷场实验相同。但是,在行动观察开始时点,在场的对角各自放置小鼠,并且拍摄10分钟的动画。通过测量2个个体间的嗅探(sniffing)、梳毛(grooming)、攻击(attack)、摆尾(tail-rattling)等社会性行动频率、时间,期望针对小鼠的社会性进行评价。
由于能够确认针对自闭症中的对人关系和社会性的障碍的效果,因此组合旷场实验和社会性试验的结果在评价药剂的asd的改善作用方面是有效的(silverman,j.l.,yang,m.,lord,c.,andcrawley,j.n.(2010).behaviouralphenotypingassaysformousemodelsofautism.nat.rev.neurosci.11,490-502.)。
使用本发明的药剂进行旷场实验和社会性测试的结果是,给予本发明的药剂的小鼠与给予生理食盐水的对照小鼠相比,焦虑显著減少(图6a~6b),此外社交性显著亢进(图7a~7b),因此暗示了作为asd的改善剂发挥功能。
下丘脑中的神经元的活化
此外,与本发明的药剂的asd改善作用关联地,进行了确认本发明的药剂对催产素神经元和加压素神经元的作用的试验。
作为垂体后叶激素而已知的催产素据报告由下丘脑室旁核(pvn)、视上核(son)神经元合成,其神经末梢透射至垂体后叶而在血中分泌,促进分娩和泌乳。催产素还作为脑内神经传递而发挥功能,催产素神经元中的一部分透射至脑内,发挥中枢神经功能。作为中枢催产素功能,报告了社会性行动改善((1)balesetal.,"long-termexposuretointranasaloxytocininamouseautismmodel",transl.psychiatry2014;4:e480、(2)huanget.al.,"chronicandacuteintranasaloxytocinproducedivergentsocialeffectsinmice."neuropsychopharmacology,2014;39:1102-1114))、抗焦虑、抗压力、学习促进、抗肥胖作用等(meyer-lindenberga.etal.,natrevneurosci.2011,12(9):524-38、blevinsjeandbaskindg,physiolbehav.2015152(ptb):438-49)。
加压素也与催产素同样,是由下丘脑室旁核、视上核合成的垂体后叶激素。加压素也与催产素同样,已知与精神分裂症、自闭症等的精神功能相关(文献:江头伸昭等人,日药理志、2009、134、3-7。meyer-lindenberga.etal.,natrevneurosci.2011,12(9):524-38.)。加压素作为具有与催产素类似的精神功能的理由之一可以认为是,加压素除了作为其受体的加压素受体(v1a、v1b、v2)之外,还容易作用于催产素受体(文献:koshimazut.etal.,physiolrev92:1813-1864,2012)。除此之外,在中枢中表达的加压素受体(v1a、v1b)也报告参与社会性行动、抑郁、焦虑等精神功能(egashiranetal.,jpharmacolsci.2009,109,44-49)。
已知通过经口给予本发明的药剂,经由传入性迷走神经而向脑传递信息,诱导饱腹感,降低摄食量(日本特开2015-164900号)。然而,本发明的药剂的经口给予作用于脑的哪一区域、特别是与下丘脑、催产素、加压素神经元的关联性是完全未知的。因此,着眼于社会性、焦虑、压力、学习、摄食、代谢相关的下丘脑,分析通过本发明的药剂的经口给予而导致的下丘脑活化区域。
通过本发明的药剂的经口给予,在下丘脑的室旁核(pvn)、视上核(son)、和腹内侧核相比更靠腹侧存在的组图谱中,在未鉴定的新的区域(新区域)中发现c-fos的表达亢进(图1a~1d)。
本发明的药剂的经口给予可知在室旁核(pvn)催产素(oxt)神经元中显著增加了c-fos表达量,进行活化(图2a和2b)。图2a中淡灰色部分为催产素阳性细胞,显示为白色的部分是指在催产素阳性细胞的核内存在的c-fos蛋白的表达。
同样地,通过本发明的药剂的经口给予,发现室旁核(pvn)的加压素(avp)神经元被活化(图2c和2d)。
此外,通过本发明的药剂的经口给予,还发现视上核(son)的催产素和加压素神经元被活化(图3a和3b)。
针对通过本发明的药剂的经口给予而活化的下丘脑的新区域,首先发现在该区域中高频率地存在催产素和加压素神经元。并且,通过本发明的药剂的经口给予,发现该新区域的催产素和加压素神经元被活化(图4a和4b)。
下丘脑中的催产素/加压素mrna表达增强
发现如果经口给予本发明的药剂,则催产素和加压素的下丘脑中的mrna的表达与对照(生理食盐水给予组)相比显著增强(图5)。即,通过本发明的药剂的经口给予,下丘脑中的催产素和加压素的基因表达亢进,其可以认为导致催产素和加压素的合成的促进,成为分泌量的增加的一个原因。
如图1~4所示那样,在下丘脑的室旁核(pvn)、视上核(son)、和新的区域(新区域)中,发现催产素和加压素的基因表达的亢进。可以认为有可能通过神经元的初始活化(c-fos表达)而促进催产素和加压素的基因表达和蛋白质合成。
旷场实验、社交互动测试中观察到的本发明的药剂的asd改善作用可以推测为基于本发明的药剂所具有的下丘脑中的催产素和加压素神经元的活化作用、和催产素和加压素mrna的表达增强作用。
根据上文,本发明提供催产素和/或加压素的分泌促进剂。优选为脑内、进一步优选为哺乳动物的脑内、特别是人的脑内的催产素和/或加压素的分泌促进剂。
<精神疾病治疗剂>
本发明的其他实施方式是精神疾病治疗剂,其包含d-阿洛酮糖作为有效成分。
如上所述,本发明的药剂在旷场实验和社会性试验中示出抗焦虑和使社会性亢进的结果,此外,对中枢催产素发挥作用,因此暗示也可以作为催产素活化所关联的其他精神疾病治疗剂。
即,显然针对社会焦虑障碍、境界性人格障碍、精神分裂症、记忆障碍等据信中枢催产素参与的精神疾病,通过本发明的药剂也能够有效地改善。
<抗焦虑剂·抗压力剂、焦虑减轻食品、压力减轻食品>
本发明的进一步的其他实施方式是抗焦虑剂或抗压力剂,其包含d-阿洛酮糖作为有效成分。
本发明的其他实施方式是焦虑减轻食品或压力减轻食品,其包含d-阿洛酮糖作为有效成分。
本发明的实施的方式中,疾病得以改善或减轻的期间没有特别限定,可以是暂时性改善或减轻,也可以是一定期间的改善或减轻。
本发明通过实施例进一步详细说明,但本发明不因实施例而受到任何限定。
实施例
实施例1:d-阿洛酮糖经口给予中的传入性迷走神经和脑的活化区域的分析
对通过d-阿洛酮糖的经口给予而活化的脑区域,用免疫染色法分析神经活化标记物(c-fos)的表达量。c-fos是指立早基因的1种,是伴随神经的活化而表达量上升的核内蛋白质,能够用作神经活化标记物。
作为实验动物,使用c57bl/6j雄性小鼠,在单独的笼内进行1周以上预备饲养和处理,顺应环境。对绝食过夜的小鼠经口胃内给予生理食盐水、或d-阿洛酮糖(1、或3g/kg)后,从给予起90分钟后用4%多聚甲醛溶液进行灌流固定,将脑摘除。脏器用4%多聚甲醛溶液进行后固定,制作冻结切片标本。使用该冻结切片标本,进行c-fos的免疫染色。在催产素/加压素和c-fos的二重免疫染色的情况下,用4%多聚甲醛、0.2%苦味酸混合溶液进行灌流固定和后固定。
所得结果为图1~4所示。
应予说明,c-fos表达量的解析实验(图1a~图1d)中,使用生理食盐水组:n=7、1g/kg和3g/kgd-阿洛酮糖组:各n=5的c57bl/6j雄性小鼠。
室旁核(pvn)催产素(oxt)神经元中的c-fos阳性神经元的解析实验(图2a和图2b)中,使用生理食盐水组:n=4、3g/kgd-阿洛酮糖组:n=6的c57bl/6j雄性小鼠。
室旁核(pvn)的加压素(avp)神经元中的c-fos阳性神经元的解析实验(图2c和图2d)中,使用生理食盐水组:n=4、3g/kgd-阿洛酮糖组:n=6的c57bl/6j雄性小鼠。室旁核(pvn)催产素(oxt)神经元或加压素(avp)神经元中的c-fos阳性神经元的解析实验(图3a和图3b)中,使用生理食盐水组:n=4、3g/kgd-阿洛酮糖组:n=6的c57bl/6j雄性小鼠。
新区域催产素(oxt)神经元或加压素(avp)神经元中的c-fos阳性神经元的解析实验(图4a和图4b)中,使用生理食盐水组:n=4、3g/kgd-阿洛酮糖组:n=6的c57bl/6j雄性小鼠。
所得结果用平均值和标准误差表示,统计学的检验使用非配对t检验,*表述风险率低于5%,**表述风险率低于1%。
(统计学的检验中,通过单因素方差分析解析后,相对于对照组进行dunnett's检验,*表述风险率低于5%,**表述风险率低于1%)。
实施例2:d-阿洛酮糖经口给予后的下丘脑催产素/加压素mrna表达变化量的分析
作为实验动物,使用c57bl/6j雄性小鼠(生理食盐水组:n=8、d-阿洛酮糖组:n=9),在单独的笼内进行1周以上预备饲养和处理,顺应环境。对绝食过夜的小鼠经口胃内给予生理食盐水、或d-阿洛酮糖(3g/kg),从给予起2小时后在麻醉下将脑下丘脑摘除。将下丘脑的总rna作为模板来合成cdna。通过定量实时pcr法,对催产素和加压素的mrna表达量进行定量。作为看家基因,使用36b4。mrna表达量按照δδct法。各样品中的目的基因表达量用36b4的表达量进行校正,求出相对于36b4的表达相对量(δct=36b4的ct值-目的基因的ct值,表达相对量=2δct)。
进一步,求出将生理食盐水组的表达相对量的平均值记作1的mrna表达量比(d-阿洛酮糖组相对于36b4的基因表达相对量的平均值/生理食盐水组相对于36b4的表达相对量的平均值),分析d-阿洛酮糖给予中的基因表达量的变化。
所得结果为图5所示。
所得结果用平均值和标准误差表示,统计学的检验中,使用非配对t检验,**表述风险率低于1%。
实施例3:行动试验
·动物
将c57bl/6j雄性小鼠(8周龄)在自由摄食下、12小时明暗循环的环境中进行一周饲养,供于旷场、社会性试验。进行试验前4天处理和探头的训练。
·旷场试验
试验开始,在30分钟前经口给予d-阿洛酮糖(1g/kg或3g/kg)或生理食盐水。为了评价对新环境的焦虑行动,使小鼠在新饲养笼(27x27x20cm3)内进行探索。测量5分钟的探索时间中的中央区域(9x9cm3)停留时间。以n=10进行的结果如图6b所示,在1g/kg的情况下,没有显著结果,但在3g/kg的情况下,与生理食盐水给予组相比,示出显著改善了焦虑行动(p<0.05(t检验))。
·社会性试验
旷场实验的30分钟后,为了评价对同性小鼠的社会性,将小鼠与首次见面的小鼠(新小鼠)一起放置在饲养笼(27x27x20cm3)中,测量10分钟的探索时间中的对新小鼠的探索行动的累积时间。以n=10进行的结果如图7b所示,在1g/kg和3g/kg的两个试验中,与生理食盐水给予组相比,示出社会性行动显著亢进(p<0.05(t检验))。
旷场试验的结果是,d-阿洛酮糖给予组与生理食盐水给予组相比,探索行动时间显著延长。因此,可以认为d-阿洛酮糖给予具有对新环境焦虑的缓解效果。
社会性试验的结果是,d-阿洛酮糖给予显示对新小鼠的探索行动的累积探索时间的增加。因此,可以认为d-阿洛酮糖对社会性行动的亢进发挥作用。
- 还没有人留言评论。精彩留言会获得点赞!