一种基于叶酸受体主动靶向的金纳米探针及其制备方法
本发明涉及化学合成和生物医学领域,具体涉及一种基于叶酸受体主动靶向的金纳米探针及其制备方法。
背景技术:
当代恶性肿瘤已成为严重威胁人类生命的多发病之一。在我国每年癌症死亡人数占全国15%以上,严重威胁国民健康水平,因此越来越多的新兴交叉学科开始注重癌症的早期诊断治疗以及新型诊疗策略的研发。目前,发展较早且广泛使用的癌症治疗方法是化学药物治疗、放射治疗及手术治疗等,但每种治疗手段都存在各自的优缺点。
针对不同的癌症,如何取各种治疗方法之所长和避之所短,成为广大科研和医务工作者孜孜不倦的追求。现有肿瘤的治疗方法主要问题在于:(1)癌细胞的早期发现不及时且不能有效区分正常细胞和癌变细胞(2)化疗药物或治疗技术对恶性肿瘤的靶向选择性不高,对周围正常肌体组织造成不必要损伤。因此,如何借助媒介实现癌症的早期精准定位以及靶向性治疗已然成为提高肿瘤治疗效果的重中之重。
为了解决癌症病灶的精准早期定位问题,达到肿瘤靶标治疗的目的,目前有研究者开拓出许多新的思路,并将纳米材料这一媒介的优势引入癌症治疗等纳米医学领域。特别地,金纳米材料由于其良好的生物相容性、合成方法简单易操作、易表面修饰、对x射线的衰减性等理化特性历来是纳米医学领域研究的热点之一,例如金纳米材料在早期肿瘤断层扫描(ct)成像、化疗药物或基因传递、光热吸收试剂、放疗增敏剂等领域已得到广泛应用。然而,如何使纳米金靶向、高效地运输到肿瘤病灶而减少在正常组织的分布成为亟待解决的关键问题。为此有研究者开发出一系列方法用于增强纳米材料的胞吞或赋予其靶向传递功能,如在金纳米材料表面修饰阳离子及聚乙烯亚胺等大分子,以增强纳米金与负电性癌细胞膜表面的静电吸附作用。也有报道针对不同癌细胞表面相应受体分子的过量表达,巧妙地采用转铁蛋白、rgd(精氨酸-甘氨酸-天冬氨酸)多肽、叶酸等特异性配体分子修饰纳米金表面,以使得纳米材料长期高效地主动运输至肿瘤病变组织。尽管在靶向修饰方面大量研究已先后报道了一系列不同的特异性分子,然而对配体分子的最优修饰比例,有关公开材料甚少,叶酸及其受体的特异性结合位点空间结构的可能影响也是未知的。
技术实现要素:
本发明通过对比叶酸接枝比率对癌细胞摄取的影响,得出一种最优的探针表面接枝配比,并基于该配比制备了一种基于叶酸受体主动靶向的金纳米探针,该金纳米探针可同时兼顾其在培养基中良好的分散性和较优的肿瘤胞吞效率。
具体而言,本发明提供了一种基于叶酸受体主动靶向的金纳米探针的制备方法,包括以下步骤:
s1:以球状银纳米颗粒为模板,利用抗坏血酸还原氯金酸制备金纳米颗粒;
s2:利用叶酸分子中的羧基和hs-peg5k-nh2中氨基的edc–nhs反应,将fa共价交联在hs-peg5k-nh2尾端,制备巯基聚乙二醇交联的叶酸hs-peg5k-fa;
s3:将hs-peg5k-fa、hs-peg5k-ome溶解后加入步骤s1中新鲜制备的金纳米颗粒水分散液,利用巯基与金原子共价连接形成au-s键的作用,在金纳米颗粒的表面共价偶联不同比例的巯基聚乙二醇甲氧基hs-peg5k-ome和巯基聚乙二醇叶酸hs-peg5k-fa,得叶酸接枝比不同的金纳米探针;
s4:选取特定的肿瘤细胞,将步骤s3制备的金纳米探针进行靶向性验证和摄取率对比试验,以兼顾分散性和胞吞率为条件,筛选出具有最优叶酸接枝比的金纳米探针。
进一步的,所述步骤s1具体包括:取新配制的haucl4溶液加入超纯水稀释,然后,取新制备的胶体银纳米粒子经离心、洗涤、重悬后逐滴加入稀释后的haucl4溶液中,立即混匀,溶液颜色由亮黄色迅速变为浅灰色,紧接着加入抗坏血酸溶液,混合均匀,静置,即得呈淡蓝色、内核中空及表面刺突状的金纳米粒子。
进一步的,所述步骤s2具体包括:将叶酸溶解于二甲基亚砜溶液中,加入1-乙基-3-(3-三甲氨丙基)碳二亚胺和n-羟基琥珀酰亚胺,混合均匀得混合液;将该混合液在室温黑暗条件下活化反应一段时间;将hs-peg5k-nh2粉末加入上述叶酸混合溶液,使氨基与叶酸分子中的羧基反应,室温搅拌过夜,该混合溶液经透析、离心、收集上清液、冻干成粉末状,即得巯基聚乙二醇修饰的叶酸靶向分子hs-peg5k-fa。
进一步的,所述叶酸、1-乙基-3-(3-三甲氨丙基)碳二亚胺和n-羟基琥珀酰亚胺的反应物摩尔比为1:10:20。
进一步的,所述步骤s4中的肿瘤细胞为4t1乳腺癌细胞。
进一步的,所述步骤s4中的最优叶酸接枝比为20%。
本发明还提供了由上述制备方法制备的具有最优叶酸接枝比的金纳米探针。
与现有技术相比,本发明的有益效果:
(1)本发明的刺突状金纳米探针在制备过程中,以30nm的球状银纳米颗粒为模板,利用抗坏血酸还原氯金酸而制得,其平均粒径约为50nm,该合成方法具有成本低、条件温和、操作简便、稳定性强等优点。另外,该探针的粒径范围有利于体内循环中其在肿瘤组织靶向中的epr(增强渗透滞留)效应。
(2)叶酸为早期活跃的肿瘤细胞增殖所需的重要营养成分之一。加之叶酸受体在大多数癌细胞表面的过量表达,而在正常细胞表达低等特性,使叶酸成为识别癌细胞的有效靶向分子。本发明制备的叶酸主动靶向金纳米探针,以叶酸这一小分子作为研究模型,有效利用叶酸-叶酸受体的特异性结合,实现了金纳米材料的靶向传递,增强了材料在肿瘤病灶的摄取效率。
(3)该金纳米探针表面共修饰长链聚乙二醇水溶性大分子,进一步增强了探针在细胞培养基和体内循环中的分散性。
(4)金纳米颗粒以au-s键共价结合表面配体分子,反应条件温和、易操作,同时避免了两种配体空间结构的干扰。金纳米探针表面共价交联的两种功能化基团分别为(a)巯基末端聚乙二醇甲氧基(hs-peg5k-ome)用来维持探针在水溶液和培养基中良好的分散性(b)巯基末端聚乙二醇叶酸(hs-peg5k-fa)赋予探针主动靶向识别和传递功能。
(5)本发明所用表面修饰配体含聚乙二醇的分子量为5k,既确保了该探针在培养基中保持分散性且不易聚沉,又避免分子量过大造成金纳米探针在分散介质中空间结构骤增,以增大其整体平均水动力学粒径,影响胞吞。
(6)探针表面修饰所采用hs-peg5k-fa和hs-peg5k-ome的加料摩尔比为1:99、1:19、1:9和1:4。通过叶酸受体过表达肿瘤细胞的摄取实验,比较得出叶酸偶联分子较优化的摩尔比为1:4;换言之,金纳米探针表面叶酸接枝率为20%时,可同时兼顾其在培养基中良好的分散性和较优的肿瘤胞吞效率。
(7)本发明所提出的叶酸靶向金纳米探针及其制备方法可作为一个探索研究平台,通过制作合成不同的纳米材料载体,并针对不同叶酸受体过表达量的肿瘤细胞,可合理配比表面叶酸靶向分子的接枝数量,为基于叶酸靶向的癌症治疗提供明确地指导方法。
附图说明
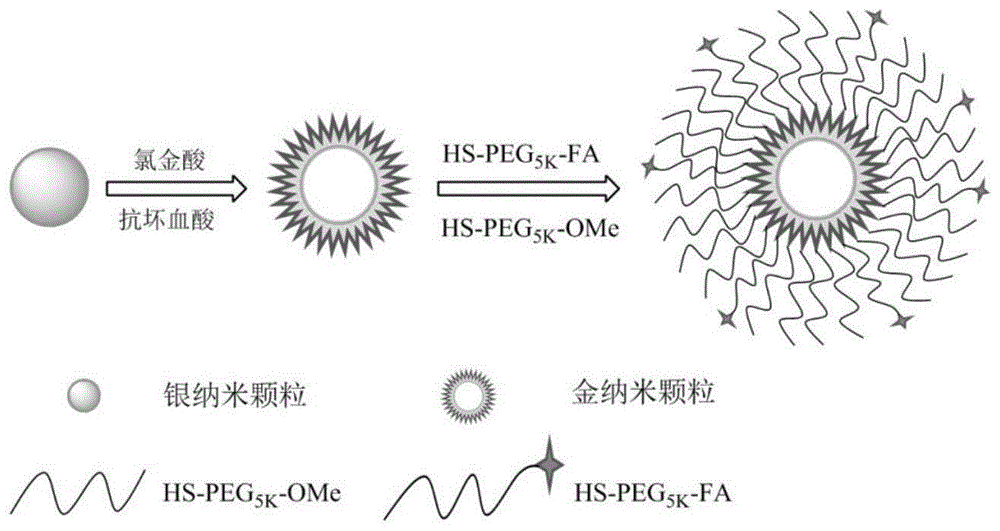
图1为叶酸受体靶向金纳米探针的制备及修饰流程示意图;
图2为合成的金纳米颗粒的透射电子显微镜图片;
图3分别为共聚焦显微镜观察探针表面不同叶酸接枝比:(a)1%、(b)5%、(c)10%、(d)20%、(e)未经叶酸修饰的金纳米材料对4t1乳腺癌细胞摄取率的影响;
图4为叶酸不同接枝比率条件下4t1乳腺癌细胞侧向散射光强度。
具体实施方式:
下面将结合本发明实施例中的附图,对本发明实施例中的技术方法进行清楚、完整地描述,显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例
实施例1
一种基于叶酸受体主动靶向的金纳米探针及其制备方法,所述金纳米探针的制备及修饰流程如图1所示。该探针主体为一种内部中空及表面刺突状的金纳米材料,粒径适中。同时,合成一种巯基聚乙二醇偶联的叶酸配体,搭配一定比率的巯基聚乙二醇,两者与金纳米材料结合形成au-s共价键。通过调节两种配体的比率即得不同叶酸含量的金纳米探针。最后,以叶酸受体过表达的肿瘤细胞为研究模型,评估不同叶酸含量的金纳米探针在肿瘤细胞中的摄取情况,从而得出最优的金纳米材料表面叶酸接枝含量。
该金纳米探针的合成及构建包括以下步骤:
(1)制备金纳米颗粒:取140μl新配制的1%haucl4溶液加入1ml超纯水稀释,然后,取新制备的5ml胶体银纳米粒子经离心(10000rpm,10min)、洗涤、重悬后逐滴加入稀释后的haucl4溶液中,立即混匀,溶液颜色由亮黄色迅速变为浅灰色。紧接着加入1ml10mm抗坏血酸溶液,混合均匀,静置,即得呈淡蓝色、内核中空及表面刺突状的金纳米粒子(aunss),其透射电子显微镜图片如图2所示。镜下观察为单分散的中空刺突状结构,平均粒径为50nm,该粒径范围在10-100nm之内,利于纳米材料在生物体内的长期循环和肿瘤靶向传递。该金纳米颗粒分散液在常温下约可稳定保存一个月以上。
(2)合成巯基聚乙二醇交联的叶酸(hs-peg5k-fa):利用叶酸(fa)分子中的羧基和hs-peg5k-nh2中氨基的edc–nhs反应,将fa共价交联在hs-peg5k-nh2尾端,制备hs-peg5k-fa,具体步骤如下:为活化叶酸分子中的羧基,将4.4mg叶酸溶解于4ml二甲基亚砜溶液中,随后加入1-乙基-3-(3-三甲氨丙基)碳二亚胺(edc)和n-羟基琥珀酰亚胺(nhs),其反应物摩尔比为1:10:20。该混合溶液在室温黑暗条件下,持续搅拌反应1h。将5mghs-peg5k-nh2粉末加入上述叶酸混合溶液,使氨基与叶酸分子中的羧基反应,室温搅拌过夜,该混合溶液经透析、离心、收集上清液、冻干成粉末状,即得巯基聚乙二醇修饰的叶酸靶向分子(hs-peg5k-fa)。
(3)几种叶酸偶联的金纳米探针的构建:将新鲜制备的金纳米颗粒(aunss)水分散液,利用巯基(-sh)与金原子共价连接形成au-s键的作用,在金纳米颗粒的表面共价偶联不同比例的巯基聚乙二醇甲氧基(hs-peg5k-ome)和巯基聚乙二醇叶酸(hs-peg5k-fa),步骤如下:所述反应物hs-peg5k-fa、hs-peg5k-ome分别溶于超纯水制成1mg/ml的储存液。分别取hs-peg5k-fa的储存液0.005ml、0.025ml、0.05ml和0.1ml,相应地取hs-peg5k-ome的储存液0.495ml、0.475ml、0.45ml和0.4ml(对应hs-peg5k-fa和hs-peg5k-ome的摩尔比分别为1:99、1:19、1:9和1:4),加入新制备的aunss(600μg),室温反应过夜。该混合物经离心和水洗后,去除上清液中的未反应物,即得hs-peg5k-fa的接枝比率分别为1%、5%、10%、20%的金纳米探针(fa-peg-aunss)。
(4)为了对所制备金纳米探针的靶向性进行验证,选取未经叶酸偶联的金纳米探针作为阴性对照。具体方法与步骤(3)基本一致,只是步骤(3)几种叶酸偶联的金纳米探针的构建中:只取hs-peg5k-ome的储存液0.5ml,加入新制备的aunss(600μg),震荡反应过夜,得hs-peg5k-ome的接枝率为100%的金纳米颗粒(peg-aunss)作为阴性对照。
实施例2
对实施例1所制备的几种金纳米探针进行靶向性验证和摄取率对比试验。
肿瘤细胞摄取成像实验:将4t1乳腺癌细胞接种于共聚焦专用8孔培养板,37℃培养箱孵育24h后,吸去原有培养基,pbs洗2次,加入含fa-peg-aunss或peg-aunss(50μg/ml)的细胞培养基,孵育24h后,pbs洗2次,加入新培养基,上机进行共聚焦明场和暗场成像观察(暗场成像监测条件:rt15/85分光镜,激发波长488nm,发射波长范围487-490nm)。叶酸接枝比率为1%、5%、10%、20%的fa-peg-aunss及阴性对照(peg-aunss)分别与4t1细胞孵育24h后的共聚焦明场和暗场成像结果如图3(a)、3(b)、3(c)、3(d)及3(e)所示。其中,明场成像中黑色颗粒和暗场成像中的白色亮点分别对应同一视野下胞吞的金纳米探针。可见,4t1乳腺癌细胞经叶酸偶联的金纳米探针孵化后,胞内的白色亮点数量明显多于未经叶酸修饰的金纳米颗粒,充分说明所制备探针对叶酸受体过表达癌细胞的靶向性。由于不同4t1癌细胞表面叶酸受体表达量的差异,内吞金纳米材料的数量呈明显不同。
流式细胞仪定量肿瘤细胞摄取率实验:细胞经胰蛋白酶消化收集于1.5ml尖底离心管中,流式细胞仪上机检测,记录每10000个细胞的平均侧向散射光强度,结果如图4所示。可见,随着叶酸接枝比率的增多,探针的胞吞率呈现先减少后增多的趋势,并非叶酸含量越多越好。由于过多叶酸的接枝比率可导致金纳米探针的分散性变差,因此在兼顾分散性和胞吞率的前提下,筛选得出较优的叶酸接枝比为20%。
- 还没有人留言评论。精彩留言会获得点赞!