一种硝苯地平控释胶囊及其制备方法与流程
本发明涉及药物制剂技术领域,具体地说是一种硝苯地平控释胶囊及其制备方法。
背景技术:
高血压是当今世界最常见的心血管疾病之一,也是心脑血管疾病的主要危险因素。我国现有高血压患者数超过1亿人,且每年以超过300万人的速度增长。硝苯地平作为抗高血压一线药物,具有较好的疗效。
硝苯地平(nifedipine)化学名称:1,4-二氢-2,6-二甲基-4-(2-硝基苯基)-3,5-吡啶二羧酸二甲酯,临床用于预防和治疗冠心病心绞痛,适用于各种类型的高血压。硝苯地平普通制剂需要日服三次,不能很好控制体内血药浓度的稳定和维持血压的平稳;血药浓度的波动可带来头痛、面红、心率增快、眩晕、乏力以及恶心、呕吐等不良反应,拜耳公司采用渗透泵控释技术研制成功硝苯地平控释片,由于采用了独特的激光打孔渗透泵控制释放系统,日服一次,24小时内接近于恒速的释药,血药浓度稳定,降压效果显著,减少了不良反应,每日间的血压维持更加稳定状态。
渗透泵控释片是目前为止最理想的口服控释制剂,其以渗透压为驱动力,使药物达到零级释放。其优点有:延长给药时间,减少给药次数,减少不良反应发生次数和程度;释药受体内条件如ph、胃肠道蠕动及食物等影响小,体内外相关性较好,极大的提高了药物的安全性和有效性。
目前上市的渗透泵片剂按照其结构特点,分为单室渗透泵片剂和双室渗透泵片剂。一般来说,水溶性药物可制成单层渗透泵控释片,难溶性药物制成双层渗透泵控释片。单层渗透泵片由片芯和半透膜组成,药物加入促渗透剂或其他辅料制成片芯,包衣后用激光或机械技术打孔制得。双层渗透泵片一层含有药物及辅料,另一层含有遇水可膨胀的促渗透聚合物。其制备工艺复杂,对片芯辅料、衣膜及生产设备的要求更高。
拜耳公司生产的硝苯地平控释片(商品名:拜新同)为双层渗透泵制剂,制备工艺复杂,首先要压制双层片,再包裹半透膜,然后进行机械或激光打孔,另外,在对包衣片的制孔工艺中,由于存在双层包衣片的双面辩识问题,制孔之前首先要对片面是否为含药层进行识别,对生产设备的性能要求较高。在硝苯地平控释片剂处方中,药物与其他辅料先制备含药层,聚氧乙烯制备成助推层,助推层吸水膨胀后,推动含药层中的混悬液从释药孔中释出。
如果不采用双层片剂结构,将作为助推剂的聚氧乙烯直接与药物混合,吸水膨胀后助推剂和药物一起从孔道内膨胀排出,在片芯的微环境内难以形成较高的渗透压来维持有效的释药速度,则不能保证药物恒速释放。
目前,文献报道采用醋酸纤维素制备微孔胶囊壳。将药物装在胶囊壳之后填充,采用封口液对囊体和囊帽进行封口制备微孔渗透泵胶囊的报道。但这种封口工艺,是在实验室条件下对每个胶囊手工封口,无法实现大工业生产。
中国发明专利cn105920000a(公开号)公开了国药集团广东环球制药发明的“硝苯地平缓释制剂及其制备方法”。其中涉及将硝苯地平与药学上可接受的辅料制备成含药缓释丸芯和含药速释层。从药物溶出曲线来看,供试品在不同条件介质中,5~6h的累积释放量就达到80%以上。缓释时间只能达到6个多小时。
中国发明专利cn102429874a(公开号)公开发明了沈阳药科大学发明的“硝苯地平骨架型缓释微丸及其制备方法和应用”。其中涉及将硝苯地平液态共研磨物与相关辅料制备成骨架缓释微丸。从药物溶出曲线来看,供试品在2h左右释放达到40%,8小时左右达到50%,药物后期释放动力不足,表现出释放不完全的趋势。
总体来说,虽然渗透泵制剂在给药系统设计上取得了较大的成功,但由于制备工艺复杂,涉及到打孔和包衣等问题,尚未得到普遍应用。
技术实现要素:
本发明的目的是提供一种硝苯地平控释胶囊及其制备方法,以解决现有渗透泵制剂制备工艺复杂的问题。
本发明的目的是通过以下技术方案实现的:一种硝苯地平控释胶囊,所述控释胶囊为在胶囊壳中填入硝苯地平、聚氧乙烯和有机酸,并在胶囊壳外进行包衣而制得;其中,所述硝苯地平、聚氧乙烯和有机酸的质量比为:硝苯地平∶聚氧乙烯∶有机酸=1~10∶1~30∶1~10,所述有机酸为酒石酸、富马酸、苹果酸、柠檬酸中的至少一种;所述包衣由纤维素、增塑剂和致孔剂混合制成,各组分重量比为:纤维素∶增塑剂∶致孔剂=10~50∶0~15∶1~25,包衣增重为未包衣含药胶囊的3~20%。
所述控释胶囊为在胶囊壳中填入硝苯地平、聚氧乙烯、有机酸、粘合剂和渗透压调节剂,并在胶囊壳外进行包衣而制得;其中,所述硝苯地平、聚氧乙烯、有机酸、粘合剂和渗透压调节剂的质量比为:硝苯地平∶聚氧乙烯∶有机酸∶粘合剂∶渗透压调节剂=1~10∶1~30∶1~10∶1~25∶0~30,所述有机酸为酒石酸、富马酸、苹果酸、柠檬酸中的至少一种;所述包衣由纤维素、增塑剂和致孔剂混合制成,各组分重量比为:纤维素∶增塑剂∶致孔剂=10~50∶0~15∶1~25,包衣增重为未包衣含药胶囊的3~20%。
所述聚氧乙烯的分子量为100000~300000。聚氧乙烯的粒径为100μm~400μm。
所述聚氧乙烯的分子量为150000~250000。聚氧乙烯的粒径为150μm~350μm。
所述硝苯地平经过预处理,预处理为硝苯地平微粉化、硝苯地平制备固体分散体或者硝苯地平制备环糊精包合物。
所述固体分散体选用聚乙二醇类(聚乙二醇4000、聚乙二醇6000)、聚维酮类(聚维酮k15、k30和k90)、多元醇类(如果糖、蔗糖)中的至少一种作为辅料。
所述纤维素选自醋酸纤维素或乙基纤维素;所述增塑剂选自甘油、丙二醇、聚乙二醇、柠檬酸三乙酯、邻苯二甲酸二乙酯、甘油酸三乙酯、蓖麻油中的至少一种;所述致孔剂选自蔗糖、乳糖、甘露醇、聚乙二醇、羟丙甲纤维素、羟丙基纤维素、泊洛沙姆、聚维酮中的至少一种。
所述粘合剂选自羟丙甲纤维素、羟丙基纤维素、聚维酮中的至少一种;所述渗透压调节剂选自蔗糖、乳糖、葡萄糖、甘露醇、山梨醇、果糖、氯化钠、氯化钾、硫酸钠、磷酸钠、磷酸二氢钠中的至少一种。
一种上述硝苯地平控释胶囊的制备方法,包括以下步骤:
(a)将硝苯地平进行预处理;
(b)将经预处理的硝苯地平与粘合剂、渗透压调节剂、有机酸混合均匀后填入胶囊壳中制备成含药胶囊;
(c)将增塑剂、致孔剂与纤维素溶于有机溶剂中配制成包衣液,对含药胶囊进行包衣,即制得硝苯地平控释胶囊。
所述预处理为硝苯地平微粉化、硝苯地平制备固体分散体或者硝苯地平制备环糊精包合物;所述有机溶剂为丙酮或丙酮与异丙醇的混合物。
实践证明:原研拜新同渗透泵片剂,如果不采用双层压片技术,而采用本发明技术手段直接把聚氧乙烯作为助推剂直接与药物混合,片芯吸水膨胀后聚氧乙烯可以从激光打孔的孔道内膨胀排出,不能有效维持片芯渗透压,从而造成制剂后期释放速度减慢,不能够恒速释放药物。
在本发明中将硝苯地平与聚氧乙烯、有机酸等辅料混合均匀,填充于胶囊中。然后在胶囊外进行包衣。不需要双层压片和激光打孔等繁琐的工艺及昂贵的设备。水分通过半透膜上的致孔剂进入药物层,药物层在水分和促渗剂等辅料的作用下形成混悬液,聚氧乙烯遇水膨胀,产生足够的渗透压。由于微孔的阻滞作用,聚氧乙烯在药物释放过程中不能够从胶囊壳中释放。这样,聚氧乙烯在囊壳中一直存在就能够恒定的维持一定渗透压,使药物能够恒速的释放部分药物混悬液可以通过微孔释放出来,当水分穿透药物层接触膨胀丸芯,推动剩余的药物混悬液释放出来,能够以近似恒定的释药速率释放出活性药物硝苯地平。
本发明的硝苯地平微孔渗透泵胶囊具有控释释放的特点,能够以近似恒定的速率释放活性药物硝苯地平,并且不受介质环境ph值、胃肠蠕动以及食物等因素的影响,具有较好的体内外相关性,可避免普通口服制剂造成的血药浓度波动,减少服药次数,极大提高药物的安全性、有效性和顺应性。
本发明的制剂工艺简单,本发明采用的设备都是制剂常用的技术设备,容易产业化。本发明将聚氧乙烯作为渗透泵助推剂与硝苯地平等辅料混合均匀,填充于胶囊中,然后在胶囊外进行包衣。所选胶囊为市售常见的hpmc胶囊壳,采用常规的胶囊填充机即可完成胶囊的填充,常规的高效包衣锅即可完成胶囊的包衣。避免了使用双层压片机和打孔激光打孔机,即可完成胶囊的制备。
附图说明
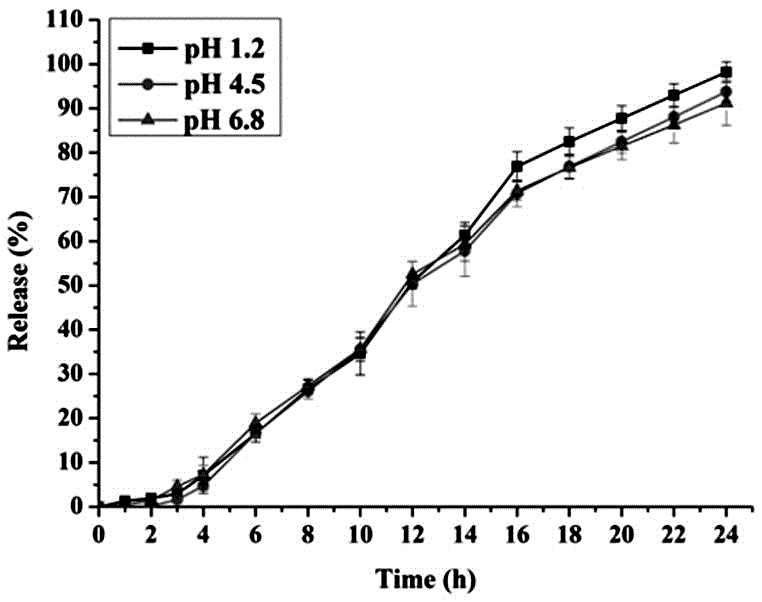
图1为实施例1微孔渗透泵控释胶囊在不同释放介质ph的药物释放曲线图。
图2为对市售制剂拜新同控释片在不同释放介质ph的药物释放曲线图。
图3为拜新同控释片和自制微孔渗透泵胶囊的平均血药浓度-时间曲线。
图4为不加酸制备的微孔渗透泵胶囊在不同释放介质ph的药物释放曲线图。
图5为聚氧乙烯用量对硝苯地平释放的影响图。
具体实施方式
以下实施例是对本发明的进一步描述,而不是对本发明范围的限制。本发明制剂能够以近似恒定的释药速率释放出硝苯地平。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。
实施例1:
处方见表1(1000粒):
表1:
制备工艺:1、胶囊的制备:将聚乙二醇6000在60-80℃加热溶解后,加入硝苯地平混匀,冷却得硝苯地平固体分散体;将黄色固体分散体研磨,过100目筛;将固体分散体粉末、聚氧乙烯、枸橼酸、滑石粉和硬脂酸镁混合,装于硬胶囊壳中;2、包衣操作:称取处方量的醋酸纤维素、泊洛沙姆188溶于丙酮溶液中,溶解完成后,将上述硝苯地平胶囊置于高效包衣锅中,将包衣液喷至硝苯地平胶囊表面,包衣锅设定条件为鼓风量18(m3/h),雾化压力1.6±0.2bar,喷液速度20±1g/min,进风温度45±2℃,物料温度28±2℃,喷液结束后,继续在包衣锅内干燥,得到硝苯地平微孔渗透泵控释胶囊。包衣增重15%。
释放度测定避光操作,取上述实施例1获得的制剂样品,按溶出度与释放度测定法(通则0931第三法),以900ml1%sds溶液为释放介质,温度(37±0.5)℃,转速为50r/min,取硝苯地平样品(n=6),每个溶出杯里放置一粒,分别在1、2、3、4、6、8、10、12、14、16、18、20、22、24h取样5ml,每次取样后即刻同时补充5ml溶出介质。取出的样品经过0.45μm水系微孔滤膜过滤,取续滤液。在238mn的波长处分别测定吸收度,代入标准曲线计算释放量。同时以市售硝苯地平控释片(拜新同,30mg/片)作为对照。改变释放介质的ph,分别测定实施例1样品和对照样品在不同ph介质中的释放曲线,测定结果如图1和图2所示。
由图1和图2可见,与原研制剂相比,硝苯地平微孔渗透泵控释胶囊可以达到近恒速释放药物。在不同ph(1.2、4.5、6.8)的释放介质中的药物释放曲线基本吻合。
实施例2硝苯地平微孔渗透泵控释胶囊药动学研究
将6只家兔随机分成两组,给药前家兔禁食(自由饮水)12h。分别将自制的微孔渗透泵胶囊(实施例1处方)和市售硝苯地平控释片(拜新同,30mg/片)置于家兔口腔深处,使其完整吞咽。给药后分别于0、0.5、1、1.5、2、2.5、3、4、5、6、8、10、12、24和36h耳缘静脉采血0.5ml,并立即移入经肝素处理过的离心管中,4000rpm离心10min。分离血浆,于-20℃冰箱中贮存待用。
精密量取血浆样品200μl,置于5ml离心管中,加入氨水60μl,涡旋振荡2min,加入无水乙醚1.6ml,涡旋10min,4000rpm离心10min。有机相转移至另一离心管中,50℃水浴挥干,残留物用100μl流动相复溶,涡旋混匀2min,6000rpm离心5min。hplc-紫外检测法测定,甲醇-水(70:30)为流动相,20μl进样。
精密称取硝苯地平原料药25.0mg,甲醇溶解并定容至100ml容量瓶中,摇匀得到250μg/ml母液。分别精密量取母液2.0、1.5、1.0和0.5ml至25ml容量瓶,甲醇定容摇匀,得到20、15、10、5μg/ml硝苯地平溶液。精密吸取1ml的20和5μg/ml硝苯地平溶液,并用甲醇稀释定容于10ml容量瓶中,制得2.0和0.5μg/ml硝苯地平溶液,再精密吸取1ml的0.5μg/ml硝苯地平溶液,并用甲醇稀释定容于10ml容量瓶中,制得0.05μg/ml硝苯地平溶液。
精密量取空白血浆200µl于离心管中,分别加入系列标准溶液20µl,配制成浓度分别为5、50、200、500、1000、1500和2000ng/ml的系列血浆样品。按照前述操作并进样分析,记录色谱图和峰面积。以硝苯地平的峰面积为纵坐标,血样浓度为横坐标作图,进行线性回归。求得的直线回归方程为a=91.52c-317.6,r2=0.998。线性范围为5~2000ng/ml。
两种制剂的药-时曲线比较见下图3,市售硝苯地平控释片tmax为8.67h,平均cmax为908.56ng/ml。口服微孔渗透泵胶囊后,家兔平均tmax为9.33h,平均cmax约为842.03ng/ml。由单剂量实验计算自制微孔渗透泵胶囊对相同剂量的市售控释片剂的平均相对生物利用度,由血药浓度-时间曲线下面积auc0~t数据计算,得出平均fx(t)=109.16%。
实施例3处方见表2(1000粒):
表2:
制备工艺:1、胶囊的制备:将聚乙二醇6000在60-80℃加热溶解后,加入硝苯地平混匀,冷却得硝苯地平固体分散体;将黄色固体分散体研磨,过100目筛;将固体分散体粉末、聚氧乙烯、滑石粉和硬脂酸镁混合,装于硬胶囊壳中;2、包衣操作:称取处方量的醋酸纤维素、泊洛沙姆188溶于丙酮溶液中,溶解完成后,将上述硝苯地平胶囊置于高效包衣锅中,将包衣液喷至硝苯地平胶囊表面,包衣锅设定条件为鼓风量18(m3/h),雾化压力1.6±0.2bar,喷液速度20±1g/min,进风温度45±2℃,物料温度28±2℃,喷液结束后,继续在包衣锅内干燥,得到硝苯地平微孔渗透泵控释胶囊。包衣增重15%。
释放度测定避光操作,取上述实施例3获得的制剂样品,按溶出度与释放度测定法(通则0931第三法),选择释放介质分别为ph1.2盐酸溶液、ph4.5乙酸盐缓冲液和ph6.8磷酸盐缓冲液(均照中国药典2015年版配制),加入1%的sds,考察药物在24h内的释放研究,温度(37±0.5)℃,转速为50r/min,取硝苯地平样品(n=6),每个溶出杯里放置一粒,分别在1、2、3、4、6、8、10、12、14、16、18、20、22、24h取样5ml,每次取样后即刻同时补充5ml溶出介质。取出的样品经过0.45μm水系微孔滤膜过滤,取续滤液。在238mn的波长处分别测定吸收度,代入标准曲线计算释放量。测定结果如图4所示。结果表明,不加枸橼酸制剂的释药行为明显与释放介质ph值有关。ph较高时,药物释放存在时滞现象,并且释药不完全。
实施例4处方见表3(1000粒):
表3:
制备工艺:1、胶囊的制备:将聚乙二醇6000在60-80℃加热溶解后,加入硝苯地平混匀,冷却得硝苯地平固体分散体;将黄色固体分散体研磨,过100目筛;将固体分散体粉末、滑石粉和硬脂酸镁混合,加入不同量聚氧乙烯(每个胶囊含有0、10、20、30、60和100mg)制备渗透泵胶囊。2、包衣操作:称取处方量的醋酸纤维素、泊洛沙姆188溶于丙酮溶液中,溶解完成后,将上述硝苯地平胶囊置于高效包衣锅中,将包衣液喷至硝苯地平胶囊表面,包衣锅设定条件为鼓风量18(m3/h),雾化压力1.6±0.2bar,喷液速度20±1g/min,进风温度45±2℃,物料温度28±2℃,喷液结束后,继续在包衣锅内干燥,得到硝苯地平微孔渗透泵控释胶囊。包衣增重15%。
释放度测定避光操作,取上述实施例4获得的制剂样品,按溶出度与释放度测定法(通则0931第三法),选择释放介质分为水,加入1%的sds,考察药物在24h内的释放研究,温度(37±0.5)℃,转速为50r/min,取硝苯地平样品(n=6),每个溶出杯里放置一粒,分别在1、2、3、4、6、8、10、12、14、16、18、20、22、24h取样5ml,每次取样后即刻同时补充5ml溶出介质。取出的样品经过0.45μm水系微孔滤膜过滤,取续滤液。在238mn的波长处分别测定吸收度,代入标准曲线计算释放量。
聚氧乙烯用量对药物释放有一定影响。不加聚氧乙烯时,药物在2h内即可达到10%的释放,之后释放极慢,24h仅释放将近20%。随着聚氧乙烯用量增加至20mg,药物释放总量有所增加,并且前期释放较快,12h可释放70%,但24h仅有82%的释放度。当聚氧乙烯用量增加至30mg,虽然药物释放度最大,但16h释放完全,未达到预期的缓释效果。随着聚氧乙烯用量的继续增加,药物释放速率逐渐减缓,直至聚氧乙烯用量为100mg时,药物释放呈均匀缓慢的趋势。
- 还没有人留言评论。精彩留言会获得点赞!