一种合成M(BH4)n和/或M2/nB12H12的方法与流程
本发明属于无机材料合成工艺领域,具体涉及一种合成m(bh4)n和/或m2/nb12h12的方法。
背景技术:
金属硼氢化物m(bh4)n是一种重要的无机化合物,在化学反应、储氢材料和固态离子电池等领域应用广泛,因此吸引了巨大的研究兴趣。在众多的m(bh4)n化合物中,硼氢化钠nabh4,是应用最广和最重要的,每年有成千上万吨的硼氢化钠被生产和消费,远远超过任何其他硼氢化物的水平。因其储氢密度高(10.7wt%,114.5kg/m3),硼氢化钠也被认为是一种很有前途的储氢材料。在硼氢化钠吸放氢循环中,形成具有稳定b12骨架的na2b12h12反应中间体,影响了其吸放氢性能。于是,na2b12h12开始吸引越来越多的关注并且人们发现它有望成为钠离子导体材料。由于na2b12h12在其有序-无序相变温度以上展示出优异的na+导电性能,许多基于na2b12h12的超离子导电材料被相继的开发出来。此外,na2b12h12作为一种无毒的药物在硼中子俘获治疗方面也有重要的应用。可见,无论nabh4还是na2b12h12都是非常有影响力的无机材料,它们在众多领域内具有广泛的应用。
硼氢化钠的工业生产通常是通过在250~280℃沸腾的油中加热nah和硼酸三甲酯b(och3)3获得,反应式为:b(och3)3+4nah→nabh4+3naoch3。在这一反应中,除了高活性和爆发力的nah,水和甲醇也被引入,经过多级分离和纯化最终得到nabh4产品。硼氢化钠还可以通过金属钠和硼硅玻璃之间的反应制备,反应式为:na2b4o7·7sio2+16na+8h2→4nabh4+7na2sio3。在这种反应中,严格的条件如高反应活性的金属钠、液氨、0.3兆帕的h2压力和高于400℃的温度,加剧了实际操作中的风险和复杂性。
na2b12h12通常是通过溶液方法合成的,有机试剂三乙胺硼烷(et3nbh3)和无机试剂naoh被使用。通过一系列复杂的净化和小心脱水过程,无水na2b12h12最终从其水合物na2b12h12·xh2o中制备得到。因此,探索便捷的无溶剂法制备无水na2b12h12以及其他的金属硼氢化物具有重要的意义。
技术实现要素:
本发明就是针对上述问题,提出了一种简单易行的可同时制备无水m(bh4)n和/或m2/nb12h12的新型无溶剂的合成方法。m(nh2)n用作反应物与b10h14相互作用,通过控制m(nh2)n和b10h14的摩尔比例以及反应条件,可以得到单一成分的m(bh4)n或m2/nb12h12,以及不同比例的m(bh4)n和m2/nb12h12混合物。
为达到上述目的,本发明采用以下技术方案:
一种合成m(bh4)n和/或m2/nb12h12的方法,具体是:m(nh2)n和b10h14反应得到,m选自li、na、k、rb、cs、be、mg、ca、sr、ba、al,n为1、2或3。
进一步地,m为na,n为1。
进一步地,m(nh2)n和b10h14的摩尔比为10:1~1:10。
进一步地,当m(nh2)n和b10h14的摩尔比为10:1~5:1时,产物为m(bh4)n;当m(nh2)n和b10h14的摩尔比为5:1~10:7时,产物为m(bh4)n和m2/nb12h12;当m(nh2)n和b10h14的摩尔比为10:7~1:10时,产物为m2/nb12h12。
进一步地,该方法包括以下步骤:将m(nh2)n和b10h14研磨或球磨均匀,所得混合物进行热处理。
进一步地,所述热处理的温度为100℃以上。
进一步地,所述热处理的时间为1h以上。
进一步地,所述热处理的温度为300℃,时间为10h。
进一步地,将氩气保护的手套箱中,将m(nh2)n和b10h14研磨或球磨均匀,所得混合物置于不锈钢反应坩埚内,密封,然后在马弗炉中加热至200~400℃并保持8~12h,冷却后即得产物。
本发明具有以下有益效果:
本发明可以通过调整原料的比例,制备单一的m(nh2)n或m2/nb12h12,以及m(nh2)n和m2/nb12h12混合物,其理论方程式如下:
5m(nh2)n+b10h14→5m(nh2)n+5bn+2h2
10m(nh2)n+7b10h14→5m2/nb12h12+10bn+29h2
从上述反应式可以看到,本发明还可以合成bn。
本发明开创了通过金属氨基化物与b10h14反应制备硼氢化物的先例,为合成金属硼氢化物材料提供了新的途径,证明等离子体策略是合成金属十二硼烷化合物的有效手段。本发明的反应条件简单、安全性高,不需要经过脱水处理就能得到产物,不需要使用溶剂,保护环境。
附图说明
图1是实施例1的反应产物的xrd和raman图;
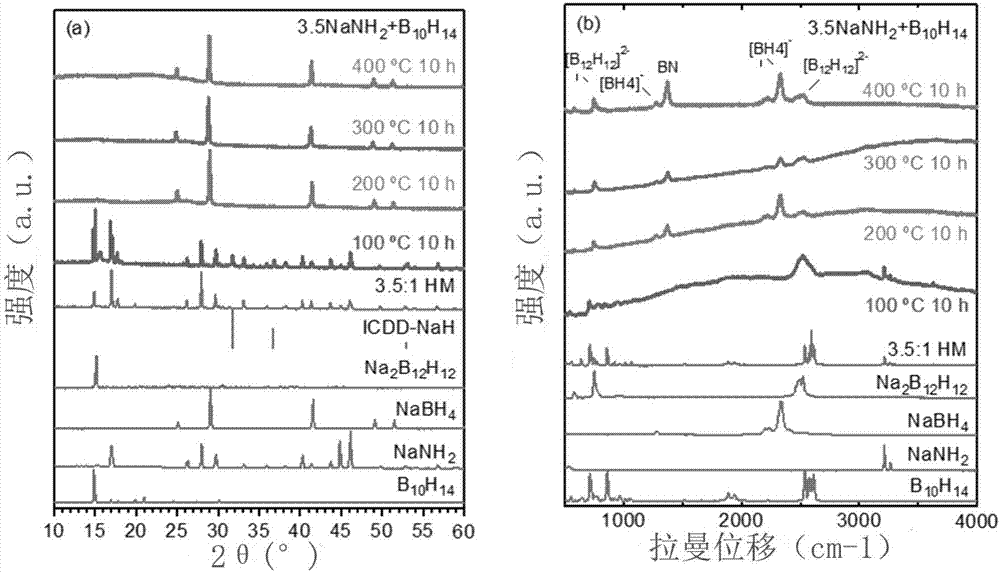
图2是实施例2的反应产物的xrd和raman图;
图3是实施例3的反应产物的xrd和raman图;
图4是实施例4的反应产物的xrd和raman图;
图5是实施例5的反应产物的xrd和raman图;
图6是实施例1和实施例5的反应产物的11bmasnmr图;
图7是实施例6的反应产物的xrd和raman图;
图8是实施例7的反应产物的xrd图;
图9是实施例8的反应产物的11bmasnmr图。
具体实施方式
下面结合具体实施例对本发明做进一步的说明。
实施例1
在纯ar保护的手套箱中,使用商业化的nanh2和b10h14作为初始反应物,nanh2和b10h14按照摩尔比例5:1在研钵中研磨30分钟直到混合均匀。
取混合均匀的样品0.15g左右置于体积0.7cm3的不锈钢反应坩埚内,密封。将密封样品后的不锈钢反应坩埚在马弗炉中加热,条件分别为:300℃保持1小时;300℃保持5小时;300℃保持10小时;400℃保持10小时。待温度降低到室温,取出反应坩埚,在ar保护手套箱中打开,回收样品。
图1是反应产物的xrd和raman图,获得了单一的nabh4。
xrd和raman两种检测手段对nabh4和na2b12h12的灵敏度是不同的,xrd更容易检测出nabh4,raman更容易检测出na2b12h12。
图6是反应产物的11bmasnmr图,na2b12h12含量极少,通过优化实验条件可以进一步提高nabh4的含量。
实施例2
在纯ar保护的手套箱中,使用商业化的nanh2和b10h14作为初始反应物,nanh2和b10h14按照摩尔比例3.5:1在研钵中研磨30分钟直到混合均匀。
取混合均匀的样品0.15g左右置于体积0.7cm3的不锈钢反应坩埚内,密封。将密封样品后的不锈钢反应坩埚在马弗炉中加热,条件分别为:100℃保持10小时;200℃保持10小时;300℃保持10小时;400℃保持10小时。待温度降低到室温,取出反应坩埚,在ar保护手套箱中打开,回收样品。
图2是反应产物的xrd和raman图,nabh4多于na2b12h12,raman图谱中能看到较弱的na2b12h12峰。除了原料比例,反应条件也能显著影响产物,100℃时反应没有发生,随着温度升高,反应比例提升。
实施例3
在纯ar保护的手套箱中,使用商业化的nanh2和b10h14作为初始反应物,nanh2和b10h14按照摩尔比例2:1在研钵中研磨30分钟直到混合均匀。
取混合均匀的样品0.15g左右置于体积0.7cm3的不锈钢反应坩埚内,密封。将密封样品后的不锈钢反应坩埚在马弗炉中加热,条件分别为:100℃保持10小时;200℃保持10小时;300℃保持10小时;400℃保持10小时。待温度降低到室温,取出反应坩埚,在ar保护手套箱中打开,回收样品。
图3是反应产物的xrd和raman图,na2b12h12多于nabh4。除了原料比例,反应条件也能显著影响产物,100℃时反应没有发生,200℃时候有部分发生。
实施例4
在纯ar保护的手套箱中,使用商业化的nanh2和b10h14作为初始反应物,nanh2和b10h14按照摩尔比例10:7在研钵中研磨30分钟直到混合均匀。
取混合均匀的样品0.15g左右置于体积0.7cm3的不锈钢反应坩埚内,密封。将密封样品后的不锈钢反应坩埚在马弗炉中加热,条件分别为:300℃保持10小时;400℃保持10小时;400℃保持20小时。待温度降低到室温,取出反应坩埚,在ar保护手套箱中打开,回收样品。
图4是反应产物的xrd和raman图,产物基本为na2b12h12,只有少量的nabh4。由于xrd更容易检测到nabh4,不容易检测出na2b12h12,在xrd中na2b12h12与nabh4的峰强度差不多,而raman中只显示出na2b12h12峰,因此判断产物基本为na2b12h12,只有少量的nabh4。
实施例5
在纯ar保护的手套箱中,使用商业化的nanh2和b10h14作为初始反应物,nanh2和b10h14按照摩尔比例1:1在研钵中研磨30分钟直到混合均匀。
取混合均匀的样品0.15g左右置于体积0.7cm3的不锈钢反应坩埚内,密封。将密封样品后的不锈钢反应坩埚在马弗炉中加热,条件分别为:100℃保持10小时;200℃保持10小时;300℃保持10小时;400℃保持10小时。待温度降低到室温,取出反应坩埚,在ar保护手套箱中打开,回收样品。
图5是反应产物的xrd和raman图,产物为na2b12h12以及剩余的原料b10h14。
图6是反应产物的11bmasnmr图,生成na2b12h12的反应是分两步完成的,第一步是nanh2与b10h14反应生成nabh4,第二部是生成的nabh4与残留的b10h14继续反应生成na2b12h12。在小的密闭坩埚中要想完全实现第二步的转化是很难的。所以会有少量nabh4残留。
实施例6
在纯ar保护的手套箱中,使用商业化的nanh2和b10h14作为初始反应物,nanh2和b10h14按照摩尔比例1:2在研钵中研磨30分钟直到混合均匀。
取混合均匀的样品0.15g左右置于体积0.7cm3的不锈钢反应坩埚内,密封。将密封样品后的不锈钢反应坩埚在马弗炉中加热到300℃并保持10小时。待温度降低到室温,取出反应坩埚,在ar保护手套箱中打开,回收样品。
图7是反应产物的xrd和raman图,产物为na2b12h12以及剩余的原料b10h14,b10h14在热处理后几乎没有raman信号,但在xrd图中可见b10h14峰。
从实施例1~6可以看到,随着初始反应物nanh2:b10h14的比例由5:1逐渐变为1:2,反应的主要硼氢化物产物由nabh4过渡到nabh4(多)+na2b12h12(少),再到nabh4(少)+na2b12h12(多),直到最后为na2b12h12+b10h14(过量)。
实施例7
在纯ar保护的手套箱中,使用商业化的linh2和b10h14作为初始反应物,linh2和b10h14按照摩尔比例2:1在研钵中研磨30分钟直到混合均匀。
取混合均匀的样品0.15g左右置于体积0.7cm3的不锈钢反应坩埚内,密封。将密封样品后的不锈钢反应坩埚在马弗炉中加热,条件分别为:370℃保持1小时。待温度降低到室温,取出反应坩埚,在ar保护手套箱中打开,回收样品。
图8是反应产物的xrd图,产物为li2b12h12。
实施例8
在纯ar保护的手套箱中,使用商业化的mg(nh2)2和b10h14作为初始反应物,mg(nh2)2和b10h14按照摩尔比例5:7在研钵中研磨30分钟直到混合均匀。
取混合均匀的样品0.15g左右置于体积0.7cm3的不锈钢反应坩埚内,密封。将密封样品后的不锈钢反应坩埚在马弗炉中加热,条件分别为:300℃保持10小时。待温度降低到室温,取出反应坩埚,在ar保护手套箱中打开,回收样品。
由于mgb12h12无定形态特征,通过xrd及raman无法检测,但固态核磁的结果可以很好的证明。如图9所示,将反应产物与合成的na2b12h12进行了比较,可以清楚的看到合成的mgb12h12主峰与na2b12h12主峰都出现在-16ppm附近,均来自于生成的[b12h12]2-的共振信号,产物基本为mgb12h12。
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何属于本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应该以权利要求的保护范围为准。
- 还没有人留言评论。精彩留言会获得点赞!