3,7‑二(叔丁基二甲基硅基氧基)‑6‑烯‑5β‑胆烷‑24‑酸甲酯的制作方法
本发明属于医药技术领域,涉及化合物3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯,制备所述化合物的方法和所述化合物用于制备奥贝胆酸的用途。本发明还涉及一种制备奥贝胆酸的方法,所述方法包括以下步骤:步骤(1):制备3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯;和步骤(2):以3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯为中间体,制备奥贝胆酸。
背景技术:
类法尼醇X受体(FXR)属于配体激活的转录因子核受体的家族成员,其天然配体包括初级胆汁酸鹅脱氧胆酸、次级胆酸石胆酸和脱氧胆酸等。FXR是胆汁传感器,其作用包括与其它核受体协调,参与胆汁酸代谢与胆固醇代谢等重要环节。
奥贝胆酸(Obeticholic acid,OCA),即6α-乙基鹅去氧胆酸(6α-ethylchenodeoxycholic acid,6-ECDCA),别名INT-747或DSP-1747,是一种人工合成的FXR配体。临床研究表明,奥贝胆酸对原发性肝纤维化、酒精性脂肪肝、胆汁酸性腹泻和门静脉高压等多种与肝脏相关的疾病有良好的治疗作用,对这些适应症的治疗正在进行II期和III期的临床研究。美国FDA于2016年5月27日加速批准了奥贝胆酸联合熊去氧胆酸(UDCA)用于患有治疗UDCA应答不充分的原发性胆汁性胆管炎(PBC)的成人患者,或作为单药治疗不能耐受UDCA的成人患者。此外,奥贝胆酸对糖尿病等代谢性疾病也有可期待的治疗作用,目前正在进行临床前研究。
文献报道的奥贝胆酸的合成工艺主要有如下三种:
1.专利US20090062526以及Steroids(Vol77,2012,pp1335)报道了如下所示的奥贝胆酸的合成工艺(文献工艺路线1):
文献工艺路线1
文献工艺路线1的特征如下:
(1)将3α-羟基-7-酮基-5β-胆烷-24-酸(化合物1)的3位羟基用四氢吡喃保护,得到3α-四氢吡喃氧基-7-酮基-5β-胆烷-24-酸(化合物2)。
(2)将化合物2在六甲基硅基磷酰胺(HMPA)中,在二异丙基氨基锂(LDA)和丁基锂存在下,与碘乙烷反应,在6位引入乙基,然后用对甲苯磺酸吡啶盐(PPTS)脱去四氢吡喃基保护,得到3α-羟基-6β-乙基-7-酮基-5β-胆烷-24-酸(化合物3),最后用硼氢化钠将化合物3的酮基还原为羟基,得到目标化合物奥贝胆酸(化合物4)。
2.专利WO2006122977A及其同族专利提供了如下所示的奥贝胆酸的合成工艺(文献工艺路线2):
文献工艺路线2
文献工艺路线2的特征如下:
(1)步骤1:将3α-羟基-7-酮基-5β-胆烷-24-酸(化合物1),转化为3α-羟基-7-酮基-5β-胆烷-24-酸甲酯(化合物5);
(2)步骤2:化合物5在甲苯中,在三乙胺的存在下,与三甲基氯硅烷反应,得到3α-(三甲基硅基氧基)-7-酮基-5β-胆烷-24-酸甲酯(化合物6);
(3)步骤3:化合物6在二异丙基氨基锂(LDA)的存在下,与三甲基氯硅烷反应,得到3α,7-二(三甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯(化合物7);
(4)步骤4:化合物7在二氯甲烷中,在三氟化硼的存在下,与乙醛发生缩合反应,然后水解,得到3α-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸甲酯(化合物8);
(5)步骤5:将化合物8进行水解,得到3α-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸(化合物9);
(6)步骤6:将化合物9进行催化氢化还原,并在碱性条件下异构化,得到3α-羟基-6α-乙基-7-酮基-5β-胆烷-24-酸(化合物3);
(7)步骤7:用硼氢化钠将化合物3的酮基还原,得到奥贝胆酸(化合物4)。
3.专利WO2013192097及其同族专利报道了提供了如下所示的奥贝胆酸的合成工艺(文献工艺路线3):
文献工艺路线3
文献工艺路线3在文献工艺路线2的基础上,将文献工艺路线2的步骤2和步骤3合并,即,在四氢呋喃中,直接将3α-羟基-7-酮基-5β-胆烷-24-酸甲酯在LDA存在的条件下,与三甲基氯硅烷反应,得到3α,7-二(三甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯。
综合分析上述三条文献工艺路线,可以发现,文献工艺路线1虽然路线较短,但这一路线也有明显的缺点,包括(1)终产物纯度不好,需要柱层析分离,不适合工业化生产;(2)第3步的收率很低,只有12-13%,使得总收率只有3.5%;(3)合成中使用的溶剂六甲基磷酰胺(HMPA)具有致癌性。因此,文献工艺路线1不适合大量生产。
文献工艺路线2和文献工艺路线3都将3α,7-二(三甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯作为关键中间体,这两种方法存在以下问题:(1)3α,7-二(三甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯(化合物7)含有两个三甲基硅醚基团,而三甲基硅醚基团性质不稳定,对酸或碱都比较敏感,使得3α,7-二(三甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯在后处理过程中可能会水解为单硅醚产物,影响终产物的收率和纯度;(2)在制备3α,7-二(三甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的过程中,需要使用LDA(四氢呋喃溶液),此试剂价格昂贵,而且必须在无水条件下密封保存,增加了贮存和运输的困难,并且使用时需要在无水条件下操作,不便于使用。
技术实现要素:
在本发明中,如果表示同一化合物时,化合物的命名与化学结构式不符,以化学结构式或化学反应式为准。
在本发明中,除非另有说明,否则本文中使用的科学和技术名词具有本领域技术人员所通常理解的含义。并且,本文中所涉及的实验室操作步骤均为相应领域内广泛使用的常规步骤。同时,为了更好地理解本发明,下面提供相关术语的定义和解释。
如本文中使用的,术语“奥贝胆酸”是指6α-乙基鹅去氧胆酸(即3α,7α-二羟基-6α-乙基-5β-胆烷-24-酸),其具有以下结构:
如本文中使用的,化合物3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯和3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯分别具有如式(1)和式(1’)所示的结构。
如本文中使用的,术语“有机碱”是指呈碱性的有机化合物,例如有机胺、有机胺的碱金属盐、醇的碱金属盐和烷基碱金属化合物。
如本文中使用的,术语“有机胺”是指含有氨基的有机化合物,包括但不限于脂肪胺(例如乙二胺、三乙胺、二异丙基乙胺、二异丙胺)、脂环胺(例如1,8-二氮杂二环十一碳-7-烯(DBU))和芳香胺(例如苯胺、二苯胺)。
如本文中使用的,术语“碱金属”包括锂、钠、钾、铷、铯、钫。
如本文中使用的,术语“室温”是指25±5℃。
本发明所述的“约”应该被本领域技术人员理解,并将随其所用之处的上下文而有一定程度的变化。如果根据术语应用的上下文,对于本领域技术人员而言,其使用不是清楚的,那么“约”的意思是不超过所述特定数值或范围的正负10%。
为了克服现有奥贝胆酸合成工艺中存在的问题,本发明人通过深入的研究和创造性的劳动,提供了以下制备奥贝胆酸的方法,所述方法以3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯为中间体。本发明可以避免现有方法中,由于3α,7-二(三甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的性质不稳定,而对后续操作、产物纯度和收率带来的不利影响。另一方面,本发明还提供了一种制备3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的方法,所述方法避免使用价格昂贵且不便于贮存、运输和操作的LDA(四氢呋喃溶液),降低了生产成本,并且使得操作简单方便。本发明的技术方案如下:
在一个方面,本发明提供了化合物3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯,其具有如式(1)所示的结构。
在一个优选的实施方案中,所述3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯为3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯,其具有如式(1’)所示的结构。
在一个方面,本发明提供了一种制备化合物3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的方法,其包括以下步骤:在有机碱和碘盐存在的条件下,使3-羟基-7-酮基-5β-胆烷-24-酸甲酯与叔丁基二甲基氯硅烷反应,得到3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯。
在一个优选的实施方案中,所述方法包括以下步骤:在有机碱和碘盐存在的条件下,使3α-羟基-7-酮基-5β-胆烷-24-酸甲酯与叔丁基二甲基氯硅烷反应,得到3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯。
在一个优选的实施方案中,所述有机碱为有机胺;更优选地,所述有机胺选自三乙胺、二异丙基乙胺和1,8-二氮杂二环十一碳-7-烯;特别优选地,所述有机胺为三乙胺。
在一个优选的实施方案中,所述碘盐选自碱金属的碘盐和四丁基碘化铵;更优选地,所述碱金属的碘盐选自碘化钠、碘化钾和碘化锂;特别优选地,所述碘盐为碘化钠。
在一个优选的实施方案中,3-羟基-7-酮基-5β-胆烷-24-酸甲酯:叔丁基二甲基氯硅烷:碘盐:有机碱的投料比(mol:mol:mol:mol)为1:3~6:3~6:4~8,例如1:3~5:4~6:4~8、1:3~5:6~8:4~8、1:5~6:4~6:4~6、1:5~6:6~8:4~6、1:3~6:4~6:4~6或1:3~6:3~4:6~8,例如1:3:5:4、1:6:6:4、1:5:6:8、1:5:3:8或1:5:5:6。
在一个优选的实施方案中,所述反应的温度为20℃~60℃,更优选为40℃~60℃。
在一个优选的实施方案中,所述反应在溶剂(例如非质子溶剂)中进行,所述溶剂选自芳香烃(例如甲苯);醚(例如四氢呋喃、二氧六环、甲基四氢呋喃或甲基叔丁基醚)、卤代烷烃(例如二氯甲烷或三氯甲烷)、乙腈、N,N-二甲基甲酰胺和丙酮中的一种或多种。
在一个优选的实施方案中,所述溶剂为由芳香烃与乙腈组成的混合溶剂。
在一个优选的实施方案中,所述芳香烃为甲苯。
在一个优选的实施方案中,所述芳香烃与乙腈的体积比为1:3~3:1,例如1:3~1:2、1:3~1:1、1:1~2:1或1:1~3:1,例如1:3、1:2、1:1、2:1或3:1。
在一个优选的实施方案中,3-羟基-7-酮基-5β-胆烷-24-酸甲酯与溶剂的质量:体积比(g:mL)为1:5~1:15,例如1:5~1:7、1:7~1:12、1:5~1:10或1:10~1:15,例如1:5、1:7、1:10、1:12或1:15。
在一个优选的实施方案中,所述反应进行3~6小时。
在一个优选的实施方案中,所述方法还包括:对3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯进行分离和/或纯化。
在一个优选的实施方案中,所述分离和/或纯化包括以下步骤中的一个或多个:
(1)对反应后的混合物进行萃取,分出有机层;
(2)使用水或者饱和食盐水对有机层进行洗涤;
(3)利用无水硫酸盐(例如无水硫酸钠)对有机层进行干燥;
(4)对干燥后的有机层进行减压蒸馏,分离出3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯;和
(5)利用硅胶柱层析对3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯进行纯化。
在一个方面,本发明提供了化合物3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯用于制备奥贝胆酸的用途。
在一个方面,本发明提供了一种制备奥贝胆酸的方法,所述方法包括以下步骤:
步骤(1):制备3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯;和
步骤(2):以3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯为中间体,制备奥贝胆酸。
在一个优选的实施方案中,通过如上所述任一项的制备3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的方法进行步骤(1)。
在一个优选的实施方案中,所述3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯为3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯。
在一个优选的实施方案中,步骤(2)进一步包括以下步骤:
步骤(2-1):将3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯转化为3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸甲酯;
步骤(2-2):将3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸甲酯转化为3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸;
步骤(2-3):将3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸转化为3-羟基-6α-乙基-7-酮基-5β-胆烷-24-酸;和
步骤(2-4):将3-羟基-6α-乙基-7-酮基-5β-胆烷-24-酸转化为奥贝胆酸。
在一个优选的实施方案中,步骤(2-1)包括:在三氟化硼的存在下,使3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯与乙醛反应,得到3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸甲酯。
在一个优选的实施方案中,所述步骤(2-1)中,3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯:三氟化硼:乙醛的投料比(mol:mol:mol)为1:2~3:1.5~2.5,例如1:2~2.5:1.5~2、1:2.5~3:2~2.5、1:2~3:1.5~2或1:2.5~3:1.5~2.5;例如1:2:1.5、1:2.5:2、1:3:1.5、1:2:2.5、1:3:2.5或1:2.5:2.5
在一个优选的实施方案中,所述步骤(2-1)的反应在溶剂(例如非质子溶剂)中进行,所述溶剂选自芳香烃(例如甲苯);醚(例如四氢呋喃、二氧六环、甲基四氢呋喃或甲基叔丁基醚)、卤代烷烃(例如二氯甲烷或三氯甲烷)、乙腈、N,N-二甲基甲酰胺和丙酮中的一种或多种。
在一个优选的实施方案中,所述溶剂选自二氯甲烷和乙腈。
在一个优选的实施方案中,所述步骤(2-1)中,所述反应的温度为-20℃~-70℃,例如-20℃~-30℃、-30℃~-40℃、-30℃~-50℃、-40℃~-60℃、-60℃~-65℃或-60℃~-70℃;更优选为-60℃~-65℃。
在一个优选的实施方案中,所述步骤(2-1)还包括对反应后的混合物进行后处理。
在一个优选的实施方案中,所述后处理包括以下步骤中的一个或多个:
(1)将反应后的混合物与碱性水溶液混合;
(2)对反应后的混合物进行萃取,分出有机层;
(3)使用水或者饱和食盐水对有机层进行洗涤;
(4)利用无水硫酸盐(例如无水硫酸钠)对有机层进行干燥;
(5)对干燥后的有机层进行浓缩。
在一个优选的实施方案中,所述步骤(2-2)包括:在碱性化合物的存在下,使3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸甲酯水解,得到3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸。
在一个优选的实施方案中,所述步骤(2-2)中的碱性化合物选自氢氧化钠、氢氧化钾、氨、碳酸钠和碳酸氢钠;优选氢氧化钠。
在一个优选的实施方案中,所述步骤(2-2)中,碱性化合物:3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸甲酯的投料比(mol:mol)大于1:1。
在一个优选的实施方案中,所述步骤(2-2)中的反应在室温或加热条件下进行。
在一个优选的实施方案中,所述步骤(2-2)包括:将3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸甲酯用溶剂溶解,并与碱性化合物的水溶液混合;所述溶剂为能够与水混溶的溶剂(例如甲醇、乙醇、丙酮、四氢呋喃、乙腈;优选甲醇)。
在一个优选的实施方案中,所述步骤(2-2)还包括对反应后的混合物进行后处理。
在一个优选的实施方案中,所述后处理包括以下步骤中的一个或多个:
(1)使用酸性化合物(例如磷酸)对过量的碱性化合物进行中和;
(2)对反应后的混合物进行萃取,分出有机层;
(3)使用水或者饱和食盐水对有机层进行洗涤;
(4)利用无水硫酸盐(例如无水硫酸钠)对有机层进行干燥;
(5)对干燥后的有机层进行浓缩。
在一个优选的实施方案中,所述步骤(2-3)包括:在催化剂(例如钯碳)存在的条件下,对3-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸进行氢化还原,并在碱性条件下异构化,得到3-羟基-6α-乙基-7-酮基-5β-胆烷-24-酸。
在一个优选的实施方案中,所述步骤(2-4)包括:对3-羟基-6α-乙基-7-酮基-5β-胆烷-24-酸进行还原反应,得到奥贝胆酸。
在一个方面,本发明提供了奥贝胆酸,其由如上所述任一项的方法得到。
有益效果
本发明的制备3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的方法,避免了使用价格较贵、并且不易储存、运输和使用的LDA,也避免了用LDA进行反应所需要的低温条件(-20℃~-40℃),可以使生产成本得到降低,使反应的操作得到简化。
本发明的制备奥贝胆酸的方法,以3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯为中间体,具有以下效果中的一个或多个:
(1)3,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的性质较稳定,在后处理过程中不容易发生水解;
(2)避免了使用价格较贵、并且不易储存、运输和使用的LDA,也避免了用LDA进行反应所需要的低温条件(-20℃~-40℃),可以使生产成本得到降低,使反应的操作得到简化;
(3)避免了使用致癌性的六甲基磷酰胺(HMPA),降低对操作人员健康的危害,减少环境污染。
具体实施方式
下面将结合附图和实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列附图和实施例仅用于说明本发明,而不应视为限定本发明的范围。附图和实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。所用无水溶剂均为市售。
附图说明
图1为实施例1得到的3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的核磁氢谱。
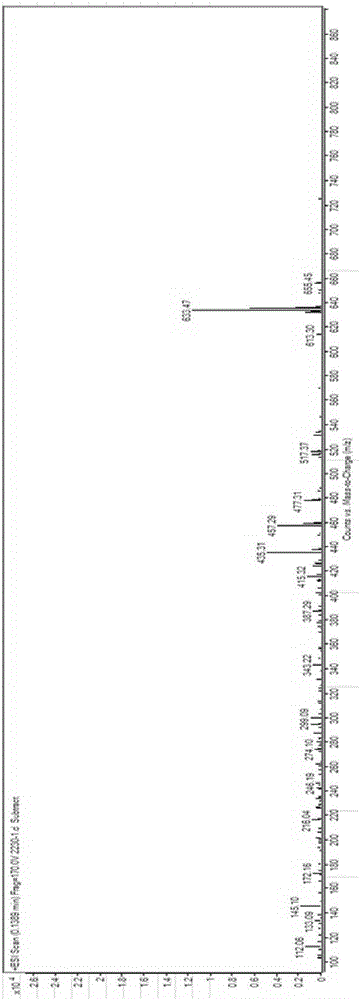
图2为实施例1得到的3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的ESI-MS谱图。
实施例1按照路线1所示的步骤,制备3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯。
路线1
制备过程:将3α-羟基-7-酮基-5β-胆烷-24-酸甲酯(136.5g,337.4mmol)加至反应容器中,所述反应容器上安装了机械搅拌装置以及配有干燥管的冷凝管。用无水乙腈(682mL)和无水甲苯(682ml)将3α-羟基-7-酮基-5β-胆烷-24-酸甲酯溶解,依次加入无水NaI(252g,1.68mol)和三乙胺(281mL,2.012mol),反应容器中的溶液变为悬浊液。分次加入叔丁基二甲基氯硅烷(253.18g,1.68mol),约15分钟加完。将反应体系的温度升至40℃,搅拌1小时,然后升温至50℃反应3-6小时。将反应混合物降温至室温,滤去不溶物,小心加至冰水混合物(1360mL)中,充分搅拌,待分层后,分出甲苯有机层;水层用682mL甲苯洗涤。合并有机层,用纯水洗涤(1540mL×3次),再用饱和盐水洗涤1000mL洗涤1次,用Na2SO4干燥。干燥后的溶液在外温低于50℃的条件下减压蒸馏,蒸发溶剂得到油状物,即为3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯粗品(收率接近100%),可直接用于后续反应。
取少量样品,经硅胶柱层析分离纯化(使用石油醚与乙酸乙酯的混合溶剂(石油醚:乙酸乙酯的体积比为100:5)洗脱,得到3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯纯品,用于表征。
产物的表征:图1为3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的核磁氢谱。核磁数据:1H-NMR(CDCl3,400MHz)δ,0.06(s,3H),0.08(s,3H),0.64(s,3H),0.77(s,3H),0.81(s,9H),0.87(s,9H),0.80-2.51(m,28H),2.19(m,1H),2.30(m,1H),3.47(m,1H),3.61(s,3H),4.66(d,J=4.48Hz,1H)。
图2为3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯的ESI-MS谱图。质谱数据:ESI-MS(m/e,%):633(MH+,100),655(MNa+)。
实施例2按照路线2所示的步骤,由3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯,制备3α-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸。
路线2
步骤1:3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯与乙醛缩合,制备3α-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸甲酯。
(1)将3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯粗品(按照100%收率折算,337.4mmol)油状物,用500mL无水THF溶解,在50℃以下,真空蒸馏除去THF,重复此步骤,直至THF中的水分含量控制在0.5%以内(用KF滴定测得)。剩余液于二氯甲烷(224mL)中溶解,预冷至-60℃~-65℃,加入乙醛(38.1ml,676mmol),在-60℃~0℃条件下保存。
(2)N2保护下,将二氯甲烷(787ml)和三氟化硼(20wt%乙腈溶液,357mL,843.5mmol)于单独反应器中,冷却至-60℃~-65℃。在此温度下,加入(1)中的含有3α,7-二(叔丁基二甲基硅基氧基)-6-烯-5β-胆烷-24-酸甲酯和乙醛的溶液。反应混合物在-60℃~-65℃下搅拌约2小时,逐渐升温至至23℃~28℃,再搅拌约3小时。将反应液冷却至2℃~10℃,加至预冷的NaOH水溶液中,强烈搅拌10min后,分出有机层,水层用二氯甲烷洗涤(150mL×2次)。有机层合并,用200mL水洗涤,再用200mL氯化钠溶液洗涤,浓缩后得到3α-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸甲粗品,直接用于后续反应。
步骤2:用3α-羟基-6-亚乙基-7-酮基-胆烷-24-酸甲酯,制备3α-羟基-6-亚乙基-7-酮基-胆烷-24-酸。
将3α-羟基-6-亚乙基-7-酮基-胆烷-24-酸甲酯(粗品,约337mmol)加至单口瓶中,50℃下,将剩余溶剂真空蒸干,残留液溶于甲醇(200mL)中,冷却至室温,加入含有23.4gNaOH的水溶液60mL,升温至50℃,反应2小时。将反应液用水(580mL)稀释,加入甲苯(194mL),充分搅拌后,分出水层。将水层转移至另一容器中,加入乙酸乙酯(600mL)。强烈搅拌下滴入稀释后的85%磷酸溶液(稀释前的体积为43mL),充分搅拌后分出有机层。水层用乙酸乙酯洗涤(100mL×2次)。合并有机层,用NaCl饱和溶液洗涤,Na2SO4干燥,过滤,浓缩,直至蒸发物中水分含量低于1%,或者达到恒定的沸点,继续浓缩至大部分溶剂蒸出。向剩余物中加入乙酸乙酯(350ml~450mL),加热一段时间后,搅拌下降温至20~25℃,放入冰箱冷藏(0-4℃过夜),抽滤,用冷乙酸乙酯洗涤(50mL×2次),风干后得到产物56g,收率40%。
3α-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸的核磁数据如下,与文献WO2013192097报道一致。1H-NMR(CDCl3,400MHz),δ,0.63(3H,s),0.92(3H,d,J=6.0Hz),0.99(3H,10s),1.04-1.50(13H,m),1.61-2.01(7H,m),1.67(3H,d,J=7.2Hz),2.21-2.28(2H,m),2.35-2.41(2H,m),2.56(1H,dd,J=12.8,4.0Hz),3.58-3.69(1H,m),6.16(lH,q,J=7.2Hz)。
参考WO2013192097的方法,在钯碳存在的条件下,对3α-羟基-6-亚乙基-7-酮基-5β-胆烷-24-酸进行氢化还原,并在碱性条件下异构化,得到3α-羟基-6α-乙基-7-酮基-5β-胆烷-24-酸。对3α-羟基-6α-乙基-7-酮基-5β-胆烷-24-酸进行还原反应,得到奥贝胆酸,收率为80%,纯度为99%。
尽管本发明的具体实施方式已经得到详细的描述,但本领域技术人员将理解:根据已经公开的所有教导,可以对细节进行各种修改和变动,并且这些改变均在本发明的保护范围之内。本发明的全部范围由所附权利要求及其任何等同物给出。
- 还没有人留言评论。精彩留言会获得点赞!