一种大环麝香酮的合成方法与流程
本发明属于化工产品技术领域,具体涉及一种医药、保健品、化妆品添加剂的合成方法,更具体地,涉及一种从蒜头果油中合成大环麝香酮的方法。
背景技术:
:
麝香是一种珍贵的动物性香料,早在东汉时期麝香就被称为香料之王。其扩散性和诱发力极强,具有特殊的柔和而优雅的香气,良好的提香作用和极佳的定香能力,它是调配高档香精中不可或缺的定香剂,广泛应用于香精香料工业、烟草工业、食品工业、日用化学品工业等行业。在香精香料的调配中,只要加入万分之一的麝香,不仅能使香精和加香产品具有优雅的麝香香气,而且还能起到定香、烘托、圆润与平衡整个香气的作用。
麝香不仅在香料工业上有重要的用途,而且在医药上也很重要。在我国药典中,它具有兴奋神经中枢、呼吸中枢和心脏,促进血液循环,促进多种腺体分泌的作用,是治疗神志昏迷的重要药物。现代医学研究表明,麝香对中枢神经、呼吸循环等系统具有开窍解痉,强心等作用,并具有较强抗炎作用。麝香在治疗肝病、癌症和抗肿瘤等方面也有明显的作用。由于麝香的疗效迅速,是目前临床上惟一可用作急救药的中药。
天然麝香来源于鹿科动物林麝、马麝的成熟雄体香囊中的干燥分泌物。最早的麝香酮是从麝的香囊中萃取分离得到,捕杀上万只麝才只能得到一公斤的纯麝香酮。随着物质水平发展,社会对麝香酮的需求逐年增加,对麝的乱捕乱猎,使麝大幅度减少,以致麝香酮的价格更加快速地上升,目前,其价格已远超过黄金。这就促使人们产生了对其进行长期研究和开发的动力,通过人工合成方法制备的合成麝香活性物质接近天然麝香,具有相同或相似理化特性,主要药理基本相同,临床疗效确切,安全可靠,可与天然麝香等同使用。因此,合成麝香是解决麝香供求矛盾的办法之一。合成麝香分为硝基麝香、多环麝香、大环麝香三大类。
硝基麝香是人类研制和使用最早的合成麝香化合物,至今已有一个世纪的历史。硝基麝香具有强烈的麝香香气,香气强度大,但香气不是很细腻、优雅。这类化合物均为固体,易于和其他精油和香料调配,还具有特别好的定香能力,加之它们的价格比其他类型的合成麝香便宜,原料充沛易得,生产稳定,因此使用极为广泛。但硝基麝香被怀疑有致癌性,许多国家已禁止将其用于化妆品及与皮肤接触的产品中。
多环麝香是20世纪50年代初问世的一类合成麝香。与硝基麝香相比,多环麝香的香气比较优雅,化学性质稳定,广泛应用于各类日用化工产品的香精配方中。但是,由于多环麝香合成困难,价格比硝基麝香高,因而多使用在较高档的产品中。硝基麝香因其安全环保问题而被禁用和限用,使多环麝香得到了很大的发展,到80年代后期几乎占据了垄断地位。
由于硝基麝香、多环麝香的毒副作用、生物降解和进入人类食物链而在人体内积累等安全环保问题,这两类麝香将逐渐被淘汰。大环麝香是天然麝香的主要成分,加之性能稳定、无毒,因此,对大环麝香的合成很快成为人们重点研究的对象,具有很大的市场潜力。
大环麝香的香气极为优雅,比那些结构不同于天然麝香结构的合成麝香具有更高级的香气质量。此外,它也是一个很好的定香剂,能使香精保持持久的芬芳气息。大环麝香无任何毒副作用,至今为止也没有发现像硝基麝香和多环麝香所存在的安全环保问题,正是由于大环麝香化合物自身的优势,其发展前景非常乐观。但是,由于大环麝香的生产工艺复杂,收率较低,成本较高,近期还没有形成市场优势,目前它主要应用于香水和高档化妆品等高级日化香精中。
蒜头果又名猴头果、山桐果等,为铁青树科马兰木属唯一的孑遗植物,是中国滇东南与桂西喀斯特地山地特有的珍稀物种,为国家二级保护植物,其分布于云南东南部的广南、富宁和广西西部等500-1640m的石灰岩山区,是喀斯特地区重要绿化造林树种,又是传统的食用油植物,具有巨大的生态服务功能和高经济价值。
蒜头果油含有40%~60%的二十四碳-15-烯酸,是一种长链单不饱和脂肪酸,因其最早是从鲨鱼脑,牛脑中分离出来而得名,二十四碳-15-烯酸是大脑发育、维持的必需营养物,对提高脑神经的活跃、防止脑神经衰弱有很重要的作用;对心血管及人体自身免疫缺乏性疾病也有相当好的疗效;它可直接作为医药和保健品应用。二十四碳-15-烯酸的不饱和键刚好在第15~16碳上,是合成高价值麝香类香料环十五内酯、环十五酮的理想原料。
目前,现有技术中未见有从蒜头果油中合成香料环十五酮的方法的报道。
技术实现要素:
:
本发明的目的在于克服现有技术中存在的大环麝香的生产工艺复杂,收率较低,成本较高,近期还没有形成市场优势的缺限,提供一种用于医药、保健品、化妆品等领域的香料环十五酮的合成方法,该方法基于蒜头果油含有40%~60%的二十四碳-15-烯酸,而二十四碳-15-烯酸的不饱和键刚好在第15~16碳上,是合成高价值麝香类香料环十五内酯、环十五酮的理想原料的机理,提供了从蒜头果油中提取环十五酮的理想的方法。
为了实现本发明的上述目的,本发明提供了如下的技术方案:
一种大环麝香酮即环十五酮的合成方法,以蒜头果油为原料,经皂化、酸化得混合脂肪酸,混合脂肪酸重结晶得二十四碳‐15‐烯酸,将二十四碳-15-烯酸在无水乙醇中,于鼓泡器通臭氧至反应终点,将臭氧化产物移入三口烧瓶,加热搅拌并加入双氧水,滴加1-2小时,加入蒸馏水抽滤,干燥,得到1,15-十五碳二酸;将干燥后的1,15-十五碳二酸溶于二氯甲烷,加入甲醇,逐滴滴加浓硫酸作为催化剂,90℃下分别加热回流4-8小时,以石油醚萃取,蒸干石油醚得到十五碳二酸二甲酯,十五碳二酸二甲酯经环化得α-羟基环十五酮,α-羟基环十五酮经还原得环十五酮。
如所述的合成方法,其中所述的蒜头果油皂化、酸化是将NaOH加入工业酒精中搅拌溶解,溶解完全后加入装有蒜头果油的容器中,于电热套中搅拌皂化4h,反应后,用稀硫酸进行酸化至pH=2,移入分液漏斗中,用热水洗涤数次。
如所述的合成方法,其中所述的混合脂肪酸重结晶是以无水乙醇或丙酮为单一溶剂,进行重结晶,甲酯化后气相检测纯度;或以吡啶与无水乙醇或与丙酮或与石油醚,分别对混合脂肪酸进行交替结晶。
如所述的合成方法,其中所述的十五碳二酸二甲酯经环化得α-羟基环十五酮是在装有机械搅拌器、恒压滴液漏斗、球形冷凝管和氮气保护装置的四口瓶中加入新鲜金属钠和新蒸出的无水二甲苯,N2保护下,开动搅拌并缓慢升温至二甲苯近沸,在氮气下高速搅拌,将钠打成银白色细小微粒,将上述体系降至室温25-30℃,在N2保护下,将十五碳二元酸二甲酯溶于无水二甲苯中,于4h内滴加完毕,110℃反应2h,反应结束,降至室温,在搅拌下,加入适量冰乙酸,停止通氮气,再加入适量水,分出二甲苯,水相用同等数量的二甲苯萃取两次,合并提取液,用水洗涤,干燥,除去溶剂,得羟基环十五酮。
如所述的合成方法,其中所述的α-羟基环十五酮经还原得环十五酮是在装有搅拌器、冷凝管、滴液漏斗和温度计四口瓶中加入α-羟基环十五酮和乙醇,加入锌粉,在90℃搅拌下,滴入浓盐酸,冷却,加水,用苯萃取,减压分馏,除去苯和水,干燥得环十五酮。
与现有技术相比,本发明的优益性在于:
本发明提供了一种从蒜头果油中合成高级香料高价值麝香类香料环十五酮(大环麝香酮)的得率高、效益好、成本低的方法,克服了现有技术中大环麝香生产工艺复杂,收率较低,成本较高,近期还没有形成市场优势的缺限。本发明基于大环麝香是一个很好的定香剂,无任何毒副作用,不存在安全环保问题,而蒜头果油含有40%~60%的二十四碳-15-烯酸,一种大脑发育、维持的必需营养物,对提高脑神经的活跃、防止脑神经衰弱有很重要的作用;对心血管及人体自身免疫缺乏性疾病也有相当好的疗效;它可直接作为医药和保健品应用。二十四碳-15-烯酸的不饱和键刚好在第15~16碳上,是合成高价值麝香类香料环十五内酯、环十五酮的理想原料。
关于蒜头果的专利和文献如下。2004年公开的发明专利“一种从蒜头果油制取环十五内脂的方法”中采用蒜头果油加入反应溶剂再通臭氧,再向臭氧化甘油酯加入还原剂反应生成含有十五碳的羟基甘油酯。但用蒜头果油直接臭氧化的缺点是蒜头果油中除了含有本发明合成环十五酮需要的二十四碳-15-烯酸外还含有二十二碳-13-烯酸和十八碳-9-烯酸等本发明不需要的成分,经过臭氧化,氧化后合成的二甲酯除了十五碳二酸二甲酯可能还含有十三碳二酸二甲酯等副产物,在进行后续反应可能会造成反应效率偏低等问题的出现,故若要以蒜头果油直接臭氧化的路线进行,甲酯化后需要增加十五碳二酸二甲酯的纯化的步骤,增加了操作的难度。故本发明采用蒜头果油经过皂化、酸化后重结晶纯度可达到88%,一次继续后续反应,就可以避免蒜头果油中其它杂质对实验产生影响。
附图说明:
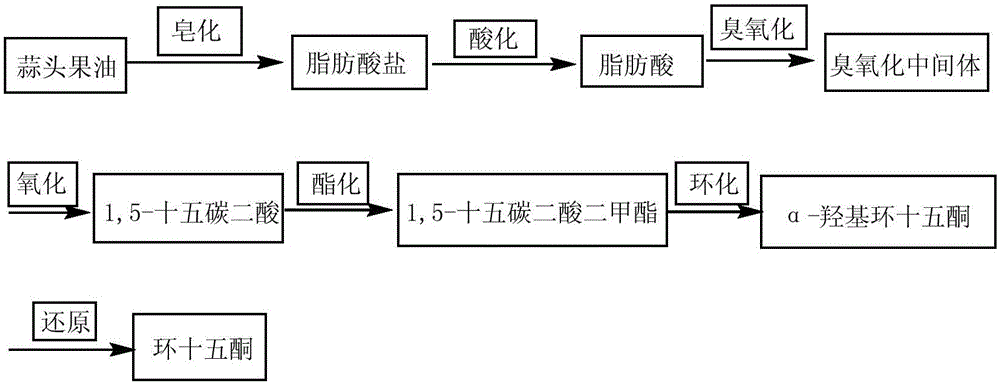
图1为本发明环十五酮(大环麝香酮)的合成路线图。
具体实施方式:
下面结合附图,用本发明的实施例来进一步说明本发明的实质性内容,但并不以此来限定本发明。
实施例1:
1.二十四碳-15-烯酸的制备、纯化。
1.1蒜头果油的提取:
蒜头果仁经研钵研细,用滤纸包裹,放入索氏提取器中,用石油醚作溶剂回流提取6h,提取的蒜头果油蒸干溶剂后贮存备用。
1.2二十四碳-15-烯酸的制备、纯化。
1.2.1蒜头果油皂化、酸化:
将NaOH加入工业酒精中搅拌溶解,溶解完全后加入装有蒜头果油的容器中,于电热套中搅拌皂化4h;反应后,用稀硫酸进行酸化至pH=2,移入分液漏斗中,用热水洗涤数次,得混合脂肪酸备用。
1.2.2二十四碳-15-烯酸重结晶:
以无水乙醇、丙酮、吡啶为单一溶剂,进行重结晶,甲酯化后气相检测纯度。
1.2.3二十四碳-15-烯酸交替结晶:以无水乙醇、丙酮、吡啶、石油醚为溶剂,进行交替结晶,甲酯化后气相检测纯度。
1.3结果
1.3.1混合脂肪酸得率:蒜头果油经皂化、酸化后所得混合脂肪酸数据见表1。由表1的数据可得,混合脂肪酸平均得率为75.235%。
表1混合脂肪酸得率
1.3.2一次结晶对二十四碳-15-烯酸纯度的影响。
实验用无水乙醇、丙酮、吡啶对混合脂肪酸进行一次结晶,实验重复三次,取平均值,结果见表2。由表2的数据可知,一次结晶所选用的溶剂对二十四碳-15-烯酸的纯度影响较小,但是以丙酮为溶剂结晶所得的二十四碳-15-烯酸得率相对两外两个要小,所以在仅重结晶一次的情况下,不宜选择丙酮作溶剂。
表2一次重结晶
1.3.3一次交替结晶对二十四碳-15-烯酸纯度的影响。
采用无水乙醇、丙酮、石油醚、吡啶分别对一次结晶所得的二十四碳-15-烯酸进行结晶,实验重复三次,取平均值,得出结果如表3。由表3的数据可知,一次交替结晶相对于一次结晶在二十四碳-15-烯酸的纯度上有了明显的提升。吡啶与无水乙醇、丙酮、石油醚交替结晶所得二十四碳-15-烯酸的得率、纯度相对较高,纯度均达到了80%以上。
表3一次交替结晶
1.3.4二次交替结晶对二十四碳-15-烯酸纯度的影响。
实验采用丙酮-无水乙醇、吡啶-无水乙醇、吡啶-丙酮、吡啶-石油醚分别对混合脂肪酸进行二次交替结晶,实验重复三次,取平均值,得出结果如表4。由表4数据可知,二次交替结晶所选用的溶剂对二十四碳-15-烯酸得率、纯度影响并不是很明显。与一次交替结晶所得数据对比,二次交替结晶对二十四碳-15-烯酸纯度还是有所提升,但提升并不明显。
表4二次交替结晶
2.环十五内酯(大环麝香内酯)的制备。
2.1合成路线(如图1)。
2.2合成方法:二十四碳-15-烯酸臭氧化法。
2.2.1 15-羟基十五烷酸的制备:
将二十四碳-15-烯酸溶于溶剂中,在冰浴下进行臭氧化反应,然后缓慢滴加KBH4溶液还原,反应结束后,用稀HCl酸化,过滤、洗涤至中性、真空干燥得15-羟基十五烷酸。分别试验不同的溶剂及臭氧化时间对15-羟基十五烷酸得率的影响。
2.2.2 15-羟基十五烷酸甲酯制备:
将15-羟基十五烷酸、甲醇、浓硫酸于圆底烧瓶,在90℃水浴下回流3h,回流结束,用乙醚萃取,洗涤至中性,减压蒸馏,真空干燥得15-羟基十五烷酸甲酯。
2.2.3环十五内酯的合成:
取15-羟基十五烷酸酯,溶于环己烷中,加入催化剂,在一定温度回流反应一定时间。结束后,经过滤,滤液经乙醚萃取,蒸馏水洗涤,减压蒸馏,真空干燥得环十五内酯。分别试验不同催化剂、不同时间、不同反应温度、不同酯基对合成环十五内酯的影响。
2.3结果:
采用二十四碳-15-烯酸臭氧化法。
2.3.1 15-羟基十五烷酸的制备:
2.3.1.1臭氧化所选溶剂对合成15-羟基十五烷酸的影响。
实验采用无水乙醇、石油醚、无水乙醇+石油醚作溶剂进行臭氧化,经还原后得15-羟基十五烷酸,实验重复三次,取平均值,结果见表5,由表5数据可知,选择不同的溶剂进行臭氧化对合成15-羟基十五烷酸影响不大。综合考虑,在臭氧化时选择混合溶剂要更加方便。
表5不同溶剂臭氧化、还原所得15-羟基十五烷酸
2.3.1.2臭氧化时间对合成15-羟基十五烷酸的影响。
实验采用无水乙醇+石油醚作溶剂进行臭氧化,臭氧化时间分别为15min、30min、60min,经还原后得15-羟基十五烷酸,结果见表6.
表6臭氧化时间所得15-羟基十五烷酸
由表6的数据可知,臭氧化时间为30min、60min时15-羟基十五烷酸平均得率均达到了88%以上,但是臭氧化时间提高到60min并没有对15-羟基十五烷酸的得率有所提高。而臭氧化时间为15min的15-羟基十五烷酸平均得率仅达到81%,说明二十四碳-15-烯酸臭氧化并不完全,导致其得率相对较低。所以,综合考虑,臭氧化时间为30min最为合适。
2.3.1.3 15-羟基十五烷酸甲酯制备:
15-羟基十五烷酸在90℃水浴下甲酯化得到15-羟基十五烷酸甲酯,结果见表7。由表7的数据可知,甲酯化过程15-羟基十五烷酸甲酯的平均得率为88.34%。
表7 15-羟基十五烷酸甲酯化
二十四碳-15-烯酸臭氧化法经过六步得到15-羟基十五烷酸甲酯,得率为19.96%,所得15-羟基十五烷酸甲酯纯度较高,达85.11%。
2.4环十五内酯的合成。
2.4.1不同催化剂对环十五内酯合成的影响。
以浓硫酸和固体酸为催化剂催化15-羟基十五烷酸甲酯合成环十五内酯,实验重复三次,取平均值,结果见表8。由表8可知,采用固体酸最催化剂,在最终得到的产物中并不含有环十五内酯。所以在后续的实验均采用浓硫酸作催化剂。
表8不同催化剂合成环十五内酯数据
2.4.2反应时间对环十五内酯合成的影响
以浓硫酸为催化剂,分别反应6h、9h、10h、11h、12h合成环十五内酯,结果见表9。由表9可知,环十五内酯的得率、纯度均随着反应时间的增长而增长。结合现有的实验条件,选定12h为15-羟基十五烷酸甲酯的关环反应时间。
表9不同反应时间所得环十五内酯
2.4.3 15-羟基十五烷酸酯不同酯基对环十五内酯合成的影响
15-羟基十五烷酸甲(乙)酯在完全相同的条件下关环得到环十五内酯,实验重复三次,取平均值,结果见表10.由表10可知,在反应条件完全相同的情况下,15-羟基十五烷酸甲酯合成环十五内酯在得率、纯度上均要比15-羟基十五烷酸乙酯好。
表10不同酯基合成环十五内酯
2.5结论
二十四碳-15-烯酸臭氧化法虽然反应流程较长,是其纯度高,对后面的反应影响很小,而且整个实验过程都较为简单、顺畅。在一定的时间范围内,环十五内酯的得率及纯度随反应时间的增长而增长。在完全相同的实验条件下,15-羟基十五烷酸甲酯合成环十五内酯的得率、纯度要比15-羟基十五烷酸乙酯高。
实施例2:
环十五酮(大环麝香酮)的合成。
实验路线(见图1):二十四碳-15-烯酸臭氧化法。
合成方法:
先制备二十四碳-15-烯酸:
1.二十四碳-15-烯酸的制备、纯化。
1.1蒜头果油的提取:
蒜头果仁经研钵研细,用滤纸包裹,放入索氏提取器中,用石油醚作溶剂回流提取6h,提取的蒜头果油蒸干溶剂后贮存备用。
1.2二十四碳-15-烯酸的制备、纯化。
1.2.1蒜头果油皂化、酸化:
将NaOH加入工业酒精中搅拌溶解,溶解完全后加入装有蒜头果油的容器中,于电热套中搅拌皂化4h;反应后,用稀硫酸进行酸化至pH=2,移入分液漏斗中,用热水洗涤数次,得混合脂肪酸备用。
1.2.2二十四碳-15-烯酸重结晶:
以无水乙醇、丙酮、吡啶为单一溶剂,进行重结晶,甲酯化后气相检测纯度。
1.2.3二十四碳-15-烯酸交替结晶:以无水乙醇、丙酮、吡啶石油醚为溶剂,进行交替结晶,甲酯化后气相检测纯度。
1.3结果
1.3.1混合脂肪酸得率:蒜头果油经皂化、酸化后所得混合脂肪酸数据见表1。由表1的数据可得,混合脂肪酸平均得率为75.235%。
表1混合脂肪酸得率
1.3.2一次结晶对二十四碳-15-烯酸纯度的影响。
实验用无水乙醇、丙酮、吡啶对混合脂肪酸进行一次结晶,实验重复三次,取平均值,结果见表2。由表2的数据可知,一次结晶所选用的溶剂对二十四碳-15-烯酸的纯度影响较小,但是以丙酮为溶剂结晶所得的二十四碳-15-烯酸得率相对两外两个要小,所以在仅重结晶一次的情况下,不宜选择丙酮作溶剂。
表2一次重结晶
1.3.3一次交替结晶对二十四碳-15-烯酸纯度的影响。
采用无水乙醇、丙酮、石油醚、吡啶分别对一次结晶所得的二十四碳-15-烯酸进行结晶,实验重复三次,取平均值,得出结果如表3。由表3的数据可知,一次交替结晶相对于一次结晶在二十四碳-15-烯酸的纯度上有了明显的提升。吡啶与无水乙醇、丙酮、石油醚交替结晶所得二十四碳-15-烯酸的得率、纯度相对较高,纯度均达到了80%以上。
表3一次交替结晶
1.3.4二次交替结晶对二十四碳-15-烯酸纯度的影响。
实验采用丙酮-无水乙醇、吡啶-无水乙醇、吡啶-丙酮、吡啶-石油醚分别对混合脂肪酸进行二次交替结晶,实验重复三次,取平均值,得出结果如表4。由表4数据可知,二次交替结晶所选用的溶剂对二十四碳-15-烯酸得率、纯度影响并不是很明显。与一次交替结晶所得数据对比,二次交替结晶对二十四碳-15-烯酸纯度还是有所提升,但提升并不明显。
表4二次交替结晶
2.1,15-十五碳二酸制备:
将二十四碳-15-烯酸在溶剂中,于鼓泡器通臭氧至反应终点,将臭氧化产物移入三口烧瓶,加热搅拌并加入的双氧水,滴加反应一定时间,加入蒸馏水抽滤,干燥,得到1,15-十五碳二酸。
3.1,15-十五碳二酸二甲酯制备:
将干燥后的1,15-十五碳二酸溶于二氯甲烷,加入甲醇,逐滴滴加浓硫酸作为催化剂,90℃下分别加热回流一定时间,以石油醚萃取,蒸干石油醚得到十五碳二酸二甲酯。
4.α-羟基环十五酮的制备:
在装有机械搅拌器、恒压滴液漏斗、球形冷凝管和氮气保护装置的四口瓶中加入新鲜金属钠和新蒸出的无水二甲苯,N2保护下,开动搅拌并缓慢升温至二甲苯近沸,在氮气氛下高速搅拌,将钠打成银白色细小微粒,将上述体系适当降温,在N2保护下,将十五碳二元酸二甲酯溶于无水二甲苯中,于4h内滴加完毕,保温反应2h,反应结束。降至室温,在搅拌下,加入适量冰乙酸,停止通氮气,再加入适量水,分出二甲苯,水相用同等数量的二甲苯萃取两次,合并提取液,用水洗涤,干燥,除去溶剂,得到羟基环十五酮。
5.环十五酮的合成:
在装有搅拌器、冷凝管、滴液漏斗和温度计四口瓶中加入,加入α-羟基环十五酮和乙醇,加入一定量的锌粉,在90℃搅拌下,滴入适量浓盐酸,滴加完毕,冷却,加水,用苯萃取,减压分馏,除去苯和水,干燥即得到环十五酮。
每一步产品均采用气相色谱检测其纯度。
6.结果。
十五碳二酸制备:
二十四碳-15-烯酸的臭氧化、氧化情况如表11所示,由表11可得,二十四碳-15-烯酸臭氧化,氧化后得到十五碳二酸的平均收率为89.83%.
表1二十四碳-15-烯酸的臭氧化、氧化
十五碳二酸甲酯甲酯化时间对得率的影响:
(1)十五碳二酸甲酯化4h收率情况如表2。由表2可知,甲酯化时间为4h,十五碳二酸二甲酯的平均收率为80.72%。
表2甲酯化时间对得率的影响
(2)十五碳二酸甲酯化6h收率情况如表3.由表3可知,甲酯化时间为6h,十五碳二酸二甲酯的平均收率为86.35%。
表3甲酯化时间对得率的影响
(3)十五碳二酸甲酯化8h收率情况如表4所示。由表4可知,甲酯化时间为8h,十五碳二酸二甲酯的平均收率为87.78%。
表4甲酯化时间对得率的影响
由表2、3、4不同的甲酯化时间可以看出,甲酯化效率随时间的增加而增加,甲酯化时间为8h比甲酯化6h收率没有明显提升,故最佳甲酯化时间为6h左右,气相色谱测定1,15-十五碳二酸二甲酯含量为73.61%。
从通过实验发现脂肪酸臭氧化法即用蒜头果油为原料经过皂化、酸化、重结晶等步骤得到的二十四碳-15-烯酸纯度较高,在进行下面的合成时以较高纯度的二十四碳-15-烯酸为原料,反应被杂质的影响较小,生成的二甲酯杂质较少,蒜头果油经过皂化、酸化后重结晶纯度可达到88%,一次继续后续反应,就可以避免蒜头果油中其它杂质对实验产生影响,便于后续反应的进行。
7.α-羟基环十五酮的制备。
以十五碳二酸二甲酯为原料制取α-羟基环十五酮收率情况见表5.由表5可知,十五碳二酸二甲酯转化为α-羟基环十五酮的收率为83.11%,气相色谱测定含量可达到35.79%。
表5羟基环十五酮的收率
醇酮缩合的温度选择。不同温度下酮醇缩合的情况如表6所示。
表6酮醇缩合的温度
由表6数据可知,随着反应温度的升高,羟基环十五酮的含量也在上升。但当温度超过110℃时,反应体系会变为红棕色,说明有其它副产物生成,故采用的反应温度为110℃。以含量为73.61%的十五碳二酸二甲酯为原料合成羟基环十五酮的含量仅为35.79%,由数据可以看出反应体系中还有一部分反应物的残留或是生成了其它副产物,造成这种结果的原因可能是反应物覆盖在钠沙表面,使钠沙失去了催化反应的活性。
8.环十五酮的合成
α-羟基环十五酮合成环十五酮收率情况如表7所示。由表7可知,羟基环十五酮还原为环十五酮,平均收率为69.51%。
表7环十五酮的收率
结论
通过实验发现,最适合成环十五酮方法为脂肪酸臭氧化法。在甲酯化过程中,随着甲酯化时间增加,收率逐渐升高,但当反应进行到6h以后,随着反应时间的增加,收率的提高不是太明显,故甲酯化时间为2-6h,不超过6小时;通过实验得出在酮醇缩合得到羟基环十五酮的过程中,最佳的反应温度为110℃。
- 还没有人留言评论。精彩留言会获得点赞!