一种电荷可翻转的还原敏感可逆交联纳米胶束的制备方法与流程
本发明涉及生物医用材料技术领域,尤其涉及一种电荷可翻转的还原敏感可逆交联纳米胶束的制备方法。
背景技术:
在过去的几十年里,为了提高化疗药物的治疗效果,纳米胶束、囊泡、微球等聚合物载体得到大力发展。聚合物药物载体通过链段与药物的亲疏水作用物理包封药物或共价结合药物,以改善药物在体内的循环稳定性,提高对治疗部位的靶向性以及有效减少对身体的副作用。然而,目前发展的纳米药物载体仍然面临一些挑战,例如载体与血液成分的相互作用、抗体液稀释稳定性差以及低的细胞摄取率等等。
载药纳米载体在进入人体之后,受到大量体液稀释,稳定性变差。为了提高稳定性,对载体进行亲水壳交联、疏水核交联或核壳界面交联,以降低稀释引起的载体解离。然而,这些传统的交联方式在稳定载体的同时也降低了药物释放的效率。此外,极少数交联结构是具有生物相容性以及生物可降解性的,这大大限制了此类载体在生物医药领域的应用。
血液中的复杂蛋白质成分,容易与携带正电荷的载体或与载体中的活性基团发生反应而使载体聚集,被清除体外。而顺利进入靶向部位的载体因细胞膜排斥减少了细胞对载药载体的摄入,影响药物的生物利用度。近年来,研究人员将酸敏感键断裂引起的电荷转换应用于药物载体,使得载体在体内循环时带负电荷,有效避免与血液中蛋白的相互作用;进入肿瘤组织中时,弱酸环境使载体带上正电荷,可增强载体与癌细胞的相互作用,提高细胞对载体的摄取。此种电荷转换的优点在于同时赋予载体抗蛋白吸附性能和提高细胞摄取能力。
目前,关于具有电荷翻转的可逆核交联的药物载体报道较少,赋予电荷翻转性质以及交联结构所需的反应繁琐,且形成的材料多不能满足生物可降解性,降低了此类材料的应用可行性。
技术实现要素:
为解决上述技术问题,本发明的目的是提供一种生物相容性良好的电荷可翻转的还原敏感可逆交联纳米胶束的制备方法。
本发明提供一种电荷可翻转的还原敏感可逆交联纳米胶束,该聚合物是由三种单体聚乙二醇二缩水甘油醚、赖氨酸和硫辛酰乙二胺通过亲核开环反应合成,合成示意图如图1所示。为了达到合适的亲疏水比例形成胶束,所选聚乙二醇二缩水甘油醚分子量为315g/mol。三种单体的投料摩尔比为1:0.9:0.1~1:0.1:0.9,可调节组分比例控制胶束的形成以及其等电点。本发明中亲核加成反应在50℃下反应三天,高温长时间反应有利于形成分子量大且均一的聚合物,使组装的胶束粒径分散性更低。三种单体单元在纳米胶束中具有各自的功能作用:1)聚乙二醇二缩水甘油醚作为连接两个功能小分子的桥梁,生物相容性好;2)赖氨酸作为人体必需氨基酸之一,分子中的羧基和胺基可在不同pH条件下实现质子化/去质子化,从而控制载体表面所带电荷,同时实现血液抗蛋白吸附以及增强的细胞吸收性能;3)硫辛酸是人体内的抗氧化剂,其五元环中的二硫键可在催化量的DTT作用下与多个相邻的二硫键形成交联结构,而此交联结构在高浓度的还原剂(如GSH)作用下可断裂,这种特殊的可逆交联结构可稳定载体在体内循环,而在细胞内部高浓度GSH作用下即可被破坏,提高药物的靶向释放能力。
本发明还提供一种电荷可翻转的还原敏感可逆交联纳米胶束的制备方法,依次包括以下步骤:
1)硫辛酸和乙二胺在催化剂N,N'-羰基二咪唑作用下反应生成硫辛酰乙二胺;
2)将硫辛酰乙二胺、不同分子量的聚乙二醇二缩水甘油醚和赖氨酸通过亲核加成反应得到三元共聚物粗液;
3)将反应粗液进行透析,干燥,得到纯净的聚合物粉末;
4)将粉末溶解,在持续搅拌下,向三元共聚物溶液中缓慢滴加超纯水;
5)滴水结束后,搅拌一段时间将溶液转入透析袋中,透析处理得到非交联纳米胶束。
6)在氮气气氛下,往非交联胶束溶液中加入催化量DTT溶液,搅拌24小时后透析24小时,得到交联纳米胶束溶液。
具体的,所述步骤1)中,硫辛酸和乙二胺酰胺化反应所选催化剂为N,N'-羰基二咪唑,反应溶剂为氯仿,反应后的产物分别用10%氯化钠、1M氢氧化钠萃取。
具体的,所述步骤2)中,选用分子量为315g/mol的聚乙二醇二缩水甘油醚进行亲核反应,在这个分子量下,可很好地控制聚合物亲疏水比例,从而形成胶束。
具体的,所述步骤2)中,三个反应组分之间的摩尔为1:0.9:0.1~1:0.1:0.9,可根据合适的粒径、等电点选择最佳反应比例。反应溶剂为甲醇与水的混合液,体积比为1:1,在氮气保护下、50℃反应3天。
具体的,所述步骤3)中,采用截留分子量为3500的透析袋进行透析,透析液为甲醇和水的混合溶液(v:v=1:1)。透析的目的在于除去低分子量的聚合物,有利于形成粒径均一的胶束。
具体的,所述步骤4)中,将聚合物溶解于二甲基亚砜中,待充分溶解后,再以30s/滴的速度滴加超纯水。
具体的,所述步骤5)中,滴完水继续搅拌两小时后转入截留分子量为3500的透析袋中,透析不少于24小时,得到纯净的非交联纳米胶束溶液。
具体的,所述步骤6)中,DTT为硫辛酰基的10mol%,过量的DTT会导致二硫键彻底断裂而无法交联。反应在25℃避光条件下进行。
本发明还提供一种电荷可翻转的还原敏感可逆交联纳米胶束,在制备化疗药物载体中的应用。胶束通过疏水作用负载疏水性抗癌药物,同时,疏水链段硫辛酰乙二胺中的二硫键可在催化量的DTT作用下交联,形成更加稳定的载药纳米胶束。由于癌细胞中特殊的生理环境,其细胞质和细胞核中的GSH含量可高达人体血液中的1000倍,这可使原先在血液中稳定包载药物循环的纳米胶束在进入癌细胞后,交联的二硫键被高浓度的GSH还原破坏,使药物在细胞内实现控制释放。
借由上述方案,本发明至少具有以下优点:
1.利用亲核加成合成聚合物,无需添加催化剂,反应温和高效。
2.赖氨酸在亲核加成过程中,侧基上的氨基受羧基影响参加反应的可能性大大降低;留下的氨基和羧基在不同pH条件下质子化/去质子化,可实现在体内循环时优异的抗蛋白吸附性能。
3.在达到肿瘤组织时,胶束表面电荷翻转为正电荷,可通过静电作用提高癌细胞对药物载体的摄取,无需与特定配体结合,增加反应难度。
4.纳米胶束中的二硫键可在催化量的DTT作用下形成内部核交联的稳定结构,在人体内实现稳定循环;而在含高浓度GSH的细胞核和细胞质中快速响应断裂。该纳米胶束可用于负载抗癌药物并实现药物的靶向释放。
5.利用聚乙二醇二缩水甘油醚和人体内源性物质为原料合成的聚合物,具有良好的生物相容性。
上述说明仅是本发明技术方案的概述,为了能够更清楚了解本发明的技术手段,并可依照说明书的内容予以实施,以下以本发明的较佳实施例并配合附图详细说明如后。
附图说明
图1为本发明中形成交联胶束示意图;
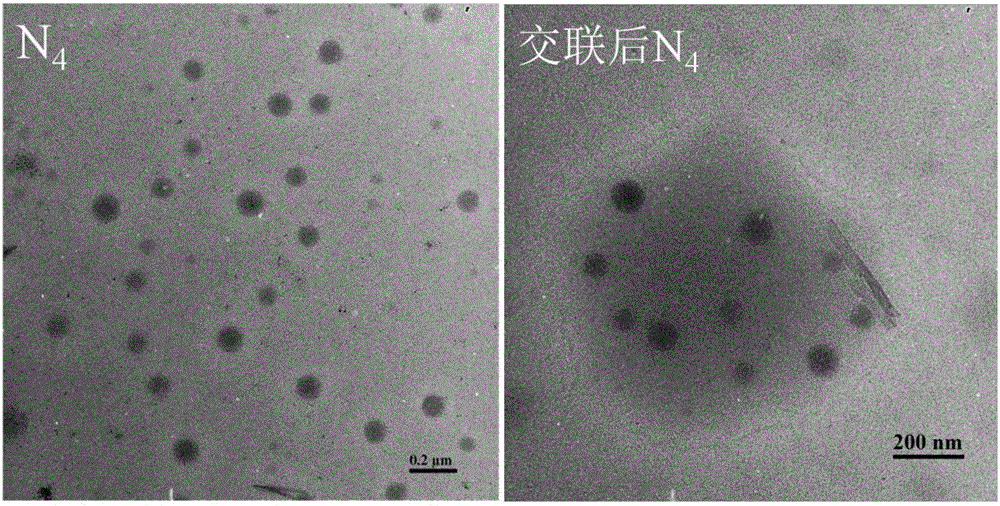
图2为本发明中电荷可翻转的还原敏感可逆交联纳米胶束交联前后的透射电镜图片,
图中,N4代表聚乙二醇二缩水甘油醚、硫辛酰乙二胺与硫辛酸以摩尔比为:1:0.3:0.7时反应所得到的电荷可翻转的还原敏感可逆交联纳米胶束;
图3为本发明中电荷可翻转的还原敏感可逆交联纳米胶束的临界胶束浓度,
图中,N1、N2、N3、N4分别代表聚乙二醇二缩水甘油醚、硫辛酰乙二胺与硫辛酸以摩尔比为:1:1:0,1:0.7:0.3,1:0.5:0.5,1:0.3:0.7时反应所得到的电荷可翻转的还原敏感可逆交联纳米胶束,C为聚合物胶束浓度,单位:mg/mL;
图4为本发明中电荷可翻转的还原敏感可逆交联纳米胶束在不同pH下的zeta电位,
图中,N1、N2、N3、N4分别代表聚乙二醇二缩水甘油醚、硫辛酰乙二胺与硫辛酸以摩尔比为:1:1:0,1:0.7:0.3,1:0.5:0.5,1:0.3:0.7时反应所得到的电荷可翻转的还原敏感可逆交联纳米胶束;
图5为本发明中电荷可翻转的还原敏感可逆交联纳米胶束在蛋白质溶液中孵育24小时的粒径变化,
图中,聚乙二醇二缩水甘油醚、硫辛酰乙二胺与硫辛酸以摩尔比为:1:0.3:0.7时反应所得到的电荷可翻转的还原敏感可逆交联纳米胶束,BSA作为模型蛋白,浓度为45g/L;
图6为本发明中电荷可翻转的还原敏感可逆交联纳米胶束稀释后的粒径变化,
图中,N4代表聚乙二醇二缩水甘油醚、硫辛酰乙二胺与硫辛酸以摩尔比为:1:0.3:0.7时反应所得到的电荷可翻转的还原敏感可逆交联纳米胶束;
图7为本发明中电荷可翻转的还原敏感可逆交联纳米胶束在10mmol/L谷胱甘肽溶液中荧光强度的变化,
图中,聚乙二醇二缩水甘油醚、硫辛酰乙二胺与硫辛酸以摩尔比为:1:0.3:0.7时反应所得到的电荷可翻转的还原敏感可逆交联纳米胶束;
图8为本发明中电荷可翻转的还原敏感可逆交联纳米胶束的细胞毒性结果。
具体实施方式
下面结合附图和实施例,对本发明的具体实施方式作进一步详细描述。以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例1
1)硫辛酰乙二胺的合成:
称取3.00g(1.45×10-2mol)硫辛酸和2.59g(1.60×10-2mol)N,N'-羰基二咪唑,溶于30mL氯仿中,25℃、氮气保护下反应1小时后,将混合液移至滴液漏斗中,逐滴滴入搅拌均匀的乙二胺(8mL,0.12mol)的氯仿(30mL)溶液中,25℃、氮气保护下反应12小时。结束反应后将反应混合液移至分液漏斗中,分别用10%NaCl(100mL)、1M NaOH(100mL)进行萃取,并收集有机相,旋转蒸发除去有机溶剂,得到黄色凝胶状化合物硫辛酰乙二胺(2.2g,61%)。
2)聚(赖氨酸-co-聚乙二醇二缩水甘油醚-co-硫辛酰乙二胺)的合成:
分别称取315mg(1mmol)聚乙二醇二缩水甘油醚、102mg(0.7mmol)赖氨酸、和75mg(0.3mmol)硫辛酰乙二胺溶于3mL甲醇与水的混合溶液中(V:V=1:1),置于25mL单口烧瓶中,50℃、氮气保护下反应72小时。反应结束后,将粗液移入截留分子量为3500的透析袋中,透析3天,冷冻干燥得到黄色产物。聚乙二醇二缩水甘油醚、硫辛酰乙二胺和赖氨酸在混合溶液中相应的溶解比例,如表1所示,本发明仅提供4种三元共聚物合成配方,具体使用过程中根据纳米胶束不同性能的应用需要,调节三种单体的配比。
表1三元共聚物合成配方一览表
3)电荷可翻转的还原敏感可逆交联纳米胶束的制备:
称取10mg聚合物溶于1mL二甲基亚砜,待完全溶解,逐滴滴加8mL超纯水。滴液结束后,继续搅拌2小时,后转入截留分子量3500的透析袋中,透析72小时,得到纯净的非交联纳米胶束溶液。纳米胶束的交联在通N2气氛下,加入催化量的DTT,具体的,DTT(77μg,0.5μmol)溶液加入到10mL非交联N4胶束(1mg/mL)溶液中,于25℃下避光搅拌24小时。通过透析法透析24小时获得纯净的交联的纳米胶束溶液。图2为交联前后的电荷可翻转的还原敏感可逆交联纳米胶束的透射电镜图片,图中N4对应表1中编号N4配方的三元共聚物,胶束在交联前后都是均一规整的球形胶束,交联之后的胶束粒径减小约20nm左右。
实施例2
电荷可翻转的还原敏感可逆交联纳米胶束(CMC)的测量:
将实施例1中所得电荷可翻转的还原敏感可逆交联纳米胶束溶液稀释成一系列不同浓度,取各浓度胶束溶液4mL,分别加入30μL浓度为1.622×10-5g/mL芘的丙酮溶液,避光置于氮气氛围的恒温震荡箱中,30℃孵育24小时。利用荧光分光光度计测定发射光谱,设定荧光激发波长λ=333nm,扫描范围λ=350~500nm,激发和发射狭缝宽度均为5nm,样品池厚1cm。通过测定一系列不同浓度纳米胶束溶液在373nm(I1)和384nm(I3)的荧光强度,以浓度对数为X轴,I1/I3为Y轴作图,由曲线的突变点求出聚合物纳米胶束的CMC值。从图3中可以看出,N1、N2、N3、N4具有较低的CMC值,分别为0.011、0.020、0.030和0.038mg/mL,随赖氨酸含量的增加而增大,均具有良好的抗稀释稳定性。
实施例3
电荷可翻转的还原敏感可逆交联纳米胶束的pH敏感性:
将实施例1中所得电荷可翻转的还原敏感可逆交联纳米胶束用0.1mol/L的氢氧化钠溶液和盐酸溶液调节至不同pH值,利用Zeta电位分析仪测定Zeta电位。结果从图4中可以看出,当载体材料组成成分中未添加赖氨酸时(即为N1),在pH 7.4条件下,纳米胶束几乎不带电;而随着pH的减小,纳米胶束表面正电荷增加。在增加赖氨酸组分之后,羧基可在碱性条件下去质子化,使得纳米胶束带上负电荷;调节三种组分配比,可调节载体的等电点,当聚乙二醇二缩水甘油醚:硫辛酰乙二胺:赖氨酸摩尔比为1:0.3:0.7时(即为N4),其等电点为7.04,即可在pH 7.4条件下使纳米胶束带负电荷,而在pH 6.5条件下,胶束表面转换为正电荷。
由于在聚乙二醇二缩水甘油醚:硫辛酰乙二胺:赖氨酸摩尔比=1:0.3:0.7的情况下,纳米胶束的粒径较为合适且在pH=7.04时实现电荷转化,可赋予纳米胶束抗蛋白吸附特性以及增强的细胞摄取,因此,本发明后续实施例中所提到的纳米胶束,在未特殊说明的情况下,均指该比例下的纳米胶束。
实施例4
电荷可翻转的还原敏感可逆交联纳米胶束的抗蛋白非特异性吸附性能:
将实施例1中所得电荷可翻转的还原敏感可逆交联纳米胶束(N4)置于浓度为45g/L的牛血清白蛋白溶液中,在不同时间用激光光散射仪测试纳米胶束的粒径变化,观察蛋白质吸附影响。结果如图5所示,图中BSA为牛血清白蛋白,在观测的24小时内,纳米胶束N4粒径没有发生较大改变,说明带负电荷的纳米胶束可有效排斥蛋白质的吸附,说明能在人体内进行稳定循环。
实施例5
电荷可翻转的还原敏感可逆交联纳米胶束的抗稀释稳定性:
将实施例1中所得电荷可翻转的还原敏感可逆交联纳米胶束(N4,0.5mg/mL)用超纯水稀释100倍,使其浓度低于CMC值,利用激光光散射仪测试纳米胶束的粒径变化。结果如图6所示,交联后,纳米胶束粒径由原先的187nm减小到162nm,与透射电镜图片所得结果一致;将交联胶束稀释到CMC值以下,发现粒径及其分布没有太大改变,说明交联后的纳米胶束具有很强的抗稀释稳定性,能避免胶束在人体体液大量稀释情况下解离。
实施例6
电荷可翻转的还原敏感可逆交联纳米胶束的还原敏感性:
将实施例1中所得电荷可翻转的还原敏感可逆交联纳米胶束中(N4,4mL,1mg/mL)加入芘的丙酮溶液,使芘浓度为5.0×10-6mol/L,在30℃恒温震荡箱中孵育24小时后,加入GSH溶液,使GSH浓度为10mmol/L,然后在特定的时间间隔里,利用荧光分光光度计测定胶束溶液中芘的激发光谱,发射波长为395nm,激发和发射狭缝宽度均为5nm。结果如图7所示,随着时间的增加,芘的荧光强度逐渐下降,说明芘由疏水环境进入亲水环境。出现这种现象的原因是由于在GSH作用下,胶束内核的二硫键断裂,导致原先的胶束结构被破坏,而释放出包裹在胶束里的芘。
实施例7
电荷可翻转的还原敏感可逆交联纳米胶束的生物相容性:
以实施例1中所得电荷可翻转的还原敏感可逆交联纳米胶束N4为研究对象。采用MTT法测试纳米胶束的细胞毒性,取对数期生长的子宫颈癌细胞(Hela细胞)或小鼠成纤维细胞(L929细胞),经胰蛋白酶(0.25%)消化后,用含10%胎牛血清的DMEM培养基对细胞进行吹打分散,用培养基将细胞稀释成浓度为1.0×104个/mL的细胞悬液,以每孔100μL接种于96孔板,置于恒温培养箱中培养24h后弃去培养基,分别加入100μL含不同聚合物浓度(5、25、50、100、250、500μg/mL)的DMEM完全培养基,每组设六个复孔,培养24小时后弃去培养基,每孔加入20μL、5mg/mL MTT溶液,继续培养4小时后弃去孔板中的溶液,每孔加入150μL二甲基亚砜,震荡溶解活细胞产生的甲臜,用酶标仪在570nm处测定吸光度,并计算细胞存活率。结果如图8所示,L929和Hela两种细胞在不同浓度的纳米胶束溶液中的细胞存活率均在90%以上,说明该纳米胶束具有良好的生物相容性。
以上所述仅是本发明的优选实施方式,并不用于限制本发明,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明技术原理的前提下,还可以做出若干改进和变型,这些改进和变型也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!