一种具有抑制HIV‑1作用的融合基因betaTrCP‑CypA及其构建方法与流程
本发明涉及一种融合基因,具体的说是一种具有抑制hiv-1作用的融合基因betatrcp-cypa及其构建方法。
背景技术:
人类免疫缺陷病毒(humanimmunodeficiencyvirus,hiv)俗称艾滋病(acquiredmedeficiencysyndrome,aids)病毒,诱发人类获得性免疫缺陷综合征。自1984年首次报道艾滋病毒(hiv-1)为引起艾滋病(aids)的病原以来,全世界大批顶尖的科学家都致力于攻克这一疫病。haart等疗法已显著降低了艾滋病的发生率和死亡率。但是,由于只能抑制hiv-1复制,无法清除细胞内感染的病毒,所以需要长期不间断用药,一旦停药即出现病毒反跳现象。长期大量的服用抗病毒药给患者带来了一系列问题,例如有些药物对病人有线粒体毒性、严重胃肠道反应等副作用等。
目前艾滋病防治方面也有针对hiv-1的有关疫苗,由于h1v基因变异问题,使得hiv-1能逃避免疫系统的监视,这是hiv-1疫苗研制的主要障碍。因此,单纯应用疫苗防治艾滋病效果不理想。
目前有关作用于hiv-1辅助受体方面的药物,似乎也逃避了hiv-1的变异问题,但其作用也只是阻止hiv-1进入细胞,不能降解或杀死病毒。
目前针对hiv-1的haart等疗法已显著降低了艾滋病的发生率和死亡率。但是,由于只能抑制hiv-1复制,无法清除细胞内感染的病毒,所以需要长期不间断用药,一旦停药即出现病毒反跳现象。
近年来,随着人们对泛素一蛋白酶体途径(ubiq-uitin-proteasomepathway,upp)认识的不断深人,人们利用upp具有特异性降解蛋白底物的功能特点,提出了靶向泛素化降解蛋白质技术,也称为蛋白质敲减技术,其核心就是构建某个能够与靶蛋白特异结合的e3,该e3含有两个结构域,即功能结构域和结合结构域。靶向泛素化降解蛋白质技术与基因沉默等技术的比较具有优势,如在敲减对象方面,靶向泛素化降解蛋白质技术能有效针对某一类修饰后的目的蛋白进行敲减,在作用时效方面,在灵活性方面,在应用规模方面更有优势。
技术实现要素:
本发明目的是为解决上述技术问题的不足,提供一种基于设计的具有抑制hiv-1作用的融合基因betatrcp-cypa及其构建方法,构建的融合基因betatrcp-cypa能够降解hiv-1gag,能抑制hiv-1病毒。
一种具有抑制hiv-1作用的融合基因betatrcp-cypa,能抑制hiv-1病毒,其基因序列如seqidno:1所示。
所述基于泛素连接酶抑制hiv-1的融合基因betatrcp-cypa的构建方法,包括以下步骤:
步骤一、根据genbank中登陆号为nm_003939记载的人betatrcp基因n端序列,利用dnastar等对betatrcp基因n端序列进行优化得到优化后的人betatrcp基因n端序列,然后进行人工合成得到优化后的betatrcp基因n端dna;优化后betatrcp基因n端dna的碱基序列如序列表seqidno:2所示;
步骤二、设计引物,引物序列如下:
b1:5'ggaattcgccaccatggacccagcagaagcagtg3';
b2:5'actgtgtcttccgcatctccag3';
b3:5'ctggagatgcggaagacacagtggctcaggatcaggctcagga
tcaggctcaatggtcaaccccaccgtgttct3';(下划线部分是含5个丝甘氨酸结构的dna)
b4:5'cgggatccttcgagttgtccacagtcagca3';
c1:5'ggaattcgccaccatggtcaaccccaccgtgttc3';
步骤三、以betatrcp基因n端dna序列为模板,以b1和b2为引物扩增betatrcp基因n端部分,得到betatrcp基因n端dna片段;以cypacdna(seqidno:3)质粒为模版,以b3和b4为引物扩增cypa部分,得到cypacdna片段;分别取1µlbetatrcp基因n端部分片段pcr产物和1µlcypadna片段pcr产物作为模板,以b1和b4为引物pcr扩增融合基因betatrcp-cypa,扩增出目的条带,大小1300bp。分别用ecori/bamhi双酶切融合基因betatrcp-cypa和pcdna3.1his载体,将酶切后的融合基因betatrcp-cypa克隆入pcdna3.1his载体。
步骤三中所述以b1和b2为引物扩增betatrcp基因n端序列,98℃预变性15s,再98℃10s,58℃15s,再72℃60s,28个循环,以cypacdna质粒为模版,以b3和b4为引物扩增cypa部分,其扩增条件均:98℃预变性15s,再98℃10s,58℃15s,再72℃30s,28个循环。
步骤三中所述以b1和b4为引物pcr扩增融合基因betatrcp-cypa,其扩增条件均:98°c预变性15s,再98°c10s,58°c15s,再72°c90s,30个循环。
有益效果是:
目前针对hiv-1的haart等疗法已显著降低了艾滋病的发生率和死亡率。但是,由于只能抑制hiv-1复制,无法清除细胞内感染的病毒,所以需要长期不间断用药,一旦停药即出现病毒反跳现象;本发明解决了该技术难题,构建的融合基因betatrcp-cypa能够降解hiv-1gag,从而抑制hiv-1病毒的组装,或降解hiv-1中的gag,从而达到抑制hiv-1的作用。
附图说明
图1pcdna3.1mychis(-)(简称pcdna3.1his)载体示意图;
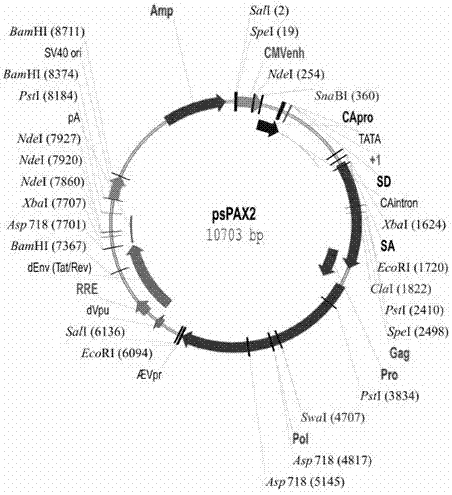
图2含hiv-1gag基因的pspax2载体;
图3betatrcp-cypa融合基因构建betatrcp-n端和c端cypa的pcr扩增图;其中,m:dl2000marker,1、表示betatrcp-cypa融合基因c端cypa基因的扩增,2表示betatrcp-n端基因的扩增图;
图4betatrcp-cypa基因pcr扩增,1:betatrcp-cypa基因的pcr扩增产物图;m:dl2000dna分子量标准;
图5pcdna3.1his/cypa基因构建cypa的pcr扩增,m:dl2000marker,1.cypa基因的扩增;
图6pcdna3.1his/betatrcp-cypa和pcdna3.1his/cypa的表达的westernblotting鉴定图,nc:空载体组,1:pcdna3.1his/betatrcp-cypa,2:pcdna3.1his/cypa;
图7westernblot分析betatrcp-cypa对hiv-1gag的降解分析,1.betatrcp-cypa组转染pcdna3.1his/betatrcp-cypa质粒2μg,pspax20.4μg,2.cypa对照组转染pcdna3.1his/cypa2μg,pspax2质粒0.4μg,3.对照组转染pcdna3.1his2μg,pspax2质粒0.4μg;
图8elisa法研究betatrcp-cypa对hiv-1的抑制率图;
图9荧光素酶活性法研究betatrcp-cypa抑制hiv-1的作用图,pcdna3.1his:对照组pcdna3.1/his组cypa:pcdna3.1his/cypa组,betatrcp-cypa组d:293t细胞对照组。
具体实施方式
所述具有抑制hiv-1作用的融合基因betatrcp-cypa的构建方法,包括以下步骤:
(1)betatrcp-cypa的抑制hiv-1的融合基因构建:利用dnastar等对betatrcp基因n端序列进行优化。优化后委托上海生工生物工程公司合成,优化后用premier5.0软件设计引物,扩增betatrcpn端部分,以cypacdna质粒为模版,扩增cypa部分,纯化后各取1µl作为模板,以外侧引物pcr扩增betatrcp-cypa融合基因,双酶切后克隆入pcdna3.1his载体。送上海生工测序加以确认。
(2)westernblot检测betatrcp-cypa、cypa重组蛋白的表达培养293t细胞,用entranstertm-d4000转染试剂将pcdna3.1his/betatrcp–cypa或pcdna3.1his/cypa2µg(entranstertm-d4000和质粒比例为3∶1)分别转入每孔,pcdna3.1his空载体转染293t细胞做对照。48h后收集细胞后用westernblot检测。
(3)betatrcp-cypa对hiv-1gag的降解分析转染前一天将293t细胞接种到六孔板中,以质粒pspax2与pcdna3.1his/betatrcp-cypa和质粒pcdna3.1his共转染。实验分3组:
(4)elisa法研究betatrcp-cypa抑制hiv-1的研究
培养293t细胞,以每孔4×l03个细胞接种于96孔板,实验分4组:(1)betatrcp-cypa组pcdna3.1his/betatrcp-cypa0.15µg,hiv-1骨架质粒pnl43luc-r-e-0.05µg;(2)cypa组pcdna3.1his/cypa0.15µg,hiv-1骨架质粒pnl43lucr-e-0.05µg;(3)对照组pcdna3.1/his0.15µg,hiv-1骨架质粒pnl43luc-r-e-0.05µg,(4)293t细胞对照组。第二天将entranstertm-d-4000和质粒以3∶1比例分别转入每孔,6h后换液,继续培养24-48h。48h后,检测上清中的p24浓度。留下细胞待裂解后进行荧光素酶活性检测。
(5)上述(4)中的细胞加入100µl报告基因细胞裂解液裂解细胞(用碧云天的萤火虫萤光素酶报告基因检测试剂盒)。加入100微升萤光素酶检测试剂,用枪打匀或用其它适当方式混匀后测定rlu(relativelightunit)。以报告基因细胞裂解液为空白对照,测定荧光值,荧光值越高hiv-1复制水平越高,通过与未感染hiv-1细胞的荧光值相比,该比值可以反应hiv-1复制水平。
相关实验例
实验例1
pcdna3.1his/betatrcp-cypa构建根据人betatrcp基因n端序列(genbank登陆号:nm_003939),利用dnastar等对betatrcp基因n端序列进行优化。优化后委托上海生工生物工程公司合成,用premier5.0软件设计引物,以b1和b2为引物扩增betatrcpn端部分,加primestarhsdnapolymerase酶等至50µl体系。扩增条件为:98℃预变性15s,再98°c10s,58°c15s,再72°c60s,28个循环,以cypacdna质粒为模版,以b3和b4为引物扩增cypa部分,加primestarhsdnapolymerase酶等至50µl体系。扩增条件为:98°c预变性15s,再98°c10s,58℃15s,再72℃,30s,28个循环,结果分别扩增出目的条带,大小分别约800bp、500bp,如图3,各取1µl作为模板,以b1'和b4为引物pcr扩增betatrcp-cypa融合基因,98°c预变性15s,再98°c10s,58℃15s,再72℃90s,30个循环,扩增出目的条带,大小约1300bp,如图4分别用ecorii/bamhi双酶切pcr产物和pcdna3.1his载体克隆入pcdna3.1his载体。送上海生工测序加以确认。
pcdna3.1his/cypa构建以puc/cypa为模版,以c1和b4为引物扩增cypa基因,加primestarhsdnapolymerase酶等至50µl体系。扩增条件为:98°c预变性15s,再98°c10s,58°c15s,再72°c30s,30个循环,结果如图5所示,分别用ecori/bamhi双酶切pcr产物和pcdna3.1his载体克隆入pcdna3.1his载体。送上海生工测序加以确认。
实验例2
westernblot检测betatrcp-cypa、cypa重组蛋白的表达
培养293t细胞,转染前一天将293t细胞以1×106个/孔的密度铺于6孔板培养。第2天,用entranstertm-d4000转染试剂将pcdna3.1his/betatrcp–cypa、pcdna3.1his/cypa各2µg(比例为3∶1)分别转入每孔,pcdna3.1his空载体转染293t细胞做对照。转染后第2天更换新鲜培养基,48h后收集细胞,提取细胞总蛋白。bca蛋白浓度测定试剂盒进行蛋白定量后用westernblot检测。蛋白经12%sds-page后,转移至pvdf膜,封闭后,分别加入his-tag单克隆抗体(pcdna3.1his/betatrcp-cypa和pcdna3.1hiscypa含his标签)孵育后,加入hrp标记的羊抗鼠igg孵育、洗膜后,用化学发光试剂盒显色。westernblot结果表明,betatrcp-cypa和cypa蛋白在相对分子质量分别为约52kd、21kd处出现特异性反应条带,而对照组293t细胞蛋白则未见此条带(见图6)。
实验例3
betatrcp-cypa对hiv-1gag的降解分析转染前一天将293t细胞接种到六孔板中,以质粒pspax2与pcdna3.1his/betatrcp-cypa和质粒pcdna3.1his共转染。参考entranstertm-d4000转染试剂说明书进行。实验分3组:(1)实验组pspax20.4µg与pcdna3.1his/betatrcp-cypa2µg;(2)cypa对照组pspax20.4µg与pcdna3.1/cypa2µg,(3)对照组pspax20.4µg与pcdna3.1his2µg,转染后48小时收细胞:吸去培养液,用1ml预冷的pbs洗1次,吸去pbs;在用碧云天的ip及western细胞裂解液裂解细胞,裂解液中加入pmsf,使pmsf的最终浓度为1mmol/l;取100µl细胞裂解液与收获细胞混匀,4℃12000r/min离心30min后收集上清,bca蛋白浓度测定试剂盒进行蛋白定量后用westernblot检测,同时作β-actin的内参对照。蛋白经12%sds-page后,转移至pvdf膜,封闭后,5%脱脂牛奶封闭h后,分别加入hiv-1p24单抗和β-actin单克隆抗体孵育,洗膜后加入偶联hrp的羊抗鼠二抗,室温孵育2h,洗膜后进行ecl显色。
western印迹分析发现,转染betatrcp-cypa的实验组,hiv-1gag蛋白量明显减弱(见图7),说明betatrcp-cypa确实可以降低hiv-1gag的稳定性。cypa似乎对hiv-1gag有一定的保护作用(条带增大)。
实验例4
elisa法研究betatrcp-cypa抑制hiv-1的研究
培养293t细胞,以每孔4×l03个细胞接种于96孔板,实验分4组:(1)betatrcp-cypa组pcdna3.1his/betatrcp-cypa0.15µg,hiv-1骨架质粒pnl43luc-r-e-(pnl43lucr-e-(从美国国立卫生院(nih)aidsresearchandreferencereagentprogram获得)0.05µg;(2)cypa组pcdna3.1his/cypa0.15µg,hiv-1骨架质粒pnl43lucr-e-0.05µg;(3)对照组pcdna3.1/his0.15µg,hiv-1骨架质粒pnl43luc-r-e-0.05µg,(4)293t细胞组,每组3个复孔,第二天用entranstertm-d4000转染试剂将entranstertm-d-4000和质粒以3∶1比例分别转入每孔,6h后换液,继续培养24-48h。48h后,检测上清中的p24浓度。留下细胞待裂解后进行荧光素酶活性检测。具体步骤如下:
1).实验设计:将包被板从密封袋中取出,根据所需数量在板架上放好微孔板条。设空白对照2孔,hiv-1不同浓度校准品a、b、c、d、e各2复孔。
2).加结合物1:每孔加入结合物125μl。
3).加样:依次分别加入样品、校准品75μl。
4).温育:用微量震荡器充分振荡混匀,用封板膜封盖反应板,37℃温育60分钟;
5).洗板:取出微孔板,吸干微孔板中所有液体,每孔加入稀释好的洗涤液400μl,浸泡至少10秒,吸干。如此洗板
次,最后在干净的吸水纸上拍干。
6).加酶:空白孔除外,每孔加入结合物2100μl。
7).温育:用新的封板膜封盖反应板,37℃温育30分钟。
8).洗板:取出微孔板,如上述洗板方法洗涤5次,最后在干净的吸水纸上拍干。
9).加底物液:每孔先加入底物显色液a50μl(或1滴),再加入底物显色液b50μl(或1滴)。
10).温育:用微量振荡器充分振荡混匀,用封板膜封盖反应板,37℃温育15分钟;
11).加终止液:每孔加入终止液50μl(或1滴),轻轻振荡混匀。
12).读数:设定酶标仪波长于450nm处,用空白孔调零点后测定各孔a值。
以hiv-1标准品的吸光值平均值为纵轴,hiv-1标准品的浓度平均值为横轴,作标准曲线。
将测得的样品吸光值在上述的标准曲线上求得样品hiv-1p24的浓度。
(pcdna3,1his组浓度-实验组p24浓度)/pcdna3,1his组p24浓度×100%算出抑制率。
结果betatrcp-cypa体现出较好的抑制效果,抑制效果达70%多。说明betatrcp-cypa具有良好的抗hiv-1活性。cypa组也有一定抑制率可能是由于cypa抑制了p24的分泌,使细胞内的p24反而增加(见图8)。
实验例5
荧光素酶活性betatrcp-cypa抑制hiv-1的研究
上述5中的细胞加入100µl报告基因细胞裂解液裂解细胞(用碧云天的萤火虫萤光素酶报告基因检测试剂盒)。加入100µl萤光素酶检测试剂,用枪打匀或用其它适当方式混匀后测定rlu(relativelightunit)。以报告基因细胞裂解液为空白对照,测定荧光值,荧光值越高hiv-1复制水平越高,通过与未感染hiv-1细胞的荧光值相比,该比值可以反应hiv复制水平。结果betatrcp-cypa体现出较好的抑制效果(见图9),说明betatrcp-cypa具有良好的抗hiv-1活性。
sequencelisting
<110>河南科技大学
<120>一种具有抑制hiv-1作用的融合基因betatrcp-cypa及其构建方法
<130>1
<160>9
<170>patentinversion3.3
<210>1
<211>1293
<212>dna
<213>人
<400>1
atggacccagcagaagcagtgcttcaggagaaggctctcaagtttatgaactcctccgag60
agggaggactgcaacaacggcgagcctcctaggaagatcatcccagagaagaactccctg120
cgccagacctacaacagctgtgcccgcctttgccttaaccaggagaccgtctgtttggct180
tcaaccgctatgaagaccgagaactgcgtggccaagacaaagctcgccaacggaactagc240
tccatgatcgtgcctaagcagagaaagctcagcgcctcttacgagaaggagaaggaactg300
tgcgtcaagtacttcgagcagtggagcgagagcgaccaggtggagttcgtggagcacttg360
atctcccagatgtgccactaccagcacggacacatcaactcctacctcaagcctatgctc420
cagagggacttcatcactgccctgccagctagagggttggaccatatcgccgaaaacatc480
ctgagctacctggatgccaagagcctgtgcgctgcagaattggtgtgcaaagagtggtac540
agagtcacaagcgatggcatgctgtggaagaaactgattgagcggatggtcaggacagat600
tctctgtggaggggactggccgagagaagaggatgggggcaatatctgtttaagaacaag660
ccacctgatgggaatgctccacctaacagtttctacagagccctgtaccccaagattatt720
caggatattgagacaattgagtcaaactggagatgcggaagacacagtggctcaggatca780
ggctcaggatcaggctcaatggtcaaccccaccgtgttcttcgacattgccgtcgacggc840
gagcccttgggccgcgtctcctttgagctgtttgcagacaaggtcccaaagacagcagaa900
aattttcgtgctctgagcactggagagaaaggatttggttataagggttcctgctttcac960
agaattattccagggtttatgtgtcagggtggtgacttcacacgccataatggcactggt1020
ggcaagtccatctatggggagaaatttgaagatgagaacttcatcctaaagcatacgggt1080
cctggcatcttgtccatggcaaatgctggacccaacacaaatggttcccagtttttcatc1140
tgcactgccaagactgagtggttggatggcaagcatgtggtgtttggcaaagtgaaagaa1200
ggcatgaatattgtggaggccatggagcgctttgggtccaggaatggcaagaccagcaag1260
aagatcaccattgctgactgtggacaactcgaa1293
<210>2
<211>798
<212>dna
<213>人
<400>2
atggacccagcagaagcagtgcttcaggagaaggctctcaagtttatgaactcctccgag60
agggaggactgcaacaacggcgagcctcctaggaagatcatcccagagaagaactccctg120
cgccagacctacaacagctgtgcccgcctttgccttaaccaggagaccgtctgtttggct180
tcaaccgctatgaagaccgagaactgcgtggccaagacaaagctcgccaacggaactagc240
tccatgatcgtgcctaagcagagaaagctcagcgcctcttacgagaaggagaaggaactg300
tgcgtcaagtacttcgagcagtggagcgagagcgaccaggtggagttcgtggagcacttg360
atctcccagatgtgccactaccagcacggacacatcaactcctacctcaagcctatgctc420
cagagggacttcatcactgccctgccagctagagggttggaccatatcgccgaaaacatc480
ctgagctacctggatgccaagagcctgtgcgctgcagaattggtgtgcaaagagtggtac540
agagtcacaagcgatggcatgctgtggaagaaactgattgagcggatggtcaggacagat600
tctctgtggaggggactggccgagagaagaggatgggggcaatatctgtttaagaacaag660
ccacctgatgggaatgctccacctaacagtttctacagagccctgtaccccaagattatt720
caggatattgagacaattgagtcaaactggagatgcggaagacacagtggctcaggatca780
ggctcaggatcaggctca798
<210>3
<211>498
<212>dna
<213>人
<400>3
atggtcaaccccaccgtgttcttcgacattgccgtcgacggcgagcccttgggccgcgtc60
tcctttgagctgtttgcagacaaggtcccaaagacagcagaaaattttcgtgctctgagc120
actggagagaaaggatttggttataagggttcctgctttcacagaattattccagggttt180
atgtgtcagggtggtgacttcacacgccataatggcactggtggcaagtccatctatggg240
gagaaatttgaagatgagaacttcatcctaaagcatacgggtcctggcatcttgtccatg300
gcaaatgctggacccaacacaaatggttcccagtttttcatctgcactgccaagactgag360
tggttggatggcaagcatgtggtgtttggcaaagtgaaagaaggcatgaatattgtggag420
gccatggagcgctttgggtccaggaatggcaagaccagcaagaagatcaccattgctgac480
tgtggacaactcgaataa498
<210>4
<211>34
<212>dna
<213>人工序列
<400>4
ggaattcgccaccatggacccagcagaagcagtg34
<210>5
<211>22
<212>dna
<213>人工序列
<400>5
tgagcctgatcctgagcctgat22
<210>6
<211>74
<212>dna
<213>人工序列
<400>6
ctggagatgcggaagacacagtggctcaggatcaggctcaggatcaggctcaatggtcaa60
ccccaccgtgttct74
<210>7
<211>43
<212>dna
<213>人工序列
<400>7
atcaggctcaggatcaggctcaatggtcaaccccaccgtgttc43
<210>8
<211>30
<212>dna
<213>人工序列
<400>8
cgggatccttcgagttgtccacagtcagca30
<210>9
<211>34
<212>dna
<213>人工序列
<400>9
ggaattcgccaccatggtcaaccccaccgtgttc34
- 还没有人留言评论。精彩留言会获得点赞!
- 一种具有抑制α‑Mn析出的Mn‑Cu基高阻尼合金添加剂及其使用方法与流程
- 具有抑制零漂功能的IC插座的制作方法与工艺
- 立体式电磁干扰抑制结构及具有该立体式电磁干扰抑制结构的电子装置的制作方法
- 具有抑制11β‑HSD1酶活性的化合物或其药学上可接受的盐及其制备方法,以及包含其作为活性成分的药物组合物与流程
- 具有抑制老年性口气功能的制作丰顺水粄组合物及丰顺水粄的制作方法与流程
- 一种具有抑制HIV‑1作用的融合基因betaTrCP‑CypA及其构建方法与流程
- 对鳞翅目害虫具有毒性或抑制性的新型嵌合杀昆虫蛋白质的制造方法与工艺
- 一种具有ACE抑制和抗氧化功能的甲鱼蛋白肽及其制备方法与制造工艺
- 环孢菌素衍生物的制作方法