鼻咽癌相关的miRNA作为生物标志物的应用及鼻咽癌检测试剂盒的制作方法
本发明涉及生物检测
技术领域:
,特别是涉及一种鼻咽癌相关的mirna作为生物标志物的应用及鼻咽癌检测试剂盒。
背景技术:
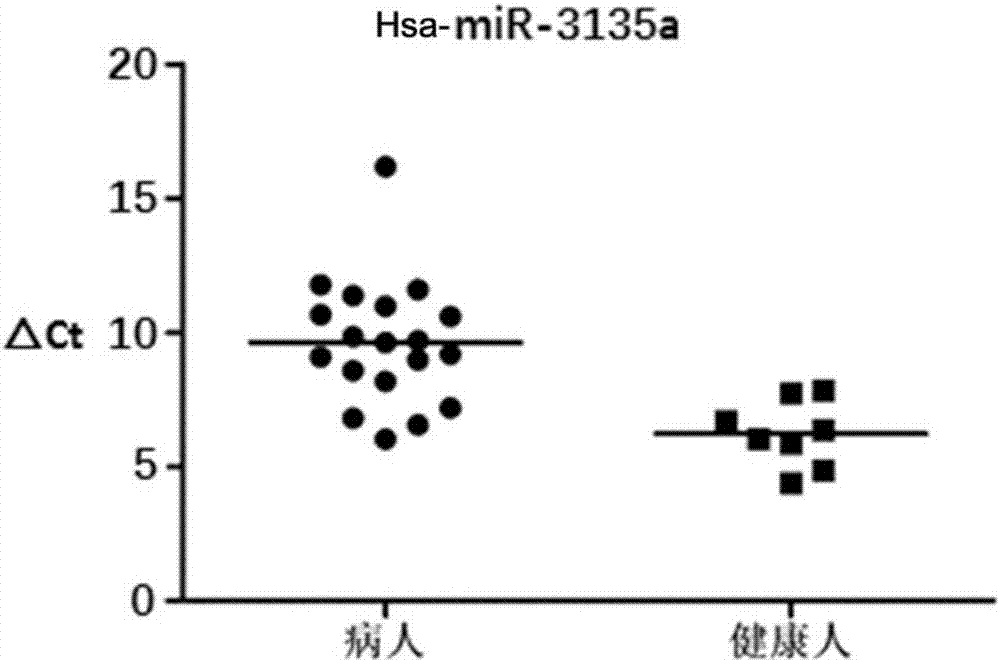
:鼻咽癌(nasopharyngealcarcinoma,npc)是指发生于鼻咽腔顶部和侧壁的恶性肿瘤,发病率为耳鼻咽喉恶性肿瘤之首。世界卫生组织调查报道,全球有80%的鼻咽癌患者在中国。鼻咽癌的发病率以中国的南方较高,如广东、广西、湖南等省。由于鼻咽癌起病隐匿,具有强烈的转移倾向,约75%的患者首诊时就己到达晚期,发生局部淋巴结和/或远处转移。一般以放疗为主的综合治疗对早期鼻咽癌非常有效,而治疗后复发或转移则预后极差,成为鼻咽癌治疗失败、生存率下降的主要原因。因此,筛查鼻咽癌的肿瘤标记物,争取早期发现、合理治疗、预测预后、监测复发,对鼻咽癌临床诊治具有极其重要的意义。研究发现,鼻咽癌的发病与爱波斯坦-巴尔病毒(epstein-barrvirus,ebv)感染、遗传因素以及环境因素密切相关。鉴于鼻咽癌与ebv感染的相关性,现有鼻咽癌的外周血标志物主要围绕eb病毒设计,如eb病毒壳抗原抗体vca-iga、早期抗体ea-iga及ebv-dna,但它们的敏感性和特异性并不高,在鼻咽癌患者中的ebv阳性率只有60%左右,存在较多的假阳性和假阴性,远远达不到临床要求。人类白细胞抗原(humanleukocyteantigen,hla)被认为是与鼻咽癌发病最显著相关的遗传因素,在鼻咽癌候选基因研究和全基因组关联性研究中均检出hla与鼻咽癌的存在相关性,但由于技术和费用等限制,目前还无法应用于临床。而其它鼻咽癌相关蛋白及其编码基因标志物的筛选,都止步于实验理论阶段,目前尚无实用的特异性的鼻咽癌标志物。随着研究的深入,研究者发现除了肿瘤相关的蛋白及其编码基因,非编码基因也与肿瘤的发生发展密切相关。特别是一类高度保守的非编码单链小分子rna(microrna,mirna),通常通过与靶基因mrna的3’端完全或部分匹配互补结合,导致靶mrna降解或抑制其翻译从而调控靶基因的表达。mirna对多种生理过程包括发育、增殖、分化凋亡和应激反应等重要功能基因的表达起调控作用。研究发现在几乎所有肿瘤组织中都检测出异常表达的mirna,越来越多的研究证实了mirna几乎参与了肿瘤发生发展中的每一个步骤,在肿瘤发病机制中发挥了超出想象的重要作用。特定的mirna可以反映肿瘤的组织来源,并对其进行分子分型,可用来预测预后及判断治疗敏感性,甚至直接参与肿瘤的治疗。若能筛选出鼻咽癌中异常表达mirna作为生物标志物,并研制相应的辅助诊断试剂盒,将有力推动我国鼻咽癌的早期诊断、预测治疗、监测复发等,具有重要的临床应用价值。然而,由于鼻咽癌mirna的研究起步较晚,循环mirna的研究更是报道较少。基于传统的鼻咽癌标记物研制的检测试剂存在如下缺点:难以在鼻咽癌早期检测,需要同时检测大量的生物标志物才能得到初步的判断,检测的灵敏度和特异性较低。技术实现要素:基于此,有必要提供一种能够用于早期检测且在检测时具有较高灵敏度和较高特异性的鼻咽癌检测试剂盒。此外,还提供一种鼻咽癌相关的mirna作为生物标志物的应用。hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198中的至少一种,作为生物标志物在制备鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置中的应用。一实施方式的应用中,所述鼻咽癌为早期鼻咽癌。一实施方式的应用中,所述生物标志物来自血液。一种鼻咽癌检测试剂盒,包括与生物标志物特异性结合的检测物,所述生物标志物选自hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198中的至少一种。在一个实施方式中,所述与生物标志物特异性结合的检测物包括能够扩增所述生物标志物的引物或能够检测所述生物标志物的探针。在一个实施方式中,所述与生物标志物特异性结合的检测物包括生物标志物pcr扩增正向引物和生物标志物pcr扩增反向引物;所述生物标志物pcr扩增正向引物包括第一正向引物、第二正向引物和第三正向引物中的至少一种,所述第一正向引物针对所述hsa-mir-1909-3p逆转录后得到的cdna设计,所述第二正向引物针对所述hsa-mir-3135a逆转录后得到的cdna设计,所述第三正向引物针对所述hsa-mir-198逆转录后得到的cdna设计。在一个实施方式中,所述第一正向引物的碱基序列如seqidno.1所示;及/或,所述第二正向引物的碱基序列如seqidno.2所示;及/或,所述第三正向引物的碱基序列如seqidno.3所示;及/或,所述生物标志物pcr扩增反向引物为通用反向扩增引物,所述生物标志物pcr扩增反向引物的碱基序列如seqidno.4所示。在一个实施方式中,还包括能够检测内参基因的试剂,所述内参基因选自u6、gapdh、β-actin中的至少一种。在一个实施方式中,还包括rna提取试剂、加a尾试剂和rna逆转录试剂;所述rna提取试剂用于提取待测样品中的rna;所述加a尾试剂用于在提取的所述rna的一端加a碱基;所述rna逆转录试剂用于将加a尾后的所述rna逆转录成cdna。在一个实施方式中,所述rna逆转录试剂包括rna逆转录引物,所述rna逆转录引物的碱基序列如seqidno.5所示。hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198均属于mirna。发明人在鼻咽癌的生物标志物方面进行了大量的探索研究,预料不到的发现,在鼻咽癌患者与健康人中hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198的表达量具有显著性的差异。hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198的表达量高低与鼻咽癌存在密切的关联性,因此能够作为鼻咽癌的生物标志物应用在制备鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置中。基于上述生物标志物研发的鼻咽癌检测试剂,能够应用于鼻咽癌早期检测中,仅需要对hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198中的至少一种mirna进行检测,操作简单且方便,工作量小,且检测的灵敏度较高、特异性较高。附图说明图1为测试一中生物标记物hsa-mir-1909-3p在鼻咽癌患者与健康人的血浆中表达水平的分布图;图2为测试一中生物标记物hsa-mir-3135a在鼻咽癌患者与健康人的血浆中表达水平的分布图;图3为测试一中生物标记物hsa-mir-198在鼻咽癌患者与健康人的血浆中表达水平的分布图;图4为采用实施例1的鼻咽癌检测试剂盒检测区分健康人和鼻咽癌患者的敏感性和特异性的roc曲线图;图5为采用实施例2的鼻咽癌检测试剂盒检测区分健康人和鼻咽癌患者的敏感性和特异性的roc曲线图;图6为采用实施例3的鼻咽癌检测试剂盒检测区分健康人和鼻咽癌患者的敏感性和特异性的roc曲线图;图7为采用实施例4的鼻咽癌检测试剂盒检测区分健康人和鼻咽癌患者的敏感性和特异性的roc曲线图。具体实施方式下面主要结合附图及具体实施例对本发明做进一步的解释说明。一实施方式的应用,hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198中的至少一种,作为生物标志物应用在制备鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置中。具体地,生物标志物是指可以标记系统、器官、组织及细胞结构或功能的改变或可能发生的改变的生化指标。具体地,hsa-mir-1909-3p是人源的mir-1909家族成员之一,来自hsa-mir-1909的3’末端。目前关于hsa-mir-1909-3p的报道较少,本研究意外发现在鼻咽癌患者与健康人中hsa-mir-1909-3p的表达量具有显著性的差异。实验结果表明,与健康人相比,hsa-mir-1909-3p的表达量下降了7.25倍。因此hsa-mir-1909-3p可作为生物标志物用于检测鼻咽癌,以及基于hsa-mir-1909-3p作为生物标记物研发形成鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置。具体地,hsa-mir-3135a是人源的mir-3135a家族成员之一。目前关于hsa-mir-3135a的报道主要是与心肌梗死疾病相关。本研究意外发现在鼻咽癌患者与健康人中hsa-mir-3135a的表达量具有显著性的差异。实验结果表明,与健康人相比,hsa-mir-3135a的表达量下降了4.32倍。因此hsa-mir-3135a可作为生物标志物用于检测鼻咽癌,以及基于hsa-mir-3135a作为生物标记物研发形成鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置。具体地,hsa-mir-198是人源的mir-198家族成员之一。目前关于mir-198的报道较少。本研究意外发现在鼻咽癌患者与健康人中hsa-mir-198的表达量具有显著性的差异。实验结果表明,与健康人相比,hsa-mir-198的表达量下降了2.46倍。因此hsa-mir-198可作为生物标志物用于检测鼻咽癌,以及基于hsa-mir-198作为生物标记物研发形成鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置。hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198三种mirna在早期鼻咽癌的病人中能够被检测且表达量与健康人有一定的差异。因此hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198能够作为早期鼻咽癌的检测生物标记物,用于鼻咽癌早期诊断、预测治疗或监测复发等。进一步地,hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198能够稳定的存在血清和血浆等多种体液中,属于循环mirna。血清、血浆这些血循环中mirna经过长期保存、反复冻融后仍可稳定存在而不发生降解,以hsa-mir-1909-3p、hsa-mir-3135a或hsa-mir-198作为鼻咽癌的生物标记物能够准确反应被检测对象中生物标志物的含量或水平。在一个实施方式中,hsa-mir-1909-3p作为生物标志物应用在制备鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置中。在另一个实施方式中,hsa-mir-3135a作为生物标志物应用在制备鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置中。在另一个实施方式中,hsa-mir-198作为生物标志物应用在制备鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置中。在另一个实施方式中,hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198中的任意两种或三种,作为生物标志物应用在制备鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置中。优选地,将hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198三种作为生物标志物应用在制备鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置中,多种组合提高检测的灵敏性和特异性。在一个实施方式中,生物标志物hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198来自血液。进一步地,生物标志物hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198来自处理后的血液,如血浆或血清等。血清、血浆这些血循环中mirna经过长期保存、反复冻融后仍可稳定存在而不发生降解,从而准确反应被检测对象中生物标志物的含量或水平。发明人在鼻咽癌的生物标志物方面进行了大量的探索研究,预料不到地发现,在鼻咽癌患者与健康人中hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198的表达量具有显著性的差异。hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198的表达量高低与鼻咽癌存在密切的关联性,因此能够作为鼻咽癌的生物标志物应用在制备鼻咽癌检测试剂、鼻咽癌检测试剂盒或鼻咽癌检测装置中。虽然hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198在循环中的存在形式及生理功能尚不明了,但推测循环中mirna主要由细胞分泌释放入血液,以外泌体(exosome)或蛋白复合体的形式存在,在细胞之间传递生物信息。将hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198作为检测鼻咽癌的生物标记物比传统的特异蛋白分子标记方法将更加有效。一实施方式的鼻咽癌检测试剂盒,包括与生物标志物特异性结合的检测物,该生物标志物选自hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198中的至少一种。具体地,hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198具体的信息请参见前文描述。在一个实施方式中,与生物标志物特异性结合的检测物为能够扩增该生物标志物的引物或能够检测该生物标志物的探针。通过扩增该生物标志物的引物或检测该生物标志物的探针定量或定性的测定生物标志物hsa-mir-1909-3p、hsa-mir-3135a或hsa-mir-198的含量。在一个实施方式中,该鼻咽癌检测试剂盒包括与生物标志物特异性结合的检测物、rna提取试剂、加a尾试剂、rna逆转录试剂和检测内参基因的试剂。具体地,rna提取试剂用于提取待测样品中的rna。具体地,加a尾试剂用于在提取的rna的一端加a碱基。优选地,通过加a尾试剂在提取的rna的一端加12个以上a碱基,例如12个~20个。具体地,rna逆转录试剂用于将加a尾后的rna逆转录成cdna。将加a尾后的rna逆转录成cdna再检测,有利于提高检测的灵敏性。具体地,rna逆转录试剂包括rna逆转录引物,该rna逆转录引物为通用rt-pcr引物,能够特异性的将加a尾后的rna逆转录成cdna。在一个实施方式中,rna逆转录引物包括针对保守区域设计的片段以及针对a尾设计的片段和简并碱基。尾端设计简并碱基有利于引物与扩增片段结合。进一步地,rna逆转录引物的碱基序列如seqidno.5所示。简并碱基v表示碱基a或碱基c或碱基g,简并碱基n表示碱基a或碱基c或碱基g或碱基t。在一个实施方式中与生物标志物特异性结合的检测物包括生物标志物pcr扩增正向引物、生物标志物pcr扩增反向引物。生物标志物pcr扩增正向引物包括第一正向引物、第二正向引物和第三正向引物中的至少一种。第一正向引物针对hsa-mir-1909-3p逆转录后得到的cdna设计。第二正向引物针对hsa-mir-3135a逆转录后得到的cdna设计。第三正向引物针对hsa-mir-198逆转录后得到的cdna设计。通过生物标志物pcr扩增正向引物和生物标志物pcr扩增反向引物扩增待测样品中hsa-mir-1909-3p、hsa-mir-3135a或hsa-mir-198,计算获得待测样品中hsa-mir-1909-3p、hsa-mir-3135a或hsa-mir-198的含量。具体地,第一正向引物的碱基序列如seqidno.1所示。具体地,第二正向引物的碱基序列如seqidno.2所示。具体地,第三正向引物的碱基序列如seqidno.3所示。具体地,生物标志物pcr扩增反向引物为通用反向扩增引物,生物标志物pcr扩增反向引物的碱基序列如seqidno.4所示。特异性的分别针对hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198设计正向引物,从而特异性的扩增对应的目标片段,计算获得待测样品中hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198的含量。在一个实施方式中,检测内参基因的试剂包括内参基因逆转录引物和内参基因pcr扩增正向引物和内参基因pcr扩增反向引物。通过检测内参基因的试剂检测内参基因的含量,以此为基准计算hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198的含量,提高检测的准确性。具体地,内参基因选自u6、gapdh、β-actin中的至少一种。在一个实施方式中,内参基因为u6,u6逆转录引物的碱基序列如seqidno.6所示。u6的pcr扩增正向引物的碱基序列如seqidno.7所示。u6的pcr扩增反向引物的碱基序列如seqidno.8所示。上述鼻咽癌检测试剂盒,通过rna提取试剂提取待测样品中的rna,通过加a尾试剂在提取的rna的一端加a碱基,通过rna逆转录试剂将加a尾后的rna逆转录成cdna。然后通过设计的与生物标志物特异性结合的检测物检测生物标志物hsa-mir-1909-3p、hsa-mir-3135a或hsa-mir-198的含量。该检测试剂盒能够应用在早期鼻咽癌的检测中,检测的灵敏度较高、特异性较高。当然,可以理解,在其他实施方式的检测试剂盒中,当已经将检测样品中的rna提取,并加a尾逆转录成cdna时,rna提取试剂、加a尾试剂和rna逆转录试剂可省略。当同一样本已经确定并测定内参含量时,检测内参基因的试剂也可省略。一实施方式的上述鼻咽癌检测试剂盒的使用方法,包括如下步骤s110~s140。s110、通过rna提取试剂提取待测样品中的rna。具体地,待测样品例如为血浆,通过rna提取试剂提取血浆中的总rna。s120、通过加a尾试剂在s110中提取的rna的一端加a碱基。具体地,在提取的rna的一端加12个以上a碱基,例如12个~20个。s130、通过rna逆转录试剂将加a尾后的rna逆转录成cdna。具体地,rna逆转录引物为通用逆转录引物,rna逆转录引物的碱基序列如seqidno.5所示。具体地,还包括在相同的条件下通过内参基因逆转录引物将加a尾后的rna逆转录成内参基因cdna。具体地,内参基因逆转录引物为u6逆转录引物,u6逆转录引物的碱基序列如seqidno.6所示。s140、通过与生物标志物特异性结合的检测物检测hsa-mir-1909-3p、hsa-mir-3135a或hsa-mir-198的含量。具体地,与生物标志物特异性结合的检测物包括生物标志物pcr扩增正向引物和生物标志物pcr扩增反向引物。pcr扩增正向引物包括第一正向引物、第二正向引物和第三正向引物中的至少一种。第一正向引物针对hsa-mir-1909-3p逆转录后得到的cdna设计。第二正向引物针对hsa-mir-3135a逆转录后得到的cdna设计。第三正向引物针对hsa-mir-198逆转录后得到的cdna设计。第一正向引物的碱基序列如seqidno.1所示。第二正向引物的碱基序列如seqidno.2所示。第三正向引物的碱基序列如seqidno.3所示。生物标志物pcr扩增反向引物通用反向扩增引物,生物标志物pcr扩增反向引物的碱基序列如seqidno.4所示。具体地,通过荧光定量pcr反应检测生物标志物hsa-mir-1909-3p、hsa-mir-3135a或hsa-mir-198的含量。pcr扩增体系为pcr缓冲液5μl,0.5μm的正向引物1μl,0.5μm的pcr扩增通用反向引物1μl,模板cdna1μl,增加rnase-freewater至10μl。当正向引物为第一正向引物时,pcr检测获得扩增hsa-mir-1909-3p的ct值(循环数)。当正向引物为第二正向引物时,pcr检测获得扩增hsa-mir-3135a的ct值。当正向引物为第三正向引物时,pcr检测获得扩增hsa-mir-198的ct值。具体地,还包括在在相同的条件下用内参基因pcr扩增正向引物和内参基因pcr扩增反向引物检测内参基因的含量。在一个实施方式中,内参基因为u6,u6逆转录引物的碱基序列如seqidno.6所示。u6的pcr扩增正向引物的碱基序列如seqidno.7所示。u6的pcr扩增反向引物的碱基序列如seqidno.8所示。具体地,内参基因pcr扩增体系为pcr缓冲液5μl,0.5μm的内参基因pcr扩增正向引物1μl,0.5μm的内参基因pcr扩增反向引物1μl,内参基因的cdna1μl,增加rnase-freewater至10μl。pcr检测获得扩增内参基因的ct值。将获得扩增hsa-mir-1909-3p的ct值、扩增hsa-mir-3135a的ct值、扩增hsa-mir-198的ct值减去扩增内参基因的ct值,得到ct值的差值(δct值)。初步诊断该待测样品来源的样本是否为鼻咽癌患者、或患鼻咽癌的风险。上述基于hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198作为鼻咽癌的生物标志物制备的鼻咽癌检测试剂,能够应用于鼻咽癌早期检测中,检测的灵敏度较高、特异性较高,检测结果快速客观,在鼻咽癌临床诊断、鼻咽癌预防检测领域具有极大的应用前景。下面为具体实施例部分。以下实施例中,如无特别说明,未注明具体条件的实验方法,通常按照常规条件,例如参见萨姆布鲁克、ef弗里奇、t曼尼阿蒂斯等(金冬雁,黎孟枫等译)所著的的分子克隆实验指南[m](北京:科学出版社,1992)中所述的条件或者试剂盒生产厂家推荐的方法实现。实施例中所使用的试剂均为市售。未特别说明,实施例中所使用的rna提取试剂为mirneasyserum/plasmakit试剂盒(#217184,购自qiagen,hilden,germany)。加a尾试剂为poly(a)tailingkit(#am1350,购自ambion,austin,tx)。第一正向引物、第二正向引物、第三正向引物、生物标志物pcr扩增反向引物、rna逆转录引物、u6逆转录引物、u6的pcr扩增正向引物、u6的pcr扩增反向引物通过基因合成的方式获得。第一正向引物的碱基序列如seqidno.1所示。第二正向引物的碱基序列如seqidno.2所示。第三正向引物的碱基序列如seqidno.3所示。生物标志物pcr扩增反向引物的碱基序列如seqidno.4所示。rna逆转录引物的碱基序列如seqidno.5所示。u6逆转录引物的碱基序列如seqidno.6所示。u6的pcr扩增正向引物的碱基序列如seqidno.7所示。u6的pcr扩增反向引物的碱基序列如seqidno.8所示。实施例1一种鼻咽癌检测试剂盒,内含有rna提取试剂、加a尾试剂、第一正向引物、生物标志物pcr扩增反向引物、rna逆转录引物、u6逆转录引物、u6的pcr扩增正向引物和u6的pcr扩增反向引物。该鼻咽癌检测试剂盒能够检测鼻咽癌生物标记物hsa-mir-1909-3p的表达量。实施例2一种鼻咽癌检测试剂盒,内含有rna提取试剂、加a尾试剂、第二正向引物、生物标志物pcr扩增反向引物、rna逆转录引物、u6逆转录引物、u6的pcr扩增正向引物和u6的pcr扩增反向引物。该鼻咽癌检测试剂盒能够检测鼻咽癌生物标记物hsa-mir-3135a的表达量。实施例3一种鼻咽癌检测试剂盒,内含有rna提取试剂、加a尾试剂、第三正向引物、生物标志物pcr扩增反向引物、rna逆转录引物、u6逆转录引物、u6的pcr扩增正向引物和u6的pcr扩增反向引物。该鼻咽癌检测试剂盒能够检测鼻咽癌生物标记物hsa-mir-198的表达量。实施例4一种鼻咽癌检测试剂盒,内含有rna提取试剂、加a尾试剂、第一正向引物、第二正向引物、第三正向引物、生物标志物pcr扩增反向引物、rna逆转录引物、u6逆转录引物、u6的pcr扩增正向引物和u6的pcr扩增反向引物。该鼻咽癌检测试剂盒能够检测鼻咽癌生物标记物hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198的表达量。测试例一(1)从南京肿瘤医院采集19个鼻咽癌患者的血浆样品及其8个健康人的血浆样品,标本储存于-80℃环境中。(2)按照操作手册步骤用mirneasyserum/plasmakit试剂盒(#217184,qiagen,hilden,germany)提取鼻咽癌早期患者和健康人的血浆中游离rna。用poly(a)tailingkit(#am1350,ambion,austin,tx)按操作手册对mirna进行加poly(a)尾,本实施例对mirna加入12个a碱基。(3)使用m-mulvreversetranscriptase(#e6300s,neb,hitchin,uk)和通用rna逆转录引物按操作手册对加poly(a)的mirna进行逆转录得到cdna。相同的条件下使用m-mulvreversetranscriptase(#e6300s,neb,hitchin,uk)和u6逆转录引物按操作手册对加poly(a)的mirna进行逆转录得到内参基因u6的cdna。通用逆转录引物的碱基序列为:gcgagcacagaattaatacgactcactataggttttttttttttvn(seqidno.5所示)。内参基因u6的逆转录引物的碱基序列为:ggaacgcttcacgaatttg(seqidno.6所示)。(4)使用实时荧光定量pcrssofasttmsupermix(bio-rad,hercules,ca)对mirna进行定量分析。先采用实时荧光定量pcr检测扩增内参基因u6的ct值,定量的反应体系如下表1所示。表1:检测内参基因u6的pcr反应体系其中u6的pcr扩增正向引物的碱基序列为:attggaacgatacagagaagatt(seqidno.7所示)u6的pcr扩增反向引物的碱基序列的碱基序列为:ggaacgcttcacgaatttg(seqidno.8所示)。反应条件:95℃2min;变性95℃20s,退火/延伸58℃40s,共40个循环。经检测,健康人提取的样本和鼻咽癌早期患者提取的样本中内参基因u6的ct均在12~13之间,平均为12.45,两者差异不显著。继续采用实时荧光定量pcr检测扩增生物标记物hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198的ct值,定量的反应体系如下表2所示。表2:检测生物标记物的pcr反应体系其中第一正向引物(hsa-mir-1909-3p的定量正向引物)的碱基序列为:cgcaggggccgggtgctcaccg(seqidno.1所示)。第二正向引物(hsa-mir-3135a的定量正向引物)的碱基序列为:tgcctaggctgagactgcagtg(seqidno.2所示)。第三正向引物(hsa-mir-198的定量正向引物)的碱基序列为:ggtccagaggggagataggttc(seqidno.3所示)。物标志物pcr扩增反向引物(定量通用反向引物)的碱基序列为:gcgagcacagaattaatacgac(seqidno.4所示)。反应条件:95℃2min;变性95℃20s,退火/延伸58℃40s,共40个循环。分别获得扩增hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198的ct值。并用每一个样本的ct值减去内参平均ct值。分布的散点图如图1~图3所示。结果表明鼻咽癌患者与健康人的血浆相比,hsa-mir-1909-3p总体表达水平分别减少了7.25倍(p<0.05),hsa-mir-3135a总体表达水平分别减少了4.32倍(p<0.05),hsa-mir-198总体表达水平分别减少了2.46倍(p<0.05),hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198三种生物标记物的在健康人和鼻咽癌患者中均具有显著的差异性。测试例二同样以南京肿瘤医院采集19个鼻咽癌患者的血浆样品及其8个健康人的血浆样品作为检测样本,每个检测样本至少3次重复。用实施例1(hsa-mir-1909-3p作为标记物)、实施例2(hsa-mir-3135a作为标记物)、实施例3(hsa-mir-198作为标记物)和实施例4(hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198同时作为标记物)的试剂盒按上述测试一的方法测试。结果如下表3所示。表3:鼻咽癌病人、健康人测试结果以上结果表明实施例1~4的检测试剂盒能够高特异性的检测区分鼻咽癌病人检测样本和健康人检测样本。进一步,以实施例1的试剂盒(hsa-mir-1909-3p作为鼻咽癌的标记物)检测区分健康人和鼻咽癌患者的检测数据,使用medcalc软件进行roc分析,得到roc曲线如图4所示。从图中看出auc为0.954,95%置信区间为0.797~0.998。说明以hsa-mir-1909-3p作为鼻咽癌的标记物检测区分健康人和鼻咽癌灵敏度较高、特异性较高。以实施例2的试剂盒(hsa-mir-3135a作为鼻咽癌的标记物)检测区分健康人和鼻咽癌患者的检测数据,使用medcalc软件进行roc分析,得到roc曲线如图5所示。从图中看出auc为0.921,95%置信区间为0.750~0.989。说明以hsa-mir-3135a作为鼻咽癌的标记物检测区分健康人和鼻咽癌灵敏度较高、特异性较高。以实施例3的试剂盒(hsa-mir-198作为鼻咽癌的标记物)检测区分健康人和鼻咽癌患者的检测数据,使用medcalc软件进行roc分析,得到roc曲线如图6所示。从图中看出auc为0.789,95%置信区间为0.590~0.921。说明以hsa-mir-198作为鼻咽癌的标记物检测区分健康人和鼻咽癌灵敏度较高、特异性较高。以实施例4的试剂盒(hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198同时作为鼻咽癌的标记物)检测区分健康人和鼻咽癌患者的检测数据,使用medcalc软件进行roc分析,得到roc曲线如图7所示。从图中看出auc为0.987,95%置信区间为0.849~1。说明以hsa-mir-1909-3p、hsa-mir-3135a和hsa-mir-198组合同时作为鼻咽癌的标记物检测区分健康人和鼻咽癌,auc为0.987,95%置信区间为0.849~1,灵敏度和特异性非常好。具体数据如下表4所示。表4:检测结果试剂盒灵敏度(%)特异性(%)auc95%置信区间实施例110087.50.9540.797~0.998实施例278.951000.9210.750~0.989实施例347.371000.7890.590~0.921实施例489.471000.9870.849~1以上所述实施例仅表达了本发明的一种或几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。序列表<110>深圳市恩普电子技术有限公司<120>鼻咽癌相关的mirna作为生物标志物的应用及鼻咽癌检测试剂盒<160>8<170>siposequencelisting1.0<210>1<211>22<212>dna<213>人工序列(artificialsequence)<400>1cgcaggggccgggtgctcaccg22<210>2<211>22<212>dna<213>人工序列(artificialsequence)<400>2tgcctaggctgagactgcagtg22<210>3<211>22<212>dna<213>人工序列(artificialsequence)<400>3ggtccagaggggagataggttc22<210>4<211>22<212>dna<213>人工序列(artificialsequence)<400>4gcgagcacagaattaatacgac22<210>5<211>46<212>dna<213>人工序列(artificialsequence)<400>5gcgagcacagaattaatacgactcactataggttttttttttttvn46<210>6<211>19<212>dna<213>人工序列(artificialsequence)<400>6ggaacgcttcacgaatttg19<210>7<211>23<212>dna<213>人工序列(artificialsequence)<400>7attggaacgatacagagaagatt23<210>8<211>19<212>dna<213>人工序列(artificialsequence)<400>8ggaacgcttcacgaatttg19当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1