一种苯并噁唑衍生物其制备方法和应用与流程
本发明属于生物医药
技术领域:
,尤其是涉及一种苯并噁唑衍生物其制备方法和应用。
背景技术:
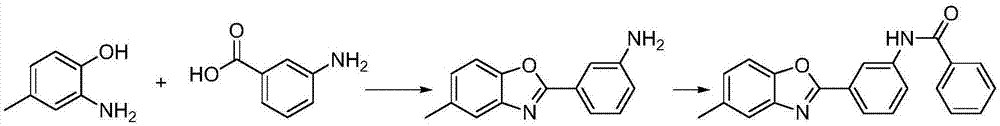
癌症是全球的主要疾病负担,每年约发生新病例1100万;全球最常见的癌症发病为肺癌、乳腺癌和结直肠癌,最常见的癌症死亡为肺癌、胃癌和肝癌。中国癌症发病占全球的20.3%,每年新发病例超过220万,最常见的癌症男性为:肺癌、胃癌、肝癌、食管癌,女性为:乳腺癌、食管癌、胃癌、肺癌、肝癌、宫颈癌。全球癌症发病总体呈上升趋势,显著上升的癌症有肺癌、乳腺癌、结直肠癌;显著下降的癌症有胃癌、宫颈癌。癌症的主要危险因素包括烟草、酒精、病毒与感染、放射与辐射、膳食与营养、环境暴露、遗传易感性等。烟草和酒精消费的增加以及现代生活方式对于肺癌、消化道癌症、乳腺癌的影响正在加剧,饮食和营养水平的提高导致了胃癌和食道癌的下降。因此,通过合成新型化合物和发现新的蛋白作用靶点寻找新的安全有效的抗癌药物是目前有效的重要方法。sirtuin蛋白家族是一类在进化过程中非常保守的蛋白酶。该家族中首先被发现并研究的酵母的sir2蛋白,研究证明sirt2被视为直接连接生物代谢状态与寿命的关键分子。而且在哺乳动物中sirt1与sir2的同源性最高。sirt1广泛表达于哺乳动物组织中,sirt1的活性和表达受到抑癌因子-肿瘤高甲基化基因1(hic1)、乳腺癌缺失因子1(dbc1)以及e2f1等的抑制。抑制sirt1可诱使肿瘤细胞生长停滞,并在不影响正常细胞的情况下促进肿瘤细胞凋亡。因此,sirt1可能是一种潜在的抗肿瘤药物靶点。苯并噁唑类化合物具有许多独特的化学和物理性质,有着其他化合物不可替代的作用被广泛用于制药、材料、荧光增白等方面。苯并噁唑类化合物是一类重要的医药中间体,这类化合物具有抗炎、抗氧化、抗菌、抗肿瘤等多种生物活性。技术实现要素:有鉴于此,本发明旨在提出一种苯并噁唑衍生物其制备方法和应用,该苯并噁唑衍生物可应用于制备抗癌候选药物。为达到上述目的,本发明的技术方案是这样实现的:一种苯并噁唑衍生物,所述苯并噁唑衍生物为5-甲基苯并噁唑-2-苯基-苯甲酰胺,其结构式如下:上述苯并噁唑衍生物在制备沉默信息调节因子sir2抑制剂的应用。上述苯并噁唑衍生物在制备果蝇体内sod、cu-zn-sod、mda、cat及相关基因的表达调控剂应用。上述苯并噁唑衍生物在制备减轻、改善、预防及治疗癌症药物中的应用。进一步的,所述癌症为肺癌、胃癌、肝癌、食管癌,乳腺癌、食管癌、胃癌、肺癌、肝癌、宫颈癌。上述苯并噁唑衍生物的制备方法,包括如下步骤:(1)制备5-甲基苯并噁唑-2-苯基-3’-胺;(2)制备5-甲基苯并噁唑-2-苯基-苯甲酰胺。进一步的,所述步骤(1)5-甲基苯并噁唑-2-苯基-3’-胺的制备方法包括如下步骤:a、向反应容器中加入4-甲基邻氨基苯酚、间氨基苯甲酸,然后搅拌均匀,然后放入强力转子,最后加入多聚磷酸,置于油浴锅内加热回流,开始加热时,设置温度为110℃,待转子开始很缓慢转动时,再慢慢升高温度至180℃,持续回流反应5h,tlc薄层监测至反应结束;b、向10%naoh的水溶液中加入nahco3,均匀搅拌,使其完全溶解制得混合溶液;在1l烧杯内加入400ml10%naoh的水溶液,然后加入9g(10.7mmol)c、将反应液趁热缓缓倒入混合溶液中,边倒反应液边加入冰块降低体系的温度,最后将体系的ph调到8~9,产生沉淀,用布氏漏斗抽滤,然后将得到的固体小圆饼捣碎,放入真空干燥箱进行干燥。待干燥完毕,再将干燥好的固体粉末溶于乙酸乙酯,过滤掉不溶物,蒸干乙酸乙酯,采用干法装柱,过硅胶柱分离纯化,用乙酸乙酯与石油醚的混合体系进行洗脱,减压浓缩除去溶剂,得到母核5-甲基苯并噁唑-2-苯基-3’-胺。进一步的,上述步骤a中使用的4-甲基邻氨基苯酚、间氨基苯甲酸、多聚磷酸的摩尔比为91.7:100.9:32.5。进一步的,上述步骤b中nahco3的添加量为每400ml10%naoh的水溶液添加10.7mmol的nahco3。进一步的,所述步骤(2)5-甲基苯并噁唑-2-苯基-苯甲酰胺的制备方法包括如下步骤:向反应容器中加入无水乙腈、苯甲酸,搅拌溶解后,依次向其中加入对甲苯磺酰氯、三乙胺、4-二甲氨基吡啶,搅拌10min后,加入5-甲基苯并噁唑-2-苯基-3’-胺,搅拌均匀后,在40℃条件下回流反应4h,tlc薄层监测反应至结束,反应结束后,在瓶内产生白色沉淀,过滤,tlc薄层监测滤液,滤液成分多为原料,将白色沉淀翻入真空干燥箱进行干燥,得到白色固体,即为5-甲基苯并噁唑-2-苯基-苯甲酰胺。进一步的,所述无水乙醇的添加量为20ml,所述苯甲酸、对甲苯磺酰氯、三乙胺、4-二甲氨基吡啶的添加量依次为1.8mmol、1.8mmol、2.7mmol、0.25mmol。相对于现有技术,本发明所述的苯并噁唑衍生物其制备方法和应用具有以下优势:本发明所述的苯并噁唑衍生物其制备方法和应用基于酵母sir2与哺乳动物sirt1的高度同源,证明苯并噁唑衍生物能抑制酵母菌的生长,抑制其代谢生长;并能显著降低果蝇体内sod、cu-znsod、mda、cat和蛋白浓度,影响sirt1极其相关基因的表达,明显抑制sirt1,可以作为sirt1抑制剂抑制癌细胞的生长。附图说明图1为本发明化合物(5-甲基苯并噁唑-2-苯基)-苯甲酰胺的合成路线示意图;图2为本发明实施例1中(5-甲基苯并噁唑-2-苯基)-3’-胺核磁共振氢谱分析图;图3为本发明实施例1中化合物5-甲基苯并噁唑-2-苯基-苯甲酰胺核磁共振氢谱分析图;图4为本发明化合物5-甲基苯并噁唑-2-苯基-苯甲酰胺对by4743酵母菌生长活性的影像图;图5为本发明化合物5-甲基苯并噁唑-2-苯基-苯甲酰胺对by4743酵母菌生长曲线斜率的比较图;图6为本发明化合物5-甲基苯并噁唑-2-苯基-苯甲酰胺对果蝇体内sod、cu-zn-sod、cat、mda活性比较图:图6-1为化合物对果蝇体内sod活性的影响图;图6-2为化合物对果蝇体内cu-zn-sod活性的影响图;图6-3为化合物对果蝇体内cat活性的影响图;图6-4为化合物对果蝇体内mda活性的影响图;图7为本发明化合物5-甲基苯并噁唑-2-苯基-苯甲酰胺对果蝇体内cat、mth、cu-zn-sod、mn-sod基因mrna的表达量比较图;图7-1为化合物对果蝇体内cat基因mrna相对表达量影响图;图7-2为化合物对果蝇体内mth基因mrna相对表达量影响图图7-3为化合物对果蝇体内cu-zn-sod基因mrna相对表达量影响图图7-4为化合物对果蝇体内mn-sod基因mrna相对表达量影响图。具体实施方式除有定义外,以下实施例中所用的技术术语具有与本发明所属领域技术人员普遍理解的相同含义。以下实施例中所用的试验试剂,如无特殊说明,均为常规生化试剂;所述实验方法,如无特殊说明,均为常规方法。下面结合实施例及附图来详细说明本发明。实施例1:一种苯并噁唑衍生物及其制备方法,步骤如下:1、制备5-甲基苯并噁唑-2-苯基-3’-胺取100ml单口反应瓶,加入91.7mmol4-甲基邻氨基苯酚、100.9mmol间氨基苯甲酸,然后用玻璃棒搅拌均匀,然后放入强力转子,最后加入110g(32.5mmol)多聚磷酸,置于油浴锅内加热回流。开始加热时,设置温度为110℃,待转子开始很缓慢转动时,再慢慢升高温度至180℃,持续回流反应5h,tlc薄层监测至反应结束。在1l烧杯内加入400ml10%naoh的水溶液,然后加入9g(10.7mmol)nahco3,均匀搅拌,使其完全溶解。将反应液趁热缓缓倒入naoh和nahco3的溶液中,边倒反应液边加入冰块降低体系的温度,最后将体系的ph调到8~9,产生沉淀,用布氏漏斗抽滤,然后将得到的固体小圆饼捣碎,放入真空干燥箱进行干燥。待干燥完毕。再将干燥好的固体粉末溶于乙酸乙酯,过滤掉不溶物,蒸干乙酸乙酯,采用干法装柱,过硅胶柱分离纯化,用乙酸乙酯与石油醚的混合体系进行洗脱,减压浓缩除去溶剂,得到白色固体(15.8g,产率66.4%)。结果分析:将得到的成品进行核磁分析,得图2,结果如下:1hnmr(400mhz,cdcl3/tms)δ:7.635,7.614(d,j=8.4,hz,1h),7.563,7.538(d,j=10.4,hz,2h),7.444,7.423(d,j=8.4hz,1h),7.313-7.274(t,j=8hz,1h),7.160-7.137(dd,j1=8.4hz,j2=1.2h,1h),6.849-6.824(dd,j1=8.4hz,j2=1.2h,1h),3.843(s,2h),2.482(s,3h)。以上结果表明,所得产物为5-甲基苯并噁唑-2-苯基-3’-胺。2、制备化合物5-甲基苯并噁唑-2-苯基-苯甲酰胺取50ml的反应瓶,加入无水乙腈20ml,苯甲酸1.8mmol,良好搅拌溶解后,依次向其中加入0.342g(1.8mmol)对甲苯磺酰氯(tsci)、0.28g(2.7mmol)三乙胺,0.03g(0.25mmol)4-二甲氨基吡啶(dmap),良好搅拌10min后,加入1.5mmol5-甲基苯并噁唑-2-苯基-3’-胺,搅拌均匀后,在40℃条件下回流反应4h,tlc薄层监测反应至结束。反应结束后,在瓶内产生白色沉淀,过滤,tlc薄层监测滤液,滤液成分多为原料,将白色沉淀翻入真空干燥箱进行干燥,得到白色固体,即为5-甲基苯并噁唑-2-苯基-苯甲酰胺。结果分析:进行核磁分析,得图3,结果如下:1hnmr(400mhz,cdcl3/tms)δ:8.387(s,1h),8.028-8.010(m,3h),7.913,7.895(d,j=4.2hz,2h),7.541-7.505(m,5h),7.455,7.435(d,j=8.4hz,1h),7.176-7.155(d,j=8.4hz,1h),2.485(s,3h)。其结构式如下:实施例2:苯并噁唑类化合物对酵母细胞生长活性的影响利用自动微生物生长分析仪(growthcurvesusa,piscataway,ni)测定酵母菌的生长活性,在100孔蜂窝板中分为2组,分别为:①297μlypd培养基、3μlypd菌液、0.3μldmso溶液,作为空白对照组。②297μlypd培养基、3μlypd菌液、0.3μl浓度为0.1m的5-甲基苯并噁唑-2-苯基)-苯甲酰胺dmso溶液。以上均为每孔加入的量,并进行三次平行实验。保持培养温度为30℃,每隔20min在600nm处测定各蜂窝孔中的od值,连续测定23h。结果分析:实验结果如图4所示,加入5-甲基苯并噁唑-2-苯基-苯甲酰胺的by1743酵母菌对数生长期时间推迟,表明5-甲基苯并噁唑-2-苯基-苯甲酰胺可能对by4743酵母菌有抑制作用。图5为酵母菌对数生长期的斜率比较图,明显加药酵母生长缓慢,说明该化合物对酵母生长有一定抑制作用。实施例3:苯并噁唑化合物5-甲基苯并噁唑-2-苯基-苯甲酰胺对果蝇的影响1.果蝇的分组、饲料配比及处理方法分别取2d龄雄性成虫果蝇600只,随机平均分为3组:①空白组:喂食基础饲料。②空油组:喂食添加有溶剂(玉米油)的基础饲料。③给药组:喂食给药饲料(实验药品溶解于玉米油中)。所有实验组每3d更换一次新鲜培养基。每组10管,每管20只果蝇。置于(25±1)℃、相对湿度(50-60)%的恒温恒湿培养箱中饲养30d后,用n2麻醉,放入-80℃冰箱中备用。每组5管取出果蝇,按1:49(mg/ml)加生理盐水,保持4℃、2500r/min离心20min进行匀浆,取上清液测定酶活性。以配置750ml基础饲料为例,加入各组分量为:无水葡萄糖72g,玉米粉72g,干酵母粉10g,琼脂粉6g,加水至750ml,煮熟后晾2分钟,加防腐剂(含1%对羟基苯甲酸乙酯的75%酒精)40ml。添加有溶剂的基础饲料:在基础饲料的基础上,加入0.05ml/ml玉米油。给药饲料:在基础饲料的基础上,加入溶于玉米油(0.05ml/ml)的实验样品(0.2mg/ml)。2.对果蝇体内sod和cu-zn-sod活性的影响利用相应试剂盒分别测定果蝇体内sod和cu-zn-sod活性。从表1、图6-1和图6-2中可见,给药30天后果蝇体内sod和cu-zn-sod活性低于空油组。表1果蝇体内sod和cu-zn-sod活性组别sod(u/mgprot)cu-zn-sod(u/mgprot)空白组477.86±27.86197.72±95.71空油组524.86±8.41267.05±35.52给药组466.87±42.22227.90±33.933.对果蝇体内cat活性的影响利用相应试剂盒测定果蝇体内cat的活性。如表2和图6-3所见,给药30天后果蝇体内cat活性低于空油对照组。表2果蝇体内cat的活性组别cat(u/mgprot)空白组54.53±5.55空油对照组65.25±8.17给药组59.58±12.144.对果蝇体内mda活性的影响利用相应试剂盒测定果蝇体内mda的活性。如表3、图6-4所见,给药30天后果蝇体内mda活性明显低于空油对照组。表3果蝇体内mda的活性组别mda(u/mgprot)空白组7.34±0.78空油对照组8.69±0.45给药组7.37±0.395.对果蝇基因表达水平的影响取-80℃保存的果蝇,每组取五管,trizol法提取mrna,反转录得cdna,-80℃备用。realtime-pcr法检测抗氧化相关基因mrna表达水平。对照rt49分析果蝇cat、mth、cu-zn-sod、mn-sod基因mrna的表达量。如图7以及7-1至7-4所示,结果显示,给药组的果蝇体内cat和mth基因表达明显低于空油组;给药组的果蝇体内cu-zn-sod和mn-sod基因的表达量明显高于空油组。综上,可以看出化合物5-甲基苯并噁唑-2-苯基-苯甲酰胺可以应用在作为沉默信息调节因子抑制剂方面,进一步可以作为抗癌药物进行研究。以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1