基于苝二酰亚胺的化合物和其荧光信号的调控方法、检测生物活性分子的方法及应用与流程
本发明涉及共轭化合物领域,具体涉及基于苝二酰亚胺的化合物和其荧光信号的调控方法、检测生物活性分子的方法及应用。
背景技术
苝二酰亚胺因其化学性质稳定、良好的光热稳定性以及优良的光电性质备受科学家关注。但是由于苝二酰亚胺主环的平面结构,分子间通过π-π堆积和疏水作用相互聚集,它的大部分衍生物只能溶于有机溶剂,因而发展具有良好水分散性的苝二酰亚胺衍生物迫在眉睫。而且目前尚未有水分散性良好、自组装能力突出的苝二酰亚胺衍生物的报道。
自组装行为可以说生物界一种独特和奇妙的现象。实现生物可调控的自组装行为一直以来是科学家的研究热点之一。而多巴胺(da)和5-脱氧氟尿苷(5’dfu)是研究最多的两种生物活性分子,它们的结构如下所示:
如何实现苝二酰亚胺衍生物的自组装行为、荧光信号受生物活性分子(例如多巴胺和5-脱氧氟尿苷)的调控,特别在模拟生物环境中时,是亟需解决的问题。
技术实现要素:
本发明的目的是为了克服现有技术存在的苝二酰亚胺衍生物水分散性差,自组装、荧光行为无法受生物活性分子的调控问题,提供基于苝二酰亚胺的化合物和其荧光信号的调控方法、检测生物活性分子的方法及应用。
为了实现上述目的,本发明第一方面提供了一种基于苝二酰亚胺的化合物,该化合物具有如式ⅰ所示的结构,
其中,ph为取代或未取代的亚苯基,r1具有如式ⅱ或式ⅲ所示的结构,
x为卤素,r2和r3各自独立地选自c1-c8的烷基、c2-c8的烷氧基、c2-c8的烯基、未取代的苯基,m为1-6的整数,在式ⅱ中,n为1-6的整数,在式ⅲ中,k为2-20的整数。
本发明第二方面提供了本发明第一方面所述化合物的荧光信号的调控方法,该方法包括:
(1)将本发明第一方面所述的化合物溶于溶剂中;
(2)向步骤(1)所得体系中加入多巴胺或5-脱氧氟尿苷。
本发明第三方面提供了本发明第一方面所述的化合物用于检测生物活性分子的方法,该方法包括:
(1)将本发明第一方面所述的化合物溶于溶剂中,制成检测液,测试其荧光强度;
(2)将待检测样品加入步骤(1)所述检测液中;
(3)测试步骤(2)所得体系的荧光强度。
本发明第四方面提供了本发明第一方面所述化合物、本发明第二方面所述调控方法、第三方面所述检测方法在分子识别、分子检测、疾病诊断、生物成像及靶向治疗中的应用。
本发明所述的基于苝二酰亚胺的化合物,在水中具有良好的分散性,并且在模拟生物环境中、甚至生理条件下其自组装行为、荧光信号可以受生物活性分子(特别是多巴胺、5-脱氧氟尿苷)的调控。反过来,根据该化合物荧光信号的变化可以检测待测样品中生物活性分子(特别是多巴胺、5-脱氧氟尿苷)的存在,进一步可以根据荧光强度的比值计算出待测样品中生物活性分子的含量,在分子识别、分子检测、疾病诊断、生物成像及靶向治疗中具有很好的应用前景。
附图说明
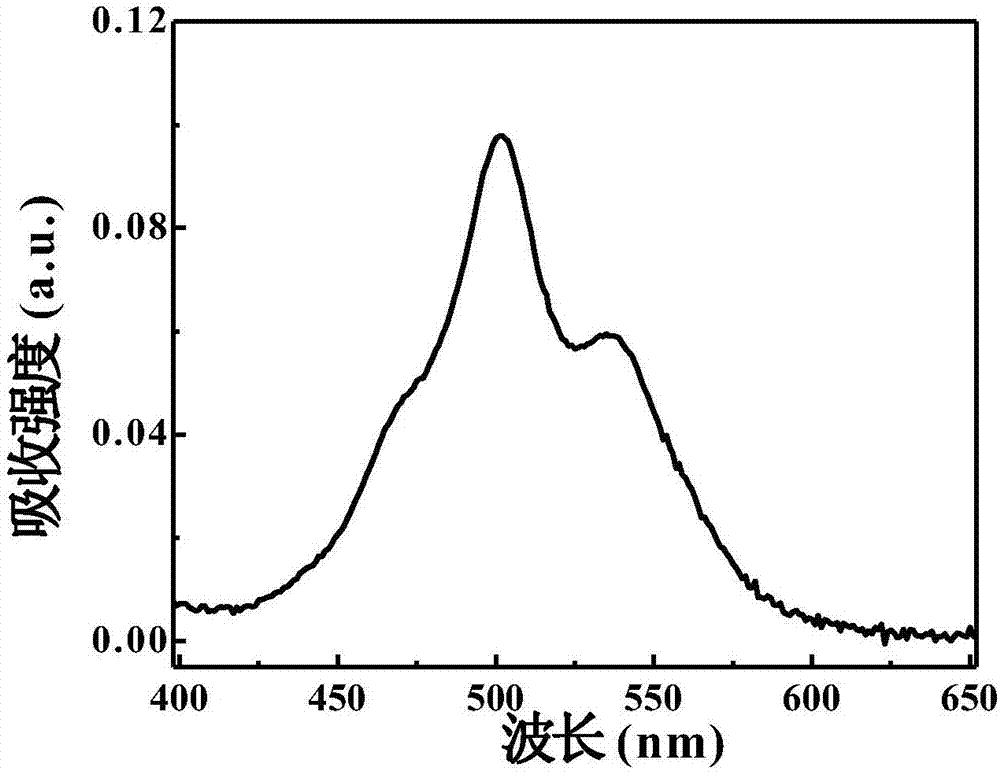
图1是本发明所述化合物1在水中的紫外-可见吸收光谱图(图1-a)和荧光发射光谱图(图1-b)。
图2是本发明所述化合物1的pka测试图。
图3示出了与多巴胺(da)作用后,本发明所述化合物1的“turnoff”型荧光行为,图3-a为本发明所述化合物1与多巴胺(da)作用后的荧光光谱图,图3-b为550nm处加入多巴胺后的荧光强度与原荧光强度的比值随多巴胺(da)浓度的变化图。
图4示出了与5-脱氧氟尿苷(5’dfu)作用后,本发明所述化合物1的“turnon”型荧光行为,图4-a为本发明所述化合物1与5-脱氧氟尿苷(5’dfu)作用后的荧光光谱图,图4-b为550nm处加入5-脱氧氟尿苷后的荧光强度与原荧光强度的比值随5-脱氧氟尿苷(5’dfu)浓度的变化图。
图5为生物活性分子检测的标准曲线图,其中图5-a、图5-b分别对应于多巴胺、5-脱氧氟尿苷。
具体实施方式
在本文中所披露的范围的端点和任何值都不限于该精确的范围或值,这些范围或值应当理解为包含接近这些范围或值的值。对于数值范围来说,各个范围的端点值之间、各个范围的端点值和单独的点值之间,以及单独的点值之间可以彼此组合而得到一个或多个新的数值范围,这些数值范围应被视为在本文中具体公开。
本发明第一方面提供了一种基于苝二酰亚胺的化合物,该化合物具有如式ⅰ所示的结构,
其中,ph为取代或未取代的亚苯基,r1具有如式ⅱ或式ⅲ所示的结构,
x为卤素,r2和r3各自独立地选自c1-c8的烷基、c2-c8的烷氧基、c2-c8的烯基、未取代的苯基,m为1-6的整数,在式ⅱ中,n为1-6的整数,在式ⅲ中,k为2-20的整数。
在本发明中,r2和r3各自独立地选自甲基、乙基、丙基、正丁基、异丁基、正戊基、异戊基、正己基、异己基、正庚基、异庚基、正辛基、异辛基、乙烯基、丙烯基、丁烯基、戊烯基、己烯基、庚烯基、辛烯基、乙氧基、丙氧基、丁氧基、戊氧基、己氧基、庚氧基、辛氧基和未取代的苯基,优选地,r2和r3各自独立地选自c1-c4的烷基、c2-c4的烷氧基或c2-c4的烯基。m可以为1、2、3、4、5或6,优选地m为1-4的整数。
在本发明的一种实施方式中,r1具有如式ⅱ所示的结构,其中n可以为1、2、3、4、5或6,优选地n为1-4的整数。
在本发明的另一种实施方式中,r1具有如式ⅲ所示的结构,其中k可以为2、3、4、5、6、7、8、10、12、15、18或20以及上述任意两个数值所组成范围中的任一整数,优选地k为5-15的整数。
在本发明中,优选地,ph的结构如式ⅳ所示,
在式ⅳ中,波纹表示ph在式i中键连的位置,在式i中ph分别与亚甲基、硼酸基团相连;r4、r5、r6和r7各自独立地选自c1-c6的烷基、c2-c6的烯基、卤素或氢,例如r4、r5、r6和r7可以各自独立地选自氢、甲基、乙基、丙基、正丁基、异丁基、正戊基、异戊基、正己基、异己基、乙烯基、丙烯基、丁烯基、戊烯基、己烯基、氟、氯、溴或碘。
在本发明中,具有式ⅰ所示结构的化合物具有较好的水分散性,并且所述化合物的pka为6-8,其中一些化合物的pka甚至为7.2-7.4。pka处于该范围的本发明所述化合物在生理环境中(ph为7.2-7.4)可以更好地与生物活性分子如多巴胺、5-脱氧氟尿苷相互作用。
在本发明中,所述化合物可以为具有如下结构的化合物,即化合物1-6,
化合物1(pdi-pba):
化合物2:
化合物3:
化合物4:
化合物5:
化合物6:
本发明所述化合物可以根据以下方法来制备,其中r1具有式ⅱ所示结构的化合物可以按照以下方程式1所示的合成流程来制备。
方程式1
其中r1具有式ⅲ所示结构的化合物可以按照以下方程式2所示的合成流程制备。
方程式2
上述方程式1和方程式2所示的制备方法都包括两个反应步骤:酸酐与氨基化合物反应生成苝酰亚胺结构的步骤(1);叔胺与卤代烃反应生成季铵盐的步骤(2)。各步反应的反应条件可以根据现有技术来选择,所需要的原料也可以按照方程式1和2中各原料的通式来选择。所述各反应原料可以通过市售得到或通过实验合成。
本发明所述化合物具有良好的水分散性,其荧光行为可由生物活性分子通过超分子方式调控。
本发明第二方面提供了本发明第一方面所述化合物的荧光信号的调控方法,该方法包括:
(1)将本发明第一方面所述的化合物溶于溶剂中;
(2)向步骤(1)所得体系中加入多巴胺或5-脱氧氟尿苷。
在本发明所述的调控方法中,步骤(1)中,所述溶剂可以常用的溶剂,优选地为极性溶剂,例如可以为水、甲醇、乙醇、水和乙醇的混合物、或缓冲溶液(例如可以为hepes缓冲溶液)。形成的溶液的浓度可以根据需要调整,例如可以为0.1μmol/l、0.2μmol/l、0.5μmol/l、1μmol/l、2μmol/l、5μmol/l、10μmol/l、20μmol/l、50μmol/l、100μmol/l、200μmol/l、500μmol/l等,优选为0.1-10μmol/l。
在本发明所述的调控方法中,在步骤(2)中,当向步骤(1)所得体系中加入多巴胺时,本发明所述化合物与多巴胺的摩尔比为1:(1-50),优选为1:(1-20)。本发明所述化合物与多巴胺接触作用后,荧光猝灭,表现出“turnoff”型荧光行为。
在本发明所述的调控方法中,在步骤(2)中,当向步骤(1)所得体系中加入5-脱氧氟尿苷时,本发明所述化合物与5-脱氧氟尿苷的摩尔比为1:(30-500),优选为1:(40-400)。本发明所述化合物与5-脱氧氟尿苷接触作用后,荧光被打开,表现出“turnon”型荧光行为。
在本发明所述的调控方法中,其中,在步骤(1)和(2)过程中,控制体系ph为7-8,温度为4-37℃。
鉴于以上所述的本发明的化合物对多巴胺或5-脱氧氟尿苷的荧光响应行为,本发明所述化合物可以用于检测未知体系中生物活性分子(具有顺式邻二醇结构的生物活性分子,特别是多巴胺或5-脱氧氟尿苷)的存在。在此所述检测不考虑作用相反的两种生物活性分子同时存在的情况,例如多巴胺和5-脱氧氟尿苷同时存在的情况。
本发明第三方面提供了本发明第一方面所述的化合物用于检测生物活性分子的方法,该方法包括:
(1)将本发明第一方面所述的化合物溶于溶剂中,制成检测液,测试其荧光强度;
(2)将待检测样品加入到步骤(1)所述检测液中;
(3)测试步骤(2)所得体系的荧光强度。
在本发明所述的检测方法中,步骤(1)中,所述溶剂可以根据需要来选择,例如可以为hepes缓冲溶液,制得的检测液中本发明所述化合物的浓度可以根据需要检测的灵敏度来选择,例如可以为0.1-10μmol/l,并测试检测液的荧光强度记为f0。
在本发明所述的检测方法中,优选地,所述生物活性分子为多巴胺或5-脱氧氟尿苷。
在本发明所述的检测方法中,在步骤(2)中,加入待检测样品后,测得体系的荧光强度记为f,若f<f0,则待检测样品中含有多巴胺;若f>f0,则待检测样品中含有5-脱氧氟尿苷。
在本发明所述的检测方法中,当f<f0时,可以根据本发明第二方面所述数据模拟f0/f的比值随多巴胺浓度变化的标准曲线(如图5-a所示),通过该曲线推定待检测样品中多巴胺的含量。
在本发明所述的检测方法中,当f>f0时,可以根据本发明第二方面所述数据模拟f/f0的比值随5-脱氧氟尿苷浓度变化的标准曲线(如图5-b所示),通过该曲线推定待检测样品中5-脱氧氟尿苷的含量。
在本发明所述检测方法的一种实施方式中,检测液中溶剂为hepes缓冲液(ph为7.98),本发明所述化合物的浓度为5μmol/l,该检测液可以分别检测出浓度为0-100μmol/l的多巴胺、浓度为0.6-2.0mmol/l的5-脱氧氟尿苷。
本发明第四方面提供了本发明第一方面所述化合物、本发明第二、第三方面所述方法在分子识别、分子检测、疾病诊断、生物成像及靶向治疗中的应用。
以下将通过实施例对本发明进行详细描述。
实施例中所使用的原料均通过商购获得。
制备例1
按照方程式3所示合成流程制备化合物1(pdi-pba)。
方程式3
将0.785g化合物a(2mmol)分散在30毫升去离子水中,向得到的溶液中加入0.882g化合物b(10mmol)然后升温至100℃反应24小时。反应停止后,用1%氢氧化钾水溶液洗涤后过滤得到滤渣,得到的滤渣经过去离子水洗(50毫升×3次),经真空干燥得到0.82g紫黑色化合物c,产率为77%。
将0.213g化合物c(0.4mmol)溶解在20毫升四氢呋喃中,向得到的溶液中加入0.214g化合物d(1mmol)然后回流反应24小时。反应停止后,将反应液过滤得到滤渣,得到的滤渣经过乙腈(20毫升×3次)和乙醚(20毫升×3次)洗涤后,经真空干燥得到0.35g棕红色固体,产率为90%。
将所得棕红色固体进行核磁氢谱测试(1h-nmr)和质谱测试(hr-ms(esi)),测试结果如下:
1h-nmr(300mhz,d2o-cf3cood,ppm):11.83(d,4h),11.78(d,4h),11.30-10.10(br,8h),7.91(t,4h),7.65(s,4h),6.67(t,4h),6.27(s,12h)。
hr-ms(esi)m/z:[m]2+为401.17,检测到401.17的峰。由上可知,得到棕红色固体为化合物1(pdi-pba)。
制备例2
参照制备例1的方法制备化合物2,对所得产物进行核磁氢谱和质谱测试,结果核磁氢谱图显示所得到的产物具有如式ⅵ所示的结构,ms(esi)m/z:[m]2+为457.23,检测到457.16的峰。由上可知,得到的产物为化合物2。
制备例3
参照制备例1的方法制备化合物3,对所得产物进行核磁氢谱和质谱测试,核磁氢谱图显示所得到的产物具有如式ⅶ所示的结构,ms(esi)m/z:[m]2+为471.25,检测到471.23的峰。由上可知,得到的产物为化合物3。
制备例4
参照制备例1的方法制备化合物4,对所得产物进行核磁氢谱和质谱测试,核磁氢谱图显示所得到的产物具有如式ⅷ所示的结构,ms(esi)m/z:[m]2+为414.68,检测到414.59的峰。由上可知,得到的产物为化合物4。
制备例5
参照制备例1的方法制备化合物5,对所得产物进行核磁氢谱和质谱测试,核磁氢谱图显示所得到的产物具有如式ⅸ所示的结构,hr-ms(esi)m/z:[m]2+为501.25,检测到501.16的峰。由上可知,得到的产物为化合物5。
制备例6
参照制备例1的方法制备化合物6,对所得产物进行核磁氢谱和质谱测试,核磁氢谱图显示所得到的产物具有如式ⅹ所示的结构,hr-ms(esi)m/z:[m]2+为869.45,检测到869.40的峰。由上可知,得到的产物为化合物6。
测试例
1、水分散性
配制5μmol/l化合物1的水溶液,使用紫外可见分光光度仪及荧光分光光度计分别测试体系的紫外可见吸收光谱图和荧光发射光谱图,测试结果如图1所示。
图1显示,化合物1在水中具有较高的紫外吸收强度和荧光强度,说明化合物1在水中的分散性较好。
同理,按照上述方法对化合物2-6进行水分散性的测试,化合物2-6在水中也具有较高的紫外吸收强度和荧光强度,说明化合物2-6在水中的分散性也较好。
2、pka的测试
配制0.25mmol/l化合物1的水溶液,用1mol/l氢氧化钠溶液调节体系ph为12,在25℃恒温下,逐渐滴加少量0.1mol/l盐酸溶液,每次滴加后测试体系的ph值,作图计算得到化合物1的pka值,如图2所示。
由图2计算出化合物1的pka值为7.2±0.1。
3、荧光行为
3.1“turnoff”荧光行为
在hepes缓冲液(ph为7.98)中,配制5μmol/lpdi-pba的溶液,测试荧光光谱,并分别加入5μmol/l、10μmol/l、15μmol/l、20μmol/l、25μmol/l、30μmol/l、35μmol/l、40μmol/l、45μmol/l、50μmol/l、55μmol/l、60μmol/l、65μmol/l、70μmol/l、75μmol/l、80μmol/l、85μmol/l、90μmol/l、95μmol/l、100μmol/l多巴胺,测试体系的荧光光谱,所测荧光图谱如图3-a所示,并读取550nm处的荧光强度值,计算加入多巴胺后的荧光强度f与原荧光强度f0的比值,制作该比值随多巴胺浓度的变化图,结果如图3-b所示。
3.2“turnon”荧光行为
在hepes缓冲液(ph为7.98)中,配制5μmol/lpdi-pba的溶液,测试荧光光谱,并分别加入0.2mmol/l、0.4mmol/l、0.6mmol/l、0.8mmol/l、1.0mmol/l、1.2mmol/l、1.4mmol/l、1.6mmol/l、1.8mmol/l、2.0mmol/l5-脱氧氟尿苷,测试体系的荧光光谱,所测荧光图谱如图4-a所示,并读取550nm处的荧光强度值,计算加入5-脱氧氟尿苷后的荧光强度f与原荧光强度f0的比值,制作该比值随5-脱氧氟尿苷浓度的变化图,结果如图4-b所示。
由图3-a、图3-b和图4-a、图4-b可知,本发明所述化合物1与多巴胺(da)作用后,荧光强度变小,荧光被猝灭,表现出“turnoff”型荧光行为;而与抗癌药物5-脱氧氟尿苷(5’dfu)作用后,荧光强度变大,荧光被打开,表现出“turnon”型荧光行为。
类似地,按照上述方法测试多巴胺、5-脱氧氟尿苷对化合物2-6的荧光行为的影响,结果显示本发明所述化合物2-6与多巴胺(da)作用后,荧光强度变小,荧光被猝灭,表现出“turnoff”型荧光行为;而与抗癌药物5-脱氧氟尿苷(5’dfu)作用后,荧光强度变大,荧光被打开,表现出“turnon”型荧光行为。
4.生物活性分子的检测
对图3-b和图4-b所示的测试数据进行模拟,分别制作图5-a和图5-b,作为生物活性分子检测的标准曲线。图5-a显示在0-100μmol/浓度范围内比值f0/f与多巴胺浓度具有良好的线性关系,工作曲线为y=0.04242x+0.8012(r2=0.9949);图5-b显示在0.6-2.0mmol/l范围内比值f/f0与5-脱氧氟尿苷浓度具有良好的线性关系,工作曲线为y=0.90139x+1.9685(r2=0.99447)。
在hepes缓冲液(ph为7.98)中配制5μmol/l的pdi-pba溶液,取出2ml作为检测液,测试检测液500nm处的荧光强度记为f0。取适量体积的待检测样品置于上述检测液中,混合均匀,测试体系500nm处的荧光强度记为f。
测试结果:若f/f0<1,则待检测样品中含有多巴胺;
若f/f0>1,则待检测样品中含有5-脱氧氟尿苷。
当f/f0<1时,根据计算的f0/f值,参考图5-a所示标准曲线推得多巴胺的浓度;当f/f0>1时,根据计算的f/f0值,参考图5-b所示的标准曲线,推得5-脱氧氟尿苷的浓度。通过多巴胺或5-脱氧氟尿苷的浓度从而计算得到待检测样品中多巴胺或5-脱氧氟尿苷的含量。
以上详细描述了本发明的优选实施方式,但是,本发明并不限于此。在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,包括各个技术特征以任何其它的合适方式进行组合,这些简单变型和组合同样应当视为本发明所公开的内容,均属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!