一种环硫化合物及其制备方法与流程
本发明属于精细化工技术领域,具体涉及一种环硫化合物及其制备方法。
背景技术:
环硫化合物,即为环氧基团中氧原子被硫原子取代形成环硫环的一类化合物。该化合物有着与环氧化合物一样优异的综合性能,同时又有着其独特的特点。环硫化合物中碳硫键的极性小,环硫基团的电子云密度低,造成环硫基团的亲电性弱,亲核性强,可以与亲核试剂发生反应,生成各种不同类型的化合物。并且环硫化合物具有较高的活性,在加热时或者有硫酸、氨水等催化剂存在时极易开环,开环后的硫离子更稳定更容易引发聚合反应。环硫官能团还能同铜、铁等金属发生反应,产生较强的粘结性能。此外,环硫化合物中由于含有硫元素而具有较高的折光指数,因此可以用来制造具有较好物理性能的光学材料。环硫化合物因其独特的性质,在合成上方便简单,原料易得,还常被应用在医药、聚合物、除草剂等领域,也常在橡胶中添加,用作橡胶交联促进剂等。这些特性赋予了环硫化合物在人们的生产生活中扮演着重要的角色,因此对于其合成与应用的研究具有十分重要的现实意义。
环硫化合物的研究是最早从二十世纪二十年代开始。1920年,delepine首次合成出纯净的硫杂环丙烷硫化物,并发现这种化合物反应活性较高,易与各种物质反应,于是这类化合物开始受到人们的重视。在1934年,dachlauer和jjachel进行烯烃氧化物与硫氰酸盐或硫脲反应的实验,发现这种方法制备环硫化合物的方法较为简便,并使之付诸于工业化生产。关于环硫化合物最重要的科学知识源于culvenor和davies在1949至1952年间对于环硫化合物进行了充分地研究有了更加深入的认识。从二十世纪五十年代开始,在世界各国掀起了对环硫化合物的研究热潮,各个国家的学者相继发表关于硫杂环丙烷的制备、反应与性能的文献,对环硫化合物的研究越来越深入。
文献报道的有关环硫化合物制备的方法很多。目前可以用来制备环硫化合物的原料化合物包括:环氧化合物、卤代硫氰酸酯、羟烷基氯化物、环酯类化合物、羟基硫醇及其衍生物、烯烃、卤代硫醇、硫酮等。尽管环硫化合物的合成方法众多,其中应用最为普遍的合成方法是通过环氧化合物作为原料进行制备,主要反应为环氧化合物中的氧硫交换反应。但是在以往报道的文献中,采用的都是两步法,先制得环氧化合物纯化之后在进行硫取代反应,不仅操作步骤多,而且需要的时间比较长。
随着对环硫化合物的深入研究,在合成方法上也不断的做出改进,许多研究者针对环氧基团环硫化反应的催化剂和反应溶剂进行研究,缩短了反应时间,提高了转化率。如路易斯酸催化剂bi(tfa)3、bi(otf)3、tio(cf3so3)2和ticl3(cf3so3)、al(ds)3·3h2o、sniv(tpp)(bf4)2等,这些催化剂催化效果较好,但在后处理上这些酸很难分离。贵金属如钯、铱、钌等贵金属的配合物作为催化剂也被用来合成环硫化合物,这些催化剂虽然具有反应活性高,产物的选择性好等特点,但是因为成本的原因限制了其推广和应用。
技术实现要素:
本发明的目的在于克服上述现有技术的缺点,提供一种环硫化合物及其制备方法;该方法采用“一锅法”合成一种环硫化合物,制备方法高效,操作简单,制备出的硫化物可以与亲核试剂、亲电试剂及自由基反应,生成各种不同类型的化合物。
为达到上述目的,本发明采用以下技术方案予以实现:
一种环硫化合物的制备方法,包括以下步骤:
步骤1,混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮和无水乙醇,搅拌均匀后得到溶液a;
步骤2,将naoh水溶液加入至溶液a中,搅拌均匀后得到溶液b;
步骤3,在溶液b中加入h2o2,反应后制得溶液c;
步骤4,向溶液c中加入甲苯溶剂,混合均匀后得到溶液e;
步骤5,混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,混合溶液d和溶液e,反应后得到反应液f;
步骤7,将步骤6制得的反应液f静置分层后合并有机相;
步骤8,步骤7中的有机相依次通过nacl溶液和蒸馏水洗涤,洗涤后通过无水硫酸镁干燥过夜,过滤后蒸除过滤产物中的甲苯后制得浅黄色透明油状液体,为所述环硫化合物。
本发明的进一步改进在于:
优选的,1-(2-呋喃基)-3-苯基-2-丙烯-1-酮和无水乙醇的混合比例为(3-4)g:25ml。
优选的,步骤2中,naoh水溶液的浓度为1-3mol/l,naoh水溶液的加入量为15ml。
优选的,步骤3中,溶液b和h2o2的反应温度为5-45℃,反应时间为1-6h。
优选的,步骤3中,溶液b中h2o2的加入量为5-25ml,h2o2通过恒压滴液漏斗加入至溶液b中。
优选的,步骤4中,溶液c中甲苯溶剂的加入量为20-50ml。
优选的,步骤5中,硫脲和水的混合比例为(1-8)g:25ml。
优选的,步骤6中,溶液d通过恒压滴液漏斗加入至溶液e中,混合后反应温度为15-55℃,反应时间为1-7h。
优选的,步骤8中,有机相分别通过nacl溶液和蒸馏水各清洗3次;过滤产物中甲苯的蒸除温度为80℃。
一种通过上述任意一项制备方法制得的环硫化合物,所述环硫化合物为浅黄色透明油状液体,化学结构式为:
所述环硫化合物的分子量为230。
与现有技术相比,本发明具有以下有益效果:
本发明公开了一种环硫化合物的制备方法:该方法中所用的氢氧化钠、乙醇、纯净水等来源广泛,生产成本低。本发明采用“一锅法”在多组分下连续发生两步反应合成了一种环硫化合物,首先通过1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(fpto)与h2o2进行环氧化反应,得到环氧化合物中间体,再以硫脲为硫化剂进行反应,反应过程包括环氧基团开环,碳原子环的walden转变,使得硫原子取代氧原子,最终完成环硫环闭环这几个阶段,得到一种环硫化合物。其中以过氧化氢作为氧化剂发生环氧化反应得到环氧化合物中间体,环境友好,具有高单位重量氧化效率;再以硫脲为硫化剂合成一种环硫化合物,避免分离提纯中间体,与现有分步合成方法相比,本方法反应具有操作简单、易分离纯化(只需通过蒸除多余溶剂即可)、高效性和环境友好等特点。
本发明还公开了一种环硫化合物,该化合物不但具有独特的三元环结构,致使其化学性质和烯烃的c=c双键有很多相似之处,可以与亲核试剂、亲电试剂及自由基反应,生成各种不同类型的化合物。而且引入硫原子,使其具有较高的折光率,这种特性在光学材料中的应用前景较为广阔。另一方面,硫原子容易与惰性金属反应生成化学键,在铜、金等惰性金属表面起到粘接作用。与环氧化合物中间体相比,环硫环具有更大的键长,键角与更小的张力能,更容易进行开环反应,开环后生成巯基,巯基具有更多的可设计性和更高的反应活性,为分子结构设计、应用领域带来新的可能和前景。
【附图说明】
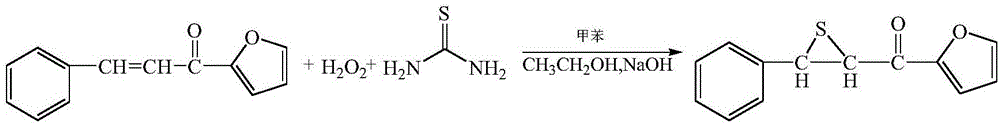
图1为本发明中制备环硫化合物的反应原理图;
图2为本发明中实施例1制得的环硫化合物的傅里叶红外示意图。
【具体实施方式】
下面结合附图、具体实施例和步骤对本发明做进一步详细描述,本发明公开了一种环硫化合物及其制备方法,具体的制备方法包括以下步骤:
步骤1,按照比例(3-4)g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为1-3mol/l的naoh水溶液;在混合溶液a中加入15ml的naoh水溶液,搅拌均匀后得到溶液b;
步骤3,取h2o25-25ml,置于恒压滴液漏斗汇总,通过恒压滴液漏斗滴加至溶液b中;滴加完毕后,整个反应体系在5-45℃反应1-6h后制得溶液c;
步骤4,向溶液c中加入20-50ml的甲苯溶剂,混合均匀后得到溶液e;
步骤5,按照比例(1-8)g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合完成后在15-55℃反应1-7h,得到反应液f;
步骤7,将步骤6制得的反应液f倾入分液漏斗中,静置分层,合并有机相。
步骤8,步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次后用无水硫酸镁干燥过夜,过滤,将过滤产物在80℃通过旋转仪旋转蒸除溶剂甲苯,得到浅黄色透明油状液体,即为一种环硫化合物,其化学结构式为:
其中,分子量为230。
参见图1,为本发明的反应原理图。本发明采用“一锅法”在多组分下连续发生两步反应合成了一种环硫化合物,首先通过1-(2-呋喃基)-3-苯基-2-丙烯-1-酮与h2o2发生环氧化反应得到环氧化合物中间体,再以硫脲为硫化剂进行反应,反应过程包括环氧基团开环,碳原子环的walden转变,使得硫原子取代氧原子,最终完成环硫环闭环这几个阶段,得到一种环硫化合物。本发明合成的环硫化合物,不但具有独特的三元环结构,致使其化学性质和烯烃的c=c双键有很多相似之处,可以与亲核试剂、亲电试剂及自由基反应,生成各种不同类型的化合物。而且引入硫原子,使其具有较高的折光率,这种特性在光学材料中的应用前景较为广阔。另一方面,硫原子容易与惰性金属反应生成化学键,在铜、金等惰性金属表面起到粘接作用。与环氧化合物中间体相比,环硫环具有更大的键长,键角与更小的张力能,更容易进行开环反应,开环后生成巯基,巯基具有更多的可设计性和更高的反应活性,为分子结构设计、应用领域带来新的可能和前景。
图2为环硫化合物的红外示意图。从图中可以看出,与原料相比,3331cm-1为环烷烃的伸缩振动峰,2800-3100cm-1为不饱和c-h的伸缩振动峰,1690cm-1为羰基的特征伸缩振动峰,1564cm-1,1463cm-1为苯环的骨架振动吸收峰,1404cm-1为苯环上c-h键的面内弯曲振动峰,1265cm-1,1162cm-1,1015cm-1为呋喃环上醚键c-o-c的伸缩振动峰,882cm-1为呋喃环中的碳碳双键上的c-h键的面外弯曲振动,760cm-1,695cm-1为苯环c-h面外弯曲振动,证明苯环取代基为单取代,628cm-1为环硫环特征吸收峰,说明环硫化合物结构与预期相符。
实施例1
步骤1,按照比例3.96g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o215ml,置于恒压滴液漏斗中,滴加完毕后,温度在25℃下反应4h后制得溶液c
步骤4,向溶液c中加入25ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例3.04g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在45℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
该实施例制备出的环硫化合物的红外示意图如图2所示。
实施例2
步骤1,按照比例3.96g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o215ml,置于恒压滴液漏斗中,滴加完毕后,温度在25℃下反应3h后制得溶液c
步骤4,向溶液c中加入25ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例3.04g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在45℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例3
步骤1,按照比例3.96g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o215ml,置于恒压滴液漏斗中,完毕后,温度在25℃下反应5h后制得溶液c
步骤4,向溶液c中加入25ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例3.04g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在45℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例4
步骤1,按照比例3.2g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取20mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o215ml,置于恒压滴液漏斗中,完毕后,温度在15℃下反应2h后制得溶液c;
步骤4,向溶液c中加入30ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例2g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在20℃反应3h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例5
步骤1,按照比例3.3g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o28ml,置于恒压滴液漏斗中,完毕后,温度在35℃下反应4h后制得溶液c;
步骤4,向溶液c中加入35ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例3.5g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在25℃反应5h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例6
步骤1,按照比例3.5g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o212ml,置于恒压滴液漏斗中,完毕后,温度在20℃下反应4h后制得溶液c;
步骤4,向溶液c中加入40ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例4g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在30℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例7
步骤1,按照比例3.6g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o218ml,置于恒压滴液漏斗中,完毕后,温度在27℃下反应4h后制得溶液c;
步骤4,向溶液c中加入45ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例5g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在40℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例8
步骤1,按照比例3.8g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为1mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o220ml,置于恒压滴液漏斗中,完毕后,温度在30℃下反应4h后制得溶液c
步骤4,向溶液c中加入42ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例6g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在50℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例9
步骤1,按照比例3.9g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为3mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o222ml,置于恒压滴液漏斗中,完毕后,温度在35℃下反应4h后制得溶液c;
步骤4,向溶液c中加入45ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例7g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在52℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例10
步骤1,按照比例3.96g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o215ml,置于恒压滴液漏斗中,完毕后,温度在25℃下反应4h后制得溶液c;
步骤4,向溶液c中加入25ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例3.04g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在35℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例11
步骤1,按照比例3.96g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o215ml,置于恒压滴液漏斗中,完毕后,温度在25℃下反应4h后制得溶液c;
步骤4,向溶液c中加入25ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例3.04g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在55℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例12
步骤1,按照比例3.96g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为2mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o215ml,置于恒压滴液漏斗中,完毕后,温度在25℃下反应4h后制得溶液c
步骤4,向溶液c中加入25ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例1.52g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在45℃反应4h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例13
步骤1,按照比例3g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为1mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o25ml,置于恒压滴液漏斗中,完毕后,温度在20℃下反应5h后制得溶液c
步骤4,向溶液c中加入20ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例1g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在15℃反应1h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
实施例14
步骤1,按照比例4g:25ml在三口烧瓶中混合1-(2-呋喃基)-3-苯基-2-丙烯-1-酮(c13h10o2)和无水乙醇,用电动搅拌器搅拌均匀后得到混合溶液a;
步骤2,将naoh溶于纯净水中,制备浓度为3mol/l的naoh水溶液,取15mlnaoh水溶液加入溶液a中,搅拌均匀后得到溶液b;
步骤3,取h2o225ml,置于恒压滴液漏斗中,完毕后,温度在45℃下反应1h后制得溶液c
步骤4,向溶液c中加入50ml甲苯溶剂,混合均匀后得到溶液e;
步骤5,制备硫脲水溶液,按照比例8g:25ml混合硫脲和水,在超声波清洗器中震荡溶解后得到溶液d;
步骤6,将溶液d用恒压滴液漏斗滴加入溶液e中,混合后在55℃反应7h,得到反应液f。
步骤7,将步骤6制得的反应液倾入分液漏斗中,静置分层,合并有机相。
步骤8,将步骤7中的有机相用1mol/lnacl溶液洗涤3次,再用蒸馏水洗涤3次,然后用无水硫酸镁干燥过夜,过滤,在80℃下旋转蒸除溶剂甲苯,得到浅黄色透明油状液体。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!