用于光电器件的有机分子的制作方法
用于光电器件的有机分子
[0001]
本发明涉及有机分子及其在有机发光二极管(oled)和其他光电器件中的用途。
[0002]
描述
[0003]
本发明的一个目的是提供适用于光电器件的分子。
[0004]
该目的通过本发明实现,本发明提供了一类新的有机分子。
[0005]
本发明的有机分子优选是纯有机分子,即它们不包含任何金属离子,这与已知用于光电器件中的金属络合物相反。因此,根据本发明,优选有机分子不含金属原子或金属离子。然而,根据现代定义,纯有机分子可以包括准金属,特别是b和si,或者特别是sn、se和ge。
[0006]
根据本发明,所述有机分子在蓝色、天蓝色或绿色光谱范围内表现出发射最大值。有机分子尤其表现出在420nm和520nm之间,在440nm和495nm之间或在450nm和470nm之间的发射最大值。特别地,根据本发明的有机分子的光致发光量子产率为20%或更高。根据本发明的分子尤其显示出热激活的延迟荧光(tadf)。在光电器件中,例如在有机发光二极管(oled)中使用根据本发明的分子使得器件的效率更高。相应的oled具有比具有已知发射体材料和相当颜色的oled更高的稳定性。
[0007]
本发明的有机发光分子包含或由以下部分组成:第一化学部分,该第一化学部分包含式i的结构或由式i的结构组成,
[0008][0009]
以及
[0010]-三个第二化学部分,它们各自独立地于彼此地包含式ii的结构或由式ii的结构组成,
[0011][0012]
其中第一化学部分通过单键连接至三个第二化学部分中的每个。
[0013]
t是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,或者
是r1。
[0014]
v是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,或者是r1。
[0015]
w是cn。
[0016]
x是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,或者是r1。
[0017]
y是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,或者是r1。
[0018]
r
t
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点。
[0019]
r
v
是r
i
。
[0020]
r
w
是r
i
。
[0021]
r
x
是cn。
[0022]
r
y
是r
i
。
[0023]
#表示将所述第二化学部分连接至所述第一化学部分的单键的结合位点;
[0024]
z在每次出现时彼此独立地选自直接键、cr3r4、c=cr3r4、c=o、
[0025]
c=nr3、nr3、o、sir3r4、s、s(o)和s(o)2;
[0026]
r1在每次出现时彼此独立地选自:
[0027]
氢,
[0028]
氘,
[0029]
c
1-c
5-烷基,
[0030]
其中一个或多个氢原子任选地被氘取代;
[0031]
c
2-c
8-烯基,
[0032]
其中一个或多个氢原子任选地被氘取代;
[0033]
c
2-c
8-炔基,
[0034]
其中一个或多个氢原子任选地被氘取代;和
[0035]
c
6-c
18-芳基,
[0036]
其任选地被一个或多个取代基r6取代。
[0037]
r
i
在每次出现时彼此独立地选自:
[0038]
氢,
[0039]
氘,
[0040]
c
1-c
5-烷基,
[0041]
其中一个或多个氢原子任选地被氘取代;
[0042]
c
2-c
8-烯基,
[0043]
其中一个或多个氢原子任选地被氘取代;
[0044]
c
2-c
8-炔基,
[0045]
其中一个或多个氢原子任选地被氘取代;和
[0046]
c
6-c
18-芳基,
[0047]
其任选地被一个或多个取代基r6取代。
[0048]
r
a
、r3和r4在每次出现时彼此独立地选自氢、氘、n(r5)2、or5、si(r5)3、b(or5)2、
oso2r5、cf3、cn、f、br、i,
[0049]
c
1-c
40-烷基,
[0050]
其任选地被一个或多个取代基r5取代并且
[0051]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0052]
c
1-c
40-烷氧基,
[0053]
其任选地被一个或多个取代基r5取代并且
[0054]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0055]
c
1-c
40-硫代烷氧基,
[0056]
其任选地被一个或多个取代基r5取代并且
[0057]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0058]
c
2-c
40-烯基,
[0059]
其任选地被一个或多个取代基r5取代并且
[0060]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0061]
c
2-c
40-炔基,
[0062]
其任选地被一个或多个取代基r5取代并且
[0063]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0064]
c
6-c
60-芳基,
[0065]
其任选地被一个或多个取代基r5取代;和
[0066]
c
3-c
57-杂芳基,
[0067]
其任选地被一个或多个取代基r5取代。
[0068]
r5在每次出现时彼此独立地选自氢、氘、n(r6)2、or6、si(r6)3、b(or6)2、oso2r6、cf3、cn、f、br、i,
[0069]
c
1-c
40-烷基,
[0070]
其任选地被一个或多个取代基r6取代并且
[0071]
其中一个或多个不相邻的ch
2-基团任选地被r6c=cr6、c≡c、si(r6)2、ge(r6)2、sn(r6)2、c=o、c=s、c=se、c=nr6、p(=o)(r6)、so、so2、nr6、o、s或conr6取代;
[0072]
c
1-c
40-烷氧基,
[0073]
其任选地被一个或多个取代基r6取代并且
[0074]
其中一个或多个不相邻的ch
2-基团任选地被r6c=cr6、c≡c、si(r6)2、ge(r6)2、sn(r6)2、c=o、c=s、c=se、c=nr6、p(=o)(r6)、so、so2、nr6、o、s或conr6取代;
[0075]
c
1-c
40-硫代烷氧基,
[0076]
其任选地被一个或多个取代基r6取代并且
[0077]
其中一个或多个不相邻的ch
2-基团任选地被r6c=cr6、c≡c、si(r6)2、ge(r6)2、sn(r6)2、c=o、c=s、c=se、c=nr6、p(=o)(r6)、so、so2、nr6、o、s或conr6取代;
[0078]
c
2-c
40-烯基,
[0079]
其任选地被一个或多个取代基r6取代并且
[0080]
其中一个或多个不相邻的ch
2-基团任选地被r6c=cr6、c≡c、si(r6)2、ge(r6)2、sn(r6)2、c=o、c=s、c=se、c=nr6、p(=o)(r6)、so、so2、nr6、o、s或conr6取代;
[0081]
c
2-c
40-炔基,
[0082]
其任选地被一个或多个取代基r6取代并且
[0083]
其中一个或多个不相邻的ch
2-基团任选地被r6c=cr6、c≡c、si(r6)2、ge(r6)2、sn(r6)2、c=o、c=s、c=se、c=nr6、p(=o)(r6)、so、so2、nr6、o、s或conr6取代;
[0084]
c
6-c
60-芳基,
[0085]
其任选地被一个或多个取代基r6取代;和
[0086]
c
3-c
57-杂芳基,
[0087]
其任选地被一个或多个取代基r6取代。
[0088]
r6在每次出现时均彼此独立地选自氢、氘、oph(ph=苯基)、cf3、cn、f,
[0089]
c
1-c
5-烷基,
[0090]
其中任选地一个或多个氢原子彼此独立地被氘、cn、cf3或f取代;
[0091]
c
1-c
5-烷氧基,
[0092]
其中任选地一个或多个氢原子彼此独立地被氘、cn、cf3或f取代;
[0093]
c
1-c
5-硫代烷氧基,
[0094]
其中任选地一个或多个氢原子彼此独立地被氘、cn、cf3或f取代;
[0095]
c
2-c
5-烯基,
[0096]
其中任选地一个或多个氢原子彼此独立地被氘、cn、cf3或f取代;
[0097]
c
2-c
5-炔基,
[0098]
其中任选地一个或多个氢原子彼此独立地被氘、cn、cf3或f取代;
[0099]
c
6-c
18-芳基,
[0100]
其任选地被一个或多个c
1-c
5-烷基取代基取代;
[0101]
c
3-c
17-杂芳基,
[0102]
其任选地被一个或多个c
1-c
5-烷基取代基取代;
[0103]
n(c
6-c
18-芳基)2,
[0104]
n(c
3-c
17-杂芳基)2;和
[0105]
n(c
3-c
17-杂芳基)(c
6-c
18-芳基)。
[0106]
取代基r
a
、r3、r4或r5彼此独立地可任选地与一个或多个取代基r
a
、r3、r4或r5形成单环或多环、脂环、芳环和/或苯并稠环系。
[0107]
根据本发明,精确地选自t、v、x和y的两个取代基代表连接第一化学部分和三个第二化学部分中的一个的单键的结合位点。
[0108]
在本发明的一个实施方案中,第一化学部分包含式ia的结构或由式ia的结构组成:
[0109][0110]
其中r
i
和r1如上文所定义,
[0111]
t
##
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,或者是r1,
[0112]
v
##
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,或者是r1,
[0113]
x
##
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,或者是r1,
[0114]
r
t
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,
[0115]
其中精确地选自x
##
、v
##
和t
##
的两个取代基代表连接第一化学部分和三个第二化学部分中的一个的单键的结合位点。
[0116]
在本发明的一个实施方案中,第一化学部分包含式iaa的结构或由式iaa的结构组成:
[0117][0118]
其中r
i
和r1如上文所定义,
[0119]
t
#
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,
[0120]
v
#
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,
[0121]
r
t
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点。
[0122]
在本发明的一个实施方案中,第一化学部分包含式iaaa的结构或由式iaaa的结构组成:
[0123][0124]
其中r
i
和r1如上文所定义,
[0125]
x
#
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,
[0126]
v
#
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点,
[0127]
r
t
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点。
[0128]
在一个实施方案中,r1和r
i
在每次出现时彼此独立地选自氢(h)、甲基、均三甲苯基、甲苯基和苯基(ph)。术语甲苯基是指2-甲苯基、3-甲苯基和4-甲苯基。
[0129]
在一个实施方案中,r1和r
i
在每次出现时彼此独立地选自氢(h)和苯基。
[0130]
在一个实施方案中,r1和r
i
在每次出现时都是氢(h)。
[0131]
在一个实施方案中,t、v和r
t
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点。
[0132]
在一个实施方案中,v、x和r
t
是将第一化学部分连接至三个第二化学部分中的一个的单键的结合位点。
[0133]
在本发明的另一个实施方案中,三个第二化学部分中的每个在每次出现时彼此独立地包含式iia的结构或由式iia的结构组成:
[0134][0135]
式iia
[0136]
其中#和r
a
如上文所定义。
[0137]
在本发明的另一个实施方案中,r
a
在每次出现时彼此独立地选自:h,
[0138]
me,
[0139]
i
pr,
[0140]
t
bu,
[0141]
cn,
[0142]
cf3,
[0143]
ph,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代,
[0144]
吡啶基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基
取代,
[0145]
嘧啶基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代,
[0146]
咔唑基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代,
[0147]
三嗪基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代,
[0148]
和n(ph)2。
[0149]
在本发明的另一个实施方案中,r
a
在每次出现时彼此独立地选自:h,
[0150]
me,
[0151]
i
pr,
[0152]
t
bu,
[0153]
cn,
[0154]
cf3,
[0155]
ph,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代,
[0156]
吡啶基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代,
[0157]
嘧啶基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代,
[0158]
三嗪基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代。
[0159]
在本发明的另一个实施方案中,r
a
在每次出现时彼此独立地选自:h,
[0160]
me,
[0161]
t
bu,
[0162]
ph,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代,
[0163]
三嗪基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代。
[0164]
在本发明的另一个实施方案中,r
a
在每次出现时为h。
[0165]
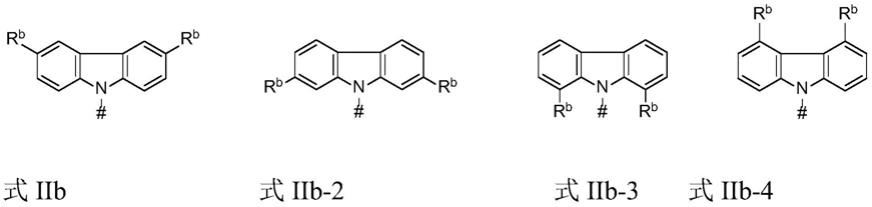
在本发明的另一个实施方案中,在每次出现时彼此独立的三个第二化学部分包含或由式iib的结构、式iib-2的结构、式iib-3的结构或iib-4的结构组成:
[0166][0167]
其中
[0168]
r
b
在每次出现时彼此独立地选自:
[0169]
h,
[0170]
氘,
[0171]
n(r5)2,
[0172]
or5,
[0173]
si(r5)3,
[0174]
b(or5)2,
[0175]
oso2r5,
[0176]
cf3,
[0177]
cn,
[0178]
f,
[0179]
br,
[0180]
i,
[0181]
c
1-c
40-烷基,
[0182]
其任选地被一个或多个取代基r5取代并且
[0183]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0184]
c
1-c
40-烷氧基,
[0185]
其任选地被一个或多个取代基r5取代并且
[0186]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0187]
c
1-c
40-硫代烷氧基,
[0188]
其任选地被一个或多个取代基r5取代并且
[0189]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0190]
c
2-c
40-烯基,
[0191]
其任选地被一个或多个取代基r5取代并且
[0192]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0193]
c
2-c
40-炔基,
[0194]
其任选地被一个或多个取代基r5取代并且
[0195]
其中一个或多个不相邻的ch
2-基团任选地被r5c=cr5、c≡c、si(r5)2、ge(r5)2、sn(r5)2、c=o、c=s、c=se、c=nr5、p(=o)(r5)、so、so2、nr5、o、s或conr5取代;
[0196]
c
6-c
60-芳基,
[0197]
其任选地被一个或多个取代基r5取代;和
[0198]
c
3-c
57-杂芳基,
[0199]
其任选地被一个或多个取代基r5取代。
[0200]
除此之外,前述定义适用。
[0201]
在本发明的另一个实施方案中,在每次出现时彼此独立的三个第二化学部分包含
或由式iic的结构、式iic-2的结构、式iic-3的结构或式iic-4的结构组成:
[0202][0203]
其中前述定义适用。
[0204]
在本发明的另一个实施方案中,r
b
在每次出现时彼此独立地选自:
[0205]
h,
[0206]
me,
[0207]
i
pr,
[0208]
t
bu,
[0209]
cn,
[0210]
cf3,
[0211]
ph,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0212]
吡啶基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0213]
咔唑基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0214]
三嗪基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0215]
和n(ph)2。
[0216]
在本发明的另一个实施方案中,r
b
在每次出现时彼此独立地选自:
[0217]
h,
[0218]
me,
[0219]
i
pr,
[0220]
t
bu,
[0221]
cn,
[0222]
cf3,
[0223]
ph,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0224]
吡啶基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0225]
嘧啶基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;以及
[0226]
三嗪基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代。
[0227]
在本发明的另一个实施方案中,r
b
在每次出现时彼此独立地选自:
[0228]
h,
[0229]
me,
[0230]
t
bu,
[0231]
ph,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0232]
三嗪基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代。
[0233]
以下显示了第二化学部分的实例:
[0234]
[0235]
[0236][0237]
其中对于#、z、r
a
、r3、r4和r5而言,前述定义适用。
[0238]
在一个实施方案中,r
a
和r5在每次出现时彼此独立地选自氢(h)、甲基(me)、异丙基(ch(ch3)2)(
i
pr)、叔丁基(
t
bu)、苯基(ph)、cn、cf3和二苯胺(nph2)。
[0239]
在本发明的另一个实施方案中,三个第二化学部分在每次出现时是相同的。
[0240]
在本发明的另一个实施方案中,三个第二化学部分中的至少两个是相同的。
[0241]
在本发明的一个实施方案中,有机分子包含式iii的结构或由式iii的结构组成:
[0242][0243]
其中前述定义适用。
[0244]
在本发明的另一个实施方案中,有机分子包含式iiia的结构或由式iiia的结构组成:
[0245][0246]
其中
[0247]
r
c
在每次出现时彼此独立地选自:
[0248]
h,
[0249]
me,
[0250]
i
pr,
[0251]
t
bu,
[0252]
ph,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0253]
吡啶基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0254]
嘧啶基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0255]
咔唑基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0256]
三嗪基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;
[0257]
和n(ph)2。
[0258]
在本发明的另一个实施方案中,有机分子包含式iiib的结构或由式iiib的结构组成:
[0259][0260]
其中前述定义适用。
[0261]
在本发明的一个实施方案中,有机分子包含式iv的结构或由式iv的结构组成:
[0262][0263]
其中前述定义适用。
[0264]
在本发明的另一个实施方案中,有机分子包含式iva的结构或由式iva的结构组成
[0265][0266]
其中前述定义适用。
[0267]
在本发明的另一个实施方案中,有机分子包含选自式ivb的结构或由选自式ivb的结构组成:
[0268][0269]
其中前述定义适用。
[0270]
在本发明的一个实施方案中,r
c
在每次出现时彼此独立地选自:
[0271]
h,
[0272]
me,
[0273]
i
pr,
[0274]
t
bu,
[0275]
ph,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代;以及
[0276]
三嗪基,其任选地被一个或多个彼此独立地选自me、
i
pr、
t
bu、cn、cf3和ph的取代基取代。
[0277]
如整个本申请中所用,术语“芳基”和“芳族”可在最广义上理解为任何单环、双环或多环芳族部分。相应地,芳基基团含有6至60个芳族环原子,杂芳基基团含有5至60个芳族环原子,其中至少一个为杂原子。尽管如此,在整个本申请中,在某些取代基的定义中,芳族环原子的数目可以下标数给出。特别地,杂芳族环包含一至三个杂原子。同样,术语“杂芳基”和“杂芳族”可在最广义上理解为包含至少一个杂原子的任何单环、双环或多环杂芳族部分。杂原子可在每次出现时相同或不同并且一个一个单独地选自n、o和s。相应地,术语“亚芳基”是指具有两个与其他分子结构的结合位点并因此充当连接基结构的二价取代基。在一些情况下,示例性实施方案中的基团与这里给出的定义不同地定义,例如,芳族环原子的数目或杂原子的数目不同于给定的定义,将应用示例性实施方案中的定义。根据本发明,稠合(有环)芳族或杂芳族多环由两个或更多个单芳族或杂芳族环构成,其经由缩合反应形成多环。
[0278]
具体地讲,如在本申请中通篇所用的,术语“芳基”或“杂芳基”包括可通过衍生自以下的芳族或杂芳族基团的任何位置结合的基团:苯、萘、蒽、菲、芘、二氢芘、苝、荧蒽、苯并蒽、苯并菲、并四苯、并五苯、苯并芘、呋喃、苯并呋喃、异苯并呋喃、二苯并呋喃、噻吩、苯并噻吩、异苯并噻吩、二苯并噻吩;吡咯、吲哚、异吲哚、咔唑、吡啶、喹啉、异喹啉、吖啶、菲
啶、苯并5,6-喹啉、苯并-6,7-喹啉、苯并-7,8-喹啉、吩噻嗪、吩噁嗪,吡唑、吲唑、咪唑、苯并咪唑、萘并咪唑、菲并咪唑、吡啶并咪唑、吡嗪并咪唑、喹喔啉并咪唑、噁唑、苯并噁唑、萘并噁唑,蒽唑,苯并噻唑,异噁唑、1,2-噻唑、1,3-噻唑、苯并噻唑、哒嗪、苯并哒嗪、嘧啶、苯并嘧啶、1,3,5-三嗪、喹喔啉、吡嗪、吩嗪、萘啶、咔啉、苯并咔啉、菲咯啉、1,2,3-三唑、1,2,4-三唑、苯并三唑、1,2,3-噁二唑、1,2,4-噁二唑、1,2,5-噁二唑、1,2,3,4-四嗪、嘌呤、蝶啶、吲哚嗪和苯并噻二唑或上述基团的组合。
[0279]
如整个本申请中所用,术语“环状基团”可以最广义地理解为任何单环、双环或多环部分。
[0280]
如整个本申请中所用,术语联苯作为取代基可以最广义地理解为邻联苯、间联苯或对联苯,其中邻、间和对位是关于与另一个化学部分的结合位点而定义的。
[0281]
如整个本申请中所用,术语“烷基”可以最广义地理解为任何直链、支链或环状烷基取代基。具体地讲,术语烷基包括取代基甲基(me)、乙基(et)、正丙基(
n
pr)、异丙基(
i
pr)、环丙基、正丁基(
n
bu)、异丁基(
i
bu)、仲丁基(
s
bu)、叔丁基(
t
bu)、环丁基、2-甲基丁基、正戊基、仲戊基、叔戊基、2-戊基、新戊基、环戊基、正己基、仲己基、叔己基、2-己基、3-己基、新己基、环己基、1-甲基环戊基、2-甲基戊基、正庚基、2-庚基、3-庚基、4-庚基、环庚基、1-甲基环己基、正辛基、2-乙基己基、环辛基、1-双环[2,2,2]辛基、2-双环[2,2,2]-辛基、2-(2,6-二甲基)辛基、3-(3,7-二甲基)辛基、金刚烷基、2,2,2-三氟乙基、1,1-二甲基-正己-1-基、1,1-二甲基正庚-1-基、1,1-二甲基正辛-1-基、1,1-二甲基正癸-1-基、1,1-二甲基正十二烷-1-基、1,1-二甲基-正十四烷-1-基、1,1-二甲基-正十六烷-1-基、1,1-二甲基-正十八烷-1-基、1,1-二乙基-正己-1-基、1,1-二乙基正庚-1-基、1,1-二乙基正辛-1-基、1,1-二乙基正癸-1-基、1,1-二乙基正十二烷-1-基、1,1-二乙基正十四烷-1-基、1,1-二乙基-正十六烷-1-基、1,1-二乙基-十八烷-1-基、1-(正丙基)-环己-1-基、1-(正丁基)-环己-1-基、1-(正己基)-环己-1-基、1-(正辛基)-环己-1-基和1-(正癸基)-环己-1-基。
[0282]
如整个本申请中所用,术语“烯基”包括直链、支链和环状烯基取代基。术语烯基基团示例性地包括取代基:乙烯基、丙烯基、丁烯基、戊烯基、环戊烯基、己烯基、环己烯基、庚烯基、环庚烯基、辛烯基、环辛烯基或环辛二烯基。
[0283]
如整个本申请中所用,术语“炔基”包括直链、支链和环状炔基取代基。术语“炔基”示例性地包括乙炔基、丙炔基、丁炔基、戊炔基、己炔基、庚炔基或辛炔基。
[0284]
如本申请中通篇所用的,术语“烷氧基”包括直链、支链和环状烷氧基取代基。例如,术语“烷氧基基团”包括甲氧基、乙氧基、正-丙氧基、异-丙氧基、正-丁氧基、异-丁氧基、仲-丁氧基、叔-丁氧基和2-甲基丁氧基。
[0285]
如整个本申请中所用,术语“硫代烷氧基”包括直链、支链和环状的硫代烷氧基取代基,其中示例性烷氧基的o被s取代。
[0286]
如整个本申请中所用,术语“卤素”和“卤代”可在最广义上理解为优选氟、氯、溴或碘。
[0287]
每当在本文中提及氢(h)时,它也可在每次出现时被替换为氘。
[0288]
应理解,当分子片段被描述为取代基或以其他方式与另一部分连接时,其名称可写成好像它是片段(例如,萘基、二苯并呋喃基)或好像它是整个分子(例如,萘、二苯并呋喃)。如本文所用,这些指定取代基或连接片段的不同方式被认为是等同的。
[0289]
在一个实施方案中,在室温下,在具有10重量%的有机分子的聚(甲基丙烯酸甲酯)(pmma)膜中,根据本发明的有机分子具有不超过150μs、不超过100μs、特别是不超过50μs、更优选不超过10μs或不超过7μs的激发态寿命。
[0290]
在本发明的一个实施方案中,根据本发明的有机分子为热活化延迟荧光(tadf)发射体,其表现出低于5000cm-1
、优选低于3000cm-1
、更优选低于1500cm-1
、甚至更优选低于1000cm-1
或甚至低于500cm-1
的δe
st
值,该值对应于第一激发单重态(s1)与第一激发三重态(t1)之间的能量差。
[0291]
在本发明的另一个实施方案中,在室温下,在具有10重量%的有机分子的聚(甲基丙烯酸甲酯)(pmma)膜中,根据本发明的有机分子在可见或最接近紫外的范围内,即在380至800nm的波长范围内具有发射峰,其半高全宽小于0.50ev,优选小于0.48ev,更优选小于0.45ev,甚至更优选小于0.43ev或甚至小于0.40ev。
[0292]
在本发明的另一个实施方案中,根据本发明的有机分子具有超过150、特别是超过200、优选超过250、更优选超过300或甚至超过500的“蓝色材料指数”(bmi),该指数通过用以%表示的光致发光量子产率(plqy)除以发射光的ciey颜色坐标来计算。
[0293]
在本发明的另一个实施方案中,根据本发明的有机分子具有大于60%,特别是大于64%、优选大于75%、更优选大于80%或甚至大于83%的plqy%。
[0294]
在本发明的另一个实施方案中,根据本发明的有机分子具有大于80%或甚至大于83%的plqy%。
[0295]
轨道能量和激发态能量可以通过实验方法或通过使用量子化学方法的计算,特别是密度泛函理论计算来确定。最高占据分子轨道e
homo
的能量通过本领域技术人员已知的方法,从循环伏安法测量中以0.1ev的精确度确定。最小未占据分子轨道e
lumo
的能量计算为e
homo
+e
gap
,其中e
gap
如下方式确定:对于主体化合物,除非另有说明,否则使用具有10重量%主体的聚(甲基丙烯酸甲酯)(pmma)膜的发射光谱的起始值作为e
间隙
。对于发射体分子,e
间隙
被确定为具有10重量%发射体的pmma膜的激发光谱和发射光谱交叉的能量。
[0296]
第一激发三重态t1的能量由通常77k的低温下发射光谱的起始值确定。对于其中第一激发单重态和最低三重态在能量上分开>0.4ev的主体化合物,磷光通常在2-me-thf中的稳态光谱中可见。三重态能量可因此以磷光光谱的起始值确定。对于tadf发射体分子,如果没有另外说明,在具有10重量%发射体的pmma膜中测量时,第一激发三重态t1的能量由在77k处的延迟发射光谱的起始值确定。对于主体和发射体化合物两者,第一激发单重态s1的能量由发射光谱的起始值确定,如果没有另外说明,则在具有10重量%主体或发射体化合物的pmma膜中测量。
[0297]
通过计算发射光谱的切线与x轴的交点来确定发射光谱的起始值。发射光谱的切线设置在发射带的高能量侧和在发射光谱的最大强度的一半的点处。
[0298]
本发明的另一方面涉及制备根据本发明的有机分子的方法(具有任选的后续反应),其中使用三-r
i-取代的3-溴-4-氟苄腈作为反应物:
[0299][0300]
对于亲核芳族取代中的氮杂环与芳基卤化物、优选芳基氟化物的反应,典型的条件包括在例如非质子极性溶剂如二甲基亚砜(dmso)或n,n-二甲基甲酰胺(dmf)中使用碱如磷酸三钾或氢化钠。
[0301]
一种备选合成路线包括经由铜-或钯-催化偶联向芳基卤化物或芳基类卤化物、优选芳基溴化物、芳基碘化物、三氟甲磺酸芳基酯或甲苯磺酸芳基酯中引入氮杂环。
[0302]
本发明的又一个方面涉及根据本发明的有机分子在光电器件中用作发光发射体或用作吸收剂、和/或用作主体材料和/或用作电子传输材料、和/或用作空穴注入材料、和/或用作空穴阻挡材料的用途。
[0303]
光电器件,也称为有机光电器件,可以广义地理解为任何基于有机材料的,适合于发射可见或最接近紫外(uv)范围内(即,在从380nm至800nm的波长范围内)的光的任何器件。更优选地,光电器件可能够发射在可见范围、即400nm至800nm内的光。
[0304]
在这种使用背景下,光电器件更特别地选自:
[0305]
●
有机发光二极管(oled),
[0306]
●
发光电化学电池,
[0307]
●
oled传感器,尤其是气体和蒸气传感器,其并未对外部气密屏蔽,
[0308]
●
有机二极管,
[0309]
●
有机太阳能电池,
[0310]
●
有机晶体管,
[0311]
●
有机场效应晶体管,
[0312]
●
有机激光器,和
[0313]
●
下变频元件。
[0314]
在这种使用背景下的一个优选的实施方案中,光电器件为选自有机发光二极管(oled)、发光电化学电池(lec)和发光晶体管的器件。
[0315]
就所述用途而言,根据本发明的有机分子在光电器件中、更特别是在oled中的发射层中的分数为1重量%至99重量%,更特别是5重量%至80重量%。在一个替代的实施方案中,发射层中有机分子的比例为100重量%。
[0316]
在一个实施方案中,发光层不仅包含根据本发明的有机分子,而且包含其三重态(t1)和单重态(s1)能级在能量上高于所述有机分子的三重态(t1)和单重态(s1)能级的主体材料。
[0317]
本发明的又一个方面涉及包含以下或由以下组成的组合物:
[0318]
(a)至少一种根据本发明的有机分子,特别是以发射体和/或主体的形式,和
[0319]
(b)一种或多种发射体和/或主体材料,其不同于根据本发明的有机分子,和
[0320]
(c)任选地一种或多种染料和/或一种或多种溶剂。
[0321]
在一个实施方案中,发光层包含一种组合物(或基本上由一种组合物组成),所述组合物包含以下或由以下组成:
[0322]
(a)至少一种根据本发明的有机分子,特别是以发射体和/或主体的形式,和
[0323]
(b)一种或多种发射体和/或主体材料,其不同于根据本发明的有机分子,和
[0324]
(c)任选地一种或多种染料和/或一种或多种溶剂。
[0325]
特别优选地,发光层eml包括组合物(或基本上由组合物组成),该组合物包含或由以下组成:
[0326]
(i)1-50重量%、优选5-40重量%、特别是10-30重量%的一种或多种根据本发明的有机分子e;
[0327]
(ii)5-99重量%、优选30-94.9重量%、特别是40-89重量%的至少一种主体化合物h;和
[0328]
(iii)任选地0-94重量%、优选0.1-65重量%、特别是1-50重量%的至少一种其他的主体化合物d,其结构不同于根据本发明的分子的结构;和
[0329]
(iv)任选地0-94重量%、优选0-65重量%、特别是0-50重量%的溶剂;和
[0330]
(v)任选地,0-30重量%、特别是0-20重量%、优选0-5重量%的至少一种其他发射体分子f,其结构不同于根据本发明的分子的结构。
[0331]
优选地,能量可以从主体化合物h转移至根据本发明的一种或多种有机分子(e),特别是从主体化合物h的第一激发三重态t1(h)转移至根据本发明的一种或多种有机分子e的第一激发三重态t1(e)和/或从主体化合物h的第一激发单重态s1(h)转移至根据本发明的一种或多种有机分子e的第一激发单重态s1(e)。
[0332]
在又一个实施方案中,发光层eml包含一种组合物(或(基本上)由一种组合物组成),所述组合物包含以下或由以下组成:
[0333]
(i)1-50重量%、优选5-40重量%、特别是10-30重量%的一种根据本发明的有机分子e;
[0334]
(ii)5-99重量%、优选30-94.9重量%、特别是40-89重量%的一种主体化合物h;和
[0335]
(iii)任选地0-94重量%、优选0.1-65重量%、特别是1-50重量%的至少一种其他的主体化合物d,其结构不同于根据本发明的分子的结构;和
[0336]
(iv)任选地0-94重量%、优选0-65重量%、特别是0-50重量%的溶剂;和
[0337]
(v)任选地,0-30重量%、特别是0-20重量%、优选0-5重量%的至少一种其他发射体分子f,其结构不同于根据本发明的分子的结构。
[0338]
在一个实施方案中,主体化合物h具有能量e
homo
(h)在-5至-6.5ev范围内的最高占据分子轨道homo(h),并且至少一种另外的主体化合物d具有能量为e
homo
(d)的最高占据分子轨道homo(d),其中e
homo
(h)>e
homo
(d)。
[0339]
在另一个实施方案中,主体化合物h具有能量为e
lumo
(h)的最低未占据分子轨道lumo(h),并且至少一种另外的主体化合物d具有能量为e
lumo
(d)的最低未占据分子轨道lumo(d),其中能量e
lumo
(h)>e
lumo
(d)。
[0340]
在一个实施方案中,主体化合物h具有能量为e
homo
(h)的最高占据分子轨道homo(h)和能量为e
lumo
(h)的最低未占据分子轨道lumo(h),并且
[0341]
至少一种另外的主体化合物d具有能量为e
homo
(d)的最高占据分子轨道homo(d)和能量为e
lumo
(d)的最低未占据分子轨道lumo(d),
[0342]
本发明的有机分子(e)具有能量为e
homo
(e)的最高占据分子轨道homo(e)和能量为e
lumo
(e)的最低未占据分子轨道lumo(e),
[0343]
其中
[0344]
e
homo
(h)>e
homo
(d),并且根据本发明的有机分子e的最高占据分子轨道homo(e)的能级(e
homo
(e))与主体化合物h的最高占据分子轨道homo(h)的能级(e
homo
(h))之间的差值在-0.5ev和0.5ev之间,更优选在-0.3ev和0.3ev之间,甚至更优选在-0.2ev和0.2ev之间或甚至在-0.1ev和0.1ev之间;并且
[0345]
e
lumo
(h)>e
lumo
(d),并且根据本发明的有机分子e的最低未占据分子轨道lumo(e)的能级(e
lumo
(e))与至少一种另外的主体化合物d的最低未占据分子轨道lumo(d)的能级(e
lumo
(d))之间的差值在-0.5ev和0.5ev之间,更优选在-0.3ev和0.3ev之间,甚至更优选在-0.2ev和0.2ev之间或甚至在-0.1ev和0.1ev之间。
[0346]
在又一个方面,本发明涉及一种光电器件,其包含这里描述的类型的有机分子或组合物,更特别是以选自以下的器件的形式:有机发光二极管(oled);发光电化学电池;oled传感器,特别是未对外部气密屏蔽的气体和蒸气传感器;有机二极管;有机太阳能电池;有机晶体管;有机场效应晶体管;有机激光器和下变频元件。
[0347]
在一个优选的实施方案中,光电器件为选自有机发光二极管(oled)、发光电化学电池(lec)和发光晶体管的器件。
[0348]
在本发明的光电器件的一个实施方案中,根据本发明的有机分子e用作发光层eml中的发光材料。
[0349]
在本发明的光电器件的一个实施方案中,发光层eml由根据这里描述的发明的组
合物组成。
[0350]
示例性地,当光电器件是oled时,它可以表现出以下层结构:
[0351]
1.衬底
[0352]
2.阳极层a
[0353]
3.空穴注入层hil
[0354]
4.空穴传输层htl
[0355]
5.电子阻挡层ebl
[0356]
6.发射层eml
[0357]
7.空穴阻挡层hbl
[0358]
8.电子传输层etl
[0359]
9.电子注入层eil
[0360]
10.阴极层,
[0361]
其中oled仅包含每个层,任选地不同的层可合并,并且oled可包含不止一个上述每种层类型的层。
[0362]
此外,光电器件可任选地包含一个或多个保护层,其保护器件使之免于暴露于环境中的有害物质,这些有害物质的示例包括湿气、蒸气和/或气体。
[0363]
在本发明的一个实施方案中,光电器件为oled,其具有以下倒置层结构:
[0364]
1.衬底
[0365]
2.阴极层
[0366]
3.电子注入层eil
[0367]
4.电子传输层etl
[0368]
5.空穴阻挡层hbl
[0369]
6.发射层b
[0370]
7.电子阻挡层ebl
[0371]
8.空穴传输层htl
[0372]
9.空穴注入层hil
[0373]
10.阳极层a,
[0374]
其中具有倒置层结构的oled仅包括每个层,任选地不同的层可合并,并且oled可包括不止一个上述每种层类型的层。
[0375]
在本发明的一个实施方案中,光电器件为oled,其可具有堆叠结构。在此结构中,与其中oled并排放置的典型布置相反,各个单元堆叠在彼此之上。可利用具有堆叠结构的oled产生混合光,特别是可通过堆叠蓝色、绿色和红led来产生白光。此外,具有堆叠结构的oled可任选地包含电荷产生层(cgl),其通常位于两个oled子单元之间并通常由n-掺杂和p-掺杂层组成,其中一个cgl的n-掺杂层通常位于更靠近阳极层的位置。
[0376]
在本发明的一个实施方案中,光电器件为oled,其在阳极和阴极之间包含两个或更多个发射层。特别地,这种所谓的串联oled包含三个发射层,其中一个发射层发射红光,一个发射层发射绿光,一个发射层发射蓝光,并任选地可在各个发射层之间包含其他层如电荷产生层、阻挡或传输层。在又一个实施方案中,发射层相邻堆叠。在又一个实施方案中,串联oled在每两个发射层之间包含电荷产生层。另外,可合并相邻的发射层或由电荷产生
层分开的发射层。
[0377]
衬底可由任何材料或材料的组合物形成。最常见的是,使用载玻片作为衬底。或者,可使用薄金属层(例如,铜、金、银或铝膜)或塑料膜或滑片。这可允许更高程度的灵活性。阳极层a主要由允许获得(基本上)透明膜的材料组成。由于两个电极中的至少一个应(基本上)透明以允许来自oled的光发射,故阳极层a或阴极层c是透明的。优选地,阳极层a包含大含量的透明导电氧化物(tco)或甚至由透明导电氧化物(tco)组成。此类阳极层a可以例如包含氧化铟锡、氧化铝锌、氟掺杂的氧化锡、氧化铟锌、pbo、sno、氧化锆、氧化钼、氧化钒、氧化钨、石墨、掺杂的si、掺杂的ge、掺杂的gaas、掺杂的聚苯胺、掺杂的聚吡咯和/或掺杂的聚噻吩。
[0378]
阳极层a(基本上)可以由氧化铟锡(ito)(例如(ino3)0.9(sno2)0.1)组成。由透明导电氧化物(tco)引起的阳极层a的粗糙度可通过使用空穴注入层(hil)来补偿。此外,hil可促进准电荷载流子(即,空穴)的注入,因为将促进准电荷载流子从tco向空穴传输层(htl)的传输。空穴注入层(hil)可以包含聚-3,4-亚乙二氧基噻吩(pedot)、聚苯乙烯磺酸盐(pss)、moo2、v2o5、cupc或cui,特别是pedot和pss的混合物。空穴注入层(hil)还可防止金属从阳极层a向空穴传输层(htl)中的扩散。hil可例如包含pedot:pss(聚-3,4-乙烯二氧噻吩:聚苯乙烯磺酸盐)、pedot(聚-3,4-乙烯二氧噻吩)、mmtdata(4,4',4
”-
三[苯基(间甲苯基)氨基]三苯胺)、螺-tad(2,2',7,7'-四(n,n-二苯基氨基)-9,9'-螺二芴)、dntpd(n1,n1'-(联苯-4,4'-二基)双(n1-苯基-n4,n4-二-间甲苯基苯-1,4-二胺)、npb(n,n'-双-(1-萘基)-n,n'-双-苯基-(1,1'-联苯)-4,4'-二胺)、npnpb(n,n'-二苯基-n,n'-二-[4-(n,n-二苯基-氨基)苯基]对二氨基联苯)、meo-tpd(n,n,n',n'-四(4-甲氧基苯基)对二氨基联苯)、hat-cn(1,4,5,8,9,11-六氮杂三亚苯基-六腈)和/或螺-npd(n,n'-二苯基-n,n'-双-(1-萘基)-9,9'-螺二芴-2,7-二胺)。
[0379]
邻近阳极层a或空穴注入层(hil),通常设置空穴传输层(htl)。在此可使用任何空穴传输化合物。例如,可使用富含电子的杂芳族化合物如三芳基胺和/或咔唑作为空穴传输化合物。htl可降低阳极层a和发光层eml之间的能垒。空穴传输层(htl)也可为电子阻挡层(ebl)。优选地,空穴传输化合物具有相对高的其三重态t1能级。例如,空穴传输层(htl)可包含星形杂环如三(4-咔唑基-9-基苯基)胺(tcta)、聚-tpd(聚(4-丁基苯基-二苯基-胺))、[α]-npd(聚(4-丁基苯基-二苯基-胺))、tapc(4,4'-亚环己基-双[n,n-双(4-甲基苯基)苯胺])、2-tnata(4,4',4
”-
三[2-萘基(苯基)氨基]三苯胺)、螺-tad、dntpd、npb、npnpb、meo-tpd、hat-cn和/或trispcz(9,9'-二苯基-6-(9-苯基-9h-咔唑-3-基)-9h,9'h-3,3'-联咔唑)。另外,htl可包含p-掺杂层,其可由无机或有机掺杂剂在有机空穴传输基质中组成。示例性地,可使用过渡金属氧化物如氧化钒、氧化钼或氧化钨作为无机掺杂剂。可以示例性地使用四氟四氰基喹啉二甲烷(f
4-tcnq)、五氟苯甲酸铜(cu(i)pfbz)或过渡金属络合物作为有机掺杂剂。
[0380]
示例性地,ebl可包含mcp(1,3-双(咔唑-9-基)苯)、tcta、2-tnata、mcbp(3,3-二(9h-咔唑-9-基)联苯)、tris-pcz、czsi(9-(4-叔丁基苯基)-3,6-双(三苯基甲硅烷基)-9h-咔唑)和/或dcb(n,n
′-
二咔唑基-1,4-二甲基苯)。
[0381]
邻近空穴传输层(htl),通常设置发光层eml。发光层eml包含至少一种发光分子。特别地,eml包含至少一种根据本发明的发光分子e。在一个实施方案中,发光层仅包含根据
本发明的有机分子e。通常,eml还包含一种或多种主体材料h。示例性地,主体材料h选自cbp(4,4
’-
双-(n-咔唑基)-联苯)、mcp、mcbp sif87(二苯并[b,d]噻吩-2-基三苯基硅烷)、czsi、sif88(二苯并[b,d]噻吩-2-基)二苯基硅烷)、dpepo(双[2-(二苯膦基)苯基]醚氧化物)、9-[3-(二苯并呋喃-2-基)苯基]-9h-咔唑、9-[3-(二苯并呋喃-2-基)苯基]-9h-咔唑、9-[3-(二苯并噻吩-2-基)苯基]-9h-咔唑、9-[3,5-双(2-二苯并呋喃基)苯基]-9h-咔唑、9-[3,5-双(2-二苯并硫代苯基)苯基]-9h-咔唑、t2t(2,4,6-三(联苯-3-基)-1,3,5-三嗪)、t3t(2,4,6-三(三苯-3-基)-1,3,5-三嗪)和/或tst(2,4,6-三(9,9'-螺二芴-2-基)-1,3,5-三嗪)。主体材料h通常应选择为表现出在能量上高于所述有机分子的第一三重态(t1)和第一单重态(s1)能级的第一三重态(t1)和第一单重态(s1)能级。
[0382]
在本发明的一个实施方案中,eml包含所谓的混合主体系统,其具有至少一种空穴主导主体和一种电子主导主体。在一个特别的实施方案中,eml包含确切地一种根据本发明的发光分子e和混合主体系统,所述混合主体系统包含t2t作为电子主导主体以及选自cbp、mcp、mcbp、9-[3-(二苯并呋喃-2-基)苯基]-9h-咔唑、9-[3-(二苯并呋喃-2-基)苯基]-9h-咔唑、9-[3-(二苯并噻吩-2-基)苯基]-9h-咔唑、9-[3,5-双(2-二苯并呋喃基)苯基]-9h-咔唑和9-[3,5-双(2-二苯并噻吩基)苯基]-9h-咔唑的主体作为空穴主导主体。在又一个实施方案中,eml包含50-80重量%、优选60-75重量%选自cbp、mcp、mcbp、9-[3-(二苯并呋喃-2-基)苯基]-9h-咔唑、9-[3-(二苯并呋喃-2-基)苯基]-9h-咔唑、9-[3-(二苯并噻吩-2-基)苯基]-9h-咔唑、9-[3,5-双(2-二苯并呋喃基)苯基]-9h-咔唑和9-[3,5-双(2-二苯并噻吩基)苯基]-9h-咔唑的主体;10-45重量%、优选15-30重量%的t2t和5-40重量%、优选10-30重量%根据本发明的发光分子。
[0383]
邻近发光层eml,可设置电子传输层(etl)。本文中可使用任何电子传输剂。示例性地,可使用贫电子的化合物如苯并咪唑、吡啶、三唑、噁二唑(例如,1,3,4-噁二唑)、膦氧化物和砜。电子传输剂也可为星形杂环如1,3,5-三(1-苯基-1h-苯并[d]咪唑-2-基)苯基(tpbi)。etl可以包含nbphen(2,9-双(萘-2-基)-4,7-二苯基-1,10-菲咯啉)、alq3(铝-三(8-羟基喹啉))、tspo1(二苯基-4-三苯基甲硅烷基苯基氧膦)、bpytp2(2,7-二(2,2'-联吡啶-5-基)三苯)、sif87(二苯并[b,d]噻吩-2-基三苯基硅烷)、sif88(二苯并[b,d]噻吩-2-基二苯基硅烷)、bmpyphb(1,3-双[3,5-二(吡啶-3-基)苯基]苯)和/或btb(4,4'-双-[2-(4,6-二苯基-1,3,5-三嗪基)]-1,1'-联苯)。任选地,etl可掺杂有材料如liq。电子传输层(etl)也可阻挡空穴或引入空穴阻挡层(hbl)。
[0384]
hbl可以例如包含bcp(2,9-二甲基-4,7-二苯基-1,10-菲咯啉=浴铜灵)、balq(双(8-羟基-2-甲基喹啉)-(4-苯基苯氧基)铝)、nbphen(2,9-双(萘-2-基)-4,7-二苯基-1,10-菲咯啉)、alq3(铝-三(8-羟基喹啉))、tspo1(二苯基-4-三苯基甲硅烷基苯基氧膦)、t2t(2,4,6-三(联苯-3-基)-1,3,5-三嗪)、t3t(2,4,6-三(三苯基-3-基)-1,3,5-三嗪)、tst(2,4,6-三(9,9'-螺二芴-2-基)-1,3,5-三嗪)和/或tcb/tcp(1,3,5-三(n-咔唑基)苯/1,3,5-三(咔唑)-9-基)苯)。
[0385]
邻近电子传输层(etl),可设置阴极层c。例如,阴极层c可以包含金属(例如,al、au、ag、pt、cu、zn、ni、fe、pb、lif、ca、ba、mg、in、w或pd)或金属合金或者可以由金属或金属合金组成。出于实际原因,阴极层也可由(基本上)由不透明金属如mg、ca或al组成。或者或另外,阴极层c还可包含石墨和/或碳纳米管(cnt)。或者,阴极层c也可由纳米级银丝组成。
[0386]
oled还可任选地在电子传输层(etl)与阴极层c之间包含保护层(其可被命名为电子注入层(eil))。该层可包含氟化锂、氟化铯、银、liq(8-羟基喹啉基锂)、li2o、baf2、mgo和/或naf。
[0387]
任选地,电子传输层(etl)和/或空穴阻挡层(hbl)也可包含一种或多种主体化合物h。
[0388]
为了进一步修改发光层eml的发射光谱和/或吸收光谱,发光层eml可以进一步包含一种或多种另外的发射体分子f。此类发射体分子f可以是本领域已知的任何发射体分子。优选地,此类发射体分子f是具有与根据本发明的分子e的结构不同的结构的分子。发射体分子f可以任选地为tadf发射体。另选地,发射体分子f可以任选地为能够改变发光层eml的发射光谱和/或吸收光谱的荧光和/或磷光发射体分子。示例性地,在通过发射与发射体分子e发射的光相比典型地红移的光而弛豫到基态s0之前,三重态和/或单重态激子可以从根据本发明的发射体分子e转移到发射体分子f。任选地,发射体分子f还可以引起双光子效应(即,最大吸收能量的一半的两个光子的吸收)。
[0389]
任选地,光电器件(例如,oled)可以例如是基本上白色的光电器件。例如,此类白色光电器件可以包括至少一种(深)蓝色发射体分子以及一种或多种发射绿光和/或红光的发射体分子。然后,如上所述,在两种或更多种分子之间还可以任选地具有能量透射率。
[0390]
如本文所用,如果未在特定的上下文中更具体地定义,则发射和/或吸收的光的颜色指定如下:
[0391][0392][0393]
相对于发射体分子,此类颜色是指最大发射。因此,例如,深蓝色发射体在>420至480nm范围内具有最大发射,天蓝色发射体在>480至500nm范围内具有最大发射,绿色发射体在>500至560nm范围内具有最大发射,红色发射体在>620至800nm范围内具有最大发射。
[0394]
深蓝色发射体的最大发射优选低于480nm、更优选低于470nm、甚至更优选低于465nm或甚至低于460nm。其通常高于420nm,优选高于430nm,更优选高于440nm,或甚至高于450nm。
[0395]
因此,本发明的另一方面涉及一种oled,其在1000cd/m2时表现出大于8%,更优选大于10%,更优选大于13%,甚至更优选大于15%或甚至大于20%的外部量子效率,和/或表现出在420nm和500nm之间,优选在430nm和490nm之间,更优选在440nm和480nm之间,甚至更优选在450nm和470nm之间的最大发射,和/或在500cd/m2时表现出大于100小时,优选大于200小时,更优选大于400小时,甚至更优选大于750小时或甚至大于1000小时的lt80值。相应地,本发明的又一个方面涉及一种oled,其发射的ciey色坐标小于0.45、优选小于
0.30、更优选小于0.20或甚至更优选小于0.15或甚至小于0.10。
[0396]
本发明的又一个方面涉及一种oled,其以不同的色点发射光。根据本发明,oled发射的光具有窄的发射带(小的半峰全宽(fwhm))。在一个方面,根据本发明的oled发射的光的主发射峰的fwhm小于0.50ev、优选小于0.48ev、更优选小于0.45ev、甚至更优选小于0.43ev或甚至小于0.40ev。
[0397]
本发明的又一个方面涉及一种oled,其发射的光的ciex和ciey色坐标接近于如itu-r建议书bt.2020(rec.2020)所定义的原色蓝色(ciex=0.131和ciey=0.046)的色坐标ciex(=0.131)和ciey(=0.046)并因此适于用在超高清(uhd)显示器例如uhd-tv中。相应地,本发明的又一个方面涉及一种oled,其发射的ciex色坐标在0.02和0.30之间、优选在0.03和0.25之间、更优选在0.05和0.20之间或甚至更优选在0.08和0.18之间或甚至在0.10和0.15之间,和/或ciey色坐标在0.00和0.45之间、优选在0.01和0.30之间、更优选在0.02和0.20之间或甚至更优选在0.03和0.15之间或甚至在0.04和0.10之间。
[0398]
在另一方面,本发明涉及用于制造光电器件的方法。在此情况下,使用本发明的有机分子。
[0399]
光电器件,特别是根据本发明的oled,可通过任何气相沉积和/或液体加工措施制造。相应地,至少一个层
[0400]-通过升华工艺制备,
[0401]-通过有机气相沉积工艺制备,
[0402]-通过载气升华工艺制备,
[0403]-是溶液加工或印刷的。
[0404]
用来制造光电器件、特别是根据本发明的oled的方法是本领域已知的。不同的层通过随后的沉积工艺一个一个单独且连续地沉积在合适的衬底上。一个一个单独的层可使用相同或不同的沉积方法沉积。
[0405]
气相沉积过程可以包括热(共)蒸发、化学气相沉积和物理气相沉积。对于有源矩阵oled显示器,使用amoled背板作为衬底。一个一个单独的层可使用适当的溶剂从溶液或分散体加工。溶液沉积工艺示例性地包括旋涂、浸涂和喷射印刷。液体加工可任选地在惰性气氛中(例如,在氮气氛中)进行并且可任选地通过现有技术中已知的措施完全或部分地除去溶剂。
[0406]
实例
[0407]
一般合成方案i
[0408][0409]
用于合成aav1的一般程序:
[0410][0411]
将3-溴-4-氟苯基苄腈(1.00当量,cas 79630-23-2)、双-(频哪醇)二硼(1.5当量,cas 73183-34-3)、三(二亚苄基丙酮)二钯(0)pd2(dba)3(0.04当量,cas 51364-51-3)、x-phos(0.08当量,cas 564483-18-7)和乙酸钾(koac,3.0当量)在氮气气氛下,在110℃的无水甲苯中搅拌16小时。在冷却至室温(rt)后,将反应混合物用乙酸乙酯/盐水萃取。收集有机相,用盐水洗涤,并用mgso4干燥。去除有机溶剂,粗产物用环己烷洗涤且从etoh中重结晶。
[0412]
用于合成aav2的一般程序:
[0413][0414]
将e1(1.00当量)、4-溴-2,3-二氟苄腈(1当量;cas 126163-58-4)、三(二亚苄基丙酮)二钯(0)pd2(dba)3(0.04当量;cas 51364-51-3)、x-phos(0.08当量,cas 564483-18-7)和磷酸钾(k3po4,3.0当量)在氮气气氛下,在100℃的无水甲苯/h2o(10:1)中搅拌16小时。在冷却至室温(rt)后,将反应混合物用乙酸乙酯/盐水萃取。收集有机相,用盐水洗涤,并用mgso4干燥。去除有机溶剂,粗产物用环己烷洗涤且从etoh中重结晶。
[0415]
用于合成aav3的一般程序:
[0416][0417]
将e1(1.00当量)、4-溴-2,6-二氟苄腈(1当量;cas 123843-67-4)、三(二亚苄基丙酮)二钯(0)pd2(dba)3(0.04当量;cas 51364-51-3)、x-phos(0.08当量,cas 564483-18-7)和磷酸钾(k3po4,3.0当量)在氮气气氛下,在100℃的无水甲苯/h2o(10:1)中搅拌16小时。在冷却至室温(rt)后,将反应混合物用乙酸乙酯/盐水萃取。收集有机相,用盐水洗涤,并用mgso4干燥。除去有机溶剂,将粗产物不经进一步纯化直接用于下一步。
[0418]
用于合成aav4的一般程序:
[0419][0420]
将4-溴-2,3-二氟苄腈(1.00当量,cas 126163-58-4)、双-(频哪醇)二硼(1.5当量,cas 73183-34-3)、三(二亚苄基丙酮)二钯(0)pd2(dba)3(0.04当量,cas 51364-51-3)、x-phos(0.08当量,cas 564483-18-7)和乙酸钾(koac,3.0当量)在氮气气氛下,在110℃的无水甲苯中搅拌16小时。在冷却至室温(rt)后,将反应混合物用乙酸乙酯/盐水萃取。收集有机相,用盐水洗涤,并用mgso4干燥。去除有机溶剂,粗产物用环己烷洗涤且从etoh中重结晶。
[0421]
用于合成aav5的一般程序:
[0422][0423]
将e2(1.00当量)、3-溴-4-氟苯基苄腈(1.00当量,cas 79630-23-2)、三(二亚苄基丙酮)二钯(0)pd2(dba)3(0.04当量,cas 51364-51-3)、x-phos(0.08当量,cas 564483-18-7)和乙酸钾(koac,3.0当量)在氮气气氛下,在110℃的无水甲苯中搅拌16小时。在冷却至室温(rt)后,将反应混合物用乙酸乙酯/盐水萃取。收集有机相,用盐水洗涤,并用mgso4干燥。去除有机溶剂,粗产物用环己烷洗涤且从etoh中重结晶。
[0424]
用于合成aav6的一般程序:
[0425][0426]
将4-溴-2,6-二氟苄腈(1当量;cas 123843-67-4)、双-(频哪醇)二硼(1.5当量,cas 73183-34-3)、三(二亚苄基丙酮)二钯(0)pd2(dba)3(0.04当量,cas 51364-51-3)、x-phos(0.08当量,cas 564483-18-7)和乙酸钾(koac,3.0当量)在氮气气氛下,在110℃的无水甲苯中搅拌16小时。在冷却至室温(rt)后,将反应混合物用乙酸乙酯/盐水萃取。收集有机相,用盐水洗涤,并用mgso4干燥。去除有机溶剂,粗产物用环己烷洗涤且从etoh中重结晶。
[0427]
用于合成aav7的一般程序:
[0428][0429]
将e3(1.00当量)、3-溴-4-氟苯基苄腈(1.00当量,cas 79630-23-2)、三(二亚苄基丙酮)二钯(0)pd2(dba)3(0.04当量,cas 51364-51-3)、x-phos(0.08当量,cas 564483-18-7)和乙酸钾(koac,3.0当量)在氮气气氛下,在110℃的无水甲苯中搅拌16小时。在冷却至室温(rt)后,将反应混合物用乙酸乙酯/盐水萃取。收集有机相,用盐水洗涤,并用mgso4干燥。
去除有机溶剂,粗产物用环己烷洗涤且从etoh中重结晶。
[0430]
用于合成aav8的一般程序:
[0431][0432][0433]
将z1或z2(各1当量)、相应的供体分子d-h(3.20当量)和磷酸三钾(3.00当量)在氮气气氛下悬浮在dmso中,并在120℃下搅拌(16小时)。在冷却至室温后,将反应混合物用乙酸乙酯/盐水萃取。收集有机相,用盐水洗涤并用mgso4干燥。在减压下除去溶剂。通过重结晶或通过快速色谱法纯化粗产物。
[0434]
特别地,供体分子d-h是3,6-取代的咔唑(例如3,6-二甲基咔唑、3,6-二苯基咔唑、3,6-二叔丁基咔唑),2,7-取代的咔唑(例如2,7-二甲基咔唑、2,7-二苯基咔唑、2,7-二叔丁基咔唑),1,8-取代的咔唑(例如1,8-二甲基咔唑、1,8-二苯基咔唑、1,8-二叔丁基咔唑),1-取代的咔唑(例如1-甲基咔唑、1-苯基咔唑、1-叔丁基咔唑),2-取代的咔唑(例如2-甲基咔唑、2-苯基咔唑、2-叔丁基咔唑)或3-取代的咔唑(例如3-甲基咔唑、3-苯基咔唑、3-叔丁基咔唑)。
[0435]
示例性地,可以使用卤素取代的咔唑,特别是3-溴咔唑作为d-h。
[0436]
在随后的反应中,可以例如在经由d-h引入的一个或多个卤素取代基的位置处引入硼酸酯官能团或硼酸官能团,以例如通过与双(频哪醇)二硼反应(cas no.73183-34-3),
产生相应的咔唑-3-基硼酸酯或咔唑-3-基硼酸。随后,可以通过与相应的卤代反应物r
a-hal,优选r
a-cl和r
a-br的偶联反应,引入一个或多个取代基r
a
代替硼酸酯基团或硼酸基团。
[0437]
另选地,可以在经由d-h引入的一个或多个卤素取代基的位置处引入一个或多个取代基r
a
,所述卤素取代基是通过与取代基r
a
的硼酸[r
a-b(oh)2]或相应的硼酸酯反应而引入。
[0438]
循环伏安法
[0439]
从在二氯甲烷或合适的溶剂和合适的支持电解质(例如0.1mol/l的四丁基六氟磷酸铵)中有机分子的浓度为10-3
mol/l的溶液中测量循环伏安图。测量是在室温下在氮气气氛下用三电极组件(工作电极和反电极:pt线,参比电极:pt线)进行的,并使用fecp2/fecp
2+
作为内标进行校准。使用二茂铁作为内标相对于sce(英语:饱和甘汞电极)校正homo数据。
[0440]
密度泛函理论计算
[0441]
采用bp86泛函和单位分解方法(ri)优化分子结构。使用采用时间依赖性dft(td-dft)方法的(bp86)优化结构计算激发能。用b3lyp泛函计算轨道和激发态能量。使用def2-svp基组(和用于数值积分的m4-网格)。所有计算使用turbomole程序包。
[0442]
光物理测量
[0443]
样品预处理:旋涂
[0444]
装置:spin150,sps euro。
[0445]
样品浓度为10mg/ml,溶解在合适的溶剂中。
[0446]
程序:1)400u/min下3s;1000u/min、1000upm/s下20s。3)4000u/min、1000upm/s下10s。涂布后,将膜于70℃下干燥1分钟。
[0447]
光致发光光谱和tcspc(时间相关单光子计数)
[0448]
稳态发射光谱通过horiba scientific的modell fluoromax-4测量,其配备有150w氙弧灯、激发和发射单色器以及hamamatsu r928光电倍增管和时间相关单光子计数选件。使用标准校正拟合校正发射和激发光谱。
[0449]
采用使用tcspc方法的相同系统用fm-2013设备和horiba yvon tcspc hub测定激发态寿命。
[0450]
激发源:
[0451]
nanoled 370(波长:371nm,脉冲持续时间:1.1ns)
[0452]
nanoled 290(波长:294nm,脉冲持续时间:<1ns)
[0453]
spectraled 310(波长:314nm)
[0454]
spectraled 355(波长:355nm)。
[0455]
使用软件套件datastation和das6分析软件进行数据分析(指数拟合)。使用卡方检验拟定该拟合。
[0456]
光致发光量子产率测量
[0457]
对于光致发光量子产率(plqy)测量,使用绝对pl量子产率测量c9920-03g系统(hamamatsu photonics)。量子产率和cie坐标使用软件u6039-05版本3.6.0确定。
[0458]
最大发射以nm给出,量子产率φ以%给出,cie坐标以x、y值给出。
[0459]
plqy使用以下方案确定:
[0460]
1)质量保证:使用在乙醇中的蒽(已知浓度)作为参比
[0461]
2)激发波长:确定有机分子的吸收最大值并使用该波长激发分子
[0462]
3)测量
[0463]
在氮气氛下测量溶液或膜样品的量子产率。使用以下公式计算产率:
[0464][0465]
其中n
光子
表示光子数,int.表示强度。
[0466]
光电器件的生产和表征
[0467]
包含根据本发明的有机分子的oled器件可经由真空沉积方法制造。如果一个层含不止一种化合物,则以%给出一种或多种化合物的重量百分数。总重量百分数值总共达到100%,因此如果未给出值,则该化合物的分数等于给定值与100%之间的差值。
[0468]
未完全优化的oled使用标准方法和测量电致发光光谱来表征,外量子效率(以%表示)取决于强度和电流,所述强度使用光电二极管检测的光计算。从在恒定电流密度下运行期间亮度的变化来获取oled器件寿命。lt50值对应于其中测得的亮度降至初始亮度的50%的时间,类似地,lt80对应于测得的亮度降至初始亮度的80%的时间点,lt95对应于测得的亮度降至初始亮度的95%的时间点,如此等等。
[0469]
进行加速寿命测量(例如,施加增大的电流密度)。使用以下公式确定500cd/m2时的示例性lt80值:
[0470][0471]
其中l0表示施加电流密度时的初始亮度。
[0472]
这些值对应于若干(通常两至八个)像素的平均值,给出了这些像素之间的标准偏差。
[0473]
hplc-ms
[0474]
通过agilent(1100系列)和ms-检测器(thermo ltq xl)在hplc上进行hplc-ms光谱分析。
[0475]
示例性地,典型的hplc方法如下:在hplc中使用来自agilent的反相柱4.6mm
×
150mm,粒径3.5μm(zorbax eclipse plusc18,4.6
×
150mm,3.5μm hplc柱)。hplc-ms测量是在室温(rt)下按以下梯度进行的:
[0476][0477]
使用以下溶剂混合物:
[0478]
溶剂a:h2o(90%)mecn(10%)溶剂b:h2o(10%)mecn(90%)溶剂c:thf(50%)mecn(50%)
[0479]
从分析物浓度为0.5mg/ml的溶液取5μl的进样量进行测量。
[0480]
使用大气压化学电离(apci)源以正(apci+)或负(apci-)电离模式进行探针的电离。
[0481]
实施例1
[0482][0483]
根据aav1(收率=64%)、aav2(收率=42%)和aav8(收率=92%)合成实施例1。
[0484]
hplc-ms:715.40m/z,100%。
[0485]1h nmr(500mhz,dmso-d6)δ9.27(d,j=2.1hz,1h),8.85
–
8.76(m,4h),8.68(dd,j=8.3,2.0hz,1h),8.25(dd,j=7.9,1.5hz,1h),7.92(s,3h),7.80
–
7.68(m,8h),7.47(td,j=7.7,1.6hz,1h),7.30(d,j=8.3hz,1h),7.25
–
6.50(m,11h),5.71(s,2h)。
[0486]
图1描绘了实施例1(在pmma中占10重量%)的发射光谱。发射最大值(λ
max
)为494nm。光致发光量子产率(plqy)为89%,半峰全宽(fwhm)为0.39ev,发射寿命为4μs。最高占据分子轨道(e
homo
)的能量为-5.76ev。
[0487]
实施例2
[0488][0489]
根据aav1(收率=64%)、aav2(收率=42%)和aav8(收率=45%)合成实施例2。
[0490]
hplc-ms:791.68m/z。
[0491]
图2描绘了实施例2(在pmma中占10重量%)的发射光谱。发射最大值(λ
max
)为490nm。光致发光量子产率(plqy)为86%,半峰全宽(fwhm)为0.41ev,发射寿命为5μs。最高占据分子轨道(e
homo
)的能量为-5.85ev。
[0492]
实施例3
[0493][0494]
根据aav6(收率=35%)、aav7(收率=82%)和aav8(收率=15%)合成实施例3。
[0495]
hplc-ms:1036.9m/z。
[0496]
图3描绘了实施例3(在pmma中占10重量%)的发射光谱。发射最大值(λ
max
)为466nm。光致发光量子产率(plqy)为83%,半峰全宽(fwhm)为0.42ev,发射寿命为25μs。最高占据分子轨道(e
homo
)的能量为-6.05ev。
[0497]
实施例4
[0498][0499]
根据aav3(收率=89%)和aav8(收率=78%)合成实施例4。
[0500]
hplc-ms:700.40m/z。
[0501]
图4描绘了实施例4(在pmma中占10重量%)的发射光谱。发射最大值(λ
max
)为466nm。光致发光量子产率(plqy)为64%,半峰全宽(fwhm)为0.50ev,ciey坐标为0.20。最高占据分子轨道(e
homo
)的能量为-6.19ev。
[0502]
实施例5
[0503][0504]
通过以下合成途径合成实施例5:基于aav8的条件,进行取代咔唑的引入,从而得到以下中间体(收率=92%)。在另外两个步骤中,完成aav7(收率=31%)和aav8(收率=74%)以获得作为最终产物的实施例5。
[0505]
hplc-ms:851.30m/z。
[0506]
图5描绘了实施例5(在pmma中占10重量%)的发射光谱。发射最大值(λ
max
)为468nm,ciey坐标为0.21。光致发光量子产率(plqy)为65%,半峰全宽(fwhm)为0.44ev,发射寿命为83μs。
[0507]
实施例d1
[0508]
在oled d1中测试实施例3,该oled被制造成具有以下层结构:
[0509][0510]
器件d1在1000cd/m2时产生的外部量子效率(eqe)为13.1
±
0.3%。发射最大值为475nm,fwhm为10.0v时为66nm。相应的ciex值为0.15,ciey为0.25。
[0511]
本发明的有机分子的其他实施例
[0512]
[0513]
[0514]
[0515]
[0516]
[0517]
[0518]
[0519]
[0520]
[0521][0522]
图
[0523]
图1 pmma中的实施例1(10重量%)的发射光谱。
[0524]
图2 pmma中的实施例2(10重量%)的发射光谱。
[0525]
图3 pmma中的实施例3(10重量%)的发射光谱。
[0526]
图4 pmma中的实施例4(10重量%)的发射光谱。
[0527]
图5 pmma中的实施例5(10重量%)的发射光谱。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1