一种腈水合酶突变体及其应用的制作方法
本发明涉及一种腈水合酶突变体及其应用,属于生物工程技术领域。
背景技术:
腈水合酶(nitrilehydratase,简称nhase,ec4.2.1.84),是一类可以催化腈类物质通过水合反应转化为高附加值酰胺类化合物的金属酶,在精细化学品烟酰胺的工业生产上有着巨大的应用潜力。酰胺类的生物法生产技术是生物法替代化学法的典型案例,具有绿色环保、反应条件较温和、安全系数高等优势,符合可持续发展和绿色生产理念。
酰胺类产品在工业、农业及医药等领域有着极大的应用价值,尤其以烟酰胺和丙烯酰胺的生物催化最为常见。其中,烟酰胺是一种重要的化工生产原料,用途广泛。烟酰胺本身为维生素b12的辅酶,可以作为维生素补剂,还可用来合成多种维生素衍生物,市场前景广阔。
腈水合酶不仅在应用层面展现了重要作用,另外,作为一种能够结合钴离子或铁离子的金属酶,其催化活性和稳定性也引起了研究者的广泛关注。腈水合酶通常由α和β两个亚基构成,研究发现,目前已报道的原核生物来源的腈水合酶大都存在稳定性差、催化活性低、催化底物谱窄的问题。许多研究团队通过构建共价键相互作用、盐键和添加link以及亚基融合等策略提高其稳定性,但是几乎没有通过酶的改造同时提高其酶活和稳定性,甚至拓宽底物谱的报道。
温泉热碱芽孢杆菌(caldalkalibacillusthermarumta2.a1)来源的腈水合酶具有较好的热稳定性,基于这一特性,可以尝试提高其催化活性及拓宽底物谱。目前工业上的大宗化学品生产,比如丙烯酰胺和烟酰胺,除了受限于热稳定性外,催化效率也不高。因此,提高腈水合酶的稳定性和催化活性具有极大的应用价值和广阔的应用前景。
技术实现要素:
针对现有的技术难点及存在的问题,本发明提供了一种来源于温泉热碱芽孢杆菌(caldalkalibacillusthermarumta2.a1)的腈水合酶的氨基酸基序及其在底物催化生产上的应用。
本发明的第一个目的是提供腈水合酶突变体,含有α亚基、β亚基以及调控蛋白。
在本发明的一种实施方式中,所述α亚基的氨基酸序列如seqidno.1。
在本发明的一种实施方式中,所述β亚基的氨基酸序列如seqidno.4或seqidno.5。
在本发明的一种实施方式中,所述调控蛋白的氨基酸序列如seqidno.3。
本发明的第二个目的是提供编码所述突变体的基因。
本发明的第三个目的是提供含有所述基因的载体。
本发明的第四个目的是提供所述腈水合酶突变体的微生物细胞。
在本发明的一种实施方式中,所述细胞是以大肠杆菌bl21为宿主,以pet系列质粒为载体。
在本发明的一种实施方式中,所述质粒为pet-24(+)。
本发明的第五个目的是提供一种提高腈水合酶酶活力的方法,是将氨基酸序列如seqidno.2所示的腈水合酶β亚基第48位亮基酸突变为天冬氨酸或组氨酸。
本发明的第六个目的是提供一种重组表达所述腈水合酶突变体的方法,将表达所述腈水合酶突变体的微生物细胞接种于lb培养基中,37℃培养至od600为0.6-0.8时,加入诱导剂iptg于24℃诱导12-16h。
本发明的第七个目的是提供上述的腈水合酶突变体或含有腈水合酶突变体的微生物细胞在生产含烟酰胺的产品中的应用。
有益效果:
本发明提供了一段cal.t-nhase的氨基酸基序及突变体的氨基酸基序,该基序与其他来源的腈水合酶基序在α亚基上酶活中心的108、111和113位点均是高度保守的,它们分别与钴离子形成配位键。本发明对腈水合酶氨基酸基序中β亚基上的第48号构建的单点突变体l48d和l48h的酶活分别为750.26±1.63u/mg、820.01±0.98u/mg,与未进行改造的野生型腈水合酶的比酶活220.30±2.28u/mg相比,都有明显的提高。其中,突变体l48d的酶活约为野生型的3.4倍,突变体l48h的酶活约为野生型的3.7倍。上述这两个氨基酸残基的突变显著改善腈水合酶催化活性,有利于应用于工业上精细化学品如烟酰胺的生产,提高催化效率,降低生产成本。
附图说明
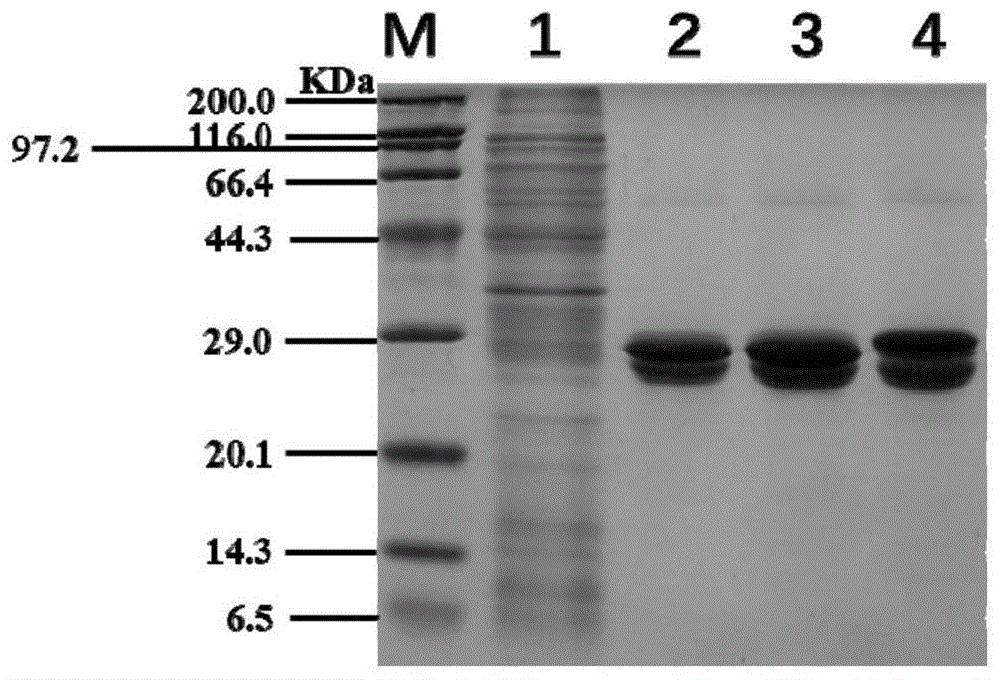
图1:纯酶的sds-page电泳图,m:蛋白marker,1:pet24a,2:wt,3:l48d,4:l48h。
图2:cal.tnhase野生酶wt与突变体l48d、l48h、a41k、y46e以及v126k的比酶活。
图3:cal.tnhase突变体l48h应用生产烟酰胺。
具体实施方式
1、培养基:
lb培养基(l-1):胰蛋白胨10g,nacl10g,酵母提取物5g,ph7.0,配制固体培养基时添加琼脂粉20g。
无甘油tb培养基(l-1):胰蛋白胨12g,酵母提取物24g,kh2po42.31g,k2hpo412.54g。
2、缓冲液:
结合缓冲液:20mmna2hpo4·12h2o,280mmnacl,6mmkcl,ph7.4
洗脱缓冲液:20mmna2hpo4·12h2o,280mmnacl,6mmkcl,2.5mmd-desthiobiotin,ph7.4。
腈水合酶的酶活力(u):单位酶活力定义为25℃下,每分钟催化烟腈生成1μmol烟酰胺所需要的酶量。
腈水合酶的比酶活(u/mg):每毫克腈水合酶所具有的酶活力。
实施例1:腈水合酶突变体的质粒构建
以野生型质粒pet24a(+)-cal.twt(张赛兰,李婷,程中一等.新型耐热腈水合酶的异源表达及其催化工艺研究[j].食品与发酵工业,2020,第46卷(14):108-113中pet24a(+)-cal.tnhase)为模板,将突变位点l48d和l48h设计在引物上,通过pcr扩增出碱基序列发生突变的质粒,所用引物序列如表1所示,扩增体系如表2所示。
pcr扩增反应条件为95℃预变性3min,98℃变性15s,55℃退火30s,72℃延伸1min45s,72℃延伸5min,共30个循环。将pcr产物用dpni消化酶消化2-3h,转化e.colidh5α,涂布于含50mg/l卡那霉素的lb培养基平板,37℃倒置过夜培养。
挑取单菌落接种于5mllb培养基,37℃、200rpm振荡培养过夜,使用商品化质粒抽提试剂盒获得重组质粒,由苏州金唯智生物科技有限公司进行测序验证,最终得到重构质粒pet24a(+)-l48d,pet24a(+)-l48h。
表1引物序列
(注:f代指上游引物,r代指下游引物)
表2pcr扩增体系
实施例2:野生酶wt与各突变体的表达与纯化
步骤1:将实施例1获得的cal.tnhase的野生型pet24a(+)-cal.twt及重构质粒pet24a(+)-l48d,pet24a(+)-l48h分别转化e.colibl21(de3),挑取单菌落至5mllb培养基,37℃、200rpm条件下培养7-8h。将种子液按1%(v/v)接种量转接至100ml2×yt培养基,37℃、200rpm条件下培养至od600至0.6-0.8,加入终浓度为0.4mm的异丙基硫代半乳糖苷(iptg)以及0.1g/l的cocl2·6h2o,改变培养温度为24℃,诱导表达12-16h。
步骤2:采用亲和层析的方法纯化野生型wt及其2个突变体,纯化柱为ge公司的streptraphp1ml柱。在10000rpm条件下离心3min收集菌体细胞,用20ml结合缓冲液重悬,于冰水混合物中超声破碎。破碎液在4℃、12000rpm条件下离心30min,取上清液过0.22μm有机滤膜。纯化柱在用结合缓冲液平衡后,进行上样,然后用结合缓冲液洗去杂蛋白,目的蛋白用100%的洗脱缓冲液洗脱并收集。蛋白浓度使用bradford蛋白浓度检测试剂盒进行定量。采用sds-page检测目的蛋白的纯化质量,检测如图1所示,可见野生型及其突变体所表达的蛋白在纯化后蛋白条带单一,纯化质量高。
实施例3:cal.tnhase的野生型及突变体催化效率检测
用10mmkpb(ph7.4)溶液将wt及其突变体纯酶的浓度稀释至0.5mg/ml,取10μl至1.5ml离心管中,置于25℃金属浴上。向离心管中加入490μl底物(200mm烟腈溶液),充分涡旋混匀,25℃下反应10min,然后加入500μl纯乙腈溶液进行终止。将反应液用纯乙腈溶液稀释适当倍数,过0.22μm滤膜。液相检测方法:流动相组成为乙腈:水=1:2(v/v),流速为0.6ml/min,检测波长为215nm,柱温为40℃,测定反应体系中产物烟酰胺的生成量。wt及突变体的比酶活计算结果如图2所示,野生酶wt的比酶活为220.30±2.28u/mg,突变体l48d和l48h的酶活分别为750.26±1.63u/mg、820.01±0.98u/mg。
两突变体酶活较野生型分别提高了约70%和73%,即当对该位点氨基酸残基发生突变时,腈水合酶的比酶活均有不同程度地提高,说明上述这个个氨基酸残基可能在两个亚基的关键结构域,对于腈水合酶的催化活性具有重要作用。
实施例4:腈水合酶野生型和突变体在烟酰胺生产上的应用
将实施例2步骤1得到的bl21(de3)/pet24a(+)-cal.tnhase-l48h菌液离心收集,水洗后再次离心收集,10mmol/l、ph=7.4h3po4缓冲溶液重悬浮,调整至菌液od600=8。调整温度为30℃,烟腈以0.4mol/l的终浓度加入到od600=8的菌液中,并不断搅拌,每隔6min添加烟腈,添加量为0.4mol/(l·次)。反应体系中产物烟酰胺的生成量的测定同实施例3,计算得到烟酰胺的浓度为706g/l,如图3所示。文献中报道的野生型腈水合酶的烟酰胺产量为495g/l(张赛兰,李婷,程中一等.新型耐热腈水合酶的异源表达及其催化工艺研究[j].食品与发酵工业,2020,第46卷(14):108-113),相对来说催化提高了42.6%。
对比例1:突变体pet24a(+)-l48h与pet24a(+)-y46e催化效率比较
具体实施方式同实施例1,区别在于,对位点46位的酪氨酸进行突变为谷氨酸,按照实施例2制备得到酶突变体,并用于烟酰胺的催化反应,结果如图2所示,其催化烟腈的酶活为375.29±0.65u/mg,相比实施例1提供的突变体l48h低了54%,突变体pet24a(+)-l48h酶活显著高于pet24a(+)-y46e。
虽然本发明已以较佳实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可做各种的改动与修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
sequencelisting
<110>江南大学
<120>一种腈水合酶突变体及其应用
<130>baa201487a
<160>5
<170>patentinversion3.3
<210>1
<211>210
<212>prt
<213>人工序列
<400>1
metlysaspasnasnlysvalhishishishisprohisprogluser
151015
phetrpseralaargalalysalaleugluserleuleuileglulys
202530
glyileleuserseraspalaileaspargvalvalglnhistyrglu
354045
hisgluleuglyprometasnglyalalysvalvalalalysalatrp
505560
thraspproalaphelysglnargleuleugluaspprogluthrval
65707580
leuarggluleuglytyrtyrglyleuglnglygluhisileargval
859095
valgluasnthraspthrvalhisasnvalvalvalcysthrleucys
100105110
sercystyrprotrpproleuleuglyleuproproalatrptyrlys
115120125
gluprothrtyrargserargilevallysgluproarglysvalleu
130135140
arggluglupheglyleuaspleuproaspthrvalgluileargval
145150155160
trpaspserserserglumetargtyrmetvalleuproglnargpro
165170175
gluglythrgluglymetthrgluglugluleualalysilevalthr
180185190
argaspsermetileglyvalalalysvalglnproserservalthr
195200205
valarg
210
<210>2
<211>225
<212>prt
<213>人工序列
<400>2
metasnglyilehisaspleuglyglymetaspglypheglylysile
151015
ileargglugluasngluproleuphehislysasptrpgluargile
202530
alapheglyleuleuileglythralaglyglnglyleutyrasnleu
354045
aspgluphearghisalailegluargmetasnprovalasptyrleu
505560
thrserglytyrtyrglyhistrpvalalaserilealathrleuleu
65707580
valglulysglyileleuaspalasergluleuvalserargthrgln
859095
thrtyrleualaglnproaspthrlysthrproargarggluasnpro
100105110
gluleuvalasnhisleugluglnvalilelysvalglyvalserthr
115120125
valarggluvalserseralaproargpheasnvalglyaspargval
130135140
lysthrlysasnilehisproserglyhisthrargleuproargtyr
145150155160
alaargasplystyrglyvalilealamettyrhisglyalahisval
165170175
pheproaspalaasnalahisglylysglygluserproglnhisleu
180185190
tyrcysileargpheglualaasngluleutrpglyileglnglngly
195200205
glualavaltyrileaspleutrpglusertyrleugluprovalser
210215220
his
225
<210>3
<211>122
<212>prt
<213>人工序列
<400>3
metglulysasncysvalserglnservalaspserlysilealatyr
151015
leuprogluseralaalaproproarglysasnglygluleuvalphe
202530
glugluprotrpgluargargserpheglymetalaleualaleutyr
354045
gluglulysargtyrthrsertrpaspasppheargthrargleuile
505560
glngluilealalystrpglusersergluasnglnasplysleuasp
65707580
trpasntyrtyrgluhistrpleualaalaleugluglnleuvalval
859095
gluthrglymetileasplyshisaspileaspalaargthrlysglu
100105110
pheleuserglygluargaspgluphephe
115120
<210>4
<211>225
<212>prt
<213>人工序列
<400>4
metasnglyilehisaspleuglyglymetaspglypheglylysile
151015
ileargglugluasngluproleuphehislysasptrpgluargile
202530
alapheglyleuleuileglythralaglyglnglyleutyrasnasp
354045
aspgluphearghisalailegluargmetasnprovalasptyrleu
505560
thrserglytyrtyrglyhistrpvalalaserilealathrleuleu
65707580
valglulysglyileleuaspalasergluleuvalserargthrgln
859095
thrtyrleualaglnproaspthrlysthrproargarggluasnpro
100105110
gluleuvalasnhisleugluglnvalilelysvalglyvalserthr
115120125
valarggluvalserseralaproargpheasnvalglyaspargval
130135140
lysthrlysasnilehisproserglyhisthrargleuproargtyr
145150155160
alaargasplystyrglyvalilealamettyrhisglyalahisval
165170175
pheproaspalaasnalahisglylysglygluserproglnhisleu
180185190
tyrcysileargpheglualaasngluleutrpglyileglnglngly
195200205
glualavaltyrileaspleutrpglusertyrleugluprovalser
210215220
his
225
<210>5
<211>225
<212>prt
<213>人工序列
<400>5
metasnglyilehisaspleuglyglymetaspglypheglylysile
151015
ileargglugluasngluproleuphehislysasptrpgluargile
202530
alapheglyleuleuileglythralaglyglnglyleutyrasnhis
354045
aspgluphearghisalailegluargmetasnprovalasptyrleu
505560
thrserglytyrtyrglyhistrpvalalaserilealathrleuleu
65707580
valglulysglyileleuaspalasergluleuvalserargthrgln
859095
thrtyrleualaglnproaspthrlysthrproargarggluasnpro
100105110
gluleuvalasnhisleugluglnvalilelysvalglyvalserthr
115120125
valarggluvalserseralaproargpheasnvalglyaspargval
130135140
lysthrlysasnilehisproserglyhisthrargleuproargtyr
145150155160
alaargasplystyrglyvalilealamettyrhisglyalahisval
165170175
pheproaspalaasnalahisglylysglygluserproglnhisleu
180185190
tyrcysileargpheglualaasngluleutrpglyileglnglngly
195200205
glualavaltyrileaspleutrpglusertyrleugluprovalser
210215220
his
225
- 还没有人留言评论。精彩留言会获得点赞!