(R)‑1‑(2‑(萘基)乙基)硫脲修饰的Al‑Anderson型杂多酸催化剂、制备方法及其应用与流程
本发明属于催化化学技术领域,尤其涉及不对称选择催化领域,具体来说,涉及一种(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂、制备方法及其应用。
背景技术:
2001年诺贝尔奖获得者Noyori教授指出:“未来的合成化学必须是经济的、安全的、环境友好的以及节省资源和能源的化学,化学家需要为实现‘完美的反应化学’而努力,即以100%的选择性和100%的收率只生成需要的产物而没有废物产生”。手性催化合成作为实现“完美合成化学”的重要途径之一,其中,手性催化剂是手性催化研究中的最核心科学问题。从反应原理上看,手性有机小分子催化是通过和反应底物以不稳定的共价键可逆地形成活性中间体或通过若相互作用,如氧键、范德华力或离子对等活化反应底物。虽然均相手性催化具有高效、高对映选择性和反应条件温和等特点,但大多数情况下,催化剂用量高摩尔分数。要实现这些催化反应在工业上的应用,必须解决昂贵催化剂的回收利用是个严重的问题。
催化是多金属氧酸盐应用中最有前途且最具实用价值的研究方向。多金属氧酸盐同时集酸碱催化剂、氧化还原催化剂、金属氧化物纳米催化剂等的优良特性于一身,被认为是一种应用广泛的绿色的多功能催化剂。早在20世纪初,人们就开始对多酸的催化性能进行了研究。到目前为,已有8个多酸催化工业化项目被成功开发。催化成为了多酸化学中一项永恒的研究课题。自从手性多金属氧酸盐被成功合成以后,人们便开始了手性多酸在不对称催化领域的探索。手性多金属氧酸盐集多酸与手性材料的各种优异性能于一身。其独特的可溶性类矿物金属-氧化物结构,为手性的非生命起源学说及无机固体中手性传递的探索提供了理想的模型;其高的负电性,可调的酸碱性、氧化还原活性及纳米尺寸,更为多功能非线性光学、纳米材料、立体选择性催化以及医药等新材料的设计、合成带来了新的希望。
目前,手性有机小分子催化剂很难实现用于工业化生产,主要由于催化剂活性较低、用量高且不易回收利用。要实现这些催化反应在工业上的应用,必须解决昂贵催化剂的回收利用是个严重的问题。
自从1993年Zubieta等人在《Nature》上报道采用水热技术成功制备了类似DNA的手性双螺旋结构的化合物(Me2NH2)K4[V10O10(H2O)4(OH)4(PO4)7]·H2O后,人们便开始了手性多酸在不对称催化领域的探索。中国科学院化学所的罗三中教授等更在以有机胺小分子催化剂作为抗衡阳离子,多酸作为催化剂负载载体的领域做出了出色的工作(Organic letters,2007,9(18):3675-3678.)。他们合成了一系列的仲胺-叔胺型脯氨酸衍生物,采用强酸性多阴离子的[PW12O40]3-替代传统酸-碱协同催化中的矿物酸,合成了一系列手性有机胺-多酸杂化材料。这些材料对醛酮的直接Aldol反应,不对称Michael加成反应等都表现出很高的催化活性和手性选择性,但这些材料没有明确的分子结构,不能进一步探究催化机理,不能解释手性胺与多酸的协同作用。大连物化所段春迎课题组利用多金属氧酸盐(POMs)的组成、结构的多样性以及电荷的可调变性,设计组装一系列具有催化功能的多孔性的POMOFs,实现了它们在多相催化中的应用(Journal of the American Chemical Society,2013,135(28):10186-10189.),但这些材料同样没有明确的分子结构,不能进一步探究催化机理,不能解释MOFs与POMs的协同作用。
综上所述,手性有机小分子催化剂很难实现用于工业化生产,主要由于手性有机小分子催化剂活性较低、用量高且不易回收利用。要实现这些催化反应在工业上的应用,必须解决昂贵催化剂的回收利用是个严重的问题。现有的手性有机小分子与POMs结合的新型材料,没有明确的分子结构,不能进一步探究催化机理,不能解释手性有机小分子与多酸的协同作用。
技术实现要素:
针对现有技术中的上述技术问题,本发明提供了一种(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂、制备方法及其应用。本发明的制备方法解决了现有手性有机小分子催化剂活性较低、用量高且不易回收利用的技术问题。得到的催化剂活性高,可用于醛氧化成酸的反应中。
本发明从有机小分子催化剂的设计思路出发,创新性地提出利用“酸-碱”协同催化策略,以具有潜在催化活性的手性有机小分子作为前躯体,通过有机修饰等方法,巧妙地使有机小分子与高Bronsted酸性的缺位多阴离子结合,构筑手性多酸材料的思路,并在实现这一思路的同时,有机修饰的多酸不但保留了多酸原有的结构,而且拓展了多酸的研究领域,使其在催化、药物和功能材料方面具有潜在应用价值。以期望实现高的催化活性和高的对映选择性催化的同时,解决昂贵催化剂的回收利用是个严重的问题。
本发明的技术方案具体介绍如下。
本发明提供一种(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂的制备方法,具体步骤如下:
1)将二水合钼酸钠与六水合三氯化铝在酸性条件下反应生成Al-Anderson型杂多酸Na3[Al(OH)6Mo6O18]·10H2O;
2)将上述得到的Al-Anderson型杂多酸母体Na3[Al(OH)6Mo6O18]·10H2O与三羟基氨基甲烷进行水热反应后,再室温下和四丁基溴化铵TBAB反应得到有机单侧氨基修饰的Al-Anderson型多金属氧酸盐[TBA]3{[NH2C(CH2O)3]AlMo6O18(OH)3};
3)以(R)-(+)-1-萘乙胺为原料合成(R)-1-(2-(萘基)乙基)异硫氰酸酯;
4)将(R)-1-(2-(萘基)乙基)异硫氰酸酯与有机单侧氨基修饰的Al-Anderson型多金属氧酸盐反应得到(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂。
本发明中,步骤)中,二水合钼酸钠和六水合三氯化铝的摩尔比为1:1~1:2,pH值在1.5~2之间。优选的,pH用盐酸或者盐酸和醋酸的混合物调节。
本发明中,步骤2)中,水热反应的温度为135~145℃,反应时间为20~30h;Al-Anderson型杂多酸母体Na3[Al(OH)6Mo6O18]与三羟基氨基甲烷的摩尔比为1:2~1:5;Al-Anderson型杂多酸母体Na3[Al(OH)6Mo6O18]和四丁基溴化铵TBAB的摩尔比为1:3~1:5。
本发明中,步骤4)中,有机单侧氨基修饰的Al-Anderson型多金属氧酸盐与(R)-1-(2-(萘基)乙基)异硫氰酸酯的摩尔比为1:3~1:5;反应温度为45~55℃,反应时间为2~3天,反应溶剂为极性非质子溶剂。
本发明还提供一种上述制备方法得到的(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂。
本发明进一步提供上述本发明中的(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂芳香醛催化氧化制备芳香羧酸反应领域中的应用。应用方法如下:取适量芳香醛,在50~70℃的温度、以水为溶剂的条件下,加入(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂,在氧化剂作用下搅拌反应,得到芳香羧酸。优选的,使用过氧化氢作为氧化剂,(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂的使用量为芳香醛的0.5mol%~2mol%。
本发明中,催化氧化反应结束后,反应结束向相体系中加入有机溶剂(乙醚、乙醇、甲醇等)后,多酸析出,处理后进行回收利用,将回收的催化剂再次用于芳香醛的催化氧化反应。
和现有技术相比,本发明的有益效果在于:本发明不仅可以利用手性有机小分子的共价修饰作用打破多酸的高对称性,引入手性,提高其在催化反应中的立体选择性,而且也能将有机手性小分子的不对称催化或生物医药活性等功能特性引入多酸,并使有机部分与无机的多阴离子有机地结合为一个整体,从而产生协同作用获得更多新颖的性质。该催化剂具有反应条件温和、环境友好、高效、高对应选择性和可回收利用等优点,可适用于工业化生产。同时,以常见非贵金属为中心原子,使得本催化剂具有更加低廉的生产成本,更具有市场推广价值。
附图说明
图1是本发明的合成路线图。
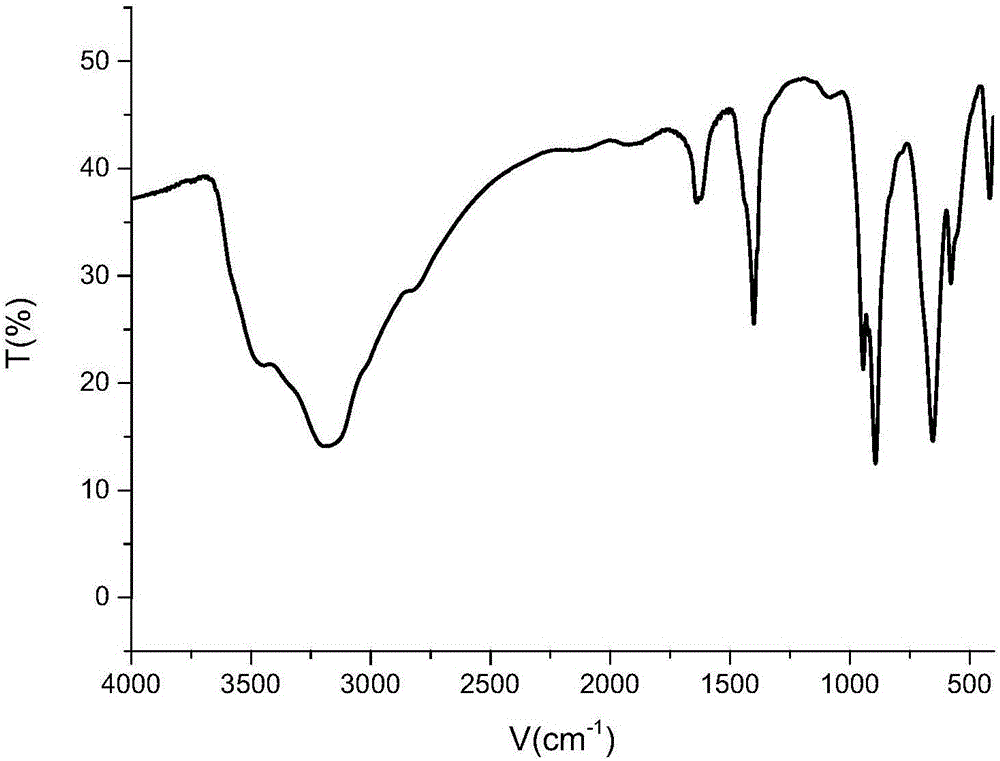
图2是母体Na3[Al(OH)6Mo6O18]的红外谱图。
图3是(R)-1-(2-(萘基)乙基)异硫氰酸酯的核磁谱图。
图4是单侧氨基修饰的Al-Anderson型多金属氧酸盐的红外谱图。
图5是(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂的核磁谱图。
具体实施方式
以下采用实施例来详细说明本发明的实施方式,借此对本发明如何应用技术手段来解决技术问题,并达成技术效果的实现过程能充分理解并据以实施。
图1是本发明的合成路线图。
实施例1
Al-Anderson型杂多酸母体Na3[Al(OH)6Mo6O18]的制备
取14g(59.6mmol)钼酸钠加入到500mL去离子水中,充分搅拌得到澄清液,室温下维持强力搅拌,开始缓慢加入6g(37.2mmol)氯化铝固体,缓慢加入200mL冰醋酸。之后滴加36%浓盐酸,将体系的pH调到1.5~2.0。停止搅拌,将液体倾倒入烧杯中静置,待白色针状晶体长出。抽滤,得到11.48g白色晶状固体原料,收率82%。
母体Na3[Al(OH)6Mo6O18]的红外谱图如图2所示。
实施例2
(R)-1-(2-(萘基)乙基)异硫氰酸酯的制备
在干燥的反应容器中加入(R)-1-萘乙胺(5mmol),用20mL醇溶解,随后分别缓慢加入加CS2(0.1142g,15mmol)和三乙胺(0.506mg,5mmol),在室温搅拌反应1h后,随后在0℃条件下加入二碳酸二叔丁酯(Boc2O)(1.091mg,5mmol)和4-二甲氨基吡啶(DMAP)(18mg,0.15mmol),在室温搅拌反应2h后(在搅拌的过程有气体产生,应注意放气减压),可获得0.7451g(R)-1-(2-(萘基)乙基)异硫氰酸酯。
(R)-1-(2-(萘基)乙基)异硫氰酸酯的核磁谱图数据如图3所示。
1H NMR(501MHz,CDCl3)δ7.3-7.5(dt,J=12.3,7.7Hz,5H),4.90-4.95(q,J=6.7Hz,1H),1.65-1.70(d,J=6.8Hz,3H).
实施例3
单侧氨基修饰的Al-Anderson型多金属氧酸盐的制备
将上述得到的Anderson母体Na3[Al(OH)6Mo6O18]1.071g(1mmol)用10mL去离子水中溶解,得到浅无色透明清液后,缓慢加入三羟基氨基甲烷0.402g(3mmol)。之后将上述体系加入水热釜,在水热釜中加热到140℃,反应进行24h后,在85℃条件下将4.83g四丁基溴化铵加如上述溶解的溶液中,产生大量白色沉淀即粗产物,抽滤即可得到无色透明液体,放置得到结晶,即为有机单侧氨基修饰的Al-Anderson型多酸[TBA]3{[CH2NH2C(CH2O)3]AlMo6O18(OH)3}。
单侧氨基修饰的Al-Anderson型多金属氧酸盐的红外谱图如图4所示。
实施例4
(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂的制备
将有机单侧氨基修饰[TBA]3{[CH2NH2C(CH2O)3]AlMo6O18(OH)3}0.5g(0.279mmol)用5mL的DMF在50℃条件下溶解后,加入(R)-1-(2-(萘基)乙基)异硫氰酸酯0.224g(1.375mmol),维持50℃搅拌条件下,反应时间2~3天,反应结束后将无色澄清液放置乙醚氛围中结晶,若干天后可得到无色透明晶体,即获得(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂。
(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂的核磁谱图数据如图5所示。
1H NMR(501MHz,DMSO)δ7.90(s,2H),7.22(d,J=52.0Hz,5H),2.99(d,J=136.8Hz,23H),1.52(s,24H),1.23(d,J=43.5Hz,24H),0.89(s,36H)。
应用实施例
(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂催化氧化芳香醛制备芳香羧酸的反应
在反应管中加入1mmol的芳香醛以及0.1mol%的(R)-1-(2-(萘基)乙基)硫脲修饰的Al-Anderson型杂多酸催化剂,加入5ml H2O作为溶剂,加入4mmol的H2O2作为氧化剂,在50~70℃下反应24h。反应进度及产率可通过GC-Ms进行测试。催化的产物及收率结果见表1。催化剂(苯甲醛催化氧化体系)回收利用所得到的结果见表2。
表1.Al-Anderson型杂多酸催化剂催化氧化芳香醛的反应结果
表2 催化剂回收利用的实验结果
所有上述的首要实施这一知识产权,并没有设定限制其他形式的实施这种新产品和/或新方法。本领域技术人员将利用这一重要信息,上述内容修改,以实现类似的执行情况。但是,所有修改或改造基于本发明新产品属于保留的权利。
以上所述,仅是本发明的较佳实施例而已,并非是对本发明作其它形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更或改型为等同变化的等效实施例。但是凡是未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与改型,仍属于本发明技术方案的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!