一种N‑乙酰L‑半胱氨酸保护的金纳米的应用及应用方法与流程
本发明属于电化学传感器和分子识别技术领域,具体涉及一种N-乙酰L-半胱氨酸保护的金纳米的应用及应用方法。
背景技术:
手性识别是化学、生物学、医药学领域的一个常见现象。手性分子是拥有完全相同的化学性质和物理性质,但是它们在生物活性和药理方面却有很大的不同,甚至是截然相反的效果。比如:天冬氨酸S型是苦味的,而R型是甜味的;沙丁胺醇S型可严重的致畸,而R型是镇静剂,可缓解妊娠妇女的晨吐反应。氯胺酮S型是麻醉剂,作为临床术前麻醉使用,而R型是致幻剂,禁止使用;乙胺丁醇S型可治疗结核,而R型可致盲。再比如酪氨酸,酪氨酸L型为人体非必须氨基酸,缺乏时可能会导致忧郁症及其他心理疾病,而过量的话会增加姐妹染色体交换的机率,影响下一代儿童的健康发育。而酪氨酸D型作为非蛋白氨基酸的一种,在研讨蛋白质的结构和运作机能方面有重要的意义。因而手性识别对映异构体具有重要的意义。
目前,手性识别方法主要有以下几种:毛细管电泳法、高效液相色谱法、荧光光谱检测法和电化学方法。其中毛细管电泳法、高效液相色谱法分析成本高,分析时间长,不利于快速检测;荧光光谱检测法检测范围窄。因此,亟待发展一种简单、快速、灵敏的手性识别方法。
技术实现要素:
本发明的目的是一种N-乙酰L-半胱氨酸保护的金纳米的应用及应用方法。
本发明的技术方案为:
一种N-乙酰L-半胱氨酸保护的金纳米的应用,用于电化学方法手性识别酪氨酸。
本发明N-乙酰L-半胱氨酸保护的金纳米的应用方法,包括以下步骤:
a.配制溶剂为0.1mol/L的KCl溶液,pH为6~7的N-乙酰L-半胱氨酸保护的金纳米溶液,采用循环伏安法沉积在玻碳电极表面,得到N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极NALC-Au/GCE;
b.将步骤a中制得的N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极NALC-Au/GCE静置在pH为6~7的L-酪氨酸或D-酪氨酸溶液中,采用循环伏安法沉积在电极表面,得到N-乙酰L-半胱氨酸保护的金纳米和酪氨酸修饰的玻碳电极NALC-Au/GCE-L-/D-Tyr;
c.将步骤b中制得的N-乙酰L-半胱氨酸保护的金纳米和酪氨酸修饰的玻碳电极NALC-Au/GCE-L-/D-Tyr在铁氰化钾/KCl的溶液中进行循环伏安和电化学阻抗手性识别。
进一步地,本发明所述步骤a中的N-乙酰L-半胱氨酸保护的金纳米溶液的浓度为10~100mmol/L,溶液pH的缓冲对由磷酸氢二钠和磷酸二氢钾组成,pH为6~7。
本发明所述的步骤a中N-乙酰L-半胱氨酸保护的金纳米沉积电压-0.75~1.6V,沉积圈数2~8圈。
本发明所述的步骤b中L-酪氨酸或D-酪氨酸溶液浓度为10~769mmol/L,溶液pH的缓冲对由磷酸氢二钠和磷酸二氢钾组成,pH为4.07~7。
本发明所述的步骤b中L-酪氨酸或D-酪氨酸溶液的沉积电位为0.4~1V,沉积圈数为1~6圈。
本发明所述的步骤c中铁氰化钾溶液的浓度为1~10mmol/L。
本发明采用上述技术方案,基于电化学阻抗的方法,进行酪氨酸对映异构体的识别,试验证明该方法制备工艺简单,检测成本低廉,稳定性好。
附图说明
图1为实施例1中N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极和对L-酪氨酸或D-酪氨酸对映体识别的循环伏安图;图1中a:GCE,b:N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极,c:N-乙酰L-半胱氨酸保护的金纳米和L-Tyr修饰的玻碳电极,d:N-乙酰L-半胱氨酸保护的金纳米和D-Tyr修饰的玻碳电极;
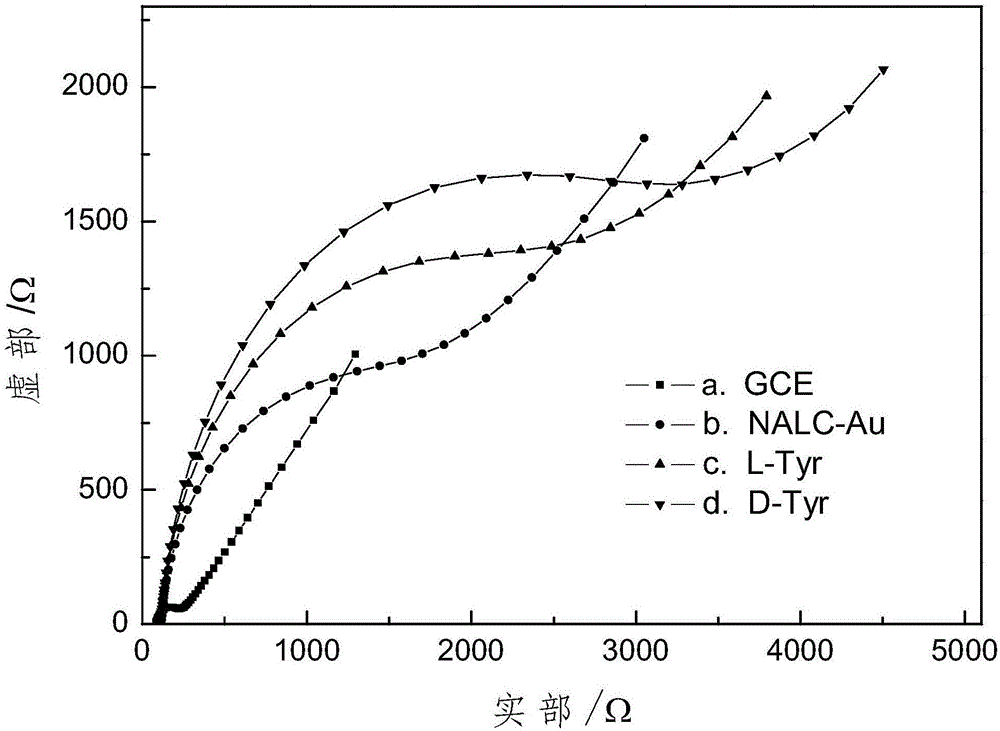
图2为实施例2中N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极和对L-酪氨酸或D-酪氨酸对映体识别的阻抗图,由图2可见,D型酪氨酸的阻抗值明显大于L型酪氨酸的阻抗值;图2中a:GCE,b:N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极,c:N-乙酰L-半胱氨酸保护的金纳米和L-Tyr修饰的玻碳电极,d:N-乙酰L-半胱氨酸保护的金纳米和D-Tyr修饰的玻碳电极;
图3为实施例3中,N-乙酰L-半胱氨酸保护的金纳米沉积圈数对电极修饰的影响;
图4为实施例3中,酪氨酸溶液沉积圈数对手性识别酪氨酸的影响;
图5为实施例4中,酪氨酸溶液pH对手性识别酪氨酸的影响;
图6为实施例5中,酪氨酸溶液浓度对手性识别酪氨酸的影响。
具体实施方式
实施例1
N-乙酰L-半胱氨酸保护的金纳米的应用方法:
制备N-乙酰L-半胱氨酸保护的金纳米:
称取0.227g N-乙酰L-半胱氨酸,溶解于10mL体积比为6:1的甲醇一冰乙酸溶液中。称取0.182g氯金酸,溶解于10mL体积比为6:1的甲醇一冰乙酸溶液中。将氯金酸溶液转移至100mL的圆底烧瓶里,冰浴搅拌下加入已配好的N-乙酰L-半胱氨酸甲醇一冰乙酸溶液,当溶液由金黄色变为橙色时,一次性快速加入5mL含硼氢化钠(0.35g)的乙醇超声分散溶液,反应30min,加入50mL丙酮停止反应。离心收集沉淀。用适量丙酮和水将上述沉淀物反复溶解、沉淀、离心、洗涤,再用8000-14000Da的透析袋透析以除去溶液中存在的杂质离子,氮气吹干后置于4℃冰箱保存。
a.配制N-乙酰L-半胱氨酸保护的金纳米溶液55mmol/L(溶剂为0.1mol/LKCl,pH=6.53),采用循环伏安法沉积在玻碳电极表面,沉积电压为-0.75~1.6V,沉积圈数6圈,得到N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极,由图1(b)、图2(b)可知,N-乙酰L-半胱氨酸保护的金纳米已成功修饰到玻碳电极表面。
b.将步骤(a)得到的电极静置在L-酪氨酸或D-酪氨酸溶液(pH=6.53)中,采用循环伏安法将L-酪氨酸或D-酪氨酸沉积在电极表面,得到N-乙酰L-半胱氨酸保护的金纳米和酪氨酸的修饰电极。由图1(c)、1(d)和图2(c)、2(d)可知,酪氨酸成功的修饰到电极表面。
c.将步骤(b)中制得的N-乙酰L-半胱氨酸保护的金纳米和酪氨酸的修饰电极置于5mmol/L铁氰化钾/0.1mol/L KCl溶液中,采用循环伏安法和电化学阻抗表征。由图2(c)、2(d)可知,D型酪氨酸阻抗值明显高于L型酪氨酸。循环伏安法电位范围为-0.2~0.6V,扫速为0.1V/s。电化学阻抗法频率范围为0.1~6·105Hz,幅度为0.01V。
实施例2
考察N-乙酰L-半胱氨酸保护的金纳米沉积圈数的影响。
N-乙酰L-半胱氨酸保护的金纳米和酪氨酸的修饰电极的制备同实施例一,NALC-Au沉积圈数分别采用2、3、5、6、7、8圈,其结果见图3,可见当NALC-Au沉积圈数为6圈时,形成的N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极修饰电极的膜的厚度最适合,电极表面的膜裸露的面积最大,可以更多的与L-酪氨酸或D-酪氨酸结合。
实施例3
考察酪氨酸沉积圈数对酪氨酸对映体识别能力的差异。
N-乙酰L-半胱氨酸保护的金纳米和酪氨酸的修饰电极的制备同实施例一,NALC-Au沉积圈数分别采用1、2、3、4、5圈,进行酪氨酸对映体的识别,其结果见图4,在沉积圈数为3圈时,N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极对酪氨酸对映体识别能力最好。
实施例4
考察酪氨酸在不同pH下,N-乙酰L-半胱氨酸保护的金纳米修饰玻碳电极极对酪氨酸对映体识别能力的差异。
N-乙酰L-半胱氨酸保护的金纳米和酪氨酸的修饰电极的制备同实施例一,酪氨酸溶液分别采用pH4.07、pH5.13、pH5.66、pH5.91、pH6.53、pH7.00,进行酪氨酸对映体的识别,其结果见图5,可见当pH为6.53时,N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极对酪氨酸对映体识别能力差别最大。
实施例5
考察酪氨酸在不同浓度下,N-乙酰L-半胱氨酸保护的金纳米修饰玻碳电极极对酪氨酸对映体识别能力的差异。
N-乙酰L-半胱氨酸保护的金纳米和酪氨酸的修饰电极的制备同实施例一,酪氨酸浓度分别采用10、25、50、164、323、476、769mmol/L进行对映体的识别,其结果见图6,在酪氨酸的浓度为245mmol/L,N-乙酰L-半胱氨酸保护的金纳米修饰的玻碳电极对酪氨酸对映体识别能力最好。
- 还没有人留言评论。精彩留言会获得点赞!