一种益母生化合剂中苦杏仁苷的高效液相色谱检测方法与流程
本发明涉及一种高效液相色谱检测方法,具体涉及一种益母生化合剂中苦杏仁苷的高效液相色谱检测方法。
背景技术:
益母生化合剂由益母草、当归、川芎、桃仁、炮姜、甘草(炙)以上六味药材炮制而成。具有活血祛瘀、温经止痛的功效,主要用于治疗产后恶露不行、血瘀腹痛。其为淡橙黄色至棕黄色液体。气香,味微甜。该益母生化合剂主要用于马、牛、羊、猪等牲畜,其中马、牛用量为200-300mL,羊、猪用量为30-50mL。
目前该制剂收载于《兽药国家标准汇编——兽药地方标准上升国家标准》(第二册),其质量标准中仅对益母草、甘草、川芎进行了薄层色谱鉴别,无含量测定标准,很难控制其质量,保证产品的安全性、有效性与质量可控性。
技术实现要素:
本发明所要解决的技术问题是:现有技术中没有用于益母生化合剂中苦杏仁苷的高效液相色谱检测方法,且采用现有苦杏仁苷的高效液相色谱检测方法导致检测结果不理想的问题,目的在于提供解决上述问题的一种益母生化合剂中苦杏仁苷的高效液相色谱检测方法。
本发明通过下述技术方案实现:
一种益母生化合剂中苦杏仁苷的高效液相色谱检测方法,包括:
(1)利用益母生化合剂制备供试品溶液;
(2)进行高效液相色谱检测,高效液相色谱检测的流动相为18∶82的甲醇和水。
进一步,所述供试品溶液的制备过程如下:
按照益母生化合剂处方,制备益母生化合剂;取5mL于25mL容量瓶中,用流动相稀释至刻度,即得。所述液相色谱检测中色谱柱采用C18色谱柱,色谱柱的检测波长为210nm,流速为1mL·min-1;柱温为30℃;进样量为10μL。
现有技术中在进行苦杏仁苷的高效液相色谱检测时,由于药物中存在其他成份,其他成份会对待测成份造成干扰作用,因而在不同的药物中,虽然待测成份一样,但适用于其中一种药物的预处理手段不一定适用于另一种药物。并且,发明人发现相同原料组成的药物,其制备工艺存在差异时,对最终成品也会造成极大影响,尤其是对于采用高效液相色谱检测而言,其中某一组分进行检测时检测结果差异极大,因而,上述因素也导致了色谱检测的效果较差的问题。
通过上述检测方法和检测条件的优化,有效避免了其他成份对苦杏仁苷检测的影响,使检测结果更加精准、检测效果更加稳定。
进一步,还包括对照品溶液与阴性对照溶液,该对照品溶液的制备方法如下:
精密称取4.65mg苦杏仁苷对照品于50mL容量瓶中,用70%甲醇溶解并定容至刻度,摇匀,即得93μg/mL苦杏仁苷对照品溶液;
该阴性对照溶液的制备方法如下:
按照益母生化合剂处方,取除桃仁外的其他药材,按处方工艺制成合剂,再取5mL于25mL容量瓶中,用流动相稀释至刻度,即得。
本发明通过优化对照药材溶液和阴性对照溶液的制备工艺,有效验证了本发明方法检测的准确性。
本发明与现有技术相比,具有如下的优点和有益效果:
通过本发明的优化设计,使检测结果更加精准、检测效果更加稳定。
附图说明
图1为实施例1的对照品溶液的色谱图。
图2为实施例1的供试品溶液的色谱图。
图3为实施例1的阴性对照溶液的色谱图。
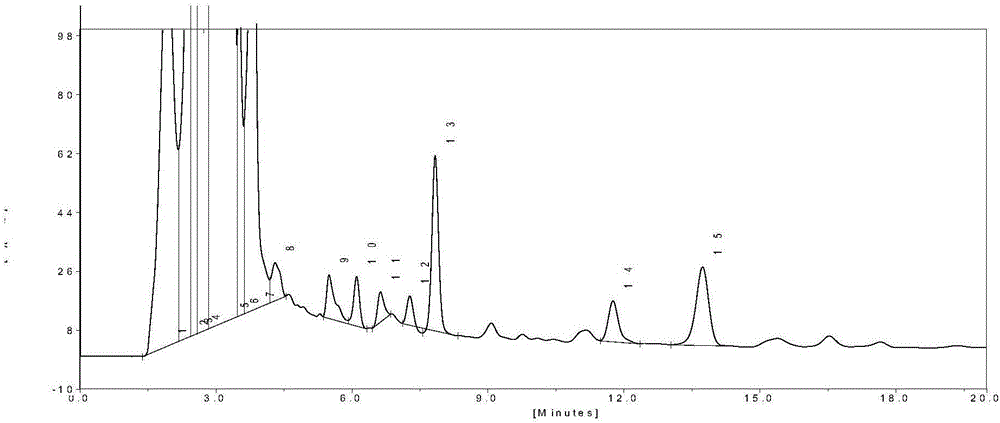
图4为实施例2中甲醇:水=20:80时供试品溶液的的色谱图。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚明白,下面结合实施例,对本发明作进一步的详细说明,本发明的示意性实施方式及其说明仅用于解释本发明,并不作为对本发明的限定。
实施例1
一种益母生化合剂中苦杏仁苷的高效液相色谱检测方法,具体检测过程如下:
(1)供试品溶液的制备:按照益母生化合剂处方,制备益母生化合剂。取5mL于25mL容量瓶中,用流动相稀释至刻度,即得。对照品溶液的制备:精密称取4.65mg苦杏仁苷对照品于50mL容量瓶中,用70%甲醇溶解并定容至刻度,摇匀,即得93μg/mL苦杏仁苷对照品溶液。阴性对照溶液的制备:按照益母生化合剂处方,取除桃仁外的其他药材,按处方工艺制成合剂,再取5mL于25mL容量瓶中,用流动相稀释至刻度,即得。
(2)采用上述三种不同的溶液进行高效液相色谱检测。其中,色谱柱:Global Chromatography C18(250mm×4.6mm,5μm);流速:1mL·min-1;柱温:30℃;进样量:10μL;检测波长:210nm。流动相:甲醇-水,甲醇:水=18:82。
检测结果,如图1-图3所示:
在供试品色谱图中,与苦杏仁苷对照品色谱图主峰相应保留时间位置处有对应峰,且与前一峰的分离度良好,阴性样品色谱图在相同的保留时间处无峰,即阴性无干扰。表明此色谱条件专属性好。
实施例2
本实施例是实施例1的对照实施例,本实施例中流动相的组成比例不同,具体检测过程如下:
分别甲醇:水=20:80的比例作为流动相,采用与实施例1相同的检测条件对供试品溶液进行检测,检测结果如4所示。并且同时采用了甲醇:水=14:86作为流动相进行检测,检测结果为:供试品色谱图中,苦杏仁苷与前一峰的分离度R=1.48<1.50,不满足HPLC基本的分离要求。
实施例3
本实施例对实施例1中的检测方法的线性关系、精密度、重复性以及稳定性进行检测,检测方法和结果如下:
线性关系考察
分别精密吸取苦杏仁苷对照品溶液6、8、10、12、14μL注入液相色谱仪中,记录苦杏仁苷峰面积,以峰面积积分值(Y)为纵坐标、对照品进样量(X)为横坐标绘制标准曲线,线性回归方程为Y=106.27X+213.45,r=0.9999(n=5)。结果表明苦杏仁苷的进样量在0.558~1.302μg范围内与峰面积积分值呈良好的线性关系。
精密度试验
取苦杏仁苷对照品溶液10μL,连续进样6次,记录色谱峰峰面积,苦杏仁苷的色谱峰峰面积的RSD为0.44%。结果表明仪器精密度良好。
重复性试验
取同一批次益母生化合剂5mL,6份,制备供试品溶液,进样分析,记录苦杏仁苷峰面积,结果苦杏仁苷峰面积的RSD为0.51%。表明本方法的重复性较好。
稳定性试验
取益母生化合剂5mL,制备供试品溶液。分别于0、2、4、6、8、10、12h进样分析,记录苦杏仁苷峰面积,计算峰面积的RSD为2.16%。结果表明供试品溶液在12h内稳定。
同时,本实施例还对加样回收率进行测定,测定方法为:精密量取益母生化合剂2.5mL,共6份,于25mL容量瓶中,各精密量取适量苦杏仁苷对照品溶液,按供试品溶液制备方法制备,分别进样,测定苦杏仁苷含量,计算回收率。测定结果如表1所示。
表1
通过上述检测结果可知:本发明优选方案的稳定性、重复性均非常优异,而且加样回收率的RSD值达到2.96,效果非常显著。
以上所述的具体实施方式,对本发明的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本发明的具体实施方式而已,并不用于限定本发明的保护范围,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!