一种桑色素的检测方法与流程
一、技术领域
本发明涉及一种分析检测方法,具体地说是一种以四氮杂十四环二烯镍配合物[nil](clo4)2催化的非线性振荡体系对桑色素的检测方法。
二、技术背景
桑色素,又名3,5,7,2′,4′-五羟黄酮,其结构如式(ⅰ)所示,属黄体酮类化合物。分子式为c15hl007·2h20。结构特点是含氧的杂环连接两个芳香环。通常为黄色或灰黄色针状结晶,久置空气中易氧化为棕色,熔点285℃~290℃(分解),微溶于水。它是从黄桑木、桑橙树等桑科植物的树皮和许多中草药中提取的一种浅黄色色素。该物质是黄酮类化合物中的一种,存在于旧黄颜木(也称染色桑或黄色巴西红木),黄桑木、桑橙树和许多中草药中提取的一种浅黄色色素。桑色素是一种化学分析中常用的显色剂,一般用来检测痕量的铁、锌、钴等。桑色素对金黄色葡萄球菌、痢疾杆菌和伤寒杆菌有较强的抗菌作用,也有抗病毒作用、有抗疱疹病毒的作用和抗马铃薯病毒的作用。桑色素对腹水型肝癌细胞具有光敏杀伤作用,抑制腹水型肝癌细胞的dna合成。在避光条件下,桑色素也具有杀伤癌细胞的能力。它对腹水型肝癌细胞的杀伤具有永久性,还能抑制胆碱酯酶而显示解痉作用在豚鼠回肠上,并且对低密度脂蛋白的氧化修饰具有抑制作用,对鼠伤寒沙门氏菌有明显的致突变作用。它能抑制醛糖还原酶,还有利尿作用。它可用于微电子行业,是点滴试验鉴定铝、铍、锌、镓、铟、钪的试剂。桑色素还可以作为羊毛等染料。但由于桑色素价格较贵,现主要用于医药和电子行业。它还具有抗癌和抗菌的作用。
目前,国内检测桑色素的方法不多,例如荧光光度法,但是大多数方法都是把桑色素与其他物质相结合用来测定其他物质,以前有人用电位法和分光光度法研究桑色素在含乙醇和丙酮的水溶液中,在硫酸性溶液中以及在有cpc存在时的离解平衡和光的吸收行为。
三、
技术实现要素:
本发明旨在为桑色素提供一种新的检测方法,即以四氮杂十四环二烯镍配合物[nil](clo4)2催化的非线性振荡体系对桑色素的检测方法,本方法是基于该配合物催化的非线性体系(即振荡体系)对桑色素的敏锐响应而开发的一种电化学振荡体系一标准曲线(工作曲线)法。具体地说对桑色素而言,就是将同一种类的不同浓度桑色素加入到非线性化学振荡体系中,利用同一种类的不同浓度的桑色素对振荡图谱的特征响应(抑制时间)不同,从而实现对桑色素的定量分析。
本发明所称四氮杂十四环二烯镍配合物是5,7,7,12,14,14-六甲基-1,4,8,11-四氮杂大环-4,11-二烯为配体的四氮杂大环镍(ⅱ)配合物,其化学式为[nil](clo4)2,其结构如式(ⅱ)所示。
本配合物的结构与生命体里肌红蛋白,血红蛋白,叶绿素和一些酶的关键结构卟啉环很相似,这种以[nil](clo4)2催化的化学振荡反应和植物和动物细胞体内的生化振荡类似,因此,该体系具有稳定的振幅,较长的振荡寿命,及对对香豆酸的敏锐响应。
[nil](clo4)2的制备分两步:1)制备l·2hclo4;2)由l·2hclo4制备[nil](clo4)2。
1)制备l·2hclo4:
将98.5ml乙二胺装入一只500ml三颈瓶中,在冰浴条件下,120分钟内搅拌下缓慢滴加126ml70%高氯酸。最初的反应剧烈并伴有白烟产生,所以滴加速度控制在每5秒钟l滴。随着反应进行可以适当加快滴加速度,直到滴加完为止,得到透明的溶液。仍然在冰水浴的条件下,向该透明溶液加入224ml无水丙酮并剧烈搅拌,溶液很快变浑浊同时形成非常粘稠混合物。仍然在冰水浴的条件下保持2-3小时以便充分反应。将所得产物转移到布氏漏斗进行抽滤分离,并用丙酮充分洗涤,可得纯白色固体。将此纯自色固体在热的甲醇-水溶液中重结晶,用硅胶干燥剂真空干燥,得80g白色晶体,此白色晶体为l·2hclo4。
参考文献:
1.curtis,n.f.andhay,r.w.,j.chem.soc.,chem.commun.,1966,p.534.
2.ganghu,panpanchen,weiwang,linhu,jimeisong,lingguangqiu,juansong,e1ectrochimicaacta,2007,vol.52,pp.7996-8002.
3.linhu,ganghu,han-hongxu,j.ana1.chem.,2006,vol.61,no.10,pp.1021-1025.
4.胡刚,中国科学技术大学博士论文,p25-27,合肥,2005年。
2)由l·2hclo4制备[nil](clo4)2:
将11gni(ac)24h2o与21g的l·2hclo4置于500ml三颈瓶中,使其溶于250ml甲醇,热水浴加热回流3小时,最后出现黄色沉淀,过滤、将滤液在热水浴中浓缩至原体积l/2,放置过夜,充分结晶,得到黄色晶体。将黄色晶体转移至布氏漏斗并用甲醇洗涤,在热的乙醇-水溶液中重结晶,真空干燥,可得8g[nil](clo4)2亮黄色晶体。
参考文献:
1.n.f.curtis,j.chem.soc.doltontran.,1972,vol.13,1357.
2.胡刚,中国科学技术大学博士论文,p42-43,合肥,2005年。
本检测方法与现有技术的区别是应用“h2so4-kio3-[nil](clo4)2-ma(丙二酸)-h2o2”briggs-rauscher非线性振荡体系作为检测溶液以及该溶液对桑色素的振荡响应,从而实现对药品中桑色素的定量分析。检测溶液中各组分的浓度如表1所示:
表1briggs-rauscher振荡反应溶液中各组分的浓度范围
具体操作如下:
1、按表1配制检测溶液,并记录该溶液电位(potential)随时间(time)变化的曲线即化学电位振荡图谱。
配制好的检测溶液加入50ml小烧杯中并放入大小合适的磁子,放在恒温磁力加热搅拌器上,保持搅拌速度在500转/分钟,在冰浴条件下使烧杯里的温度维持在-2~2℃。然后,把准备好的工作电极(铂电极)和参比电极(双盐桥甘汞电极)插入溶液中,准备对溶液进行电位监测。工作电极和参比电极的另一端通过放大器(instrumentamplifier)连接到数据采集器(go!link)再连接至计算机。打开计算机中loggerlite程序对采集时间和取样速度进行设置后,迅速点击开始键从而对溶液进行电位监测。计算机记录所采集的电位值随时间变化的曲线,即化学电位振荡图谱。当需要检测某种物质的时候,在振荡图谱达到振荡体系稳定时迅速加入,通常在第3次到第5次振荡电位处于最低电位时迅速加入。
振荡图谱的基本参数包括:
诱导时间:加入最后一种物质到溶液起振前所需要的时间
振荡振幅:在振荡过程中从一个最低电位到下一个最高点位之间的电位差值。
振荡周期:在振荡过程中从一个最低(高)点位到下一个最低(高)点位所需时间。
最高电位:稳定振荡时体系出现的电位最高点。
最低电位:稳定振荡时体系出现的电位最低点。
振荡寿命:自振荡开始到振荡结束所需要的时间。
平衡电位:体系达到热力学平衡状态时的电位。此刻,电位不随时间的变化而变化。
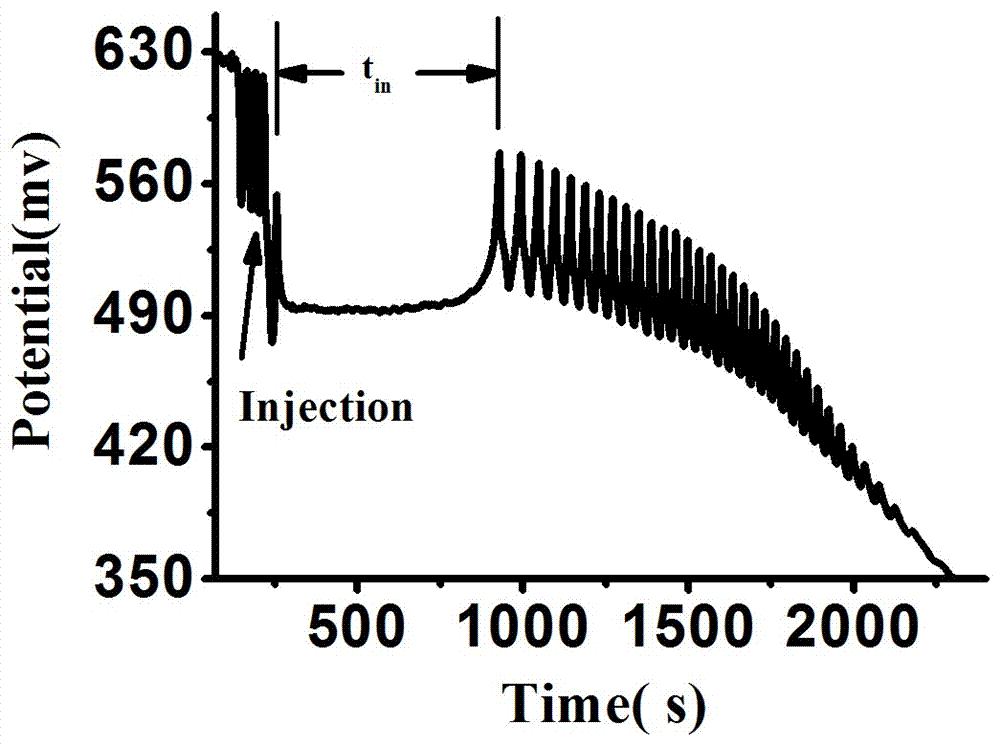
抑制时间(tin):从加入桑色素溶液振荡受到抑制开始,到重新恢复振荡所需的时间。
2、建立桑色素样本浓度与振荡特征响应参数(抑制时间)之间关系的工作曲线
配制系列浓度为2.44×10-6到1.3×10-5moll-1的桑色素溶液作为样本溶液。将配制的样本溶液加入已稳定的振荡体系中,并固定在第3次到第5次振荡、电位处于最低电位时时加入。加入的桑色素会暂时抑制振荡一段时间,然后振荡恢复,也即产生了抑制时间tin。振荡特征响应参数为抑制时间(tin)。
以抑制时间tin为纵坐标,桑色素样本溶液浓度为横坐标作图,得到工作曲线。
3、桑色素的定量分析
将待测试样加入已稳定振荡的振荡体系中,(待测试样均在第3次到第5次振荡、电位处于最低电位时加入),振荡响应为产生了抑制时间,得到tin值,根据工作曲线可求得待测试样中的桑色素的浓度。
本方法可以方便快捷地检测出食品或药品中的桑色素的含量,实验表明,试样中的其他物质对检测无干扰。
四、附图说明
图1是实施例1中检测溶液(未加入样本)的化学电位振荡图谱。
图2是实施例1中加入1.3×10-5mol/l桑色素后振荡体系的振荡响应图谱。
图3是实施例1中桑色素浓度与抑制时间(tin)的工作曲线图。
五、具体实施方式
实施例1
应用h2so4-kio3-[nil](clo4)2-ma(丙二酸)-h2o2的briggs-rauscher振荡体系作为检测溶液,对桑色素进行定量分析。加入不同浓度的桑色素样本溶液到振荡体系中,建立起被测物浓度与抑制时间tin之间关联的工作曲线(如线性关系图),达到检测试样中桑色素含量的目的。
(1)配制桑色素检测溶液
首先用98%的浓硫酸配制0.025mol/l的硫酸溶液作为溶剂;然后用0.025mol/l的硫酸溶剂分别配制0.14mol/l的碘酸钾溶液,2.0mol/l的丙二酸溶液,4.0mol/l的过氧化氢溶液和0.0173mol/l的[nil](clo4)2溶液。然后,向50ml烧杯的开放体系中逐次加入14.5ml,0.025mol/l的硫酸溶液;6.5ml,0.14mol/l的碘酸钾溶液;2ml,0.0173mol/l的催化剂;3ml,2.0mol/l的丙二酸溶液;14ml,4.0mol/l的过氧化氢溶液。最后,体系中硫酸的浓度为0.025mol/l,碘酸钾的浓度为0.02275mol/l,催化剂的浓度为8.65×10-4mol/l,丙二酸的浓度为0.15mol/l,过氧化氢的浓度为1.4mol/l。
同时配制系列不同浓度的桑色素样本溶液。
(2)获得振荡图谱
配制好的检测溶液(振荡体系)的振荡图谱用计算机记录。如图1所示。在配制好的振荡溶液中分别加入微量不同浓度的桑色素样本溶液,每次加入的时间都是第4次振荡开始、电位处于最低电位时,加入的桑色素会暂时抑制振荡一段时间,然后振荡恢复,也即产生了抑制时间tin。图2是加入1.3×10-5mol/l桑色素后振荡体系的振荡响应图谱。
(3)分析
根据桑色素的浓度与抑制时间(tin)之间的关系建工作曲线,如图3所示,其中横坐标是被加入到振荡溶液中的桑色素的浓度,纵坐标是抑制时间tin,当桑色素的浓度在2.44×10-6到1.3×10-5moll-1之间时,抑制时间tin与桑色素溶液的浓度成一次线性关系,据此可以实现对试样中桑色素的定量分析。
- 还没有人留言评论。精彩留言会获得点赞!