一种同时测定锌电解液中铜镉镍钴含量的方法与流程
本发明涉及分析测试技术领域,更具体地,涉及一种测定锌电解液中铜镉钴镍含量的方法。
背景技术:
锌是支撑国民经济和国防军工发展的基础原料和战略性物资,目前80%左右的锌是通过湿法冶金产生的。对于锌的湿法冶金来说,过量的杂质离子不仅影响电解过程中的电流效率,而且影响沉积锌的表面形貌和阴极极化。电沉积锌过程中影响较大的杂质主要有铜镉镍钴,因此需严格监控流入电解槽的锌电解液中这几种杂质的含量。
锌电解液中zn2+的含量高达130~170g/l,锌和微量杂质离子的质量比最高可达到107倍以上,从而严重干扰锌电解液中杂质离子的测定。目前,实验室中测定锌电解液中铜镉镍钴含量的方法主要有分光光度法,原子吸收法,原子发射光谱法,极谱法等。其中,分光光度法灵敏度低,操作复杂,一般需要对锌电解液进行预处理,而且难以实现对铜镉镍钴的同时测定;原子吸收法和原子发射光谱法,仪器昂贵,且会受到基体干扰;此外,利用现有极谱法测定锌电解液中铜镉镍钴含量时,由于锌电解液中锌离子含量过高,易造成波峰重叠(特别是钴波),且不同金属离子在同一检测体系中灵敏度不同,很难实现包括铜镉镍钴在内的多种金属离子的同时测定,实际应用中还仅限于单离子检测的极谱法无疑提高了检测时间和工作量,不利于对杂质离子的实时监测。
综上所述,在现有测试理论及研究成果的基础上,克服现有检测方法中所存在的缺陷,研究开发一种简单快捷能实现锌电解液中多种金属离子同时检测的方法是目前亟需解决的关键技术问题,具有重要的理论和实际意义。
技术实现要素:
针对现有技术存在的不足,本发明提供了一种测定锌电解液中铜镉钴镍含量的方法。
本发明采用如下技术方案:
一种同时测定锌电解液中铜镉镍钴含量的方法,包括,将待测锌电解液与检测体系反应,测定反应混合物的铜、镉、镍和钴各络合物的吸附极谱波,通过获得的二阶导数波峰电流计算待测锌电解液中的铜、镉、镍和钴的含量;所述检测体系包括硼酸钠、柠檬酸钠和丁二酮肟。
在上述技术方案中,将待测锌电解液与检测体系反应后,在测定反应混合物的铜、镍和钴各络合物的吸附极谱波前,调节ph值为8.2~10.5,优选为9.3;在测定反应混合物的镉络合物吸附极谱波前,调节ph值为3.5~4.8,优选为4.0。
在上述技术方案中,所述反应混合物中柠檬酸钠的浓度为0.3~0.7mol/l,优选为0.3mol/l。
在上述技术方案中,所述反应混合物中硼酸钠的浓度为0.01~0.1mol/l,优选为0.06mol/l。
在上述技术方案中,所述反应混合物中丁二酮肟的浓度为5×10-4~3×10-3mol/l,优选为1.4×10-3mol/l。
优选地,在上述技术方案中,所述丁二酮肟以丁二酮肟乙醇溶液的形式添加,其浓度为5~12g/l,优选为11g/l。
具体地,上述测定锌电解液中铜镉镍钴含量的极谱法,包括以下步骤:
s1、取体积为v0的待测锌电解液与所述检测体系反应,调节ph值为8.2~10.5,定容,测定反应混合物的铜、镍和钴各络合物的吸附极谱波,获得铜、镍和钴的二阶导数波峰电流i1、i2、i3,再调节ph值为3.5~4.8,测定反应混合物的镉络合物的吸附极谱波,获得镉的二阶导数波峰电流i4;
s2、分别取体积为v0的待测锌电解液、与步骤s1等量的所述检测体系以及体积为v1的含c1mol/lcu2+、c2mol/lcd2+、c3mol/lni2+和c4mol/lco2+的混合标准溶液,将三者混合反应,所述加入的混合标准溶液中所含cu2+、cd2+、ni2+和co2+的摩尔量分别与待测锌电解液中cu2+、cd2+、ni2+和co2+的摩尔量相当,调节ph值与步骤s1中测定铜、镍和钴各络合物的吸附极谱波前的ph值相同,定容到与步骤s1中相同的体积,测定反应混合物的铜、镍和钴各络合物的吸附极谱波,获得铜、镍和钴的二阶导数波峰电流i11、i22、i33,再调节ph值与步骤s1中测定镉络合物的吸附极谱波前的ph值相同,测定反应混合物的镉络合物的吸附极谱波,获得镉的二阶导数波峰电流i44;
s3、按如下公式计算分别待测锌电解液中cu2+、cd2+、ni2+和co2+的浓度:
其中,a=1~4。
在上述技术方案中,步骤s1和s2中,在测定反应混合物的铜、镍和钴各络合物的吸附极谱波前,调节ph值为9.3;在测定反应混合物的镉络合物吸附极谱波前,调节ph值为4.0。
本发明与现有方法相比,具有以下有益效果:
(1)本发明所提供的极谱法通过采用硼酸钠、柠檬酸钠和丁二酮肟为检测体系,通过调节ph值达到同时测量铜、镉、镍、钴离子的含量;且该检测体系能完全掩蔽锌离子的干扰,无需对被测锌电解液进行预处理;
(2)本发明所提供的极谱法通过引入标准加入法,进一步减弱了待测锌电解液中其他共存离子的影响,选择性高,测量结果准确可靠;线性范围宽,从而使本发明对整个工艺过程的锌电解液的铜、镉、镍、钴离子含量均能检测;检测速度快,结果可靠;
(3)本发明所提供的极谱法所用分析仪器价格便宜,操作简单;所用试剂种类少,稳定性好,价格便宜;检测过程无沉淀生成,不仅适用于实验室中常规分析,更易实现自动化,便于在线检测中使用。
附图说明
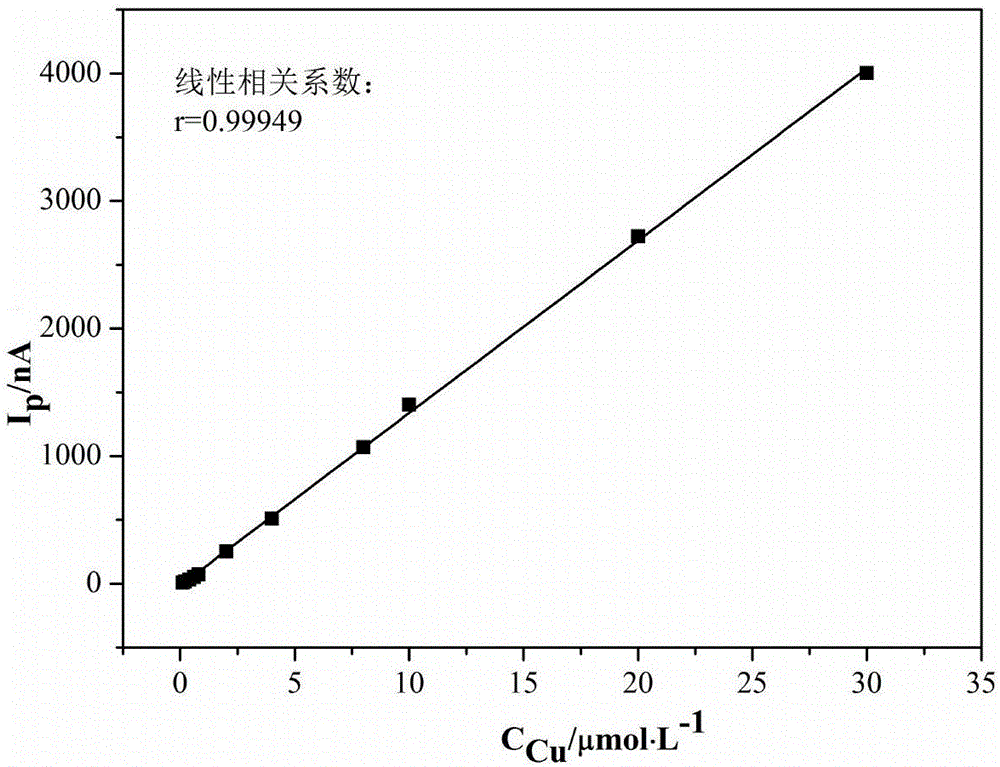
图1为本发明实施例1的锌电解液中铜离子的标准曲线;
图2为本发明实施例1的锌电解液中镉离子的标准曲线;
图3为本发明实施例1的锌电解液中镍离子的标准曲线;
图4为本发明实施例1的锌电解液中钴离子的标准曲线;
图5为本发明实施例2步骤(1)中测定锌电解新液中的铜离子、镍离子和钴离子的二阶导数极谱波;
图6为本发明实施例2中步骤(1)中测定锌电解新液中的镉离子的二阶导数极谱波;
图7为本发明实施例2步骤(2)中测定锌电解新液中的铜离子、镍离子和钴离子的二阶导数极谱波;
图8为本发明实施例2中步骤(2)中测定锌电解新液中的镉离子的二阶导数极谱波;
图9为本发明实施例2步骤(1)中测定中性上清液中的铜离子、镍离子和钴离子的二阶导数极谱波;
图10为本发明实施例2中步骤(1)中测定中性上清液中的镉离子的二阶导数极谱波;
图11为本发明实施例2步骤(2)中测定中性上清液中的铜离子、镍离子和钴离子的二阶导数极谱波;
图12为本发明实施例2中步骤(2)中测定中性上清液中的镉离子的二阶导数极谱波。
具体实施方式
下面结合具体实施例,对本发明的具体实施方式作进一步详细描述。以下实施例仅用于说明本发明,并不用来限制本发明的具体保护范围。
本发明实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器末注明生产厂商者,均为可通过正规渠道商购买得到的常规产品。
本发明实施例所用试剂和规格:
丁二酮肟的乙醇溶液:11g/l;柠檬酸钠溶液:1mol/l;硼酸钠溶液:0.15mol/l;氢氧化钠溶液:2mol/l;硫酸(1:2):6mol/l。
本发明实施例所用仪器和测试条件:
仪器:jp-303e型示波极谱仪;测铜、镍和钴各络合物的吸附极谱波的扫描区间:-250~-1400mv,测镉络合物的吸附极谱波的扫描区间:-400~-800mv;扫描速度:500mv/s;滴汞时间:9.5s;静止时间:8s。
以下实施例中待测样品锌电解液、锌电解新液、中性上清液由湖南省株洲冶炼厂提供。
实施例1cu2+、cd2+、ni2+和co2+测定体系的标准曲线的确定
(1)取cu2+标准溶液用二次蒸馏水稀释到合适浓度的cu2+标准溶液;分别量取1×10-6mol/l、2×10-6mol/l、4×10-6mol/l、6×10-6mol/l、8×10-6mol/l、2×10-5mol/l、4×10-5mol/l、8×10-5mol/l、1×10-4mol/l、2×10-4mol/l、3×10-4mol/l、6×10-4mol/l、8×10-4mol/l的cu2+标准溶液各0.5ml于13个10ml的容量瓶中,分别向容量瓶中加入1.0mlzn2+溶液(2.6mol/l)和0.15ml丁二酮肟乙醇溶液(11g/l),晃动3min,然后依次加入3ml柠檬酸钠溶液(1mol/l)、4ml硼酸钠(0.15mol/l)和1ml氢氧化钠溶液(2mol/l),定容,静置5min,分别把溶液倒入电解杯中测定产生的cu2+络合物吸附极谱波,获得各浓度cu2+对应的二阶导数波峰电流,绘制标准曲线如图1所示(横坐标表示容量瓶定容后的cu2+的摩尔浓度,纵坐标表示二阶导数波峰电流)。
(2)取cd2+标准溶液用二次蒸馏水稀释到合适浓度的cd2+标准溶液;分别量取4×10-6mol/l、6×10-6mol/l、8×10-6mol/l、2×10-5mol/l、4×10-5mol/l、6×10-5mol/l、8×10-5mol/l、2×10-4mol/l、4×10-4mol/l、8×10-4mol/l、1×10-3mol/l、2×10-3mol/l、4×10-3mol/l、8×10-3mol/l的cd2+标准溶液各0.5ml于14个10ml的容量瓶中,分别向容量瓶中加入1.0mlzn2+溶液(2.6mol/l)和0.15ml丁二酮肟乙醇溶液(11g/l),晃动3min,然后依次加入3ml柠檬酸钠溶液(1mol/l)、4ml硼酸钠(0.15mol/l)和0.5ml硫酸(6mol/l),定容,静置5min,分别把溶液倒入电解杯中测定产生的cd2+络合物吸附极谱波,获得各浓度cd2+对应的二阶导数波峰电流,绘制标准曲线如图2所示(横坐标表示容量瓶定容后的cd2+的摩尔浓度,纵坐标表示二阶导数波峰电流)。
(3)取ni2+标准溶液用二次蒸馏水稀释到合适浓度的ni2+标准溶液;分别量取2×10-7mol/l、4×10-7mol/l、6×10-7mol/l、8×10-7mol/l、2×10-6mol/l、3×10-6mol/l、4×10-6mol/l、6×10-6mol/l、7×10-6mol/l、8×10-6mol/l、1×10-5mol/l、2×10-5mol/l、4×10-5mol/l的ni2+标准溶液各0.5ml于13个10ml的容量瓶中,参照步骤(1)的方法,分别测各浓度ni2+对应的二阶导数波峰电流,绘制标准曲线如图3所示(横坐标表示容量瓶定容后的ni2+的摩尔浓度,纵坐标表示二阶导数波峰电流)。
(4)取co2+标准溶液用二次蒸馏水稀释到合适浓度的co2+标准溶液;分别量取1×10-7mol/l、2×10-7mol/l、4×10-7mol/l、6×10-7mol/l、8×10-7mol/l、2×10-6mol/l、4×10-6mol/l、6×10-6mol/l、1.2×10-5mol/l的co2+标准溶液各0.5ml于9个10ml的容量瓶中,参照步骤(1)的方法,分别测各浓度co2+对应的二阶导数波峰电流,绘制标准曲线如图4所示(横坐标表示容量瓶定容后的co2+的摩尔浓度,纵坐标表示二阶导数波峰电流)。
实施例2锌电解新液中cu2+、cd2+、ni2+和co2+含量的测定
(1)量取1ml的锌电解新液置于10ml容量瓶中,加入丁二酮肟的乙醇溶液0.15ml,晃动3min至均匀,然后依次加入3ml柠檬酸钠溶液(1mol/l)和4ml硼酸钠(0.15mol/l),通过滴加2mol/l氢氧化钠溶液调节其ph值为9.4,定容,静置5min,把溶液倒入电解杯中测定产生的cu2+、ni2+、co2+络合物的吸附极谱波,获得其对应的二阶导数波峰电流分别为125.2na、667.1na、214.7na,检测结果如图5所示,并在此基础上滴加6mol/l硫酸调节其ph值为4.2,测定产生的cd2+络合物的吸附极谱波,获得其对应的二阶导数波峰电流分别为36.2na,检测结果如图6所示(横坐标表示扫描电压/mv,纵坐标表示二阶导数波峰电流/na);
(2)量取1ml的锌电解新液和0.5ml的混合标准溶液(cu2+:2×10-5mol/l,cd2+:6×10-5mol/l,ni2+:2×10-6mol/l,co2+:4×10-6mol/l)置于10ml容量瓶中,加入丁二酮肟的乙醇溶液0.15ml,晃动3min至均匀,然后依次加入3ml柠檬酸钠溶液(1mol/l)和4ml硼酸钠(0.15mol/l),通过滴加2mol/l氢氧化钠溶液调节其ph值为9.4,定容,静置5min,把溶液倒入电解杯中测定产生的cu2+、ni2+、co2+络合物的吸附极谱波,获得其对应的二阶导数波峰电流分别为230.6na、813.1na、414.9na,,检测结果如图7所示,并在此基础上滴加6mol/l硫酸调节其ph值为4.2,测定产生的cd2+络合物的吸附极谱波,获得其对应的二阶导数波峰电流分别为65.8na,检测结果如图8所示(横坐标表示扫描电压/mv,纵坐标表示二阶导数波峰电流/na);
(3)根据公式计算得到,锌电解新液中cu2+、cd2+、ni2+和co2+含量分别为cu2+:1.188×10-5mol/l,cd2+:3.669×10-5mol/l,ni2+:4.569×10-6mol/l,co2+:2.145×10-6mol/l。
实施例3中性上清液中cu2+、cd2+、ni2+和co2+含量的测定
(1)量取1ml中性上清液于100ml容量瓶中,用二次蒸馏水定容,以此为待测溶液;
(2)量取1ml的待测溶液置于10ml容量瓶中,加入丁二酮肟的乙醇溶液0.15ml,晃动3min至均匀,然后依次加入3ml柠檬酸钠溶液(1mol/l)和4ml硼酸钠(0.15mol/l),通过滴加2mol/l氢氧化钠溶液调节其ph值为9.3,定容,静置5min,把溶液倒入电解杯中测定产生的cu2+、ni2+、co2+络合物的吸附极谱波,获得其对应的二阶导数波峰电流分别为22.5na、53na、233.1na,,检测结果如图9所示,并在此基础上滴加6mol/l硫酸调节其ph值为4.0,测定产生的cd2+络合物的吸附极谱波,获得其对应的二阶导数波峰电流分别为23.7na,检测结果如图10所示(横坐标表示扫描电压/mv,纵坐标表示二阶导数波峰电流/na);
(3)量取1ml的待测溶液和0.5ml的混合标准溶液(cu2+:1×10-5mol/l,cd2+:6×10-5mol/l,ni2+:1×10-6mol/l,co2+:4×10-6mol/l)置于10ml容量瓶中,加入丁二酮肟的乙醇溶液0.15ml,晃动3min至均匀,然后依次加入3ml柠檬酸钠溶液(1mol/l)和4ml硼酸钠(0.15mol/l),通过滴加2mol/l氢氧化钠溶液调节其ph值为9.3,定容,静置5min,把溶液倒入电解杯中测定产生的cu2+、ni2+、co2+络合物的吸附极谱波,获得其对应的二阶导数波峰电流分别为71.25na、124na、426.8na,,检测结果如图11所示,并在此基础上滴加6mol/l硫酸调节其ph值为4.0,测定产生的cd2+络合物的吸附极谱波,获得其对应的二阶导数波峰电流分别为54na,检测结果如图12所示(横坐标表示扫描电压/mv,纵坐标表示二阶导数波峰电流/na);
(4)根据公式计算得到,中性上清液中cu2+、cd2+、ni2+和co2+含量分别为cu2+:2.308×10-4mol/l,cd2+:2.347×10-3mol/l,ni2+:3.732×10-5mol/l,co2+:2.407×10-4mol/l。
对比例1干扰离子的影响实验
各干扰离子对测定zn2+溶液中cu2+含量影响实验:
(1)量取1ml2.6mol/l的zn2+标准溶液和0.1ml5×10-5mol/l的cu2+溶液置于10ml容量瓶中,加入丁二酮肟的乙醇溶液0.15ml,晃动3min至均匀,然后依次加入3ml柠檬酸钠溶液(1mol/l)、4ml硼酸钠(0.15mol/l)和1ml氢氧化钠溶液(2mol/l),定容,静置5min,把溶液倒入电解杯中测定产生的cu2+络合物的吸附极谱波,获得其二阶导数波峰电流分别为i1;
(2)量取1ml2.6mol/l的zn2+标准溶液和0.1ml5×10-5mol/l的cu2+溶液置于10ml容量瓶中,分别加入一定量含待研究的干扰离子的溶液,然后加入丁二酮肟的乙醇溶液0.15ml,晃动3min至均匀,然后依次加入3ml柠檬酸钠溶液(1mol/l)、4ml硼酸钠(0.15mol/l)和1ml氢氧化钠溶液(2mol/l),定容,静置5min,把溶液倒入电解杯中测定产生的cu2+络合物的吸附极谱波,获得其二阶导数波峰电流分别为i2,取(i2-i1)/i1≤5%时混合溶液中的干扰离子浓度为所能加入的最大浓度。
采用上述相同的方法研究各干扰离子对测定zn2+溶液中cd2+(1×10-6mol/l)、ni2+(2×10-7mol/l)、co2+(2×10-7mol/l)含量的影响。
各干扰离子对测定zn2+溶液中cu2+、cd2+、ni2+、co2+含量测定的影响如下表1所示。
表1各干扰离子对测定cu2+、cd2+、ni2+、co2+含量的影响≤5%时的干扰离子浓度与待测离子浓度比
对比例2两种方法测定不同锌电解液样品中的cu2+、cd2+、ni2+、co2+含量
为了验证本发明测定结果的准确性,选择不同锌电解液样品为测试样品,分别采用原子吸收分光光度法和本发明所提供的方法测定其cu2+、cd2+、ni2+、co2+含量,实验结果如下表2所示。
表2两种方法测定锌电解液样品中cu2+、cd2+、ni2+、co2+含量的结果比较
由表2可以看出,本发明的方法测定锌电解液中cu2+、cd2+、ni2+、co2+含量的结果与原子吸收分光光度法的测定结果吻合度好,相对误差为-2.7%~+3.57%,说明本发明的测定方法的准确可靠。
对比例3样品加标回收率实验
样品加标回收实验结果如下表3所示。
表3加标回收实验结果及回收率
由表3可以看出,采用本发明进行样品加标回收实验,回收率为97%-104.1%,证明本方法准确可靠。
最后,以上仅为本发明的较佳实施方案,并非用于限定本发明的保护范围。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!