一种基于双单抗夹心的磁酶免疫双重定量ELISA检测方法与流程
本发明涉及定量elisa检测方法,具体涉及一种基于双单抗夹心的磁酶免疫双重定量elisa检测方法。
背景技术:
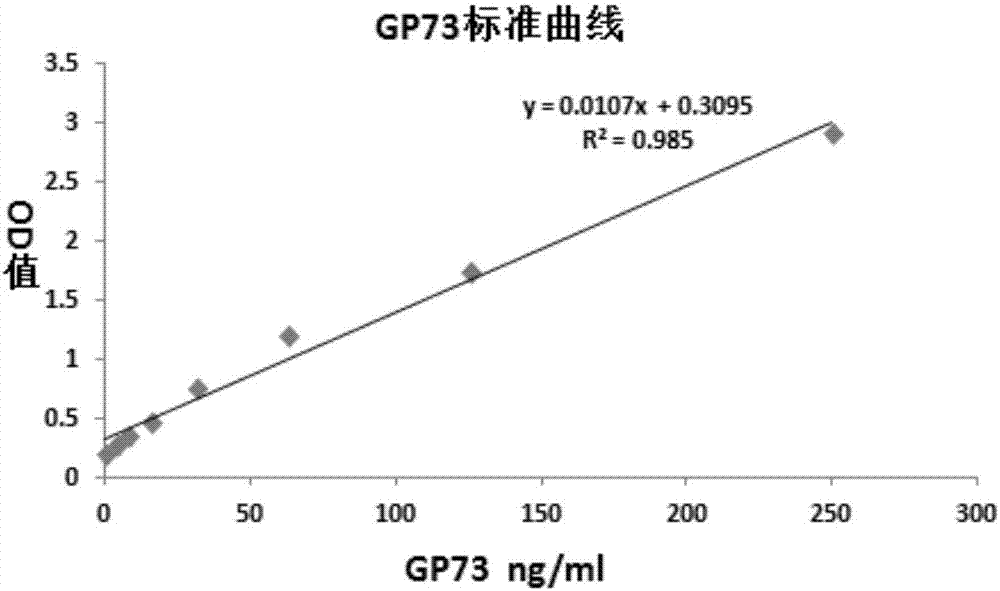
:免疫磁珠酶联免疫法(immunomagneticbeadelisa,imb-elisa)简称磁酶免疫法,是20世纪80年代末发明的一种标记免疫检测技术,该方法将磁微粒分离与酶联免疫测定技术相结合,以高均一的磁性微球为固相支持物,采用超顺磁性微粒液相分离代替普通酶联免疫酶标板包被法的固相分离,在外加磁场的作用下方便地分离游离物和结合物。由于纳米磁珠颗粒小、表面积大,可结合更多的诊断分子,使蛋白吸附能力超出酶标板载体的1000倍以上,从而使该方法的敏感性高于以普通酶标板为载体的elisa方法。磁珠上的蛋白质和其相应配基结合并不影响被分离物或其它生物材料的生物学性状和功能,同时具有操作简单、不需昂贵的仪器设备的特点,因而在免疫检测中具有巨大的应用前景。不过,目前的磁酶免疫法都是对目标蛋白a和目标蛋白b分别进行检测,检测过程较繁琐,耗费样本量较大。技术实现要素:本发明的目的是提供一种基于双单抗夹心的磁酶免疫双重定量elisa检测方法,可同时进行两种蛋白的检测,该检测方法灵敏度高,特异性好,操作简单快速。本发明的目的是通过以下技术方案来实现的:一种基于双单抗夹心的磁酶免疫双重定量elisa检测方法,用样品稀释液将目标蛋白a单克隆抗体包被的免疫磁珠稀释后,按100ul/孔加入目标蛋白b单克隆抗体包被酶标板,磁性分离洗涤后,分别加入不同浓度梯度的目标蛋白a和目标蛋白b标准品混合液和10倍梯度稀释的待测血清样品,37℃避光震荡孵育20min-60min,磁性分离洗涤后再加入辣根过氧化物酶(hrp)或碱性磷酸酶(arp)标记的目标蛋白a和目标蛋白b抗体混合液,从而形成以免疫磁珠为液相载体的目标蛋白a双抗夹心复合物和以酶标板为固相载体的目标蛋白b双抗夹心复合物,37℃避光震荡孵育20min-60min,将以免疫磁珠为液相载体的目标蛋白a双抗夹心复合物转移至新的微孔板上,对目标蛋白a双抗夹心复合物进行磁性分离洗涤,对目标蛋白b双抗夹心复合物进行常规elisa洗涤后,加入显色液,37℃避光显色1min-20min,之后加入反应终止液终止反应,然后上机检测读取检测值,根据各浓度目标蛋白a和目标蛋白b标准品对应的检测值,进行线性拟合绘制标准曲线,然后根据标准曲线的线性关系即可计算待测血清样品中目标蛋白a和目标蛋白b的含量。本发明所述的检测值包括吸光值、发光值和荧光值。所述的显色液包括tmb显色液、化学发光显色液或荧光显色液。优选地,所述目标蛋白a单克隆抗体包被的免疫磁珠采用以下方法来制备:以商业化羧基修饰的超顺磁性微球作为磁珠载体,经ph5.0-6.0的10-15mmmes缓冲液进行清洗后,按1:1的体积比加入1.25m的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐溶液(edc),在室温下避光振荡反应25-35min后进行磁性分离,得到活化的磁珠,而后按40-60ug抗体/mg磁珠的比例加入样品稀释液稀释的目标蛋白a单克隆抗体,37℃下避光震荡反应1-3h,磁性分离清洗后,加入含0.1%tween-20的pbst溶液进行室温震荡反应25-35min,以封闭未结合抗体的游离醛基,最后即得到目标蛋白a单克隆抗体包被的免疫磁珠。优选地,所述制备目标蛋白b单克隆抗体的包被酶标板采用以下方法来制备:用ph9.6的0.03-0.06m碳酸盐缓冲液将目标蛋白b单克隆抗体以1ug/ml浓度进行稀释,100ul/孔加到酶标板进行4°包被过夜,用含0.05%tween-20的pbs溶液进行清洗后,再用1%bsa的pbs溶液37℃下封闭1.5-2.5h,晾干即得到目标蛋白b单克隆抗体的包被酶标板。所述不同浓度梯度的目标蛋白a和目标蛋白b标准品混合液为0-500ng/ml浓度梯度的目标蛋白a抗原溶液和0-500ng/ml浓度梯度的目标蛋白b抗原溶液等体积混合而得。所述目标蛋白a抗原溶液和目标蛋白b抗原溶液分别由样品稀释液稀释目标蛋白a抗原或目标蛋白b抗原而得。所述辣根过氧化物酶(hrp)或碱性磷酸酶(arp)标记的目标蛋白a和目标蛋白b单克隆抗体混合液为抗体稀释液稀释的辣根过氧化物酶(hrp)或碱性磷酸酶(arp)标记的目标蛋白a单克隆抗体溶液与辣根过氧化物酶(hrp)或碱性磷酸酶(arp)标记的目标蛋白b单克隆抗体溶液按等体积混合而成。所述辣根过氧化物酶(hrp)或碱性磷酸酶(arp)标记的目标蛋白a抗体溶液中目标蛋白a单克隆抗体与抗体稀释液的体积比1﹕100-1﹕10000。所述辣根过氧化物酶(hrp)或碱性磷酸酶(arp)标记的目标蛋白b单克隆抗体溶液中目标蛋白b抗体与抗体稀释液的体积比1﹕100-1﹕10000。本发明所述的样品稀释液和抗体稀释液均为ph7.4的含1%bsa的pbs溶液。所述反应终止液为超纯水配制的终浓度为2m的浓硫酸溶液。本发明所涉及的洗涤和清洗均采用清洗缓冲液,所述清洗缓冲液为含0.05%tween-20的pbst缓冲液。本发明与现有技术相比具有以下有益效果:本发明提供的基于双单抗夹心的磁酶免疫双重定量elisa检测方法,同步联合定量检测目标蛋白a和目标蛋白b,该检测方法灵敏度高,特异性好,操作简单快速,检测效率快和准确率高。附图说明图1是采用本发明同步检测gp73和afp,绘制的afp标准曲线。图2是采用本发明同步检测gp73和afp,绘制的gp73标准曲线。图3是采用本发明同步检测各组临床血清样品中gp73和afp含量,左图为健康对照、肝炎、肝硬化、肝癌患者血清中gp73含量比较,右图为健康对照、肝炎、肝硬化、肝癌患者血清中afp含量比较。图4是采用本发明同步检测gp73和afp,联合诊断肝癌的roc曲线。具体实施方式下面将结合附图,进一步对本发明优选实施例,进行详细说明。实施例1各材料所含具体成分及制备方法1.制备人afp单克隆抗体i包被的免疫磁珠:选用商业化羧基修饰的超顺磁性微球(thermofisherscientific,65012)作为磁珠载体,经ph6.0的15mmmes(sigma,m2933)缓冲液进行清洗后,按1:1的体积比加入1.25m的edc(bio-rad,1762410)溶液,在室温下避光振荡反应30min后进行磁性分离,得到活化的磁珠。按50ug抗体/mg磁珠的比例加入样品稀释液稀释人afp单克隆抗体i,37℃下避光震荡反应2h,磁性分离清洗后,加入含0.1%tween-20的pbst溶液进行室温震荡反应30min,以封闭未结合抗体的游离醛基,最后即得到贮存在含0.1%tween-20及0.1%bsa的pbst溶液中的人afp单克隆抗体i包被的免疫活性磁珠。2.制备人gp73单克隆抗体i的包被酶标板:用ph9.6的0.05m碳酸盐缓冲液将人gp73单克隆抗体i以1ug/ml浓度进行稀释,100ul/孔加到酶标板进行4℃包被过夜,用含0.05%tween-20的pbs溶液进行清洗后,再用1%bsa的pbs溶液进行37℃下封闭2h,甩干后晾干得到人gp73单克隆抗体的包被酶标板。3.制备各浓度梯度afp和gp73标准品混合液:用样品稀释液将gp73融合蛋白稀释成浓度为1ug/ml的抗原溶液,用样品稀释液将afp稀释成200ng/ml的抗原溶液,二者以1:1体积比混匀,进行倍比梯度稀释,得到浓度分别为0、0.78、1.56、3.125、6.25、12.5、25、50、100ng/ml的afp和浓度分别0、3.9、7.8、15.6、31.25、62.5、125、250、500ng/ml的gp73标准品混合液。4.制备hrp标记抗体混合液:用抗体稀释液按1/6千比例分别稀释hrp标记的gp73单克隆抗体ii,以及hrp标记的afp单克隆抗体ii,二者1:1体积比混匀得到hrp标记的抗体混合液。5.试剂:样品稀释液和抗体稀释液均为:ph7.4的含1%bsa的pbs溶液;清洗缓冲液:含0.05%tween-20的pbst缓冲液:显色液:tmb显色反应液;终止反应液:用超纯水配制终浓度为2m的浓硫酸溶液。实施例2同步测定afp和gp73采用实施例1提供的各材料进行检测,具体步骤如下:用样品稀释液将特异性afp抗体免疫磁珠以1/300比例稀释,按100ul/孔加到人gp73单克隆抗体包被酶标板,磁性分离洗涤后,分别加入100ul/孔各浓度梯度的afp和gp73标准品混合液和10倍稀释的待测血清样品,37℃避光震荡孵育1h,磁性分离洗涤后再加入100ul/孔hrp标记的afp和gp73抗体混合液,从而形成以免疫磁珠为液相载体的afp双抗夹心复合物和以酶标板为固相载体的gp73双抗夹心复合物,37℃避光震荡孵育1h,将以免疫磁珠为液相载体的afp双抗夹心复合物转移至新的微孔板上,对目标蛋白a双抗夹心复合物进行磁性分离洗涤,对目标蛋白b双抗夹心复合物进行常规elisa洗涤后,加入100ul/孔tmb显色液,37℃避光显色10min,再加入50ul/孔终止反应液,最后读取450nm处的od值。根据各浓度标准品对应的od值,进行线性拟合绘制标准曲线,根据标准曲线的线性关系即可计算待测样品中afp和gp73的含量。同步检测afp和gp73标准品含量:每个梯度标准品各做两个复孔,根据测定的平均od值,分别绘制标准曲线,其结果如表1和图1-2所示。由图可见,得到的标准曲线线性关系良好,其中afp标准曲线回归系数r2为0.9978,检测范围在0.78~100ng/ml,gp73标准曲线回归系数r2为0.9903,检测范围在3.9~500ng/ml。表1gp73标准品(ng/ml)od平均值afp标准品(ng/ml)od平均值2502.8021003.7251251.7215502.2562.51.193251.01231.250.737512.50.428515.60.4636.250.24757.80.3393.1250.1293.90.26451.560.0891.950.2340.780.068500.187500.0525回归系数r20.985回归系数r20.991实施例3用于临床样品检测及诊断潜力分析根据实施例2的方法,对一批临床血清样品包括肝炎患者22份,肝硬化患者20份,肝癌患者132份以及正常人血清样品40份,同步检测血清中所含afp和gp73蛋白含量,用graphpadprism5进行统计学分析,其结果如图3所示,可以看出肝癌患者血清afp和gp73含量均显著性高于正常人血清含量。进一步分析评估afp和gp73作为肝癌诊断指标的临床价值,从表2和图4结果显示,以健康对照组afp或gp73水平值的95%可信区间为正常值范围,afp作为单独指标诊断肝癌,其cut-off值为10.84ng/ml时,roc曲线下面积(auc)为0.6477,灵敏度60.61%,特异性77.5%;gp73作为单独指标诊断肝癌,其临床界值(cut-off)为186.9ng/ml时,roc曲线下面积(auc)为0.8275,灵敏度78.03%,特异性85%。表2项目auc(95%ci)灵敏度%特异性%阳性预测值%阴性预测值%afp0.6477(0.5699-0.7255)64.77%77.5%60.61%(80/132)77.5%(31/40)gp730.8275(0.7682-0.8867)78.03%85%78.03%(103/132)85%(34/40)当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1