荆芥的特征图谱构建方法和质量检测方法与流程
本发明涉及中药检测
技术领域:
,具体涉及荆芥的特征图谱的构建方法和质量检测方法。
背景技术:
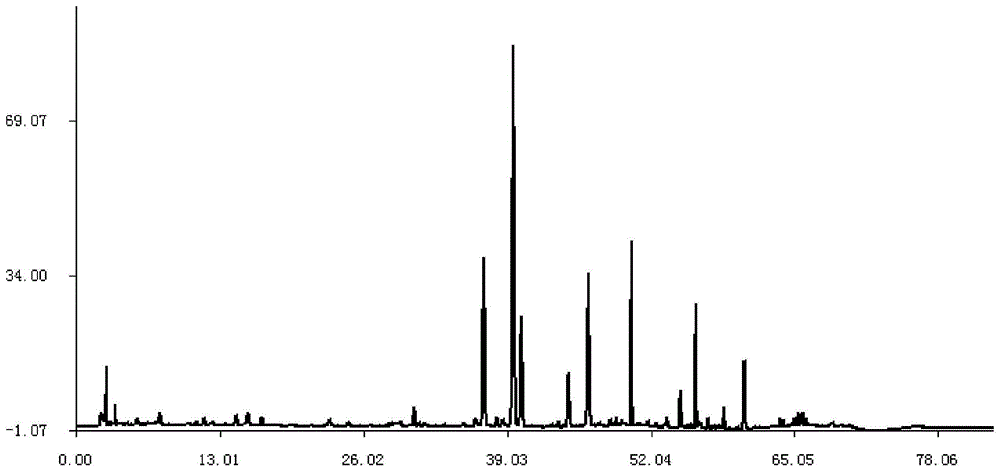
:荆芥,性微温,味辛,具有解表散风、透疹和消疮的功效,用于感冒、头痛、麻疹、风疹和疮疡,是常用的中药药材之一。在对药物的质量日益关注的今天,对中药材的质量监控非常重要。随着色谱技术的发展,荆芥药材质量标准不仅包括简单的性状、鉴别、常规检查和浸出物测定等方面,还包括高效液相指纹图谱的测定。中药指纹图谱是一种综合的、可量化的鉴别手段,是当前符合中药特色的、评价中药真实性、稳定性和一致性的质量控制模式之一。指纹图谱的作用主要是反映复杂成分的中药及其制剂内在质量的均一性和稳定性。色谱专家认为应该分离度越高越好,分出的峰越多越好;信息处理专家也认为给出的数据越多越好。但国际协调会议关于定量分析的精密度和准确度的问题说“分析的结果并非越精密越准确越好,而是达到分析对象的要求即可”,即指纹图谱的峰不是越多越好,而是达到构成指纹特征的目的即可,而作为药物,在保证安全性的基础上,能够监测有效成分就已经达到目的。据报道,荆芥主要有效成分有挥发油、多种黄酮类化合物、单萜苷等,其中挥发油主要成分为胡薄荷酮、薄荷酮,可作为挥发油的代表物质;黄酮类成分中橙皮苷含量较高,且具有一定的药理作用。现有中国文献“hplc法同时测定荆芥配方颗粒中4种成分的含量”(journalofchinesemedicinalmaterials,2016年10月,第39卷第10期2285-2287)公开了一种使用高效液相色谱法检测荆芥配方颗粒中主要有效成分咖啡酸、橙皮苷、迷迭香酸和胡薄荷酮的含量,该方法能通过有效成分含量的测定提供一种荆芥产品全面有效的质量控制。但是上述方法使用的是配方颗粒,并没有从原材料荆芥药材或饮片来从源头控制,而有效成分成分胡薄荷酮一部分存在非挥发性成分中,还有一部分存在于挥发油中,而且薄荷酮也是荆芥的有效成分,薄荷酮则主要存在于挥发油中,因此该法并不能从对荆芥有效成分进行全面的质量控制。而进一步改进荆芥药材的质量控制,除了有效成分,重金属及有害元素、农药残留量等安全性指标在实际应用过程中具有重要的影响,影响用药安全,因此,结合安全性控制的中药质量控制将使中药有效性的控制更具现实意义,建立荆芥全面、有效和安全的质量控制方法。技术实现要素:因此,本发明要解决的第一个技术问题在于克服现有技术中荆芥特征图谱所涉及的有效成分不够全面的缺陷,从而提供一种荆芥特征图谱的构建方法,该特征图谱构建方法包括非挥发性有效成分特征图谱和挥发性有效成分特征图谱的构建,对荆芥有效成分的特征色谱峰的构建更全面。本发明要解决的第二个技术问题是克服现有技术不能从有效性和安全性两个方面对荆芥进行全面质量控制的缺陷,建立了一种荆芥质量检测方法。本发明公开了一种荆芥特征图谱的构建方法,包括非挥发性成分特征图谱的构建方法和挥发性成分特征图谱的构建方法:a、所述非挥发性成分特征图谱的构建方法,包括如下步骤:供试品溶液i的制备:取荆芥供试样品制备供试品溶液ⅰ;参照物溶液i的制备:取荆芥对照药材制备对照药材参照物溶液i;取橙皮苷对照品制备对照品参照物溶液i;色谱条件与系统适用性试验:照高效液相色谱法测定,以十八烷基键合硅胶为色谱柱填充剂;以乙腈为流动相a,以体积分数为0.2%的磷酸水溶液为流动相b进行洗脱;测定法:分别精密吸取参照物溶液i与供试品溶液i,注入液相色谱仪,测定,即得;和b、所述挥发性成分特征图谱的构建方法,包括如下步骤:供试品溶液ii的制备:取由荆芥供试样品制备的挥发油,制备供试品溶液ii;参照物溶液ii的制备:取胡薄荷酮和薄荷酮分别制备对照品的参照物溶液ii;色谱条件与系统适用性试验:照气相色谱法测定,以n2为载气,以peg为固定相,控制进样口温度、检测器温度、柱温和流速;测定法:分别精密吸取参照物溶液ii与供试品溶液ii,注入气相色谱仪,测定,即得。优选的,还包括对照特征图谱的构建,利用国家药典委员会的中药色谱指纹图谱相似度评价系统,对得到的至少15批供试品溶液i特征图谱进行分析,生成非挥发性成分对照特征图谱;和/或利用国家药典委员会的中药色谱指纹图谱相似度评价系统,对得到的至少15批供试品溶液ii的气相特征图谱进行分析,生成挥发性成分对照特征图谱。优选的,所述非挥发性成分特征图谱包括6个特征峰,特征峰为:1号峰为橙皮苷,2号峰为迷迭香酸,3号峰、4号峰、5号峰为共有特征峰,6号峰为胡薄荷酮;以1号峰为参照峰,各峰号相对保留时间分别为:1号峰:1.00;2号峰:1.07;3号峰:1.09;4号峰:1.20;5号峰:1.25;6号峰:1.64;和/或所述挥发性成分特征图谱包括3个特征峰,特征峰为:1号峰为薄荷酮,2号峰为胡薄荷酮,3号峰为共有特征峰;以2号峰为参照峰,各峰号相对保留时间分别为:1号峰:0.67;2号峰:1.00;3号峰:1.50。优选的,在所述非挥发性成分特征图谱的构建方法中,洗脱方式选择梯度洗脱方式,梯度洗脱程序为:0-15min,流动相a:流动相b的体积比为8-12%:92-88%→12-16%:88-84%;15-40min,流动相a:流动相b的体积比为12-16%:88-84%→24-28%:76-72%;40-55min,流动相a:流动相b的体积比为24-28%:76-72%→58-62%:42-38%;55-60min,流动相a:流动相b的体积比为58-62%:42-38%→83-87%:17-13%;60-65min,流动相a:流动相b的体积比为83-87%:17-13%→83-87%:17-13%;优选的,所述梯度洗脱程序为:0-15min,流动相a:流动相b的体积比为10%:90%→14%:86%;15-40min,流动相a:流动相b的体积比为14%:86%→26%:74%;40-55min,流动相a:流动相b的体积比为26%:74%→60%:40%;55-60min,流动相a:流动相b的体积比为60%:40%→85%:15%;60-65min,流动相a:流动相b的体积比为85%:15%→85%:15%;优选的,色谱条件为:柱温为25-40℃;流速为0.8-1.2ml/min;检测波长为278-288nm;优选的,色谱条件为:柱温为40℃;流速为1ml/min;检测波长为283nm。优选的,在所述挥发性成分特征图谱的构建方法中,控制柱温呈梯度升温,所述梯度升温程序为:初始温度为55-65℃,保持1-3min;温度从55-65℃升至115-125℃,然后保持4-6min,升温速率为1.5-2.5℃/min;温度从115-125℃升至155-165℃,升温速率为2.5-3.5℃/min;温度从155-165℃升至235-245℃,升温速率为4.5-5.5℃/min;优选的,所述梯度升温程序为:初始温度为60℃,保持2min;温度从60℃升至120℃,保持5min,升温速率为2℃/min;温度从120℃升至160℃,升温速率为3℃/min;温度从160℃升至240℃,升温速率为5℃/min;优选的,进样口温度为245-255℃,检测器温度为245-255℃,总流量3.5-3.9ml/min;优选的,进样口温度为250℃,检测器温度为250℃,总流量3.7ml/min。优选的,所述供试品溶液ⅰ或对照药材参照物溶液i的制备方法包括:取荆芥供试样品或荆芥对照药材制成粉末,精密称取0.5-1g,加溶剂15-30ml,密塞,进行提取处理,放冷,用所述溶剂补足减失的重量,摇匀,取上清液滤过,取续滤液,即得供试品溶液ⅰ或对照药材参照物溶液i;优选的,所述对照品参照物溶液i的制备方法包括:取橙皮苷对照品加所述溶剂溶解制成含55-65μg/ml橙皮苷的对照品参照物溶液i;优选的,所述供试样品选自荆芥原药材或者荆芥饮片;优选的,所述溶剂为甲醇、乙醇或水;优选的,所述提取处理采用超声30-90min、回流30-120min或者浸渍12-24h;优选的,所述对照品参照物溶液i为含60μg/ml橙皮苷的对照品参照物溶液i。优选的,所述参照物溶液ii为含有3-6mg/ml胡薄荷酮和3-6mg/ml薄荷酮的对照品溶液,其溶剂为乙酸乙酯;所述供试药材溶液ⅱ制备方法包括:取荆芥供试样品,采用《中华人民共和国药典》2015年版四部通则2204挥发油测定的甲法制得挥发油,精密吸取25-50ul,加乙酸乙酯定容至2ml,除水干燥即得。本发明还提供了一种荆芥质量检测方法,包括采用上述荆芥特征图谱构建方法对荆芥产品进行质量检测。优选的,按照上述荆芥特征图谱构建方法同法操作检测待测荆芥产品,得到的荆芥非挥发性成分特征图谱和荆芥挥发性成分特征图谱,所述非挥发性特征图谱呈现6个特征峰,并应与对照药材参照物特征图谱中的6个特征峰相对应,其中峰1、峰6应与对照品参照物峰保留时间相一致;所述挥发性成分特征图谱呈现3个特征峰,其中峰1、峰2应与对照品参照物峰保留时间相一致。优选的,还包括对荆芥进行含量测定的步骤,包括如下步骤:供试品溶液iii:取荆芥供试样品制备供试品溶液iii;对照品溶液:取橙皮苷对照品溶于溶剂,制备对照品溶液;色谱条件与系统适用性试验:照高效液相色谱法测定,以十八烷基键合硅胶为色谱柱填充剂;以乙腈为流动相a,以体积分数为0.2%的磷酸水溶液为流动相b进行梯度洗脱,按照以下程序进行梯度洗脱:0-28min,流动相a:流动相b的体积比为17-19%:83-81%→17-19%:83-81%;28-29min,流动相a:流动相b的体积比为17-19%:83-81%→84-86%:16-14%;29-39min,流动相a:流动相b的体积比为84-86%:16-14%→84-86%:16-14%;柱温为25-35℃;流速为0.8-1.2ml/min;检测波长为278-288nm;理论板数按橙皮苷计不低于3000;测定法:分别精密吸取对照品溶液与供试品溶液iii,注入液相色谱仪,测定,即得。优选的,还包括薄层色谱法鉴别的步骤、重金属及有害元素测定的步骤和/或浸出物测定的步骤:c、所述非挥发性成分薄层色谱法鉴别步骤,包括如下步骤:分别取荆芥供试样品的粗粉和荆芥对照药材粗粉0.5-1.0g,加乙酸乙酯15-25ml,超声处理15-25分钟,滤过,滤液挥至1ml,作为供试品溶液ⅳ和对照药材溶液,然后各吸取1-5ul,分别点于同一薄层板上,于展开剂中展开,取出,晾干,置波长为361nm-371nm的紫外光下检视;优选的,所述薄层板选用硅胶g板或h板;优选的,所述展开剂选用三氯甲烷-乙酸乙酯-冰醋酸混合溶液,其体积比为(9-11):1:(0.3-0.8);和/或d、所述挥发性成分薄层色谱法鉴别步骤,包括如下步骤:取荆芥供试样品粗粉适量,照挥发油测定法《中华人民共和国药典2015年版四部通则2204》测定,分取挥发油0.1~0.3ml,加乙酸乙酯稀释至1.5~4.5ml,作为供试品溶液ⅴ。另取(-)-薄荷酮、胡薄荷酮对照品,加乙酸乙酯制成每1ml含5~30mg的溶液,作为对照品溶液。各吸取1-5ul,分别点于同一薄层板上,于展开剂中展开,取出,晾干,喷以2%~8%香草醛硫酸乙醇溶液,在105℃加热至斑点显色清晰;优选的,所述薄层板选用硅胶g板或h板;优选的,所述展开剂选用石油醚(60~90℃)-乙酸乙酯,其体积比为(11-13):1;和/或;e、所述重金属及有害元素的测定包括重金属铅、镉、砷、汞、铜的含量测定,包括如下步骤:所述农药残留量测定包括总六六六、总滴滴涕和五氯硝基苯的含量测定;和/或f、所述浸出物测定的步骤包括:所述浸出物测定操作步骤为:取荆芥供试药材粗粉2-5g,精密称定,置250~300ml的锥形瓶中,精密加溶剂100ml,密塞,冷浸,前6小时内时时振摇,再静置18小时,用干燥滤器迅速滤过,精密量取续滤液20ml,置已干燥至恒重的蒸发皿中,在水浴上蒸干后,于105℃干燥3小时,置干燥器中冷却30分钟,迅速精密称定重量,以干燥品计算供试品中浸出物的含量(%);其中,溶剂为乙醇,体积比分数为50-90%本发明技术方案,具有如下优点:1、本发明提供的荆芥特征图谱的构建方法,包括包括非挥发性有效成分特征图谱和挥发性有效成分特征图谱的构建,一方面,所述非挥发性有效成分特征图谱包括橙皮苷、迷迭香酸、胡薄荷酮的特征色谱峰,所述挥发性有效成分特征图谱包括薄荷酮和胡薄荷酮的特征色谱峰,其中胡薄荷酮既能与非挥发性有效成分共存又能与挥发性有效成分共存,通过液相色谱分析和气相色谱分析,能有效地评价检测药材中的胡薄荷酮,同时能针对性地对荆芥中其他的有效成分:迷迭香酸、橙皮苷和薄荷酮进行全面检测,既包括非挥发性的有效成分又包括挥发性的有效成分,且色谱峰分离完全,峰形佳且无干扰。另一方面,采用高效液相色谱法对荆芥非挥发性有效成分进行特征图谱的构建,分离效能高,灵敏度好,速度快,经过多次试验,以乙腈(a)-0.2%磷酸水(b)为流动相,能完全分离目标物质迷迭香酸、橙皮苷和胡薄荷酮;采用气相色谱法与高效液相色谱法互相补充,分析荆芥中的挥发性有效成分,经过多次试验采用的色谱条件与升温程序相互配合,使得薄荷酮和胡薄荷酮得到很好的分离,气相色谱分析方法和液相色谱分析方法的联用,能全面分离荆芥的非挥发性有效成分和挥发性有效成分,使荆芥的有效成分能够得到全面的分离和检测,有效成分色谱峰充分分离,峰形好且无干扰,且该特征图谱检测方法具有简单快速、稳定可靠、精密度高、重现性好、易于掌握等优点。2、本发明提供的荆芥特征图谱的构建方法,采用荆芥原药材和荆芥饮片作为供试品,能有效从药材的源头监测药材质量,提高特征图谱的实际应用价值;对液相色谱分析测试法供试样品的前处理调整了溶剂和提取操作,优选方案使用甲醇作为溶剂,回流作为提取操作,使得有效成分溶解效果好,显著增加溶出量,且制备过程易于过滤和处理,增加色谱分析的灵敏度;本发明采取药典中的挥发性成分制备方法,方法成熟,制得的挥发性成分纯度高,进行乙酸乙酯的溶解稀释,得到适于分析的合适浓度,其乙酸乙酯作为背景溶剂,不对测试结果产生干扰,气相检测结果准确,灵敏度高,速度快。3、本发明提供的荆芥特征图谱构建方法,液相色谱分析过程中,通过多次试验,乙腈(a)-0.2%磷酸水(b)为流动相,采用的检测波长在278nm-288nm,在这个波长范围内,荆芥非挥发性有效成分分离度好,配合梯度洗脱程序,能很好地分离荆芥的各个有效成分特征色谱峰,且得到的特征图谱基线平稳,峰形好,在气相色谱分析过程中,采用的升温程序是经过多次的试验评估而得,在该升温程序下,气相色谱峰分离度好,简单快速。4、本发明提供的荆芥质量检测方法,包括荆芥的安全性质量检测和有效性质量检测,安全性质量检测包括重金属及有害元素检查、农药残留量测定,通过药典中的方法检测,该检测方法标准,检测灵敏度和准确性好;有效性质量检测包括利用上述的非挥发性有效成分检测方法和挥发性有效成分检测方法检测样品的特征图谱,并建立特征图谱作为对照,所述特征图谱具有特征色谱峰,用来作为待控荆芥药材特征图谱的对照,通过相似性能简便地评价待测药材的有效成分情况;有效性质量检测还包括橙皮苷的含量测定,与特征图谱的检测项目相辅相成,对荆芥样品进行定性和定量的质量评价,还包括薄层色谱法鉴别和浸出物测定,通过这一系列的检测项目,能够全面且有针对性地对荆芥药材进行质量控制,控制方法简便易行,稳定性重复性好。5、本发明提供的荆芥质量检测方法,其中橙皮苷含量测定方法,采用供试品溶液ⅰ的制备工艺制备含量测定供试品溶液ⅲ,调整洗脱程序,使橙皮苷的液相色谱峰得到最好的呈现,使得橙皮苷含量检测结果准确,灵敏度高。6、本发明提供的荆芥质量检测方法中的薄层色谱法鉴别,优化了药典中已有的方法,使用乙酸乙酯作为溶剂,三氯甲烷-乙酸乙酯-冰醋酸为展开剂,不使用显色剂,改用荧光检视,在荧光下得到的荧光斑点清晰,分离度好,且该鉴别方法稳定可靠,重复性好,且该处理方法具有操作简单、节省时间等优点。7、本发明提供的荆芥质量检测方法中的挥发油薄层色谱法鉴别,以荆芥挥发油为供试品,石油醚(60~90℃)-乙酸乙酯为展开剂,香草醛硫酸乙醇溶液为显色剂,显色得到的斑点清晰,分离度好,能清晰的鉴别出薄荷酮、胡薄荷酮等有效成分,且该鉴别方法稳定可靠,重复性好。8、本发明提供的荆芥质量检测方法中的浸出物测定,采用药典中已有的方法,使用50-90%的乙醇作为溶剂,该溶剂下有效成分能很好地溶出,增加浸出物测定的准确性和灵敏度。附图说明为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。图1为实施例1中对照药材参照物溶液ⅰ的特征图谱;图2为实施例1中橙皮苷对照品参照物溶液ⅰ的特征图谱;图3为实施例1中供试品溶液ⅰ的特征图谱;图4为实施例1中供试品溶液ⅱ的特征图谱;图5为实施例4中荆芥非挥发性成分对照特征图谱;图6为实施例4中荆芥挥发性成分对照特征图谱;图7为实施例5中橙皮苷对照品溶液的液相色谱图;图8为实施例5中供试品溶液ⅲ的液相色谱图;图9为实施例5中橙皮苷含量测定时的回归曲线;图10为实施例8所述薄层色谱图;图11为实施例11所述薄层色谱图;图12为实验例中采用药典方法得到的薄层色谱图;图13为实验例中薄层色谱检测方法的低温考察薄层色谱图;图14为实验例中薄层色谱检测方法的18%的湿度考察薄层色谱图;图15为实验例中薄层色谱检测方法的72%的湿度考察薄层色谱图;图16为实验例中薄层色谱检测方法的专属性考察薄层色谱图;图17为实验例中薄层色谱检测方法的耐用性考察青岛海洋化工分厂硅胶g薄层板薄层色谱图;图18为实验例中薄层色谱检测方法的耐用性考察烟台市化学工业研究所硅胶g薄层板薄层色谱图;图19为实验例中薄层色谱检测方法的重现性考察一名实验人员操作得到的薄层色谱图;图20为实验例中薄层色谱检测方法的重现性考察另一名实验人员操作得到的薄层色谱图;图21为实验例中挥发油薄层色谱检测方法的低温考察薄层色谱图;图22为实验例中挥发油薄层色谱检测方法的18%的湿度考察薄层色谱图;图23为实验例中挥发油薄层色谱检测方法的72%的湿度考察薄层色谱图;图24为实验例中挥发油薄层色谱检测方法的专属性考察薄层色谱图;图25为实验例中挥发油薄层色谱检测方法的耐用性考察青岛海洋化工分厂硅胶g薄层板薄层色谱图;图26为实验例中挥发油薄层色谱检测方法的耐用性考察烟台市化学工业研究所硅胶g薄层板薄层色谱图;图27为实验例中挥发油薄层色谱检测方法的重现性考察一名实验人员操作得到的薄层色谱图;图28为实验例中挥发油薄层色谱检测方法的重现性考察另一名实验人员操作得到的薄层色谱图;图29为实验例中含量测定液相色谱条件考察中洗脱方法1得到的液相色谱图;图30为实验例中含量测定液相色谱条件考察中洗脱方法2得到的液相色谱图;图31为实验例中含量测定液相色谱条件考察中洗脱方法3得到的液相色谱图;图32为实验例中含量测定液相色谱条件考察中洗脱方法4得到的液相色谱图;图33为实验例中荆芥dad全波长扫描图谱;图34为实验例中非挥发性成分hplc液相色谱条件考察中洗脱方法1得到的液相色谱图;图35为实验例中非挥发性成分hplc液相色谱条件考察中洗脱方法2得到的液相色谱图;图36为实验例中非挥发性成分hplc液相色谱条件考察中洗脱方法3得到的液相色谱图;图37为实验例非挥发性成分对照特征图谱;图38为试验例中挥发性成分气相色谱法检测升温程序1得到的气相色谱图;图39为试验例中挥发性成分气相色谱法检测升温程序2得到的气相色谱图;图40为试验例中挥发性成分气相色谱法检测升温程序3得到的气相色谱图;图41为试验例中挥发性成分气相色谱法检测升温程序4得到的气相色谱图;图42为试验例中挥发性成分气相色谱法检测升温程序5得到的气相色谱图;图43为实验例中挥发性成分对照特征图谱。具体实施方式提供下述实施例是为了更好地进一步理解本发明,并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征进行组合而得出的任何与本发明相同或相近似的产品,均落在本发明的保护范围之内。实施例中未注明具体实验步骤或条件者,按照本领域内的文献所描述的常规实验步骤的操作或条件即可进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规试剂产品。下面对本发明实施例的荆芥特征图谱检测方法进行具体说明。1、本发明实施例采用的实验仪器与试剂见表1.表1实验仪器与试剂统计表2、下面结合实施例对本发明进一步说明:实施例1本实施例提供了一种荆芥特征图谱的构建方法,包括非挥发性成分特征图谱的构建方法和挥发性成分特征图谱的构建方法,具体如下:a、所述非挥发性成分特征图谱的构建方法,包括如下步骤:供试品溶液i的制备:取产自安徽的供试荆芥药材粉末(过二号筛)0.5g,置具塞三角瓶内,加甲醇25ml,密塞,称定重量,回流30分钟,放冷,用甲醇补足减失的重量,摇匀,取上清液滤过,取续滤液,即得;参照物溶液i的制备:取荆芥对照药材粉末(过二号筛)0.5g,置具塞三角瓶内,加甲醇25ml,密塞,称定重量,回流30分钟,放冷,用甲醇补足减失的重量,摇匀,取上清液滤过,取续滤液,即得对照药材参照物溶液i;称取橙皮苷对照品适量,加甲醇溶解,制成每1ml含橙皮苷60μg的对照品参照物溶液i;色谱条件与系统适用性试验:照高效液相色谱法测定,以十八烷基键合硅胶为色谱柱填充剂,选择waters柱(250mm×4.6mm,5μm);以乙腈为流动相a,以体积分数为0.2%的磷酸水溶液为流动相b,按照如下程序进行梯度洗脱:0-15min,流动相a:流动相b的体积比为10%:90%→14%:86%;15-40min,流动相a:流动相b的体积比为14%:86%→26%:74%;40-55min,流动相a:流动相b的体积比为26%:74%→60%:40%;55-60min,流动相a:流动相b的体积比为60%:40%→85%:15%;60-65min,流动相a:流动相b的体积比为85%:15%→85%:15%;柱温为40℃;流速为1ml/min;检测波长为283nm,理论板数按橙皮苷计不低于3000;测定法:分别精密吸取参照物溶液i与供试品溶液i各10μl,注入液相色谱仪,测定,即得;所述对照药材参照物溶液ⅰ的特征图谱如图1所示,所述橙皮苷对照品参照物溶液i的特征图谱如图2所示,所述供试品溶液i的特征图谱如图3所示。b、所述挥发性成分特征图谱的构建方法,包括如下步骤:供试品溶液ii的制备:取产自安徽的供试荆芥药材用《中华人民共和国药典》2015年版四部通则2204挥发油测定的甲法制得挥发油,精密吸取50μl,加乙酸乙酯定容至2ml,加无水硫酸钠干燥,摇匀,取续滤液即得;参照物溶液ii的制备:精密称定胡薄荷酮和薄荷酮各0.5g,溶于30ml乙酸乙酯溶液,再定容至100ml,得到含有胡薄荷酮5mg/ml、薄荷酮5mg/ml的混合对照品溶液;色谱条件与系统适用性试验:照气相色谱法测定,以n2为载气,以peg(db-wax,30m*0.530mm)为固定相,进样口温度为250℃,检测器温度为250℃,控制柱温呈梯度升温,所述梯度升温程序为:初始温度为60℃,保持2min;温度从60℃升至120℃,然后保持5min,升温速率为2℃/min;温度从120℃升至160℃,升温速率为3℃/min;温度从160℃升至240℃,升温速率为5℃/min;总流量3.7ml/min,理论板数按胡薄荷酮峰计算为3200;测定法:分别精密吸取参照物溶液ii与供试品溶液ii各5μl,注入气相色谱仪,测定,即得;所述供试品溶液ii的特征图谱如图4所示。实施例2本实施例提供了一种荆芥特征图谱的构建方法,包括非挥发性成分特征图谱的构建方法的步骤和挥发性成分特征图谱的构建方法的步骤,具体如下:a、所述非挥发性成分特征图谱的构建方法,包括如下步骤:供试品溶液i的制备:取产自安徽的供试荆芥药材粉末(过二号筛)1g,置具塞三角瓶内,加甲醇15ml,密塞,称定重量,回流60分钟,放冷,用甲醇补足减失的重量,摇匀,取上清液滤过,取续滤液,即得;参照物溶液i的制备:取荆芥对照药材粉末(过二号筛)1g,置具塞三角瓶内,加甲醇15ml,密塞,称定重量,回流60分钟,放冷,用甲醇补足减失的重量,摇匀,取上清液滤过,取续滤液,即得对照药材参照物溶液i;称取橙皮苷对照品适量,加甲醇溶解,制成每1ml含橙皮苷55μg的对照品参照物溶液i;色谱条件与系统适用性试验:照高效液相色谱法测定,以十八烷基键合硅胶为色谱柱填充剂,选择alchrombond-aq柱(250mm×4.6mm,5μm);以乙腈为流动相a,以体积浓度为0.2%的磷酸水溶液为流动相b,按照如下程序进行梯度洗脱:0-15min,流动相a:流动相b的体积比为8%:92%→12%:88%;15-40min,流动相a:流动相b的体积比为12%:88%→24%:76%;40-55min,流动相a:流动相b的体积比为24%:76%→58%:42%;55-60min,流动相a:流动相b的体积比为58%:42%→83%:17%;60-65min,流动相a:流动相b的体积比为83%:17%→83%:17%;柱温为35℃;流速为0.8ml/min;检测波长为278nm,理论板数按橙皮苷计为12035;测定法:分别精密吸取参照物溶液i与供试品溶液i各10μl,注入液相色谱仪,测定,即得。b、所述挥发性成分特征图谱的构建方法,包括如下步骤:供试品溶液ii的制备:取产自安徽的供试荆芥药材用《中华人民共和国药典》2015年版四部通则2204挥发油测定的甲法制得挥发油,精密吸取25μl,加乙酸乙酯定容至2ml,加无水硫酸钠干燥,摇匀,取续滤液即得;参照物溶液ii的制备:精密称定胡薄荷酮和薄荷酮各0.3g,溶于30ml乙酸乙酯溶液,再定容至100ml,得到含有胡薄荷酮3mg/ml、薄荷酮3mg/ml的混合对照品溶液;色谱条件与系统适用性试验:照气相色谱法测定,以n2为载气,以peg(db-wax,30m*0.530mm)为固定相,进样口温度为245℃,检测器温度为245℃,控制柱温呈梯度升温,所述梯度升温程序为:柱温初始温度为55℃,保持1min;温度从55℃升至115℃,然后保持4min,升温速率为1.5℃/min;温度从115℃升至155℃,升温速率为2.5℃/min;温度从155℃升至235℃,升温速率为4.5℃/min;总流量3.5ml/min,理论板数按胡薄荷酮峰计算为4000;测定法:分别精密吸取参照物溶液ii与供试品溶液ii各5μl,注入气相色谱仪,测定,即得。实施例3本实施例提供了一种荆芥特征图谱的构建方法,包括非挥发性成分特征图谱的构建方法步骤和挥发性成分特征图谱的构建方法步骤,具体如下:a、所述非挥发性成分特征图谱的构建方法,包括如下步骤:供试品溶液i的制备:取产自河北的供试荆芥饮片粉末(过二号筛)0.8g,置具塞三角瓶内,加乙醇30ml,密塞,称定重量,回流120分钟,放冷,用乙醇补足减失的重量,摇匀,取上清液滤过,取续滤液,即得;参照物溶液i的制备:取荆芥对照药材粉末(过二号筛)0.8g,置具塞三角瓶内,加乙醇30ml,密塞,称定重量,回流120分钟,放冷,用乙醇补足减失的重量,摇匀,取上清液滤过,取续滤液,即得对照药材参照物溶液i;称取橙皮苷对照品适量,加甲醇溶解,制成每1ml含橙皮苷65μg的对照品参照物溶液i;色谱条件与系统适用性试验:照高效液相色谱法测定,以十八烷基键合硅胶为色谱柱填充剂,选择phenomex-luna柱(250mm×4.6mm,5μm);以乙腈为流动相a,以0.2%磷酸的水溶液为流动相b,按照如下程序进行梯度洗脱:0-15min,流动相a:流动相b的体积比为12%:88%→16%:84%;15-40min,流动相a:流动相b的体积比为16%:84%→28%:72%;40-55min,流动相a:流动相b的体积比为28%:72%→62%:38%;55-60min,流动相a:流动相b的体积比为62%:38%→87%:13%;60-65min,流动相a:流动相b的体积比为87%:13%→87%:13%;柱温为25℃;流速为1.2ml/min;检测波长为288nm,理论板数按橙皮苷计为10253;测定法:分别精密吸取参照物溶液i与供试品溶液i各10μl,注入液相色谱仪,测定,即得。b、所述挥发性成分特征图谱的构建方法,包括如下步骤:供试品溶液ii的制备:取产自安徽的供试荆芥药材用《中华人民共和国药典》2015年版四部通则2204挥发油测定的甲法制得挥发油,精密吸取80μl,加乙酸乙酯定容至2ml,加无水硫酸钠干燥,摇匀,取续滤液即得;参照物溶液ii的制备:精密称定胡薄荷酮和薄荷酮各0.6g,溶于30ml乙酸乙酯溶液,再定容至100ml,得到含有胡薄荷酮6mg/ml、薄荷酮6mg/ml的混合对照品溶液;色谱条件与系统适用性试验:照气相色谱法测定,以n2为载气,以peg(db-wax,30m*0.530mm)为固定相,进样口温度为245℃,检测器温度为245℃,控制柱温呈梯度升温,所述梯度升温程序为:柱温初始温度为65℃,保持3min;温度从65℃升至125℃,然后保持6min,升温速率为2.5℃/min;温度从125℃升至165℃,升温速率为3.5℃/min;温度从165℃升至245℃,升温速率为5.5℃/min;总流量3.9ml/min,理论板数按胡薄荷酮峰计算为5000;测定法:分别精密吸取参照物溶液ii与供试品溶液ii各5μl,注入气相色谱仪,测定,即得。实施例4本实施例提供了一种荆芥特征图谱的构建方法,包括荆芥非挥发性成分对照特征图谱的构建和挥发性成分对照特征图谱的构建:a、荆芥非挥发性成分对照特征图谱的构建包括:随机选取不同批次的样品共20个,按照实施例1所述荆芥非挥发性有效成份的特征图谱构建方法测得20个荆芥样品的非挥发性有效成分的特征色谱,利用国家药典委员会的中药色谱指纹图谱相似度评价系统,得到荆芥非挥发性成分的对照特征图谱,如图5所示;由图6中可知,所述非挥发性成分对照特征图谱包括6个特征峰,共有特征峰为:1号峰为橙皮苷,2号峰为迷迭香酸,3号峰、4号峰、5号峰为共有特征峰,6号峰为胡薄荷酮;以1号峰为参照峰,各峰号相对保留时间分别为:1号峰:1.00;2号峰:1.07;3号峰:1.09;4号峰:1.20;5号峰:1.25;6号峰:1.64;上述6个特征峰与对照药材参照物溶液i的特征色谱图中的6个特征峰相对应,其中1号峰和6号峰与对照品参照物溶液i的色谱图中的相对保留时间一致;b、荆芥挥发性成分特征图谱的构建包括:随机选取不同批次的荆芥样品共20个,按照实施例1所述荆芥挥发性有效成份的特征图谱检测方法测得荆芥挥发性有效成分的特征色谱,利用国家药典委员会的中药色谱指纹图谱相似度评价系统,得到荆芥挥发性成分对照特征图谱,如图6所示;由图6中可知,所述荆芥挥发性成分特征图谱包括3个特征峰,共有特征峰为:1号峰为薄荷酮,2号峰为胡薄荷酮,3号峰为共有特征峰;以2号峰为参照峰,各峰号相对保留时间分别为:1号峰:0.67;2号峰:1.00;3号峰:1.50;其中1号峰和2号峰与实施例1中参照物溶液ii的特征图谱中参照物峰的相对保留时间一致。实施例5本实施例提供了一种荆芥的质量检测方法,包括对荆芥进行含量测定的步骤,包括如下步骤:供试品溶液iii:取产自安徽的供试荆芥饮片制成粉末(过二号筛)0.5g,置具塞三角瓶内,加甲醇25ml,密塞,称定重量,回流30分钟,放冷,用甲醇补足减失的重量,摇匀,取上清液滤过,取续滤液,即得;对照品溶液:称取橙皮苷(c28h34o15)对照品适量,加甲醇溶解,制成每1ml含橙皮苷68.231μg的对照品溶液①,再进行连续稀释,制成浓度分别为34.116μg/ml、17.058μg/ml、8.529μg/ml、4.264μg/ml、2.132μg/ml的橙皮苷对照品溶液②-⑥;色谱条件与系统适用性试验:照高效液相色谱法测定,以十八烷基键合硅胶为色谱柱填充剂,选择waters柱(250mm×4.6mm,5μm);以乙腈为流动相a,以含体积浓度为0.2%的磷酸水溶液为流动相b进行梯度洗脱,按照以下程序进行梯度洗脱:0-28min,流动相a:流动相b的体积比为0-28min,流动相a:流动相b的体积比为18%:82%→18%:82%;28-29min,流动相a:流动相b的体积比为18%:82%→85%:15%;29-39min,流动相a:流动相b的体积比为85%:15%→85%:15%;柱温为30℃;流速为1ml/min;检测波长为283nm;理论板数按橙皮苷计为9000;测定法:分别精密吸取对照品溶液与供试品溶液iii10ul,注入液相色谱仪,测定,即得;所述对照品溶液①的色谱图如图7所示,所述供试品溶液iii的色谱图如图8所示;计算:将对照品溶液①-⑥分别检测两次,分别计算峰面积和平均峰面积,如表2所示,得到橙皮苷浓度与平均峰面积的线性关系,并拟合供试品的回归方程,橙皮苷在2.132μg/ml~68.231μg/ml范围内线性关系良好,所述回归方程为y=21954x,r=0.9997,所述回归方程的曲线图如图7所示;用外标一点法计算橙皮苷的含量,计算得到的橙皮苷含量见下表3,本供试品按干燥品计算,含橙皮苷(c28h34o15)不得少于0.06。表2荆芥橙皮苷线性关系考察浓度(μg/ml)峰面积1峰面积2平均峰面积2.1324568947099463944.2649494694734948408.52919011018797218904117.058375568347321361444.534.11669668075534072601068.231154129514835021512399表3样品中橙皮苷的含量样品名橙皮苷(%)样品10.309实施例6本实施例提供了一种荆芥的质量检测方法,包括对荆芥进行含量测定的步骤,包括如下步骤:供试品溶液iii:取产自安徽的供试荆芥药材粉末(过二号筛)1g,置具塞三角瓶内,加甲醇15ml,密塞,称定重量,回流60分钟,放冷,用甲醇补足减失的重量,摇匀,取上清液滤过,取续滤液,即得;对照品溶液:按照实施例5所述橙皮苷对照品溶液制备方法来制备;色谱条件与系统适用性试验:照高效液相色谱法测定,以十八烷基键合硅胶为色谱柱填充剂,选择alchrombond-aq柱(250mm×4.6mm,5μm);以乙腈为流动相a,以体积分数为0.2%的磷酸水溶液为流动相b进行梯度洗脱,按照以下程序进行梯度洗脱:0-28min,流动相a:流动相b的体积比为17%:83%→17%:83%;28-29min,流动相a:流动相b的体积比为17%:83%→84%:16%;29-39min,流动相a:流动相b的体积比为84%:16%→84%:16%;柱温为35℃;流速为0.8ml/min;检测波长为278nm;理论板数按橙皮苷计为11235;测定和计算:按照实施例5所述测定和计算方法得到本实施例所述荆芥供试药材的橙皮苷含量,如表4所示。表4样品中橙皮苷的含量样品名橙皮苷(%)样品0.187实施例7本实施例提供了一种荆芥的质量检测方法,包括对荆芥进行含量测定的步骤,包括如下步骤:供试品溶液iii:取产自河北的供试荆芥药材粉末(过二号筛)0.8g,置具塞三角瓶内,加乙醇30ml,密塞,称定重量,回流120分钟,放冷,用乙醇补足减失的重量,摇匀,取上清液滤过,取续滤液,即得;对照品溶液:按照实施例5所述橙皮苷对照品溶液制备方法来制备;色谱条件与系统适用性试验:照高效液相色谱法测定,以十八烷基键合硅胶为色谱柱填充剂,选择phenomex-luna柱(250mm×4.6mm,5μm);以乙腈为流动相a,以0.2%磷酸的水溶液为流动相b进行梯度洗脱,按照以下程序进行梯度洗脱:0-28min,流动相a:流动相b的体积比为19%:81%→19%:81%;28-29min,流动相a:流动相b的体积比为19%:81%→86%:14%;29-39min,流动相a:流动相b的体积比为86%:14%→86%:14%;柱温为33℃;流速为1.2ml/min;检测波长为288nm;理论板数按橙皮苷计不低于3000;测定和计算:按照实施例5所述测定和计算方法得到本实施例所述荆芥供试药材的橙皮苷含量,如表5所示。表5样品中橙皮苷的含量样品名橙皮苷(%)样品30.174实施例8本实施例提供了一种荆芥的质量检测方法,还包括对荆芥进行非挥发性成分薄层色谱鉴别的步骤,具体如下:取产自安徽的供试荆芥原药材、产自河北的荆芥饮片和荆芥对照药材各0.8g,分别加乙酸乙酯20ml,以功率为250w,频率为40khz的超声处理20分钟,滤过,滤液挥至1ml,得到3份滤液,各精密吸取2ul,分别点于同一硅胶g板,板置展开缸中预饱和20分钟,于体积比为10:1:0.5的三氯甲烷-乙酸乙酯-冰醋酸混合展开剂中展开,取出,晾干,置波长为366nm紫外光下检视,结果如图10所示,其中序号1为荆芥对照药材,序号2为荆芥原药材,序号3为荆芥饮片。实施例9本实施例提供了一种荆芥的质量检测方法,还包括对荆芥非挥发性成分进行薄层色谱鉴别的步骤,具体如下:取产自安徽的供试荆芥原药材、产自河北的荆芥饮片和荆芥对照药材各0.5g,分别加乙酸乙酯15ml,以功率为250w,频率为40khz的超声处理15分钟,滤过,滤液挥至1ml,各精密吸取1ul,分别点于同一硅胶h板,于体积比为9:1:0.3的三氯甲烷-乙酸乙酯-冰醋酸混合展开剂中展开,取出,晾干,置波长为361nm紫外光下检视。实施例10本实施例提供了一种荆芥的质量检测方法,还包括对荆芥进行非挥发性成分薄层色谱鉴别的步骤,具体如下:取产自安徽的供试荆芥原药材、产自河北的荆芥饮片和荆芥对照药材各1g,分别加乙酸乙酯25ml,超声处理25分钟,滤过,滤液挥至1ml,各精密吸取5ul,分别点于同一硅胶h板,于体积比为11:1:0.8的三氯甲烷-乙酸乙酯-冰醋酸混合展开剂中展开,取出,晾干,置波长为371nm紫外光下检视。实施例11本实施例提供了一种荆芥的质量检测方法,还包括对荆芥挥发性成分进行薄层色谱鉴别的步骤,具体如下:取产自安徽的供试荆芥原药材、荆芥饮片,照挥发油测定法(中华人民共和国药典2015年版四部通则2204)测定,分取挥发油0.2ml,加乙酸乙酯稀释至3ml,得到2份供试品溶液。另取(-)-薄荷酮、胡薄荷酮对照品,加乙酸乙酯制成每1ml含20mg的溶液,得到2份对照品溶液。各吸取上述溶液1ul,分别点于同一硅胶g板上,于体积比为12:1的石油醚(60~90℃)-乙酸乙酯混合展开剂中展开,取出,晾干,喷以5%香草醛硫酸乙醇溶液,在105℃加热至斑点显色清晰,结果如图11所示,其中序号1为(-)-薄荷酮,序号2为胡薄荷酮,序号3为荆芥药材,序号4为荆芥饮片。实施例12本实施例提供了一种荆芥的质量检测方法,还包括对荆芥挥发油进行薄层色谱鉴别的步骤,具体如下:取产自安徽的供试荆芥原药材、荆芥饮片,照挥发油测定法(中华人民共和国药典2015年版四部通则2204)测定,分取挥发油0.1ml,加乙酸乙酯稀释至1.5ml,得到2份供试品溶液。另取(-)-薄荷酮、胡薄荷酮对照品,加乙酸乙酯制成每1ml含30mg的溶液,得到2份对照品溶液。各吸取上述溶液2ul,分别点于同一硅胶g板上,于体积比为11:1的石油醚(60~90℃)-乙酸乙酯混合展开剂中展开,取出,晾干,喷以4%香草醛硫酸乙醇溶液,在105℃加热至斑点显色清晰。实施例13本实施例提供了一种荆芥的质量检测方法,还包括对荆芥挥发性成分进行薄层色谱鉴别的步骤,具体如下:取产自安徽的供试荆芥原药材、荆芥饮片,照挥发油测定法(中华人民共和国药典2015年版四部通则2204)测定,分取挥发油0.3ml,加乙酸乙酯稀释至4.5ml,得到2份供试品溶液。另取(-)-薄荷酮、胡薄荷酮对照品,加乙酸乙酯制成每1ml含10mg的溶液,得到2份对照品溶液。各吸取上述溶液5ul,分别点于同一硅胶g板上,于体积比为13:1的石油醚(60~90℃)-乙酸乙酯混合展开剂中展开,取出,晾干,喷以6%香草醛硫酸乙醇溶液,在105℃加热至斑点显色清晰。实施例14本实施例提供了一种荆芥的质量检测方法,还包括对荆芥进行浸出物检测的步骤,具体如下:取产自安徽的供试荆芥原药材制备的粗粉4g,精密称定,精密加体积分数为70%的乙醇100ml,振摇6小时,静置18h,滤过,精密量取续滤液20ml,置已干燥至恒重的蒸发皿中,蒸干,于105℃干燥3小时,置干燥器中冷却30分钟,称定重量,计算浸出物的含量;测得浸出物测定含量为8.03%。实施例15本实施例提供了一种荆芥的质量检测方法,还包括对荆芥进行浸出物检测,具体如下:取产自安徽的供试荆芥药材粗粉2g,精密称定,精密加体积分数为50%的乙醇100ml,振摇4小时,静置16小时,滤过,精密量取续滤液10ml,置已干燥至恒重的蒸发皿中,蒸干,于100℃干燥3小时,置干燥器中冷却30分钟,称定重量,计算浸出物的含量;测得浸出物测定含量为8.54%。实施例16本实施例提供了一种荆芥的质量检测方法,还包括对荆芥进行浸出物检测,具体如下:取产自河北的供试荆芥饮片制备的粗粉5g,精密称定,精密加体积分数为95%的乙醇100ml,振摇9小时,静置36小时,滤过,精密量取续滤液30ml,置已干燥至恒重的蒸发皿中,蒸干,于120℃干燥5小时,置干燥器中冷却30分钟,称定重量,计算浸出物的含量;测得浸出物测定含量为19.20%。实施例17本实施例提供了一种荆芥的质量检测方法,还包括重金属及有害元素的测定,包括重金属铅、镉、砷、汞、铜的含量测定,所采用的供试品为产自安徽的供试荆芥药材(样品1)、产自河北的供试荆芥药材(样品2)、产自河北的供试荆芥饮片(样品3),具体如下步骤:照铅、镉、砷、汞、铜测定法(《中国药典》通则2321原子吸收分光光度法或电感耦合等离子体质谱法)测定,铅不得过5mg/kg;镉不得过0.3mg/kg;砷不得过2mg/kg;汞不得过0.2mg/kg;铜不得过20mg/kg。样品铅、镉、砷、汞、铜含量见下表6。表6样品中铅、镉、砷、汞、铜含量测定结果样品名铅(mg/kg)镉(mg/kg)砷(mg/kg)汞(mg/kg)铜(mg/kg)样品10.290.0220.120.0101.48样品20.790.0670.260.0185.71样品31.120.1500.160.0145.18照农药残留量测定法(《中国药典》通则2341有机氯类农药残留量测定法-第一法)测定。含总六六六(α-bhc、β-bhc、γ-bhc、δ-bhc之和)不得过0.2mg/kg;总滴滴涕(pp'-dde、pp'-ddd、op'-ddt,pp'-ddt之和)不得过0.2mg/kg;五氯硝基苯不得过0.1mg/kg。样品农药残留量结果见下表7。表7样品农药残留量测定结果样品名总六六六(mg/kg)总滴滴涕(mg/kg)五氯硝基苯(mg/kg)样品1未检出(<0.01)未检出(<0.01)未检出(<0.01)样品2未检出(<0.01)未检出(<0.01)未检出(<0.01)样品3未检出(<0.01)未检出(<0.01)未检出(<0.01)实验例1、荆芥薄层色谱法鉴别方法1.1方法优化按照《中华人民共和国药典》2015年版中荆芥项下薄层鉴别方法对荆芥药材进行鉴别,如下:取荆芥药材粗粉0.8g,加石油醚(60~90℃)20ml,密塞,时时振摇,放置过夜,滤过,滤液挥至1ml,作为供试品溶液。另取荆芥对照药材0.8g,同法制成对照药材溶液;照薄层色谱法(《中华人民共和国药典》2015年版四部通则0502)试验,吸取上述两种溶液各10μl,分别点于同一硅胶h薄层板上,以正己烷-乙酸乙酯(17:3)为展开剂,展开,取出,晾干,喷以5%香草醛的5%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。采用药典方法得到的薄层色谱图见图12。图中“对照”-对照药材色谱,由左至右2号、8号、10号、11号和12号依次代表5种不同产地的供试的荆芥药材。由图中可看出,采用药典方法鉴别白术效果不佳,因此,对其进行优化。(1)提取方法考察药典方法为:取荆芥粗粉0.8g,加石油醚(60~90℃)20ml,密塞,时时振摇,放置过夜,滤过,滤液挥至1ml,作为供试品溶液;为了缩短时间,通过不同提取方法、不同提取溶剂对比,确定提取方法为:取荆芥饮片粗粉0.8g,加乙酸乙酯20ml,超声20分钟,滤过,滤液挥至1ml,作为供试品溶液。(2)显色方法考察药典方法为:喷以5%香草醛的5%硫酸乙醇溶液,在105℃加热至斑点显色清晰。研究发现,展开后的薄层板在紫外光灯366nm下有多个明显的荧光斑点,且较喷显色剂效果更好、更环保,因此选择在紫外光灯366nm下检视。(3)展开剂选择对展开剂的种类及配比进行了摸索,分别选用石油醚-乙酸乙酯、正己烷-乙酸乙酯、甲苯-乙酸乙酯、环己烷-乙酸乙酯-异丙醇-甲酸、正己烷-丙酮-冰醋酸、二氯甲烷-乙酸乙酯-冰醋酸、二氯甲烷-乙醇-冰醋酸、环己烷-二氯甲烷-乙酸乙酯-冰醋酸、三氯甲烷-乙酸乙酯-冰醋酸等作为展开剂,最终选用三氯甲烷-乙酸乙酯-冰醋酸为展开剂,比例10:1:0.5为佳。(4)薄层板考察通过硅胶g板、h板、gf254板等考察,确定硅胶g板分离效果最佳。1.2方法学考察(1)低温考察按照本发明实施例8中的方案进行操作,点样,于4℃冰箱中展开,取出,晾干,置紫外光灯(366nm)下检视,结果显示,在4℃下的环境中展开效果良好,见图13,图中1-对照药材;2-荆芥药材;3-荆芥饮片。(2)湿度考察按照本发明实施例8中的方案进行操作,点样,于18%、72%的相对湿度中展开,取出,晾干,置紫外光灯(366nm)下检视,结果显示,在不同的湿度环境中展开效果均较好,见图14(18%)、图15(72%),图14-15中,1-对照药材;2-荆芥药材;3-荆芥饮片。(3)专属性考察按照本发明实施例8中的方案进行操作,利用乙酸乙酯试剂作为空白溶液,点样,展开,取出,晾干,置紫外光灯(366nm)下检视,结果显示,乙酸乙酯无干扰,证明该方法具有良好的专属性,见图16,图中1-乙酸乙酯;2-对照药材;3-荆芥药材;4-荆芥饮片。(4)耐用性考察按照本发明实施例8中的方案进行操作,分别点样与青岛海洋化工分厂和烟台市化学工业研究所的硅胶g薄层板上,展开,取出,晾干,置紫外光灯(366nm)下检视,结果显示,在2种板上均有较好的分离效果,证明该方法具有良好的耐用性,见图17、图18,图17-18中,1-对照药材;2-荆芥药材;3-荆芥饮片。(5)重现性考察由2名实验人员同时按照本发明实施例8中的方案进行操作,结果证明该方法具有良好的重现性,见图19、图20,图19-20中,1-对照药材;2-荆芥药材;3-荆芥饮片。2、荆芥挥发油薄层色谱法鉴别方法2.1方法优化(1)展开剂选择对展开剂的种类及配比进行了摸索,分别选用正己烷-乙酸乙酯、甲苯-乙酸乙酯、石油醚-乙酸乙酯等作为展开剂,最终选用石油醚(60~90℃)-乙酸乙酯为展开剂,比例12:1为佳。(2)薄层板考察通过硅胶g板、h板、gf254板等考察,确定硅胶g板分离效果最佳。2.2方法学考察(1)低温考察按照本发明实施例11中的方案进行操作,点样,于4℃冰箱中展开,取出,晾干,喷以5%香草醛硫酸乙醇溶液,在105℃加热至斑点显色清晰,结果显示,在4℃下的环境中展开效果良好,见图21,图中1-(-)-薄荷酮;2-胡薄荷酮;3-荆芥药材;4-荆芥饮片。(2)湿度考察按照本发明实施例11中的方案进行操作,点样,于18%、72%的相对湿度中展开,取出,晾干,喷以5%香草醛硫酸乙醇溶液,在105℃加热至斑点显色清晰,结果显示,在不同的湿度环境中展开效果均较好,见图22(18%)、图23(72%),图22-23中,1-(-)-薄荷酮;2-胡薄荷酮;3-荆芥药材;4-荆芥饮片。(3)专属性考察按照本发明实施例11中的方案进行操作,利用乙酸乙酯试剂作为空白溶液,点样,展开,取出,晾干,喷以5%香草醛硫酸乙醇溶液,在105℃加热至斑点显色清晰,结果显示,乙酸乙酯无干扰,证明该方法具有良好的专属性,见图24,图中1-(-)-薄荷酮;2-胡薄荷酮;3-荆芥药材;4-荆芥饮片;5-乙酸乙酯。(4)耐用性考察按照本发明实施例11中的方案进行操作,分别点样与青岛海洋化工分厂和烟台市化学工业研究所的硅胶g薄层板上,展开,取出,晾干,喷以5%香草醛硫酸乙醇溶液,在105℃加热至斑点显色清晰,结果显示,在2种板上均有较好的分离效果,证明该方法具有良好的耐用性,见图25、图26,图25-26中,1-(-)-薄荷酮;2-胡薄荷酮;3-荆芥药材;4-荆芥饮片。(5)重现性考察由2名实验人员同时按照本发明实施例11中的方案进行操作,结果证明该方法具有良好的重现性,见图27、图28,图27-28中,1-(-)-薄荷酮;2-胡薄荷酮;3-荆芥药材;4-荆芥饮片。3.荆芥重金属及有害元素测定3.1.1方法采用原子吸收分光光度法测定荆芥药材中的铅、镉、砷、汞、铜。具体方法为《中华人民共和国药典》2015年版四部通则2321铅、镉、砷、汞、铜测定法。3.1.2结果对20个批次荆芥药材进行了铅、镉、砷、汞、铜测定,测定结果见表8。表8荆芥药材重金属及有害元素测定结果(ppm,mg/kg)3.2荆芥药材农药残留量测定3.2.1方法采用气相色谱法测定荆芥药材中总六六六(α-bhc、β-bhc、γ-bhc、δ-bhc之和)、总滴滴涕(pp'-dde、pp'-ddd、op'-ddt、pp'-ddt之和)、五氯硝基苯。具体方法为《中华人民共和国药典》2015年版四部通则2341有机氯类农药残留量测定法—第一法。3.2.2结果对20个批次荆芥药材进行了总六六六(α-bhc、β-bhc、γ-bhc、δ-bhc之和)、总滴滴涕(pp'-dde、pp'-ddd、op'-ddt、pp'-ddt之和)、五氯硝基苯测定,测定结果见表9。表9荆芥药材农药残留量测定结果(ppm,mg/kg)4.荆芥药材浸出物测定4.1方法考察取荆芥药材4g,分别加溶剂(表中稀乙醇、体积分数为70%乙醇溶液和乙醇)100ml,振摇6小时,浸渍18小时,滤过,滤液吸取20ml,置已干燥至恒重的蒸发皿中,蒸干,置105℃下干燥3小时,称定重量。计算浸出物的含量(%),结果见表10。表10浸出物考察结果溶剂稀乙醇70%乙醇乙醇浸出物(%)8.0910.078.64从考察结果看,以70%乙醇提取效果最佳,故选择70%乙醇作为浸出物溶剂。4.2结果各批次荆芥药材浸出物测定结果见表11。表11荆芥药材浸出物测定结果5.荆芥药材含量测定5.1色谱条件的考察按照本发明实施例5中的方案进行操作,其中梯度洗脱程序分别选择按照表12~表15中的梯度洗脱方法洗脱,色谱图依次见图29~图32;根据结果可知,梯度洗脱方法4得到的色谱图橙皮苷峰形较好,纯度分析表明峰纯度良好,分离度为2.11,usp拖尾因子为1.02,对称因子为1.02,usp理论塔板数为14032。表12梯度洗脱方法1时间(min)甲醇5%醋酸水0~4530%70%表13梯度洗脱方法2时间(min)乙腈0.2%磷酸水0~1510%~14%90%~86%15~4014%~26%86%~74%40~5526%~60%74%~40%55~6060%~85%40%~15%60~6585%15%表14梯度洗脱方法3时间(min)乙腈0.2%磷酸水0~2820%80%28~2920%~85%80%~15%29~3985%15%表15梯度洗脱方法4时间(min)乙腈0.2%磷酸水0~2818%82%28~2918%~85%82%~15%29~3985%15%5.2提取方法的考察5.2.1提取溶剂的考察按照本发明实施例5中的方案进行操作,在供试品溶液的制备步骤中,分别选择加入下表中的提取溶剂25ml,回流处理30min,结果见下表。表16提取溶剂考察结果溶剂甲醇乙醇水含量(mg/g)0.9470.5730.700由表中数据可知,甲醇作为提取溶剂时提取率最高,明显优于乙醇和水,故选择提取溶剂为甲醇。5.2.2提取方式的考察按照本发明实施例5中的方案进行操作,在供试品溶液的制备步骤中,分别选择下表中的提取方式处理30min,结果见下表。表17提取方式考察结果提取方式超声回流浸渍过夜含量(mg/g)0.9471.2250.974由表中数据可知,回流提取提取率最高,明显优于超声提取与浸渍过夜,故选择提取方式为回流提取。5.2.3称样量的考察按照本发明实施例5中的方案进行操作,在供试品溶液的制备步骤中,分别选择下表中的称样量称取供试品,结果见下表。表18称样量考察结果称样量0.5g1g2g含量(mg/g)1.2991.2251.198由表中数据可知,称样量为0.5g时提取率最高,故选择称样量为0.5g。5.2.4提取时间的考察按照本发明实施例5中的方案进行操作,在供试品溶液的制备步骤中,分别回流30min、60min、120min,结果见下表。表19提取时间考察结果回流时间30min60min120min含量mg/g1.2991.2481.198由表中数据可知,提取时间为30min时提取率最高,故选择提取时间为30min。5.3方法学考察5.3.1线性关系考察称取橙皮苷对照品14.2mg(96.1%),置25ml量瓶中,加甲醇溶解,再加甲醇稀释至刻度,摇匀。精密吸取上述溶液5ml,置10ml量瓶中,加甲醇稀释至刻度,摇匀,即得272.924μg/ml的对照品溶液,依次逐级稀释,分别得到浓度为136.462μg/ml、68.231μg/ml、34.116μg/ml、17.058μg/ml、8.529μg/ml、4.264μg/ml、2.132μg/ml的对照品溶液。标准曲线绘制分别吸取上述浓度为68.231μg/ml、34.116μg/ml、17.058μg/ml、8.529μg/ml、4.264μg/ml、2.132μg/ml对照品溶液10μl,按照实施例7中的色谱条件和测定法测定,注入液相色谱仪,结果见表20。表20线性关系考察浓度(μg/ml)峰面积1峰面积2平均峰面积2.1324568947099463944.2649494694734948408.52919011018797218904117.058375568347321361444.534.11669668075534072601068.231154129514835021512399结果显示,橙皮苷线性回归方程为y=21954x,r=0.9997,在2.132μg/ml~68.231μg/ml范围内线性关系良好,所述回归方程的曲线图见图10所示,可用外标一点法进行计算。5.3.2精密度考察称取荆芥样品粉末(过二号筛)0.5g,按照本发明实施例5中的方案操作。连续进样6次,根据峰面积计算rsd值为0.47%,表明精密度良好。表21精密度考察5.3.3稳定性考察称取荆芥样品粉末(过二号筛)0.5g,按照本发明实施例5中的方案操作。分别在0,2,4,8,12,24小时进样,根据峰面积计算rsd值,考察供试品的稳定性。结果显示,供试品溶液中橙皮苷在24小时内基本稳定。表22稳定性考察5.3.4重复性考察称取荆芥样品粉末(过二号筛)0.5g共6份,按照本发明实施例5中的方案操作。进样,根据峰面积计算含量,结果显示,含量为1.30mg/g(0.130%),rsd值为1.98%,表明本方法重复性良好。表23重复性考察5.3.5准确度考察取荆芥粉末(过二号筛)0.25g,精密加入配置的545.848μg/ml的橙皮苷对照品溶液0.6ml,再精密加入甲醇24.4ml,密塞,称定重量,回流30min,放冷,加甲醇补足减失的重量,摇匀,取续滤液,即得供试品溶液,然后按照本发明实施例5中的方案操作。连续制样6份,进样,计算加样回收率。结果表明,本方法加样回收率良好。表24准确度考察5.3.6耐用性考察称取荆芥样品粉末(过二号筛)0.5g,按照本发明实施例5中的方案操作。以3根不同的色谱柱检测,计算含量及rsd值。结果表明,本方法耐用性良好。表25不同色谱柱测定样品含量色谱柱厂家watersagilentkromasilrsd(%)含量(mg/g)1.301.231.262.78本研究建立了高效液相色谱法测定荆芥中橙皮苷含量的检测方法。通过对流动相洗脱条件的考察,确定了最优色谱条件,并对方法学进行了全面考察;通过考察提取溶剂、提取方式、提取时间、称样量对荆芥中橙皮苷提取效果的影响,优化得到样品前处理条件。该方法简单,测定结果准确可靠、重复性好,实用性强,可用于对荆芥饮片的质量评价。6.荆芥药材非挥发性成分hplc特征图谱研究6.1.1波长的选择荆芥dad全波长扫描图谱见图33,由图可知,样品在283nm波长处的各色谱峰相对比较均衡,因此选择283nm为荆芥药材及饮片特征图谱的检测波长。6.1.2色谱条件的考察按照本发明实施例1的方案进行操作,其中梯度洗脱方法分别按照下表26-28中的梯度洗脱方法洗脱,色谱图依次见图34-36,根据结果可知,梯度洗脱方法3得到的色谱图各峰形、分离度良好,因此,选择该法作为特征图谱鉴别方法。表26梯度洗脱方法1时间(min)乙腈0.2%磷酸水0~2020%80%20~3025%75%30~5030%70%50~6050%50%60~7080%20%表27梯度洗脱方法2时间(min)乙腈0.05%三氟乙酸水0~405%~40%95%~60%40~6040%~60%60%~40%60~6560%~5%40%~95%65~905%95%表28梯度洗脱方法3时间(min)乙腈0.2%磷酸水0~1510%~14%90%~86%15~4014%~26%86%~74%40~5526%~60%74%~40%55~6060%~85%40%~15%60~6585%15%6.2方法学考察6.2.1精密度考察按照本发明实施例1中的方案操作,精密吸取同一荆芥供试品溶液,连续进样7次,以1号峰为参照峰(s),各特征峰相对保留时间的rsd<3.0%,相对峰面积的rsd<5.0%,表明仪器精密度良好。表29精密度相对保留时间计算结果s1s2s3s4s5s611.001.071.091.201.251.6421.001.071.091.211.251.6431.001.071.091.211.261.6441.001.071.091.211.261.6351.001.071.091.211.261.6361.001.071.091.211.261.6371.001.071.091.211.261.63rsd%0.000.250.170.190.100.18表30精密度相对峰面积计算结果s1s2s3s4s5s611.000.390.640.230.500.3921.000.390.640.230.500.3931.000.390.640.230.490.3841.000.390.640.230.490.3851.000.390.640.230.490.3861.000.380.620.220.530.3771.000.390.630.230.540.38rsd%0.001.100.931.673.361.686.2.2稳定性考察按照本发明实施例1中的方案操作,精密吸取同一荆芥供试品溶液,分别于供试品溶液制备后第0h,1h,3h,6h,9h,12h,24h进样,以1号峰为参照峰(s),各特征峰相对保留时间的rsd<3.0%,相对峰面积的rsd<6.0%,表明供试品溶液在制备后24h内稳定。表31稳定性相对保留时间计算结果s1s2s3s4s5s60h1.001.071.091.201.251.641h1.001.071.091.211.251.643h1.001.071.091.211.261.646h1.001.071.091.211.261.639h1.001.071.091.211.261.6312h1.001.081.101.211.261.6324h1.001.071.091.211.261.64rsd%0.000.310.220.240.130.24表32稳定性相对峰面积计算结果s1s2s3s4s5s60h1.000.390.640.230.500.391h1.000.390.640.230.500.393h1.000.390.640.230.490.386h1.000.390.640.230.490.389h1.000.390.630.230.540.3812h1.000.390.640.240.560.3824h1.000.400.650.220.520.39rsd%0.000.960.902.405.201.366.2.3重复性考察按照本发明实施例1中的方案操作,取同一批荆芥粉末约0.5g,平行6份,精密称定,分别进样,记录特征图谱,以1号峰为参照峰(s),各特征峰相对保留时间的rsd<3.0%,相对峰面积的rsd<6.0%,表明该方法的重复性良好。表33重复性相对保留时间计算结果表34重复性相对峰面积计算结果s1s2s3s4s5s611.000.390.640.230.500.3921.000.380.600.210.520.3531.000.380.630.230.520.3641.000.390.620.230.500.3951.000.380.610.200.480.3661.000.390.600.210.510.40rsd%0.001.192.265.933.085.196.2.4耐用性考察按照本发明实施例1中的方案操作,检测采用不同色谱柱下的色谱图,检查各峰分离度。waters柱、alchrombond-aq柱、phenomex-luna柱各峰分离度良好。表35不同色谱柱测定样品相对保留时间色谱柱厂家watersalchrombond-aqphenomex-lunas11.001.001.00s21.071.071.07s31.091.141.09s41.201.201.20s51.251.231.25s61.641.491.59表36不同色谱柱测定样品相对峰面积6.3特征图谱采集采用国家药典委员编制的《中药色谱指纹图谱相似度评价系统》(v2.0),对荆芥各批次样品的检测结果进行了分析。采用中位数法,时间窗参数为0.30,由软件生成对照特征图谱(r指纹图谱)。6.3.1特征峰标定按照本发明实施例1中的方案构建荆芥药材代表性供试品的特征图谱并进行分析,取每批供试品特征图谱中都出现的典型色谱峰作为特征峰。在283nm,共6个特征峰,1号峰为橙皮苷,2号峰为迷迭香酸,3号峰、4号峰、5号峰为共有特征峰,6号峰为胡薄荷酮,各色谱峰分别以1~6的序号表示。6.3.2各批次样品的测定及对照特征图谱的建立各批次样品的相对保留时间和相对峰面积见表37~表38,生成的对照特征图谱,见图37,各批次样品的特征图谱中应呈现6个特征峰,以s1、s2、s3、s4、s5、s6为标记。表37荆芥药材各批次6个特征峰相对保留时间编号s1s2s3s4s5s6j11.001.071.091.211.261.66j21.001.071.091.211.261.63j31.001.081.101.201.251.63j41.001.091.111.221.271.65j51.001.071.091.211.261.64j61.001.061.091.201.251.65j71.001.071.101.211.261.63j81.001.081.101.211.261.63表38荆芥药材各批次6个特征峰相对峰面积编号s1s2s3s4s5s6j11.000.410.250.640.460.42j21.000.260.180.180.260.19j31.002.710.620.020.020.42j41.000.600.010.050.030.62j51.004.820.850.401.641.22j61.000.750.210.170.380.23j71.000.700.180.270.770.16j81.001.250.250.230.470.267.荆芥药材挥发油gc特征图谱的研究7.1.1色谱条件选择按照本发明实施例4的方案操作,其中的柱温升温程序按照下表39~表43的升温程序;采用升温程序1-5得到的特征图谱如图38-42所示,结果表明,升温程序3得到的色谱图峰形较好,故选择升温程序3。表39升温程序1速率℃/min温度℃保持时间min——602312053130103160052300表40升温程序2表41升温程序3速率℃/min温度℃温度℃——602212053160052200表42升温程序4速率℃/min温度℃速率℃/min——6022140552100102200表43升温程序5速率(℃/min)温度(℃)温度(℃)——60221205517051022007.2方法学考察7.2.1精密度考察按照本发明实施例4中的方法操作,精密吸取同一荆芥供试品溶液,连续进样6次,以2号峰为参照峰(s),各特征峰相对保留时间的rsd<3.0%,相对峰面积的rsd<3.0%,表明仪器精密度良好。表44精密度相对保留时间计算结果表45精密度相对峰面积计算结果s1s2s311.051.000.0321.021.000.0331.051.000.0341.041.000.0351.051.000.0361.051.000.0371.031.000.03rsd%1.090.001.617.2.2稳定性考察按照本发明实施例4中的方法操作,精密吸取同一荆芥供试品溶液,分别于供试品溶液制备后第0h,1h,3h,6h,9h,12h,24h进样,以2号峰为参照峰(s),各特征峰相对保留时间的rsd<3.0%,相对峰面积的rsd<5.0%,表明供试品溶液在制备后24h内稳定。表46稳定性相对保留时间计算结果表47稳定性相对峰面积计算结果s1s2s30h1.051.000.031h1.021.000.033h1.041.000.036h1.031.000.039h1.041.000.0312h1.041.000.0324h1.071.000.03rsd%1.390.003.127.2.3重复性考察按照本发明实施例4中的方法操作,取同一批荆芥粉末,平行6份,分别进样,记录气相色谱图,以2号峰为参照峰(s),各特征峰相对保留时间的rsd<3.0%,相对峰面积的rsd<3.0%,表明该方法的重复性良好。表48重复性相对保留时间计算结果s1s2s310.671.001.5120.671.001.5130.671.001.5140.671.001.5150.671.001.5060.671.001.50rsd%0.080.000.10表49重复性相对峰面积计算结果s1s2s311.041.000.0321.041.000.0331.041.000.0341.041.000.0351.061.000.0361.041.000.03rsd%0.880.002.657.3特征图谱采集采用国家药典委员编制的《中药色谱指纹图谱相似度评价系统》(v2.0),对荆芥各批次气相图谱的检测结果进行了分析。采用中位数法,时间窗参数为0.30,由软件生成对照特征图谱(r指纹图谱)。7.3.1特征峰标定按照本发明实施例4中的方案构建荆芥药材代表性供试品的特征图谱并进行分析,取每批供试品特征图谱中都出现的典型色谱峰作为特征峰。共3个特征峰,共有特征峰为:1号峰为薄荷酮,2号峰为胡薄荷酮,3号峰,各色谱峰分别以1~3的序号表示。7.3.2各批次样品的测定及对照特征图谱的建立各批次样品的相对保留时间和相对峰面积见表50~表51,生成的对照特征图谱见图43,各批次样品的特征图谱中应呈现3个特征峰,以s1、s2、s3为标记。表50荆芥药材各批次3个特征峰相对保留时间表51荆芥药材各批次3个特征峰相对峰面积编号s1s2s3j10.441.000.05j20.201.000.04j30.591.000.02j40.711.000.03j50.271.000.02j60.391.000.01j70.201.000.02j80.461.000.01显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1