评估和预测有机磷酸酯阻燃剂对模拟生物膜损伤的方法与流程
本发明属于面向生态风险评价的测试策略和海洋监测领域,具体涉及一种评估和预测有机磷酸酯阻燃剂对模拟生物膜损伤的方法。
背景技术
随着海洋资源的开发,海洋污染日益严重。某些新兴污染物质在海洋以及海洋生物体内被陆续检出。由于污染物质环境浓度较低,目前不足以引起明显的生物效应。但由于污染物自身的持久性和生物积累性,使得化合物存在巨大的环境风险。其中,有机磷酸酯阻燃剂(opfrs)作为典型的新兴污染物质,其在海洋水体及生物(青鱼,鲈鱼,贝类)脂肪中有明显检出。目前关于opfrs环境暴露监测的报道日益增多,其生态环境风险引起了广泛关注。由于opfrs本身结构复杂,作用机制多样,描述每一种opfrs对海洋生物的影响需要消耗大量的人力和物力,所以发明一种便捷准确的方法评估opfrs的生态风险是极为必要的。
作为溴代阻燃剂(bfrs)的主要替代材料,opfrs凭借其优良的阻燃和增塑特性,其生产和使用量逐渐增加,成为新兴的环境污染物质。由于opfrs不与主体聚合物材料化学键合,从而更易通过挥发,浸出或磨损等方式扩散到环境介质中,导致大量opfrs在环境中普遍存在。研究表明,opfrs对神经系统和免疫系统具有毒性作用,磷酸三(1,3-二氯异丙基)酯(tdcpp)通过抑制pc12细胞的dna合成,减少细胞数量并改变神经分化从而引起神经发育毒性;tdcpp通过改变斑马鱼胚胎/幼虫中下丘脑-垂体-甲状腺(hpt)轴的mrna表达进而改变全身甲状腺激素浓度。
生物膜作为生物体抵御外界的第一道屏障,膜系统的完整性对于细胞正常的生命活动来说至关重要。有研究表明,在200倍相差显微镜下观察到高浓度的磷酸三丁酯(tbp)和三(2-丁氧基乙基)磷酸酯(tbep)暴露会造成细胞畸形,破坏膜结构。在海洋生物脂肪内检出的高浓度opfrs可能会对生物体产生毒性作用。opfrs是否通过破坏细胞膜或者其他方式与膜相互作用,进而产生毒性作用是个亟待解决的问题。
生物膜复杂的结构和功能不利于研究膜与物质间的相互作用,构建模拟生物膜系统是研究生物膜的基础和前提。生物膜系统包括双层类脂膜、自组装单分子层膜、固体支撑双分子层类脂膜等,其中固体支撑双分子层类脂膜相较于传统的类酯膜,具有良好的电化学特性和稳定性,适合用于研究膜与化合物之间的相互作用。
采用电化学技术能够表征模拟生物膜的结构变化。目前使用的电化学技术主要包括循环伏安法(cv)和电化学交流阻抗法(eis)。其中eis是通过输入小振幅的电信号扰动体系产生相应的输出信号,进而线性拟合得到频响函数。在一系列不同的频率下测得的一组频响函数值形成电化学阻抗谱,能够用于探测膜结构的变化。
qsar模型在化合物毒性机理解释和预测方面的应用日益广泛。模型通过研究化合物的分子结构信息如结构编码、拓扑学参数、量子化学参数、理化性质参数等分析化合物的环境行为和毒理作用。
目前,opfrs与生物膜间的相互作用研究多基于实验测试,例如通过荧光探针和电镜等实验手段研究opfrs对膜的影响。但是测定多种具有不同取代基的opfrs需要消耗大量的人力和物力。急需发明一种简便快捷的评估opfrs对模拟生物膜损伤的方法,用于评估opfrs的生态风险。
技术实现要素:
针对上述技术问题,本发明提供一种方便、高效、省时省力的方法评估和预测opfrs对模拟生物膜的损伤,为opfrs的海洋监测和生态风险评估提供基础理论数据。
本发明采用的技术方案是:评估和预测有机磷酸酯阻燃剂对模拟生物膜损伤的方法,根据opfrs对模拟生物膜作用的阻抗值构建qsar模型;根据软件计算表征待测opfrs的分子结构的分子描述符,通过qsar模型进行opfrs对模拟生物膜损伤的评估和预测。
所述opfrs对模拟生物膜作用的阻抗值通过电化学交流阻抗法测定。
所述模拟生物膜为磷脂双分子层生物膜。
所述opfrs为16种,包括8个苯环取代的opfrs、2个氯取代的opfrs、5个含烷基取代的opfrs和1个烷氧基取代的opfrs。
所述qsar模型如下:
logy=-1.82×dls_04-4.35×10-2cats2d_05_pl+1.22×10-1mor04v
-9.33×10-3rdf080m-4.80×10-1gats6m+3.00×10-1gats7p
+1.70
其中,logy为opfrs对模拟生物膜作用的阻抗值的对数,dls_04、cats2d_05_pl、mor04v、rdf080m、gats6m、gats7p为分子描述符;dls_04表示类药性指数,rdf080m表示原子质量加权的径向分布函数,gats6m、gats7p分别为表示质量加权、极化率加权的geary自相关指数,cats2d_05_pl表示分子亲油亲脂特性,mor04v表示基于原子范德华体积加权的三维分子结构。
所述分子描述符dls_04、cats2d_05_pl、mor04v、rdf080m、gats6m、gats7p通过以下步骤得到:
对opfrs的分子结构进行优化,利用dragon软件计算分子结构描述符,通过逐步回归得到9个描述符;
1)首先,建立包含9个变量的偏最小二乘模型,得到对应的因变量方差比例q2cum;
2)随后,将每个描述符依次从偏最小二乘模型中剔除,得到一系列包含8个描述符的偏最小二乘模型和相对应的q2cum,比较q2cum值与阈值的大小,q2cum值越大,模型的性能越好;
3)随后在步骤2)所得的一系列偏最小二乘模型,选择q2cum大于设定值的某个模型,继续剔除一个变量即描述符,得到新的偏最小二乘方程和q2cum,返回步骤3),遍历所有的8个偏最小二乘模型;
4)对于每个新的偏最小二乘方程,依次剔除不同的变量,得到一系列偏最小二乘方程和q2cum值,比较每个偏最小二乘方程对应的q2cum值,选择最大的q2cum所对应的dls_04、cats2d_05_pl、mor04v、rdf080m、gats6m、gats7p6个描述符构建qsar模型,用于解释作用机制。
所述根据软件计算表征待测opfrs的分子结构的分子描述符通过qsar模型进行opfrs对模拟生物膜损伤的评估和预测包括以下步骤:
将待测opfrs的分子结构进行优化,利用dragon软件得到待测opfrs的分子描述符:dls_04、cats2d_05_pl、mor04v、rdf080m、gats6m、gats7p;
将分子描述符代入qsar模型,得到待测opfrs对模拟生物膜作用的阻抗值的对数logy;
根据logy和分子描述符评估和预测opfrs对模拟生物膜的损伤。
所述根据logy和分子描述符评估和预测opfrs对模拟生物膜的损伤具体为:
阻抗值的大小代表电解液中的铁氰化钾分子探针到达金电极表面时受到的阻力大小;logy值越小,分子探针到达金电极表面时受到的阻力越小,化合物越容易侵入细胞膜内层,破坏生物膜的完整性,使得其他化合物更易进入膜造成机体损伤;logy值越大,分子探针到达金电极表面时受到的阻力越大,更容易与膜上的生物大分子发生较强的偶极-诱导偶极作用,与受体蛋白产生相互作用,干扰膜上的信号传递及相关通路。
所述根据对数和分子描述符评估和预测opfrs对模拟生物膜的损伤具体如下:
首先,dls_04和gats7p是影响opfrs与膜相互作用的关键因素:
dls_04值越大,分子中所含的取代官能团的空间结构和位阻越小,测定的膜修饰的电极阻抗值越小,化合物越容易与生物体系发生相互作用,侵入细胞膜内层,破坏生物膜的完整性,使得其他化合物更易进入膜造成机体损伤;
gats7p值越大,原子极化能力越强,其获得偶极的能力也越强,测定的膜修饰的电极阻抗值越大,更容易与膜上的生物大分子发生较强的偶极-诱导偶极作用,从而在膜上聚集;分子中含有卤素取代和烷氧基取代的官能团的电负性越强,越容易与受体蛋白产生相互作用,干扰膜上的信号传递及相关通路;
其次,cats2d_05_pl,原子的三维排布与空间结构也影响opfrs与生物膜的相互作用。
所述待测opfrs包括烷基磷酸酯、烷氧基磷酸酯、卤代烷基磷酸酯和芳基磷酸酯中的一种。
本发明的有益效果及优点如下:
本发明通过构建qsar模型研究opfrs对膜损伤的微观机制,为opfrs的生态风险评估提供基础数据。本发明构建的qsar模型能够准确便捷的评价应用域内opfrs对模拟生物膜的损伤,模型的应用域包括烷基磷酸酯、烷氧基磷酸酯、卤代烷基磷酸酯和芳基磷酸酯等4类不同取代基的16种opfrs。建立的qsar模型简便快捷、操作方便、应用域广,能够节省实验测试所需要的大量人力物力,为opfrs的风险评价和海洋监测提供基础数据。
本发明的方法仅需要计算表征化合物结构的描述符,通过qsar模型即可简捷准确地判断其对模拟生物膜的损伤。
附图说明
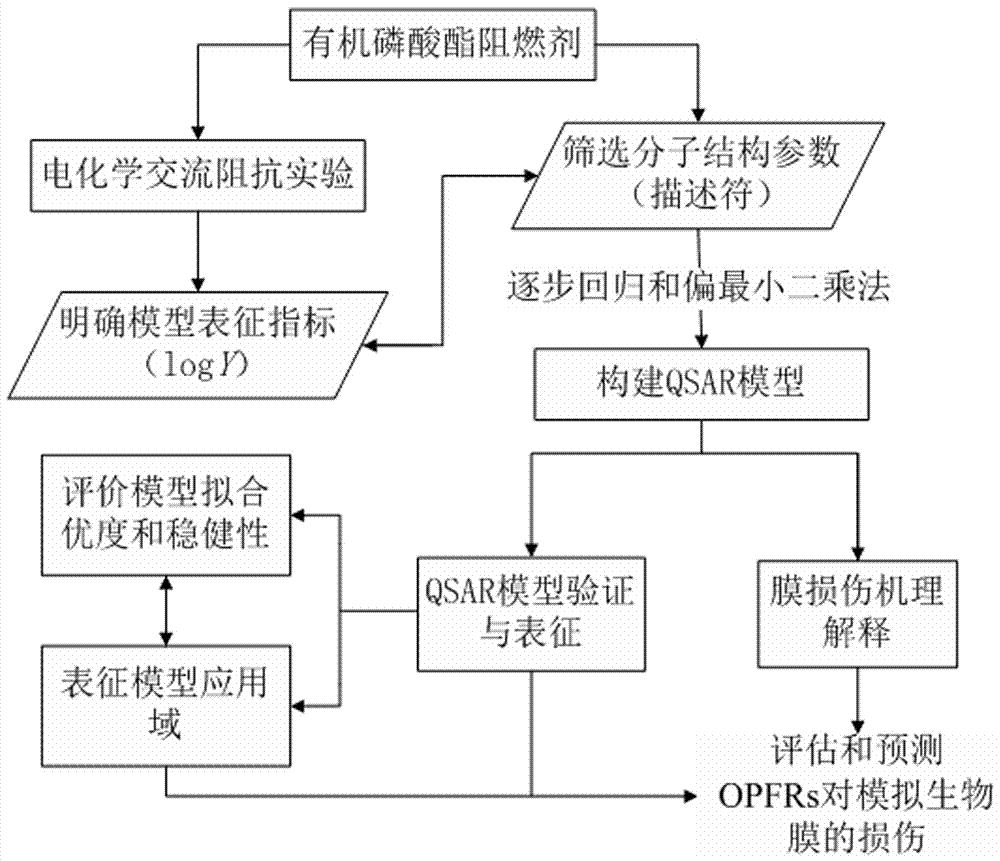
图1为本发明的流程图;
图2为拟合交流阻抗谱数据的等效电路图;
图3为logy的实测值与预测值的拟合图;
图4为表征应用域的欧几里得距离图;
图5为表征应用域的williams图。
具体实施方式
结合附图和实施例对本发明做进一步的详细说明。
本发明通过电化学交流阻抗法测定了16种典型opfrs作用下的膜修饰电极的阻抗值。采用逐步回归和偏最小二乘法(pls)建立了qsar模型,阐明了opfrs对膜损伤的微观作用机制,评估和预测应用域内opfrs对模拟生物膜的损伤,为opfrs的海洋监测和生态风险评估提供基础理论数据。
构建qsar模型评估和预测opfrs对膜的损伤。
所述模拟生物膜模型是通过“冰冻-涂抹”法在金电极表面构建的磷脂双分子层生物膜。首先,2-二棕榈酰甘油-3-磷酸巯基乙醇(dppte)分子与处理后的金电极通过“au-s”共价键形成单层膜;随后采用“涂抹-冻结”法在单层膜表面添加dppc层构建出磷脂双分子层膜。采用电化学交流阻抗法测定不同opfrs作用下的膜修饰电极阻抗值。
对研究的16种opfrs进行结构优化,将优化后的结构导入dragon软件,计算得到表征分子结构的4885个描述符,通过逐步回归法选取描述符,利用偏最小二乘法建立qsar模型。
所述qsar模型为:
logy=-1.82×dls_04-4.35×10-2cats2d_05_pl+1.22×10-1mor04v
-9.33×10-3rdf080m-4.80×10-1gats6m+3.00×10-1gats7p
+1.70
n=16,r2adj=0.881,f=119.45,se=0.114,p<0.001(95%置信区间),
r2x=0.735,r2y=0.905,q2cum=0.778,rmse=0.110
在qsar模型中,化合物的类药性指数(dls_04)和极化能力(gats7p)是影响opfrs与膜相互作用的关键因素。dls_04值越大,分子中所含的取代官能团的空间结构和位阻越小,测定的膜修饰的电极阻抗值(logy)越大,化合物越容易与生物体系发生相互作用,侵入细胞膜内层,破坏生物膜的完整性,使得其他化合物更易进入膜造成机体损伤。gats7p值越大,原子极化能力越强,其获得偶极的能力也越强,测定的膜修饰的电极阻抗值(logy)越小,更容易与膜上的生物大分子发生较强的偶极-诱导偶极作用,从而在膜上聚集。分子中含有卤素取代和烷氧基取代的官能团的电负性越强,越容易与受体蛋白产生相互作用,干扰膜上的信号传递及相关通路。其次,化合物的亲油亲脂性,原子的三维排布与空间结构也会影响opfrs与膜的相互作用。
该发明通过计算16种opfrs化合物分子结构参数,建立关于结构参数和阻抗值的qsar模型,用于分析opfrs对膜修饰电极损伤的作用机理,为opfrs生态风险评价和管理提供参考数据。如图1所示,包括如下步骤:
(1)金电极表面支撑磷脂双层膜的构建
将金电极用3000目砂纸打磨,然后用麂皮(氧化铝粉末和水)抛光金电极,将抛光后的金电极用无水乙醇和超纯水中清洗,将清洗后的电极置于现配的混合溶液(浓硫酸-过氧化氢体积比为3:1)中浸泡3min,以除去电极表面杂质。取出电极用超纯水冲洗,将冲洗后的电极连接到电化学工作站,使用0.1mol/l的硫酸溶液作为电解液,通过循环伏安法(cv)进行电位扫描,以进一步去除电极表面的杂质。电位区间0~1.6v,扫描速度100mv/s,扫描20周,扫描完成后使用超纯水清洗,吹干备用。
将dppte粉末溶解于无水乙醇中,配制成2mmol/ldppte溶液。将dppc粉末溶解于正癸烷中,制成浓度为20mg/ml的dppc正癸烷溶液。向1.5mlep中加入0.5mldppte无水乙醇溶液,将上述备用的金电极浸入dppte溶液16h,dppte分子通过头部的巯基与金共价结合形成“au-s”键,在裸金电极表面自组装形成单层膜。电极取出后,用无水乙醇清洗2min,以除去电极表面非共价结合的dppte分子,之后用超纯水清洗,吹干后,向其表面滴加10μl配制好的dppc溶液,先置于室温下约10min后,再在−20oc冰箱放置约30min,使正癸烷溶剂挥发。溶剂挥发后将电极取出,在室温下放置约15min,待溶剂完全挥发后,将金电极置于0.1mol/lkcl溶液中浸泡2h,,dppc分子在亲水和疏水作用力的共同作用下在dppte单层膜表面自发形成第二层磷脂膜,作为实验研究所用的模拟生物膜。
(2)电化学实验
电化学交流阻抗法,作为一种电化学检测技术,能够精准表征磷脂双层膜,能探测膜结构变化。本实验采用chi760d电化学工作站,通过三电极系统对模拟生物膜进行电化学检测。电解液为0.1mol/l氯化钾、0.1mol/lpbs和5mmol/l铁氰化钾或亚铁氰化钾(ph=6.8)。以双层膜修饰的金电极为工作电极,饱和甘汞电极为参比电极,铂电极为辅助电极。扫描频率范围为0.01hz~100khz,信号振幅为5mv,测定交流阻抗数据,使用电化学工作站自带软件绘制电化学阻抗谱图,如图2所示,将eis的实验结果通过zview3.1软件绘制模拟等效电路图进行数据拟合。rs表示电解液电阻,rm表示磷脂双层膜电阻,qm表示常相位元件。
(3)数据集的构建
通过chemdrawultra绘制16种典型opfrs(表1)的二维分子结构,之后使用chem3dultra软件的最小能量法(最小rms梯度为0.001)对模型化合物的分子结构进行初步优化,得到能量最低构型。将结果文件输入dragon软件(https://chm.kode-solutions.net/products_dragon.php),计算表征化合物原子类型、拓扑和几何参数、三维排布和结构、类药性指数等特征29类4885个分子描述符。表1为16种典型opfrs基本信息及结构分布表。
表1
(4)qsar模型的构建
以16种典型的opfrs作用下双层膜修饰的金电极的阻抗值logy作为qsar模型的因变量。将初始的4885个分子描述符通过逐步回归分析进行初筛,得到9个描述符,分别是dls_04、cats2d_05_pl、mor04v、rdf080m、gats6m、gats7p、sph、mats8v、rdf065e。采用simca软件中偏最小二乘(pls)回归建立模型。采用leave-group-out交叉验证确定pls成分,首先,建立包含9个变量的pls模型,软件计算得到对应的因变量方差比例q2cum,随后将每个描述符依次从模型中剔除依次,得到一系列包含8个描述符的新模型和相对应的q2cum,随后重复上述操作过程,每次剔除一个变量,得到相应的偏最小二乘方程和q2cum,比较每个模型对应的q2cum值,选择最大的q2cum所对应的dls_04、cats2d_05_pl、mor04v、rdf080m、gats6m、gats7p6个描述符构建qsar模型,用于解释作用机制的qsar模型。q2cum值越大,模型的性能越好,一般认为q2cum≥0.5,模型有很好的显著性和预测能力;筛选得到qsar模型中描述符基本信息如表2。
表2
adls_04陈等人修改的类药性结构指数
bcats2d_05_pl描述化合物亲油亲脂性
cmor04v表示信号04基于原子范德华体积加权的三维分子结构
drdf080m表示由原子质量加权的径向分布函数
egats6m表示由原子质量加权的geary自相关
fgats7p表示由原子极化率加权的geary自相关
qsar模型的表达式为:
logy=-1.82×dls_04-4.35×10-2cats2d_05_pl+1.22×10-1mor04v
-9.33×10-3rdf080m-4.80×10-1gats6m+3.00×10-1gats7p
+1.70
n=16,r2adj=0.881,r2x=0.735,r2y=0.905,q2cum=0.719,rmse=0.110
在模型中,logy表示为6个描述符变量的函数,训练集数据n=16。模型检验的统计量f=119.45,标准误差se=0.114,显著性水平p<0.001(95%置信区间),复决定系数r2adj=0.881,复相关系数平方r2x=0.735,复相关系数平方r2y=0.905,均方差误差rmse=0.110表明模型有很好的拟合优度,交叉验证系数q2cum=0.719表明模型有很好的稳健性,模型的r2y和q2cum之差小于0.3表明模型没有过拟合。表3表示,16种典型的opfrs的logy的实测值和预测值,图3表示,16种典型的opfrs的logy的实测值和预测值的拟合结果。采用训练集/验证集拆分法检验模型的稳健性,内部交叉验证系数q2in=0.778,说明模型有很好的稳健性。各变量间的诊断因子方差膨胀因子vif<10,容差tolerance>0.1,状态指数conditionindex<30,说明各自变量之间独立不存在严重的多重共线性。表3为16种典型的opfrs的logy的实测值和预测值。
表3
qsar模型中,logy为双层膜修饰的金电极相对阻抗值,dls_04描述化合物类药性指数,这个指标考虑了一系列的性质,包括分子形成氢键时,氢键供体和受体的数量,亲脂性以及不饱和指数等;cats2d_05_pl描述化合物亲油亲脂性质;mor04v描述通过使用不同的角散射函数来计算所有原子范德华体积的总和,表示原子的三维排列对分子大小和形状的影响;rdf080m描述由原子质量加权的径向分布函数,用于表示特定的三维空间结构中的特定信息;gats6m描述由质量加权的2d自相关函数,用于表示特定的分子结构,自相关性越强则gats6m值越小;gats7p描述相同拓扑距离的原子极化能力。
如表4,根据描述符投影重要性指标(vip)值分析表明,化合物的类药性指数(dls_04)和极化能力(gats7p)是影响opfrs与膜作用的关键因素。dls_04值越大,分子中所含的取代官能团的空间结构和位阻越小,化合物越容易与生物体系发生相互作用,侵入细胞膜内层,破坏生物膜的完整性,使得其他化合物更易进入膜造成机体损伤。gats7p值越大,原子极化能力越强,其获得偶极的能力也越强,更容易与膜上的生物大分子发生较强的偶极-诱导偶极作用,从而在膜上聚集。分子中含有卤素取代和烷氧基取代的官能团的电负性越强,越容易与受体蛋白产生相互作用,干扰膜上的信号传递及相关通路。此外,化合的亲油亲脂性,原子的三维排布与空间结构也会影响opfrs与膜的相互作用。表4为qsar模型中描述符投影重要性指标(vip)值。
表4
(5)qsar模型应用域表征
qsar模型的应用域通过欧几里得距离图和williams图进行表征,如图4,欧几里得距离图通过ambitdiscoveryv0.04软件绘制,欧几里得距离小于1.29,训练集的化合物都在模型应用域中,说明模型的训练集具有良好的代表性。如图5,williams图化合物的标准残差都在(-2.5,2.5)以内,化合物的杠杆值均小于警戒值1.31,说明模型没有离群点。通过表征应用域,未发现离群点和误估点,确保模型分析结果可信。
本发明所构建的opfrs数据集中,包括8个苯环取代的opfrs、2个氯取代的opfrs、5个含烷基取代的opfrs和1个烷氧基取代的opfrs。
实施例1
磷酸三(2-乙基己基)酯(tehp):采用williams图法计算得到其杠杆值hi为0.521<h*(预警值)=1.31,标准残差(se)=1.40<2.50,说明此化合物在qsar模型应用域内。实验测定的tehp阻抗值为为0.673相较于同为烷基取代的磷酸三丁酯(tbp)的-阻抗值0.626明显增加,根据qsar模型进行机理分析,tehp由于空间结构较大的支链取代基,使得表征原子空间排布和三维结构的描述符mor04v的数值从0.147增加到1.95,类药性指数从0.80减小到0.30,表征原子极化率的gats7p从0.557增加到1.10,从而使得化合物更易于插入或附着在膜外表面,使膜的电极阻抗值增加,干扰膜上的信号传递及相关通路。
实施例2
磷酸三(2-氯乙基)酯(tcep):采用williams图法计算得到其杠杆值hi为0.218<h*(预警值)=1.31,标准残差(se)=-0.484>-2.50,说明此化合物在qsar模型应用域内。tbp的碳链末端的烷基取代变成卤素(cl)取代,实验测定的卤素(cl)取代的tcep阻抗值为为0.0173相较于烷基取代的磷酸三丁酯(tbp)的阻抗值0.626明显增加,根据qsar模型进行机理分析,tcep由于含有卤素取代官能团,导致化合物电负性增强,使得类药性指数从3减小到0,表征原子极化率的gats7p从0.557增加到0.674,易于与受体蛋白分子产生作用力插入或附着在膜外表面,从而增加膜修饰的电极阻抗值,干扰膜上的信号传递及相关通路。
实施例3
三甲苯磷酸酯(tmtp):采用williams图法计算得到其杠杆值hi为0.678<h*(预警值)=1.31,标准残差(se)=-0.911>-2.50,说明此化合物在qsar模型应用域内。实验测定的tmtp阻抗值为为-0.406相较于同为芳环取代的三对甲苯磷酸酯(tptp)的阻抗值0.577明显增加,根据qsar模型进行机理分析,芳环取代和tmtp,由于苯环上的甲基的取代位置由对位到间位,使得化合物的空间位阻减少,表征原子空间排布和三维结构的描述符mor04v的数值从0.797减少到-0.257,表征原子极化率的gats7p从1.87减少到0.431,表征脂溶性cats2d_05_pl从3增加到6,使膜的电极阻抗值降低,化合物更易侵入膜的内层,改变膜结构,破坏膜的完整性。
- 还没有人留言评论。精彩留言会获得点赞!