用于钠离子蓄电池的阳极组合物及其制备方法与流程
本公开涉及可作为用于钠离子蓄电池的阳极的组合物及用于制备和使用其的方法。
背景技术:
已经引入各种阳极组合物以用于在二次钠离子蓄电池中使用。此类组合物在例如下列文献中有所描述:Jiang Wei Wang et,al,“Microstructural Evolution of Tin Nanoparticles during In Situ Sodium Insertion and Extraction”,Nano Letters(Jiang Wei Wang等人,“在原位插入和提取钠的过程中锡纳米颗粒的微结构演变”,《纳米快报》);Yunhua Xu et.Al,“Electrochemical Performance of Porous Carbon/Tin Composite Anodes for Sodium-Ion and Lithium-Ion Batteries”,Advanced Energy Materials(Yunhua Xu等人,“用于钠离子蓄电池和锂离子蓄电池的多孔碳/锡复合阳极的电化学性能”,《先进能源材料》);Lifen Xiao et.al,“High capacity,reversible alloying reactions in SnSb/C nanocomposites for Na-ion battery applications”,Chem.Comm.48(2012)3321(Lifen Xiao等人,“用于Na离子蓄电池应用的SnSb/C纳米复合物的高容量可逆合金化反应”,《化学通讯》,48(2012)3321);美国专利申请公布2012/0199785;Tuan T.Tran et.al,“Alloy Negative Electrodes for High Energy Density Metal-Ion Cells”,J.Electrochem.Soc.158(2011)A1411(Tuan T.Tran等人,“用于高能量密度金属离子电池的合金负极电极”,《电化学会志》,158(2011)A1411);V.L.Chevrier et al.,“Challenges for Na-ion Negative Electrodes”,J.Electrochem.Soc.158(2011)A1011(V.L.Chevrier等人,“钠离子负极所面临的挑战”,《电化学会志》,158(2011)A1011);以及Shanmugan et al.,“Na2/3Ni1/3Ti2/3O2:“Bi-Functional”Electrode Materials for Na-Ion Batteries”,Electrochem.Lett.,3(2014)A23(Shanmugan等人,“Na2/3Ni1/3Ti2/3O2:用于Na离子蓄电池的“双功能”电极材料”,《电化学杂志》,3(2014)A23)。
技术实现要素:
在一些实施方案中,提供了钠离子蓄电池。该钠离子蓄电池具有包含钠的阴极;和包含具有下式的材料的阳极组合物:
AaBbCcDdO, (I)
其中A为碱金属、碱土金属或它们的组合,其中B为钛,C为钒,D为除钛或钒之外的一种或多种过渡金属元素,a+b+c+d≤1,a≥0,b+c>0,b≥0,c≥0,d>0,并且其中该材料具有钛铁矿结构、VFeO4三斜晶结构、Ca5Co4(VO4)6立方结构、重铬酸盐结构、斜方晶结构、钛铀矿结构、钪钇石结构、斜方晶结构或伪金红石结构。
在一些实施方案中,提供了钠离子蓄电池。该钠离子蓄电池具有包含钠的阴极;和包含具有下式的材料的阳极组合物:
A’eB’fC’gO, (II)
其中A’为碱金属、碱土金属或它们的组合,其中B’为钛,C’为钒,e+f+g≤1,e≥0,f>0,并且g>0。
在一些实施方案中,提供了制备钠离子蓄电池的方法。该方法包括提供包含钠的阴极和阳极。阳极包含钒、钛或它们的组合,以及任选的碱金属或碱土金属以及任选的除钛或钒之外的过渡金属。该方法还包括将阴极和阳极引入到包含电解质的蓄电池中,其中该电解质包含钠。
在一些实施方案中,提供了钠离子蓄电池。该钠离子蓄电池具有包含钠的阴极;和包含选自以下的一种或多种材料的阳极组合物:CoTiO3、Ca5Co4(VO4)6、CoV3O8、NiTiO3、Co2V2O7或MnV2O6。
本公开的上述发明内容并非旨在描述本发明的每个实施方案。本公开的一个或多个实施方案的细节也阐述于以下具体实施方式中。根据本说明书和权利要求书,本发明的其他特征、对象和优点将显而易见。
附图说明
结合附图来考虑本公开的各种实施方案的以下详细描述可更完全地理解本公开,其中:
图1示出具有铁板钛矿结构的Fe2TiO5材料的XRD图;
图2示出图1的Fe2TiO5材料的电压容量曲线;
图3示出具有钛铁矿结构的NiTiO3材料的XRD图。
图4示出图3的NiTiO3材料的电压容量曲线。
图5A示出实施例2的实验XRD图,并且CoTiO3的已知峰位置用菱形表示(粉末衍射文件(PDF)#00-15-0866);并且图5B示出用实施例2的材料制备的电池的对应电压曲线。
图6A示出实施例3的实验XRD图,并且VFeO4的已知峰位置用菱形表示(PDF#00-38-1372);并且图6B示出用实施例3的材料制备的电池的对应电压曲线。
图7A示出实施例4的实验XRD图,并且Ca5Co4(VO4)6的已知峰位置用菱形表示(PDF#00-052-1884);并且图7B示出用实施例4的材料制备的电池的对应电压曲线。
图8A示出实施例5的实验XRD图,并且Co2V2O7的已知峰位置用菱形表示(PDF#00-038-0193);并且图8B示出用实施例5的材料制备的电池的对应电压曲线。
图9A示出实施例6的实验XRD图,并且CoV3O8的已知峰位置用菱形表示(PDF#00-022-0598);并且图9B示出用实施例6的材料制备的电池的对应电压曲线。
图10A示出实施例7的实验XRD图,并且MnV2O6的已知峰位置用菱形表示(PDF#00-35-0139);并且图10B示出用实施例7的材料制备的电池的对应电压曲线。
图11A示出实施例8的实验XRD图,并且Mn2V2O7的已知峰位置用菱形表示(PDF#00-073-1806);并且图11B示出用实施例8的材料制备的电池的对应电压曲线。
图12A示出实施例9的实验XRD图,并且MnTiO3的已知峰位置用菱形表示(PDF#00-089-3742);并且图12B示出用实施例9的材料制备的电池的对应电压曲线。
图13A示出实施例10的实验XRD图,并且CrVO4的已知峰位置用菱形表示(PDF#00-038-1376);并且图13B示出用实施例10的材料制备的电池的对应电压曲线。
图14A示出实施例11的实验XRD图,并且TiVO4的已知峰位置用菱形表示(PDF#00-077-0332);并且图14B示出用实施例11的材料制备的电池的对应电压曲线。
具体实施方式
钠离子蓄电池作为用于例如电动汽车或固定网格存储应用中的低成本、高能量密度的化学蓄电池受到关注。已经提出将硬碳作为合适的负极材料以用于钠离子蓄电池中。然而,硬碳具有仅约450Ah/L的体积容量,或小于锂离子电池中石墨体积容量的约2/3。
已证明钠可在低电压下插入金属氧化物诸如CuO中。然而,此类金属氧化物通常发生下列类型的置换(或转化)反应:
2Na+CuO→Cu+Na2O
虽然这些反应是可逆的,但引入此类金属氧化物作为活性阳极材料的电极具有低效率和短循环寿命。
同样已证明钠可在低电压下插入钛酸盐(例如,Na2Ti3O7)中。这种材料中的钠化机理是通过可逆的嵌入机理。然而,Na2Ti3O7为白色绝缘粉末,这是钛酸盐的典型特征。此类材料不在电极中起作用,除非磨成小尺寸并与大量含碳材料(例如炭黑)混合。因此,认为由这类材料制成的电极具有低体积容量。因此,期望的是在钠离子蓄电池中使用的不与上述缺陷相关联的负极材料。
出乎意料的是,现已发现,某些过渡金属钛酸盐和钒氧化物在低电压下可用作钠离子蓄电池的有效负极,而无需大量的含碳材料。具体地讲,据发现,某些过渡金属钛酸盐和钒氧化物通过高度可逆的反应钠化。
定义
在本文件中:
术语“钠化”和“钠化反应”是指用于将钠添加到电极材料的过程;
术语“脱钠化”和“脱钠化反应”是指用于从电极材料去除钠的过程;
术语“充电”和“进行充电”是指用于为电池提供电化学能量的过程;
术语“放电”和“进行放电”是指用于从电池去除电化学能量的过程,例如在使用电池以进行所需的工作时;
术语“阴极”是指在放电过程中发生电化学还原和钠化反应的电极(通常称为正极);
术语“阳极”是指在放电过程中发生电化学氧化和脱钠反应的电极(通常称为负极);
术语“合金”是指包括金属、准金属、半金属中的任一种或全部的材料;并且
术语“粉末”是指以颗粒形式存在的包括多个颗粒的材料,其中颗粒的平均尺寸小于200微米。
如本文所用,PDF#可参考2002发行的国际衍射数据中心PDF-2加以理解。
如本文所用,单数形式“一个”、“一种”、和“所述”包括复数指代,除非所述内容清楚地表示其他含义。在本说明书和所附实施方案中所用的术语“或”通常以其包括“和/或”的含义使用,除非所述内容清楚地表示其他含义。
如本文所用,通过端点表述的数值范围包括此范围内所含的所有数值(例如1至5包括1、1.5、2、2.75、3、3.8、4和5)。
除非另外指明,否则说明书和实施方案中所用的表达数量或成分、性质量度等的所有数值在所有情况下均应理解成被术语“约”修饰。因此,除非有相反的说明,否则前述说明书和所附实施方案列表中阐述的数值参数可根据本领域技术人员使用本公开的教导内容寻求获得的所需性质而变化。在最低程度上且不试图将等同原则的应用限制到受权利要求书保护的实施方案的范围的前提下,至少应当根据所报告的数值的有效数位并通过应用普通四舍五入法来解释每个数值参数。
在一些实施方案中,本公开涉及用于钠离子蓄电池的阳极组合物。阳极组合物可包含具有下式的材料:
AaBbCcDdO, (I)
其中A为碱金属、碱土金属或它们的组合,其中B为钛,C为钒,且D为除钛或钒之外的一种或多种过渡金属元素,O为氧,a+b+c+d≤1,a≥0,b+c>0,b≥0,c≥0,d>0,并且其中该材料具有钛铁矿结构、VFeO4三斜晶结构、Ca5Co4(VO4)6立方结构、重铬酸盐结构、斜方晶结构、钛铀矿结构、钪钇石结构、斜方晶结构或伪金红石结构。在各种实施方案中,(b+c)/d≥1、2或3;a=0,或a>0.05、0.1或0.2;a+b+c+d<1、0.7、0.6或a+b+c+d=0.5;b+c>0.2、0.3、0.4,或b+c=0.5。在例示性的实施方案中,D为镍、钴、锰、铁、铬或它们的组合。在一些实施方案中,b>0且c=0。在一些实施方案中,b=0且c>0。在一些实施方案中,b>0且c>0。在各种实施方案中,A为钠、锂、镁或钙。
阳极组合物还可包含具有下式的材料:
A’eB’fC’gO, (II)
其中A’为碱金属、碱土金属或它们的组合,其中B’为钛,C’为钒,O为氧,e+f+g≤1,e≥0,f>0并且g>0。在各种实施方案中,A’为钠、锂、镁或钙。在一些实施方案中,该材料具有伪金红石结构。
在例示性的实施方案中,阳极组合物的具体示例可包括具有下式的那些:CoTiO3、Ca5Co4(VO4)6、CoV3O8、NiTiO3、Co2V2O7或MnV2O6。
在一些实施方案中,本公开的阳极组合物还可包含一种或多种添加剂,诸如粘结剂、导电性稀释剂、填料、增粘剂、用于涂料粘度调节的增稠剂如羧甲基纤维素、聚丙烯酸、聚偏二氟乙烯、聚丙烯酸锂、炭黑以及本领域技术人员已知的其他添加剂。在一些实施方案中,本公开的阳极组合物还可包括其他活性阳极材料,诸如在D.A.Stevens and J.R.Dahn,J.Electrochem.Soc.,148(2001)A803(D.A.Stevens和J.R.Dahn,《电化学会志》,148(2001)A803)中所述的硬碳(基于排除集电器的电极元件的总重量计,最多至10重量%、20重量%、50重量%或70重量%)。
在一些实施方案中,包含本公开的电化学活性阳极材料的阳极在掺入到钠离子蓄电池中并经历多个充放电循环后,可具有高比容量(mAh/g)保持(即,改善的循环寿命)。例如,当该蓄电池相对于Na在OV和2V之间或者5mV和1.2V之间循环并且温度保持在约室温(25℃)或在30℃或在60℃或甚至更高时,此类阳极可具有大于50mAh/g、大于100mAh/g、大于500mAh/g或甚至大于1000mAh/g的比容量。
本公开还涉及制备上述阳极组合物的方法。示例性的阳极组合物可通过任何已知的方法来制备,例如,通过通常在高于300℃的温度下,在加热炉中加热前体材料。加热过程中的气氛没有限制。该气氛可为空气、惰性气氛、还原性气氛诸如含氢气的气氛、或气体的混合。对前体材料也无限制。合适的前体材料可以是一种或多种金属氧化物、金属碳酸盐、金属硝酸盐、金属硫酸盐、金属氯化物或它们的组合。这些前体材料可通过磨削、机械研磨、从溶液沉淀来混合,或通过本领域中已知的其他方法混合。前体材料还可以是溶胶-凝胶的形式。焙烧之后,可对氧化物进行进一步加工处理,诸如通过机械研磨实现无定形或纳米晶结构、磨削和颗粒定径、涂覆表面涂层,以及通过本领域已知的其他方法来进行处理。示例性的阳极组合物也可通过对前体材料进行机械研磨而不焙烧来制备。合适的研磨可通过使用多种技术来实现,诸如垂直球磨、水平球磨或本领域技术人员已知的其他研磨方法。
本公开还涉及制备用于钠离子蓄电池的电极的方法。在一些实施方案中,该方法可包括将上述阳极材料连同任何添加剂诸如,粘结剂、导电性稀释剂、填料、增粘剂、用于涂料粘度调节的增稠剂以及本领域技术人员已知的其他添加剂一起在合适的涂料溶剂诸如,水或N-甲基吡咯烷酮中混合,以形成涂料分散体或涂料混合物。可将涂料分散体充分混合,然后通过任何合适的涂布技术施用至箔集电器上,所述涂布技术诸如为刮刀涂布、凹口棒涂、浸涂、喷涂、电喷涂布或凹版涂布。集电器可为导电金属的薄箔,诸如铜、铝、不锈钢或镍箔。可将浆液涂布至集电器箔上,然后使其在空气或真空中干燥,并任选地在加热烘箱中,通常在约80℃至约300℃下干燥约1小时以去除溶剂。
在各种实施方案中,本公开的电极作为钠离子蓄电池的负极可为尤其有用的。为制备蓄电池,负极可与电解质和阴极相结合。合适的阴极的示例包括含钠阴极,诸如由化学式NaxMO2表示的钠过渡金属氧化物,其中M为过渡金属并且x为0.7至1.2。合适的阴极材料的具体示例包含NaCrO2、NaCoO2、NaNi0.5Mn0.5O2、NaMn0.5Fe0.5O2。电解质的形式可以为液体、固体或凝胶。电解质通常包含盐和溶剂。固体电解质溶剂的示例包括聚合物,诸如聚环氧乙烷、聚四氟乙烯、含氟共聚物以及它们的组合。液体电解质溶剂的示例包括碳酸亚乙酯、碳酸二乙酯、丙二醇碳酸酯、氟代碳酸亚乙酯及它们的组合。电解质盐的示例包括含钠的盐,诸如NaPF6和NaClO4、Na[N(SO2CF3)2]2、NaCF3SO3和NaBF4。微孔隔板,诸如可购自北卡罗来纳州夏洛特的Celgard有限公司(Celgard LLC,Charlotte,N.C.)的微孔材料可掺入到蓄电池中并用于防止负极直接与正极接触。
本发明所公开的电化学电池可用于多种器件中,包括但不限于便携式计算机、平板显示器、个人数字助理、移动电话、电动化器件(例如,个人或家用电器和车辆)、器械、照明装置(如闪光灯)以及加热装置。本发明的一个或多个电化学电池可组合以形成蓄电池组。
本公开的操作将参照以下详述的实施例进一步描述。提供这些实施例以进一步说明多种具体实施方案和技术。然而,应当理解,可在不脱离本公开的范围的前提下进行多种变型和修改。
实施例
比较例1—制备Fe2TiO5(铁板钛矿结构)
为制备Fe2TiO5,向40ml球磨小瓶中加入4.00g Fe2O3(5μm,≥99%,西格玛-奥德里奇公司(Sigma-Aldrich))和2.00g TiO2(特纯,99%-100.5%,西格玛-奥德里奇公司(Sigma-Aldrich))。使用化学计量量的每种化合物。将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨半小时。然后使粉末在1000℃下在氩气中加热24小时。在合成之后,将样品直接转移到填充有氩气的手套箱中而未暴露于空气中。
使用配备有Cu阳极X射线管和双探测器的Rigaku Ultima IV X射线衍射仪,通过X射线粉末衍射(XRD)来表征样品。使用带衍射光束单色器的闪烁检测器来测量粉末样品的XRD图。
将粉末XRD样品装载到填充有氩气的手套箱中的气密性X射线样品夹持器(新斯科舍省Hebbville的DPM Solutions公司(DPM Solutions,Hebbville NS))中。样品夹持器具有以弧形安装的镀铝聚酯薄膜窗口,使得其垂直于入射和散射X射线束并且不利于所测量的XRD图。X射线样品夹持器配备有气体配件,这使得氦气在XRD测量过程中连续地流动。使用Rietica软件进行如上所制备粉末的粉末衍射数据的Rietveld精修和轮廓匹配。通过这种方法确定制备的Fe2TiO5样品具有铁板钛矿结构。
在钠电池中组装2325类硬币电池以评估电化学性能。电极由Fe2TiO5样品、炭黑(Super P,Erachem Europe公司(Erachem Europe))和PVDF(聚偏二氟乙烯,Kynar HSV 900)以重量比8:1:1组成。在Retsch PM200滚动球磨机(100rpm,1小时)中,这些组分与两个碳化钨球在N-甲基-2-吡咯烷酮(西格玛-奥德里奇公司(Sigma-Aldrich),无水99.5%)中充分混合,得到均一的黑色浆液。然后将该浆液涂覆到铝箔上,并在120℃真空下干燥2小时。从所得涂料中冲压出面积为2cm2的圆形电极。硬币电池的制备在填充有氩气的手套箱中进行。从由钠锭块(西格玛-奥德里奇公司(Sigma-Aldrich),ACS试剂纯)轧制的薄箔(0.015英寸)中冲压出钠箔盘阳极。该电解质为溶于丙二醇碳酸酯(诺莱特科技(Novolyte Technologies))的1M NaPF6(西格玛-奥德里奇公司(Sigma-Aldrich),98%)。将一个Celgard 3501和一个BMF(吹塑微纤维隔板,3M公司(3M Company))用作隔板。电池在Maccor系列4000自动循环仪上进行测试,并在恒定电流C/10下循环,这是根据使电压从0.005V循环到4.3V的112mAh/g容量计算的。
图1示出比较例1的具有铁板钛矿结构的Fe2TiO5材料的XRD图。
图2示出比较例1的Fe2TiO5材料的电压容量曲线。其具有非常低的容量,在大电压范围内仅具有45mAh/g可逆容量。
实施例1—制备NiTiO3(钛铁矿结构)。
为制备NiTiO3,向40ml球磨小瓶中加入2.90g NiO(-325目,99%,阿法埃莎公司(Alfa Aesar))和3.10g TiO2(特纯,99%-100.5%,西格玛-奥德里奇公司(Sigma-Aldrich))。使用化学计量量的每种化合物。将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨半小时。然后使粉末在1000℃下在空气中加热10小时。
使用配备有Cu阳极X射线管和双探测器的Rigaku Ultima IV X射线衍射仪,通过X射线粉末衍射(XRD)来表征样品。使用带衍射光束单色器的闪烁检测器来测量粉末样品的XRD图。
将粉末XRD样品装载到填充有氩气的手套箱中的气密性X射线样品夹持器(新斯科舍省Hebbville的DPM Solutions公司(DPM Solutions,Hebbville NS))中。样品夹持器具有以弧形安装的镀铝聚酯薄膜窗口,使得其垂直于入射和散射X射线束并且不利于所测量的XRD图。X射线样品夹持器配备有气体配件,这使得氦气在XRD测量过程中连续地流动。使用Rietica软件进行如上所制备粉末的粉末衍射数据的Rietveld精修和轮廓匹配。通过这种方法确定制备的NiTiO3样品具有钛铁矿结构。
在钠电池中组装2325类硬币电池以评估电化学性能。电极由NiTiO3样品、炭黑(Super P,Erachem Europe公司(Erachem Europe))和PVDF(聚偏二氟乙烯,Kynar HSV 900)以重量比8:1:1组成。在Retsch PM200滚动球磨机(100rpm,1小时)中,这些组分与两个碳化钨球在N-甲基-2-吡咯烷酮(西格玛-奥德里奇公司(Sigma-Aldrich),无水99.5%)中充分混合,得到均一的黑色浆液。然后将该浆液涂覆到铝箔上,并在120℃真空下干燥2小时。从所得涂料中冲压出面积为2cm2的圆形电极。硬币电池的制备在填充有氩气的手套箱中进行。从由钠锭块(西格玛-奥德里奇公司(Sigma-Aldrich),ACS试剂纯)轧制的薄箔(0.015英寸)中冲压出钠箔盘阳极。该电解质为溶于丙二醇碳酸酯(诺莱特科技(Novolyte Technologies))的1M NaPF6(西格玛-奥德里奇公司(Sigma-Aldrich),98%)。将一个Celgard 3501和一个BMF(吹塑微纤维隔板,3M公司(3M Company))用作隔板。电池在Maccor系列4000自动循环仪上进行测试,并在恒定电流C/10下循环,这是根据在0.005V和4.3V之间的173mAh/g容量计算的。
图3示出实施例1的具有钛铁矿结构的NiTiO3材料的XRD图。
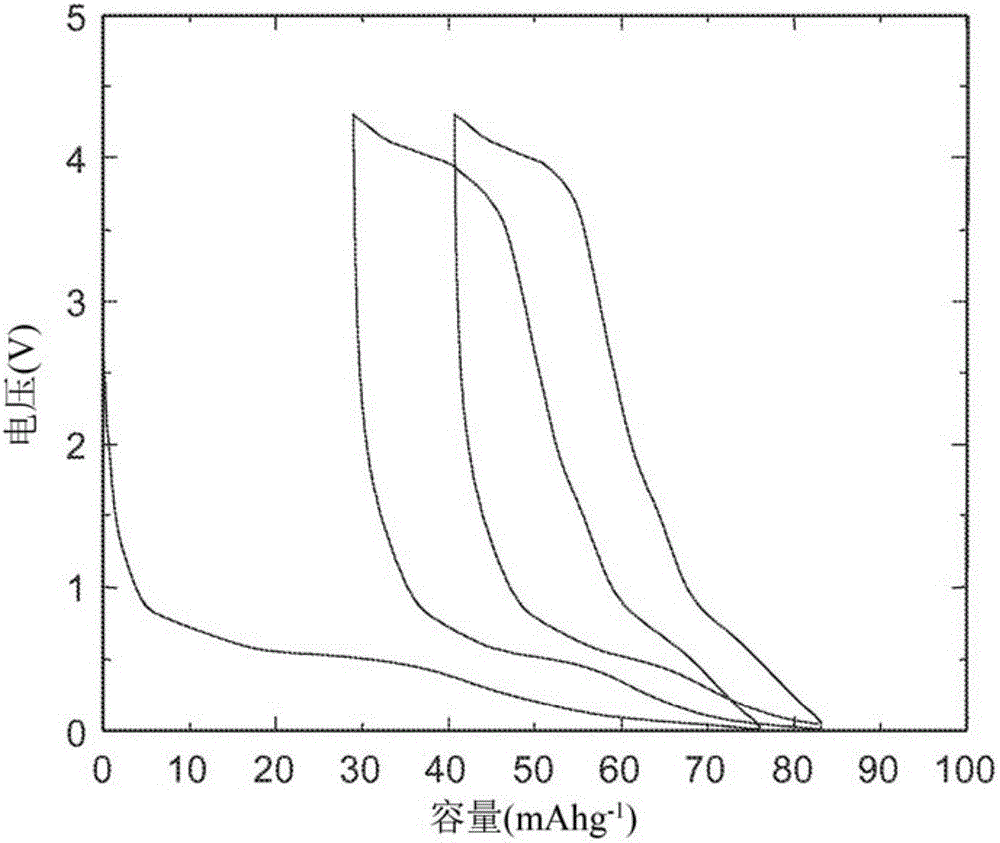
图4示出实施例1的NiTiO3材料的电压容量曲线。其示出175mAh/g的可逆容量。存在低于1伏的倾斜的低电压平台。
样品制备—实施例2-11
实施例2—制备CoTiO3(钛铁矿结构)。
向40ml球磨小瓶中加入2g Co3O4(<10μm,西格玛-奥德里奇公司(Sigma-Aldrich))和2g TiO2(特纯,99%-100.5%,西格玛-奥德里奇公司(Sigma-Aldrich))。将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨两小时。然后使粉末在800℃下在空气中加热10小时。
实施例3—VFeO4(VFeO4三斜晶结构)。
向40ml球磨小瓶中加入2.13g V2O5(>99.6%,西格玛-奥德里奇公司(Sigma-Aldrich))和1.87g Fe2O3(<5μm,>99%,西格玛-奥德里奇公司(Sigma-Aldrich))。将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨一小时。然后使粉末在550℃下在空气中加热24小时。
实施例4—制备Ca5Co4(VO4)6(Ca5Co4(VO4)6立方结构)。
向40ml球磨小瓶中加入0.725g CaO(99.9%,西格玛-奥德里奇公司(Sigma-Aldrich))、0.956g CoO(325目,西格玛-奥德里奇公司(Sigma-Aldrich))和2.319g V2O5(>99.6%,西格玛-奥德里奇公司(Sigma-Aldrich))。氩气下将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨一小时。然后使所得粉末在750℃下在氩气中加热10小时。在合成之后,将粉末直接转移到填充有氩气的手套箱中而未暴露于空气中。
实施例5—制备Co2V2O7(重铬酸盐结构)。
向40ml球磨小瓶中加入1.88g Co3O4(<10μm,西格玛-奥德里奇公司(Sigma-Aldrich))和2.12g V2O5(>99.6%,西格玛-奥德里奇公司(Sigma-Aldrich))。将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨一小时。然后使粉末在600℃下在空气中加热30小时。
实施例6—制备CoV3O8(斜方晶结构)。
向40ml球磨小瓶中加入0.88g CoO(325目,西格玛-奥德里奇公司(Sigma-Aldrich))、0.98g V2O4(99.9%,微量金属基点)和2.14g V2O5(>99.6%,西格玛-奥德里奇公司(Sigma-Aldrich))。氩气下将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨一小时。然后使粉末在600℃下在氩气中加热12小时。在合成之后,将粉末直接转移到填充有氩气的手套箱中而未暴露于空气中。
实施例7—制备MnV2O6(钛铀矿结构)。
向40ml球磨小瓶中加入1.21g Mn2O3(325目,99%,西格玛-奥德里奇公司(Sigma-Aldrich))和2.79g V2O5(>99.6%,西格玛-奥德里奇公司(Sigma-Aldrich))。将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨一小时。然后使粉末在600℃下在空气中加热30小时。
实施例8—制备Mn2V2O7(钪钇石结构)。
向40ml球磨小瓶中加入1.75g MnO(60目,99%,西格玛-奥德里奇公司(Sigma-Aldrich))和2.25g V2O5(>99.6%,西格玛-奥德里奇公司(Sigma-Aldrich))。将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨一小时。然后使粉末在800℃下在空气中加热30小时。
实施例9—制备MnTiO3(钛铁矿结构)。
向40ml球磨小瓶中加入3.13g MnO2(60-230目,>99%,西格玛-奥德里奇公司(Sigma-Aldrich))和2.87g TiO2(特纯,99%-100.5%,西格玛-奥德里奇公司(Sigma-Aldrich))。氩气下将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨一小时。然后使粉末在1100℃下在氩气中加热10小时。在合成之后,将粉末直接转移到填充有氩气的手套箱中而未暴露于空气中。
实施例10—制备CrVO4(斜方晶结构)。
向40ml球磨小瓶中加入1.82g Cr2O3(50μm,>98%,西格玛-奥德里奇公司(Sigma-Aldrich))和2.18g V2O5(>99.6%,西格玛-奥德里奇公司(Sigma-Aldrich))。将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨一小时。然后使粉末在800℃下在空气中加热30小时。
实施例11—制备TiVO4(伪金红石结构)。
向40ml球磨小瓶中加入2.94g TiO2(特纯,99%-100.5%,西格玛-奥德里奇公司(Sigma-Aldrich))和3.06g V2O5(>99.6%,西格玛-奥德里奇公司(Sigma-Aldrich))。氩气下将该前体在高能球磨机(Spex Certiprep公司(Spex Certiprep))中球磨30分钟。然后使粉末在1000℃下在氩气中加热16小时。在合成之后,将粉末直接转移到填充有氩气的手套箱中而未暴露于空气中。
表征和评估—实施例2-11
使用配备有Cu阳极X射线管和双探测器的Rigaku Ultima IV X射线衍射仪,通过X射线粉末衍射(XRD)来表征实施例2-11。使用带衍射光束单色器的闪烁检测器来测量粉末样品的XRD图。
使用在实施例2-11中制备的材料,在钠电池中组装2325类硬币电池以评估电化学性能。电极由样品、炭黑(Super P,Erachem Europe公司(Erachem Europe))和PVDF(聚偏二氟乙烯,Kynar HSV 900)以重量比8:1:1组成。在Retsch PM200滚动球磨机(100rpm,1小时)中,这些组分与两个碳化钨球在N-甲基-2-吡咯烷酮(西格玛-奥德里奇公司(Sigma-Aldrich),无水99.5%)中充分混合,得到均一的黑色浆液。然后将该浆液涂覆到铝箔或铜箔上,并在120℃真空下干燥2小时。从所得涂料中冲压出面积为2cm2的圆形电极。硬币电池的制备在填充有氩气的手套箱中进行。从由钠锭块(西格玛-奥德里奇公司(Sigma-Aldrich),ACS试剂纯)轧制的薄箔(0.015英寸)中冲压出钠箔盘阳极。电解质为溶于3/6/1的碳酸亚乙酯/碳酸二乙酯/单氟代碳酸乙烯酯(均得自诺莱特科技(Novolyte Technologies))的1M NaPF6(西格玛-奥德里奇公司(Sigma-Aldrich),98%)。将两个Celgard 2300和一个BMF(吹塑微纤维隔板,3M公司)用作隔板。电池在Maccor系列4000自动循环仪上进行测试,并在恒定电流速率C/10和C/40下循环,分别微电流放电至C/20和C/80,这是根据从0.005V循环到2.5V和/或从0.005V循环到4.5V的100mAh/g和200mAh/g之间的容量计算的。
实验结果—实施例2-11
图5示出与CoTiO3的文献图相比,实施例2的实验XRD图(上图)以及由实施例2材料制备的电池的对应电压曲线(下图)。实施例2为具有R-3(148)空间群(钛铁矿结构)的纯相CoTiO3。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
图6示出与VFeO4的文献图相比,实施例3的实验XRD图(上图)以及由实施例3材料制备的电池的对应电压曲线(下图)。实施例3为具有P-1(2)空间群(VFeO4三斜晶结构)的纯相VFeO4。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
图7示出与Ca5Co4(VO4)6的文献图相比,实施例4的实验XRD图(上图)以及由实施例4材料制备的电池的对应电压曲线(下图)。未得到纯相;具有Ia-3d(230)空间群(Ca5Co4(VO4)6立方结构)的Ca5Co4(VO4)6相以含微量Co3V2O8杂质的形式存在。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
图8示出与Co2V2O7的文献图相比,实施例5的实验XRD图(上图)以及由实施例5材料制备的电池的对应电压曲线(下图)。实施例5为具有P21/c(14)空间群(重铬酸盐结构)的纯相Co2V2O7。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
图9示出与CoV3O8的文献图相比,实施例6的实验XRD图(上图)以及由实施例6材料制备的电池的对应电压曲线(下图)。未得到纯相;具有Cmce(64)空间群(斜方晶结构)的CoV3O8相以含微量氧化钴/氧化钒杂质的形式存在。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
图10示出与MnV2O6的文献图相比,实施例7的实验XRD图(上图)以及由实施例7材料制备的电池的对应电压曲线(下图)。实施例7为具有C2/m(12)空间群(钛铀矿结构)的纯相MnV2O6。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
图11示出与Mn2V2O7的文献图相比,实施例8的实验XRD图(上图)以及由实施例8材料制备的电池的对应电压曲线(下图)。实施例8为具有C2/m(12)空间群(钪钇石结构)的纯相Mn2V2O7。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
图12示出与MnTiO3的文献图相比,实施例9的实验XRD图(上图)以及由实施例9材料制备的电池的对应电压曲线(下图)。实施例9为具有R-3(148)空间群(钛铁矿结构)的纯相MnTiO3。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
图13示出与CrVO4的文献图相比,实施例10的实验XRD图(上图)以及由实施例10材料制备的电池的对应电压曲线(下图)。实施例10为以微量未识别的杂质存在的具有Cmcm(63)空间群(斜方晶结构)的纯相CrVO4。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
图14示出与TiVO4的文献图相比,实施例11的实验XRD图(上图)以及由实施例11材料制备的电池的对应电压曲线(下图)。实施例11为具有P42/mmm(136)空间群(伪金红石结构)的纯相TiVO4。该材料具有可逆低平均电压容量,其示出用作钠离子蓄电池中的负极材料的潜能。
- 还没有人留言评论。精彩留言会获得点赞!