食品中的植物甾醇组合物的制作方法
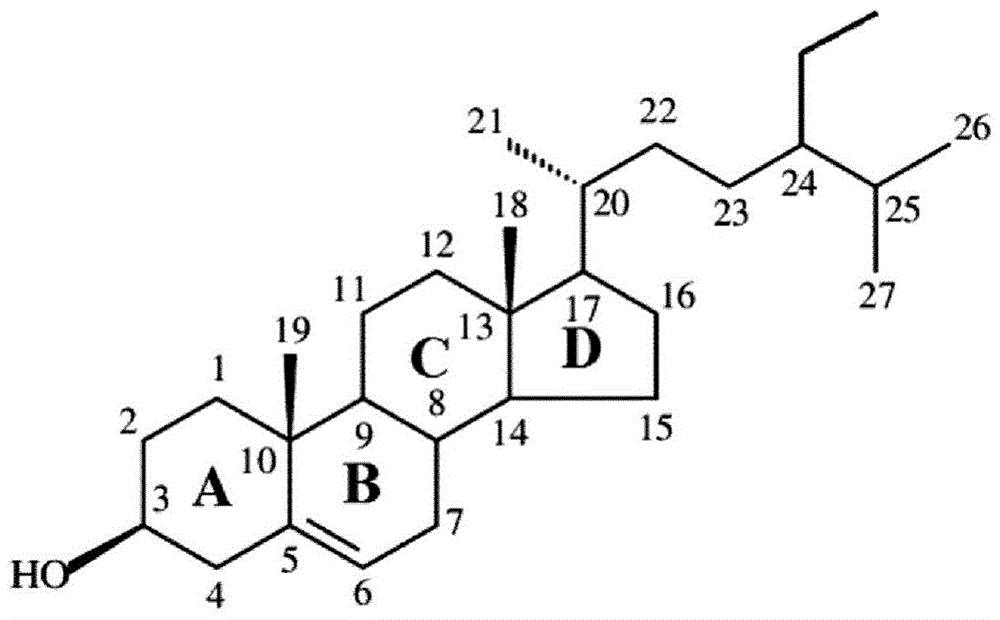
发明领域本发明涉及食品的制备。本发明涉及降低食品中硬浆(hardstock)的量的方法。本发明进一步涉及植物甾醇酯的用途。发明背景食品制造商目前寻找配制具有更好的脂肪级分营养特征(即,饱和脂肪酸低和不饱和脂肪酸高)且优选不使用棕榈油,但当然同时保持相同产品质量特征的产品的多种方法[patel,a.edibleoilstructuring:conceptmethodsandapplications,firstedit.;theroyalsocietyofchemistry,2017]。然而,这非常有挑战性,因为富含饱和脂肪酸的脂肪(例如,脂、椰子油和棕榈油)在室温下是固体,而富含不饱和脂肪酸的脂肪(例如,橄榄油)在室温下是液体。富含饱和脂肪酸的脂肪的主要功能作用是在食品中提供期望的质感(例如,硬度、延展性)和口感[pateletal.(2016)foodfunct.7,20-29]。最近,已经研究了多种不同策略来降低食品中的饱和脂肪的量。第一种方法是脂肪的酯交换。该技术可导致饱和脂肪的降低有限。第二种方法是用液体油和结构化剂(也称为凝胶因子(gelator))替代饱和脂肪。这些化合物通过形成互连网络赋予液体油固体脂肪功能,所述互连网络将所述液体油转化成胶状物质,其有时被称为油凝胶(oleogel)或有机凝胶[marangonietal.(2012)softmatter,8,1275-1300]。尽管在文献中已经描述了这些凝胶因子,但是目前没有包含油凝胶的食品销售,因为每种类型的凝胶因子都有阻止其应用的限制。用于涂抹、烘焙和蒸煮的奶油的使用越来越多地被人造奶油的使用所代替,人造黄油是一种油包水型乳剂。而且,对于人造奶油的制备,仍然一直寻求用不饱和脂肪酸代替饱和脂肪酸和反式不饱和脂肪酸。使用人造奶油作为面包涂抹料要求产品可以作为均质乳液储存在冰箱中,足够柔软至用刀等操作,并且当人造奶油被消耗和达到体温时提供一定的口感。为了获得这些性质,人造奶油包含部分硬脂(在室温下为固体)和油(在室温下为液体)。人造奶油消耗有关的健康方面很重要。为了健康的原因,饱和脂肪酸和反式不饱和脂肪酸优选地被未氢化单不饱和的脂肪酸和多不饱和脂肪酸所替代。其他人造奶油也可包含植物甾醇基成分(甾烷醇酯(stanolesters)),已知当其以足够高量摄入时,同时降低血液中全胆固醇且特别是低密度脂蛋白(ldl)胆固醇的水平。由于植物甾醇的正常饮食摄入量不足以引起血液中的胆固醇显著降低,将植物甾醇基成分掺入人造奶油中是一种给予较高量的植物甾醇的好方法,该较高量的植物甾醇对于得益于其降低胆固醇性质是足够的[salo,etal.(2003).ingunstone(ed.)lipidsforfunctionalfoodsandnutraceuticals.bridgwater,england:theoilypress]。使用这样的产品能够使用较低量的他汀类,同时仍然获得了血液中ldl胆固醇的相同量的降低(marangoni&poli(2010)pharmacol.res.61,193–169)。植物甾醇的另一个有益性质是他们不会被吸收到体内,因此对于体内能量摄入没有贡献。植物甾醇酯是经由用脂肪酸酯化来自植物的植物甾醇产生的,所述脂肪酸也来自于植物。植物甾醇酯由约60%重量的植物甾醇和40%重量的脂肪酸组成。如果脂肪酸来源于常见植物油,则植物甾醇酯的脂肪酸组成与用作脂肪酸来源的植物油类似。在商业规模上,植物甾醇可以来源于植物油和木材。植物甾烷醇(plantstanol)在自然界中仅少量存在,可以通过氢化市售可获得的主要是不饱和的植物甾醇产生。在氢化期间,植物甾醇分子中的双键通过加氢而饱和。然后,通过用也来源于植物的脂肪酸混合物后续酯化所述植物甾烷醇来制备甾烷醇酯。植物甾醇酯(phytosterolester)与植物甾烷醇酯(phytostanolester)具有类似的药用性质,但是具有不同的物理化学性质。因为它们的熔融特性有差异,甾烷醇酯相对于甾醇酯用作人造奶油中的成分是优选的,因为它们可以部分地替代硬的级分。在脂肪掺合物中使用植物甾醇酯仍然需要大量的硬浆(hardstock)来获得用于制备人造奶油和相关产品的合适产品。wo9819556讨论了含有植物甾醇酯和植物甾烷醇酯的不同脂肪掺合物的性质。然而,为了获得具有期望性质(例如,质地、稠度、口感)的产品,富含植物甾醇或植物甾烷醇的市售产品仍然在脂肪掺合物中包含相当大量的硬浆,如棕榈油,以及与其相关的至少20%的饱和脂肪酸。尽管植物甾醇作为功能食品成分的存在超过了20年,但是仍然需要具有高植物甾醇含量但低量的饱和脂肪的人造奶油类的组合物。由于包含植物甾醇酯的组合物的固体脂肪含量甚至更低,这些化合物不能被认为是以部分地替代硬浆且由此降低人造奶油中饱和脂肪酸的含量的植物甾烷醇酯的替代选择。us20030068425提议在甜食如巧克力的制备中使用植物甾醇酯。us20110287156公开了植物甾醇酯组合物改善食品组合物的贮存期限和氧化稳定性。该文件没有区别植物甾醇酯和植物甾烷醇酯,并且没有讨论硬浆(在20℃下的脂肪固体)。发明简述本发明是基于如下发现:含有非常低含量的饱和脂肪酸和期望的降低ldl性质的某些植物甾醇酯(谷甾醇酯)具有与含有高含量的饱和脂肪酸如棕榈油和棕榈硬脂的脂肪相当的物理化学性质。这具有的好处是在例如人造奶油中使用该类植物甾醇酯不需要用富含饱和脂肪酸的硬浆来弥补。本发明进一步克服了需要将植物甾醇转化成植物甾烷醇。常规硬浆如含脂肪食品的棕榈油可以被主要包含不饱和脂肪酸的本发明中所述特定类型的甾醇酯完全替代。因此,本发明具有的优点是在例如人造奶油中的饱和脂肪酸(存在于硬浆中)的浓度可以显著地降低,甚至降低至非常低的量,同时仍然提供必须的质地和期望的口感。本发明具有的优点是例如橄榄油的油酸脂肪酸链可以用于植物甾醇酯中,引起不饱和脂肪酸增加。本发明具有的其他优点是,由于本发明的产品的植物甾醇酯含量较高,为了获得2,5g植物甾醇/植物甾烷醇酯/天的所提议剂量,需要消耗更少的人造奶油,或者按照摄入约20g/天的平均人造奶油消耗,达到所提议的每日摄入量的可能性增加。本发明提供一种产品,其具有脂肪级分的有益营养特征(即,饱和脂肪酸低和不饱和脂肪酸高),同时保持相同的产品质量特性。本发明提供具有期望的硬度和在低温度(冰箱)下铺展性和当消耗时的口感的产品。本发明的方法和组合物在没有使用凝胶因子(其形成将液体油转化成胶状材料(油凝胶或有机凝胶)的互连网络)下,能够降低食品中饱和脂肪的量,而没有脂肪的酯交换。本发明的方法和组合物能够减少饱和脂肪酸和反式不饱和脂肪酸,而所述产品可以作为均质乳液储存在冰箱中,足够柔软至用刀等操作,并且当人造奶油被消耗和达到体温时提供一定的口感。本发明的方法和组合物能够进一步提高植物甾醇的每日摄入量,其允许使用较低量的他汀类,同时仍然获得了血液中ldl胆固醇的相同量的降低。本发明的方法和组合物能够提供具有高植物甾醇含量但低量的饱和脂肪的人造奶油类组合物。本发明以如下声明进行概述:1.一种可食用可涂抹的乳液,其具有脂肪含量在10-90%、20-90%(w/v)、30-90%(w/v)、40-90%(w/v)、50-90%(w/v)、10-30%(w/v)、10-40%(w/v)%(w/v)、10-50%(w/v)、10-60%(w/v)、10-30%(w/v)、20-40%(w/v)、30-50%(w/v)、40-60%(w/v)、50-70%(w/v)、60-80%(w/v)、70-90%(w/v)、20-50%(w/v)、30-60%(w/v)、40-70%(w/v)、50-80%(w/v)、60-90%(w/v)、10-50%(w/v)、20-60%(w/v)、30-70%(w/v)或40-80%(w/v)之间,其中脂肪级分中的植物甾醇酯、硬浆和液体油的组合由以下组成:-10–50、15-45、20-40%、20-50%、30-50%、10-40%或10-30%(w/w)的植物甾醇酯,包含至少65%(w/w)、70%(w/w)、75%w/w.或80%(w/w)的植物甾醇油酸酯,-0-20%、0-5%、0-10%、0-15%、5-10%、5-15%(w/w)的硬浆,-液体油,直至100%。2.根据声明1所述的乳液,其中所述植物甾醇酯包含至少50%、60%、70%、75%、80%、85%或90%(w/w)的植物甾醇油酸酯。3.根据声明1或2所述的乳液,其中所述硬浆含有所述脂肪级分的小于15%、小于10%.或小于5%或小于2.5%(w/w),或者其中所述脂肪级分不包含硬浆。4.根据声明1至3中任一项的乳液,其中所述脂肪级分中饱和脂肪酸的量为总脂肪酸含量的低于20%、低于15%、低于10%或低于5%(w/w)。5.根据声明1至4中任一项的乳液,其不含植物甾烷醇酯。6.根据声明1至5中任一项的乳液,其中所述植物甾醇酯包含至少50%、55%、60%、65%、70%、75%或80%(w/w)的谷甾醇酯。7.根据声明1至6中任一项的乳液,其中所述植物甾醇酯包含小于20%的多不饱和脂肪酸。8.根据声明1至7中任一项的乳液,其是具有在50-70%、55-70%、60-70、50-60%、50-65%、60-70%(w/v)之间的脂肪含量的人造奶油类组合物。9.根据声明1至7中任一项的乳液,其是具有在30至40%之间的脂肪含量的涂抹类组合物。10.根据声明1至9中任一项的乳液,其包含小于10%、小于5%或小于2.5%(w/w)的饱和脂肪酸。11.根据声明1至10中任一项的乳液,其中所述液体油为橄榄油、葵花籽油、菜籽油、亚麻籽油或其混合物。12.根据声明1至10中任一项的乳液,其中所述液体油为橄榄油。13.包含至少65%的植物甾醇油酸酯的植物甾醇酯在制备可食用乳液中的用途。14.根据声明13的用途,用于制备人造奶油。15.脂肪掺合物(fatblend),其中脂肪级分中植物甾醇酯、液体油和硬浆的组合由以下组成:-10-50%、15-45%、或20-40%、10-30%、20-50%、10-40%、20-50(w/w)%的植物甾醇酯,其包含至少65%植物甾醇油酸酯,-0-20%、0-5%、0-10%、0-15%、5-10%、10-15%、15-20%、5-15%或10-20(w/w)的硬浆,-液体油,直至100%,其中在所述脂肪级分中饱和脂肪酸的量在总脂肪酸含量的0至20%之间,例如总脂肪酸含量的低于20%、低于15%、低于10%或低于5%(w/w)。16.根据声明15的脂肪掺合物,其中所述植物甾醇酯包含至少50%、55%、60%、65%、70%、75%或80%的植物甾醇油酸酯。17.根据声明15或16所述的脂肪掺合物,其中所述硬浆含有所述脂肪级分的小于15%、小于10%、小于5%或小于2.5%(w/w),或者其中所述脂肪级分不包含硬浆。18.根据声明15至17中任一项的脂肪掺合物,其中所述脂肪级分中饱和脂肪酸的量为总脂肪酸含量的低于20%、低于15%、低于10%或低于5%。19.根据声明15至18中任一项的脂肪掺合物,其不含植物甾烷醇酯。20.根据声明15至19中任一项的脂肪掺合物,其中所述植物甾醇酯包含至少50%、55%、60%、65%、70%、75%或80%的谷甾醇酯。21.根据声明15至20中任一项的脂肪掺合物,其中所述植物甾醇酯包含小于20%的多不饱和脂肪酸。22.根据声明15至21中任一项的脂肪掺合物,其包含小于10%的饱和脂肪酸。23.根据声明15至22中任一项的脂肪掺合物,其中所述液体油为橄榄油、葵花籽油、菜籽油、亚麻籽油或其混合物。24.根据声明15至23中任一项的混脂肪掺合物,其中所述液体油为橄榄油。25.根据声明15至24中任一项的脂肪掺合物在制备可食用乳液中的用途。26.根据声明25的用途,用于制备人造奶油。27.植物甾醇酯用于替代可涂抹乳液中硬浆的用途。28.根据声明27所述的用途,其中所述植物甾醇酯包含至少65%的植物甾醇油酸酯,其中所述硬浆包含棕榈油、棕榈硬脂、椰子油或脂,并且其中所述乳液是人造奶油。发明详述图1:β-谷甾醇的化学结构(soupasetal.(2005)eur.j.lipidsci.technol.107,107–118.)图2:在10℃下回火72小时之后,β-谷甾醇基油酸酯的熔融曲线。图3:在10℃下回火72小时之后,β-谷甾醇基油酸酯的waxd图。图4:在10℃下回火72小时之后,β-谷甾醇基油酸酯的saxs图。图5:在10℃下回火72小时之后,结晶的β-谷甾醇基油酸酯网络的显微镜检查照片。黑色柱代表100μm。图6:在10℃下回火72小时之后,棕榈油与β-谷甾醇基油酸酯(pe油酸酯)的掺合物的dsc熔融曲线。不同的曲线代表β-谷甾醇基油酸酯的不同浓度。a图:纯棕榈油到含有50%的β-谷甾醇基油酸酯的棕榈油。b图:含有50%的β-谷甾醇基油酸酯的棕榈油到纯β-谷甾醇基油酸酯。图7:在10℃下回火72小时之后,在不同(ff.)β-谷甾醇基油酸酯的浓度下,棕榈油与β-谷甾醇基油酸酯的掺合物的平均峰最大值±标准偏差(n=5)。图8:在10℃下回火72小时之后,在不同(ff.)β-谷甾醇基油酸酯的浓度下,棕榈油与β-谷甾醇基油酸酯的掺合物的平均熔融焓±标准偏差(n=5)。图9:在10℃下回火72小时之后,棕榈油与β-谷甾醇基油酸酯的掺合物的waxd图。不同曲线代表不同浓度的β-谷甾醇基油酸酯。图10:在10℃下,在回火72小时之后,棕榈油与β-谷甾醇基油酸酯的掺合物的saxs图。不同曲线代表不同浓度的β-谷甾醇基油酸酯。图11:在10℃下回火72小时之后,棕榈油与β-谷甾醇基油酸酯的掺合物的晶体网络的显微镜照片。黑色条代表100μm。图12:不同人造奶油和β-谷甾醇基油酸与菜籽油的掺合物的sfc特征。图13:含有来源于葵花籽油和橄榄油的脂肪酸的甾醇酯、棕榈油和棕榈硬脂的sfc特征。图14:菜籽油与含有来源于葵花籽油的脂肪酸的甾醇酯的掺合物的sfc特征。图15:菜籽油与含有来源于橄榄油的脂肪酸的甾醇酯的掺合物的sfc特征。定义可食用可涂抹的乳液,涉及包含在4℃和20℃下为固体和在37℃下为液体的组合物的脂肪。这样的组合物的脂肪含量在约10至90%、25至80%、或50至70%(w/v)的范围内。可食用可涂抹的乳液包含被称为人造奶油或halvarine的产品和涂抹料(spreads)(通常,在30至40%之间的脂肪含量(w/v))。落入该种类的其它商业食品是可涂抹的乳酪。如按照欧盟的指令所定义的人造奶油,是指“来源于具有至少10%但小于90%的脂肪含量的植物/动物脂肪的油包水型乳剂,其在20℃的温度下仍然是固体,并且作为涂抹料是合适的”。在本发明中,人造奶油通常仅包含植物脂肪和油。在本发明中,人造奶油的优选的实施方案通常具有在50至70%之间的脂肪含量。植物甾醇,是具有与胆固醇类似化学结构的三萜。如图1所示,它们由四-环甾核组成,其具有连接a-环的c-3原子的羟基和连接d-环的c-17原子的脂肪族侧链。植物甾醇包括超过250种不同的植物甾醇和甾烷醇和相关化合物,但是更富集的一种是β-谷甾醇、豆甾醇和菜籽甾醇。植物甾醇仅在它们的侧链方面不同。可能的侧链变化包括在c-24原子上存在支链的甲基或乙基及单个双键的存在和位置(piironenetal.(2000)j.sci.foodagric.80,939-966.)。植物甾烷醇,是植物甾醇的饱和的氢化产品,其中甾醇环中的双键不存在。植物甾醇酯,是脂肪和植物甾醇的反应产物。根据脂肪的类型,脂肪酸组成可以变化。为了清晰起见,植物甾烷醇的酯化形式(植物甾烷醇酯)不会在本发明的植物甾醇酯的定义下再分类。这与例如us20110287156不同,其中植物甾醇酯是植物甾醇和植物甾烷醇两者的酯的总称(collectivename)。然而,植物甾醇酯及其相应的甾烷醇酯的熔点显著不同,导致质地和/或口感不同。本发明的合适的植物甾醇酯进一步具有至少65、70、75、80或85%的不饱和脂肪酸,其中所述不饱和脂肪酸通常为油酸(c18:1)。具有c16:1、c20:1或c24:1链的脂肪酸可以等价地被使用,但是仅以有限量发生在有限数量的植物种子中。在本发明的上下文中,合适的植物甾醇酯主要地含有油酸作为脂肪酸,即至少65、70%、80%或90%。一种优选的植物甾醇酯组合物包含至少65、70、80、90%的谷甾醇油酸酯。油酸的这些含量可以通过酯化橄榄油获得,根据批次之间,其具有的油酸含量通常在74至80%之间。而且,具有高油酸含量的其它油如高油酸葵花籽油(约80%)、高油酸大豆油(约82-84%)、高油酸红花油(约78%)和高油酸芥花油(canolaoil)(约78-84%)在本发明的上下文中是合适的。其它商业油具有基本上更低的油酸含量(低芥酸菜籽油约60%,高芥酸菜籽油约15%;大豆油约25%,玉米油约27%,棉籽油约41%,葵花籽油约21%,红花油约18%,脂油约30%,棕榈油约40%,棕榈仁油约15%,椰子油约8%或更少)。硬浆,是指其在室温下为固体的脂肪级分,其与液体油差不多地掺入产品如人造奶油中。硬浆也定义为在人造奶油的脂肪级分中的固体脂肪级分。脂肪级分是固体脂肪和油的混合物。通常用于在这样的产品中提供硬浆的脂肪是天然的,如棕榈油或椰子油或氢化油,如氢化菜籽油或氢化葵花籽油或黄油。棕榈油的级分如棕榈硬脂和棕榈中间级分通常也用于提供硬浆。本发明能够替代在人造奶油中使用的大量的或所有的硬浆。因此,本发明的实施方案可以包括每100克的人造奶油小于4、3、2、小于1.5或小于0.5克的饱和脂肪酸。“硬浆”与通用术语“甘油三酯脂肪”不同,后者可以指固体以及液体脂肪及其混合物。液体油,即在20℃下为液体,是可涂抹乳液如人造奶油的一部分。在本发明的上下文中,液体油的典型的实例为菜籽油、葵花籽油或亚麻籽油。脂肪掺合物是通过如下制备的:首先,在高于脂肪的熔化温度的温度下分别加热所述脂肪,以抹除晶体记忆,直到它们完全是液体。随后,将所述液体油混合,并搅拌,同时在高于两种脂肪的熔化温度的温度下加热,直到得到可见的均质掺合物。虽然本发明的脂肪级分主要成分是植物甾醇酯、液体油和硬浆,但组合物如人造奶油,可以包括化合物如甘油单酯、甘油二酯、和聚甘油缩合蓖麻醇酸酯(polyglycerolpolyricinoleate)(pgpr)。标准人造奶油加工方法是本领域已知的,且包括步骤:-通过在高于熔化温度的温度下加热硬浆,直到其完全熔融,并将其与液体油(例如,菜籽油或葵花籽油)掺合来制备油相(oilphase)。随后,将乳化剂分散在油相(fatphase)中,并且也可能将抗氧剂和着色剂加入到所述油相中。-通过将盐、蛋白、糖、防腐剂、调味剂和也可能有稳定剂溶于水中来制备水相。-通过混合所述油相和所述水相制备乳液。任选地,将该乳液巴氏杀菌以避免微生物污染。在巴氏灭菌之后,将该乳液保持在约43℃的温度下以避免形成核。-在刮板式表面换热器(scrapedsurfaceheatexchanger)中冷却所述乳液,以诱导脂质结晶。-使人造奶油经过销工作单元(pin-worker),其中所冷却的乳液完成其结晶,并且其中产生期望的人造奶油质地。(miskandaretal.(2005)asiapacjclinnutr14,387-395andyoungn.,wassellp.(2008)margarineandspreads.in:hasenhuettlg.l.,hartelr.w.(eds)foodemulsifiersandtheirapplications.springer,newyork,ny)。上述的成分的实例为盐(氯化钠或氯化钾)、卵磷脂、磷脂、聚甘油缩合蓖麻醇酸酯(pgpr)、奶粉、乳糖、甘油单酯和甘油二酯的柠檬酸酯、碳酸氢钠和柠檬酸作为ph-调节剂、β-胡萝卜素作为着色剂、调味剂、防腐剂如edta二钠钙、没食子酸丙酯、没食子酸辛酯和没食子酸十二酯、bht、bha、抗坏血酸棕榈酸酯、抗坏血酰硬脂酸酯、柠檬酸硬脂酰酯、柠檬酸异丙酯和山梨酸和苯甲酸及它们的钠盐、钾盐和钙盐、可食用蛋白质如酪蛋白、酪蛋白酸盐、白蛋白、乳清蛋白、植物蛋白或大豆蛋白分离物、乳化剂如甘油单酯和甘油二酯、增稠剂如明胶、果胶、角叉菜胶、琼脂、黄原胶、结冷胶、淀粉或淀粉衍生物、海藻酸盐、或甲基纤维素衍生物(youngn.,wassellp.(2008)margarinesandspreads.in:hasenhuettlg.l.,hartelr.w.(eds)foodemulsifiersandtheirapplications.springer,newyork,ny)。植物甾醇的最富集的天然来源是植物油,接着是谷粒和坚果。植物甾醇被提取用于药物、化妆品和食品应用(fernandes&cabral(2007)bioresourcetechnol.98,2335-2350;上述引用的piironenetal.(2000))。用于大量植物甾醇提取的两种主要原料是植物油和妥尔油(牛皮浆加工的副产物)(helminenetal.(2006)organicprocessres.&dev.10,51–63;thompson&grundy(2005)am.j.cardiol.96,3-9)。流行病学和实验研究表明在西方社会中,植物甾醇对于最常见的癌症可以提供保护,但是他们的主要有益的健康作用在于降低循环胆固醇浓度。41个试验的综合分析表明采用最佳摄入植物甾醇2g/天可得到ldl-胆固醇的血液水平降低10%,超过该量仅观察到边缘效应(mensinketal.(2003)theam.j.ofclinicalnutrition77,1146–1155)。进一步,存在指征:ldl-胆固醇每降低1%相当于冠心病相对危险性降低1%,特别是对于处于高心血管风险的受试者,像受到2型糖尿病影响的那些受试者(上述引用的marangoni&poli(2010))。摄入植物甾醇以降低ldl-胆固醇没有显示出副作用,除了处于类胡萝卜素缺乏风险的儿童和孕妇之外(nesteletal.(2001)eurjclinnutr.55,1084-1090;sioenetal.(2011)britishj.nutrition105,960–966.)。基于在成年人中植物甾醇的平均每日摄入量仅达到在150至400mg/天之间的事实,植物甾醇必须以较高浓度施用,以便从它们的促进健康性质受益(ntanios(2001)eur.j.clin.nutrition103,102–106.)。一种可能的施用方法是将植物甾醇掺入食品基质中。然而,从技术和食品质量的观点来看,食品中富集游离植物甾醇很难,因为它们不溶于水且难溶于膳食脂肪,同时它们的熔点相当高(约140–150℃)(上述引用的piironenetal.(2000))。因此,进行更多研究以发现克服这些限制的方法。用脂肪酸(fa)在a-环的c-3位酯化植物甾醇得到了植物甾醇酯(pe),提高了它们的脂质溶解度,降低了它们的熔点,且因此便于它们掺入到含脂肪的食品中(ostlund(2007)ann.rev.nutrition22,533-549.)。在现代功能食品配制中,植物甾醇酯目前已经被用作食品成分。人造奶油和可食用涂抹料是理想的介质,尽管奶油干酪、沙拉调料和酸乳酪也都用作递送系统(vaikousietal.(2007)j.agric.foodchem.55,1790–1798.)。从比利时市场上富含胆固醇的脂肪降低的食品如人造奶油和涂抹料的分析,推导出在这些产品的油相中应用的植物甾醇酯的浓度在10至50%的范围内,取决于产品类型(例如,轻人造奶油、具有黄油或橄榄油的人造奶油等)。然而,将植物甾醇酯加入到食品的油相中可能影响其结晶行为,并且因此可导致在制备过程期间出现问题或在终产品的宏观特性中出现问题(rodriguesetal.(2007)foodres.int.40,748-755,)。然而,关于该主题的基础研究非常缺乏。据我们所知,在文献中仅两次报道了加入植物甾醇酯影响可食用脂肪的物理性质。vuetal.(2004)foodres.int.37,175-180显示将自制的植物甾醇酯加入到液体玉米油中会引起不期望的植物甾醇酯结晶高于某一阈浓度。上述引用的rodriguesetal.(2007)研究了如何通过混合市售植物甾醇酯的混合物改变乳脂的结晶行为。他们显示将植物甾醇酯加入到乳脂会引起稠度更软和固体脂肪含量更低。然而,这些作者没有报道关于纯底物的熔融和多晶型行为的任何信息,也没有它们的掺合物的任何信息,因为没有进行差示扫描量热法(dsc)或x-射线衍射(xrd)分析。进一步,仅以两种不同浓度加入植物甾醇酯,对于含有乳脂的植物甾醇酯掺合物的相特性,仅给出有限的洞察力。实施例实施例1.加入β-谷甾醇基油酸酯对于“平衡状态”的棕榈油的结晶行为的影响材料β-谷甾醇(≥70%)和油酸(≥90%)购自sigmaaldrich(brondby,denmark)。棕榈油得自unilever(thenetherlands)。β-谷甾醇具有80.5%的纯度,无需进一步纯化使用。杂质为菜籽甾醇和β-谷甾烷醇(sitostanol),各自具有10%的最大浓度。β-谷甾醇基油酸酯的合成和纯化基于panpipatetal.(2013b)biochem.engin.j.70,55-62的方法合成β-谷甾醇基油酸酯。将β-谷甾醇与油酸在800ml己烷中0.2m浓度以1.0:1.0(mol/mol)的摩尔比例混合。将固定脂肪酶南极假丝酵母脂肪酶a(cala,codexis,pasadena,usa)以20%(β-谷甾醇的wt%)的量加入到所述掺合物中。在50℃下,在连续搅拌和62.5%(β-谷甾醇的wt%)分子筛的存在下,在具有机械搅拌器的1l密闭的反应器中进行反应48小时,以从溶剂除去水。通过在真空压力下过滤出固定脂肪酶和分子筛终止反应(sigma-aldrich,brondby,denmark)。将残余物用己烷洗涤,以除去任何底物或产物。通过薄层色谱(tlc)进行酯化反应产率的第一次粗略估计。因此,将10μl所得到的反应混合物与10μl的β-谷甾醇和作为参照的油酸一起施用于tlc。将所述板用两种不同的显影溶剂展开:首先用氯仿/甲醇/水(64:10:1,v:v:v)展开直到所述板的一半,并干燥,接着用氯仿/甲醇/乙酸(97.5:2.5:1,v:v:v)展开至接近所述板的顶部,并再次干燥。通过将所述板短暂地浸入硫酸溶液(在甲醇中的30%h2so4)中,接着在100℃下用吹风机加热所述板1分钟,来进行所述板上斑点的鉴别。β-谷甾醇和β-谷甾醇基油酸酯的斑点显示为紫色,而油酸的斑点为白色。β-谷甾醇、油酸和β-谷甾醇基油酸酯的保留因子(rf)值分别为0.63、0.47和0.91。基于β-谷甾醇斑点与由反应混合物得到的β-谷甾醇基油酸酯斑点的相对强度估计反应产率。产率显然低于90%,且估计在40%至60%之间。使用低压二氧化硅柱纯化合成的β-谷甾醇基油酸酯。使用填装300ml分散在己烷中的硅胶(sigma-aldrich,overrijse,belgium)的玻璃柱(4cm×40cm)从β-谷甾醇基油酸酯除去β-谷甾醇和油酸。首先,在60℃下,通过混合反应产物与八匙在己烷中硅胶5分钟,将10g的反应产物涂层在硅胶上,之后除去溶剂。将二氧化硅涂层的反应产物研磨成粉末,然后装载到所述柱上。然后,使1.8l的溶剂己烷/乙酸乙酯(40:1,v:v)流过所述柱,并将洗脱液收集在30ml的管中。如用tlc检测的,在该溶剂中β-谷甾醇、油酸和β-谷甾醇基油酸酯的rf值分别为0.00、0.00和0.35。使用tlc,通过将每个试管10μl施用于tlc板,检测每个管中β-谷甾醇、油酸和β-谷甾醇基油酸酯的存在。将所述板用氯仿/甲醇/水(64:10:1,v:v:v)展开直到所述板的一半,接着用氯仿/甲醇/乙酸(97.5:2.5:1,v:v:v)展开至接近所述板的顶部,并再次干燥。使用如上所述的硫酸溶液显影所述板上β-谷甾醇、油酸和β-谷甾醇基油酸酯的存在。收集仅含有β-谷甾醇基油酸酯的管,并蒸发溶剂。棕榈油和β-谷甾醇基油酸酯的脂肪酸组成通过甲基化棕榈油和油酸测定脂肪酸组成。以这种方式,形成“脂肪酸甲基酯”(fame),然后经由采用火焰电离检测的气相色谱(gc-fid)进行分离。通过将5mg的脂质、1ml的甲苯和2ml的1%硫酸加热至50℃过夜进行甲基化。然后,加入5ml采用水作为溶剂的5%氯化钠溶液,并用3ml的己烷萃取fame。采用冷柱上进样,用gc-fid(tracegcultra,thermofisherscientific,interscience,belgium)得到fame的分离和定量。在ecwax柱(长度:30m,内径:0.32mm,膜:0.25μm)(grace,belgium)上,使用特定温度时间程序(70℃-180℃(5℃/min)、180℃-235℃(2℃/min)、235℃(9.5分钟))分离fame。通过使用标准系列的35种不同fame(nucheck,usa)进行峰鉴别。采用用于windows软件的chromcard(interscience,belgium)进行峰面积的定量。该测定以一式三份进行(ryckeboschetal.(2012)jaocs89,189-198)。表1.β-谷甾醇基油酸酯和棕榈油的脂肪酸组成(%)脂肪酸棕榈油β-谷甾醇基油酸酯c14:01.0-c16:045.43.0c18:04.34.0c18:139.691.2c18:29.8-c24:1-1.7该值显示三次测量的平均值。误差为0.2%。掺合物的制备采用浓度范围10至90%的β-谷甾醇基油酸酯,以10%的组成间隔,制备β-谷甾醇基油酸酯与棕榈油的九种掺合物。在80℃的温度下,将纯脂质在烘箱中完全熔融。使熔融的纯脂质在锥形管中装配,并保持在80℃30分钟,同时采用涡旋定期地混合。结晶至“平衡”状态在该实施例中,显示加入β-谷甾醇基油酸酯对于“平衡”状态的棕榈油结晶的影响。首先,在15分钟期间,将样品在80℃下熔融,此后,将其置于10℃的水浴中进行快速冷却(约5℃/min)。根据现有的文献(aocs,1997a),使用在10℃下72h的时间-温度分布曲线使样品处于“平衡”状态。观察到当保持在10℃下比48小时更长时,棕榈油的dsc熔融焓和熔化曲线的峰最大值不再显著改变。在水浴中进行所描述的样品的回火。差示扫描量热法(dsc)采用装有自动采样器的dscq2000(tainstruments,newcastle,usa)和氮气作为吹扫气体,进行dsc实验。使用蓝宝石和铟进行基线校正,并使用空锅作为参照。给密封的铝锅(tainstruments,brussels,belgium)装填约10mg熔融的脂肪。将约10-20mg熔融的样品密封到tzero密封铝锅(tainstruments,brussels,belgium)中。在达到“平衡”状态之后,将样品以20℃/min加热至80℃。采用程序universalanalysis,通过使用水平基线整合熔融曲线,计算熔融焓(δh),即,在熔融期间释放的热量。棕榈油与β-谷甾醇基油酸酯的掺合物的熔融曲线显示一个在70℃的固定终点线性积分的峰。也使用universalanalysis确定熔融曲线中峰的峰最大值(tmax)。x-射线衍射在棕榈油与0、20、40、60、80和100%的β-谷甾醇基油酸酯的掺合物达到“平衡状态”之后,对其进行xrd分析。使用装有mar345图像板检测器(marresearch,norder-stedt,germany)的xenocsxeussx-射线照相机(xenocs,sassenage,france)取得x-射线散射图。genix3dmolybdenum超低散度x-射线光束源具有50kv(1ma)的功率,得到了的恒定强度光束。将约25-30mg熔融的样品密封在tzero密封铝锅(tainstruments,brussels,belgium)中。在达到“平衡”状态之后,将样品置于光束前面的温度控制的linkamdsc600台(linkamscientificinstruments,surrey,uk)上。在10℃的恒温下,记录组合的小角度x-射线散射(saxs)和大角度x-射线衍射(waxd)图。采用conex软件处理所有x-射线图,所述conex软件也使用空的dsc锅测量和采用山酸银样品的校准测量(gommes&goderis(2010)j.appl.crystall.43,352–355.)。偏振光显微镜(plm)对于plm,利用玻璃pasteur移液管,将每种掺合物和两种纯组分的一滴熔融均质样品转移到显微镜玻璃板。将该小滴盖上盖玻片。然后,将样品置于烘箱以再次熔融样品,以便得到均匀且均一的样品层厚度。采用装有数字照相机infinity2(lumeneracorporation,canada)的偏光显微镜olympusbx51(olympusopticalco.ltd.,japan)研究样品的微观结构。在达到“平衡状态”之后,将样品置于温度控制的linkampe120片(linkamscientificinstruments,uk)上。使用infinity捕获软件(lumeneracorporation,canada),以40x和100x的放大倍率采集图像。结果纯β-谷甾醇基油酸酯差示扫描量热法β-谷甾醇基油酸酯的熔融曲线显示在图2中。在该熔融曲线中观察到一个单峰。β-谷甾醇基油酸酯的甾醇基部分由不同类型的植物甾醇组成。纯β-谷甾醇基油酸酯的dsc测量显示用一个脂肪酸酯化的不同甾醇的这些混合物由于它们良好的可溶混性实际上表现得像纯组分。因此,所观察到的作用可能完全归因于植物甾醇酯中脂肪酸的类型,而不是不同植物甾醇之间的变化。所述熔融曲线的峰最大值为29.9℃±0.9℃,其与po的峰最大值并没有显著不同。该值对应于文献中所显示的熔点(leeson&(2002)foodres.int.35,983-991)。熔融焓为53.9j/g±2.1,其与po的熔融焓并没有显著不同。该值也与上述引用的文献中显示的熔融焓接近(leeson&(2002))。因为仅存在一个单峰,在加热期间不会出现多晶型转化,并且β-谷甾醇基油酸酯以一个级分结晶(panpipatetal.(2013a)j.coll.interfacesci.407,177-186.)。x-射线衍射在图3中,在p-油酸酯的waxd图中观察到七个峰:两个小峰位于2θ=4.04°和2θ=5.33°一个强峰位于2θ=6.76°一个宽的双峰位于2θ=8.15°和2θ=8.41°另一个强峰位于2θ=9.68°和最后一个小峰位于2θ=10.72°图4显示saxs图。三个峰可见,从在位置2θ=0,73°的中间峰开始,接着是在位置2θ=1,48°的尖峰和在2θ=2,20°的小峰。因为在saxs和waxd图中都存在几个峰,所以β-谷甾醇基油酸酯显然以结晶相存在(dijkstraetal.(2007),in“thelipidhandbook”.thirdedition.taylor&francisgroup,bocaraton)。为了解释这些峰,不能使用与tag脂质例如棕榈油相同的术语。关于提及相同的结晶形式,植物甾醇酯的分子结构也与tag的分子结构十分不同。在过去,尚未研究来自植物甾醇酯的xrd数据。因为胆甾醇基酯(ce)和植物甾醇酯具有类似的分子结构,所以这项工作比较了β-谷甾醇基油酸酯的xrd数据与ce的xrd数据。与ce相比,在β-谷甾醇基酯中出现额外的乙基,跳出了平面。ginsburgetal.(1984)[prog.lipidres.23,135-167]显示处于结晶相、液相和介晶相的胆甾醇油酸酯(ce油酸酯)的xrd图。ce油酸酯的结晶相的xrd图大致对应于纯pe油酸酯的xrd图。在ce油酸酯中,由于ce油酸酯的层状结构,在saxs图中存在多个峰。因此,β-谷甾醇基油酸酯可能也发现于层状结构中(souzaetal.(2011)chem.physicslipids164,664-671.)。对于具有至少六个碳原子的脂肪酸链的ce,已经描述了三种结晶形式:“单层1型”、“单层2型”和“双层”。分子间链-链相互作用、环-环相互作用和链-环相互作用的相对重要性是确定形成哪种结晶形式的因素。这些相互作用决定了所述结晶形式在一定温度下的相对稳定性。所有三种结晶形式都属于单斜晶结构(上述引用的ginsburgetal.(1984))。ce油酸酯的结晶形式为单层2型,特征在于作为在单层之间的层厚,这些晶体是单斜晶,每个晶胞具有两个分子(上述引用的ginsburgetal.(1984);guo&hamilton(1995)biophysicaljournal68,2376-2386);上述引用的souzaetal.(2011);das&de(2011)chem.phys.lipids164,33-41)。该值也反映在β-谷甾醇基油酸酯的saxs图中,但是强度比在位置2θ=1,48°的峰低得多。对于单层1型,该层厚是相当典型的。对于双层结构,具有距离的第三峰的层厚也是典型的(dorset(1987)j.lipidres.28,993-1005;上述引用的das&de(2011))。所述峰的相对强度取决于分子长轴相对于单层平面的定向。对于一些峰而言降低强度是由于微晶的优选定向的影响引起的(上述引用的das&de(2011))。另外,上述引用的dorset(1987),也引用了几个距离,对应于ce-肉豆蔻酸酯的双层结构,其也在β-谷甾醇基油酸酯的waxd中被发现。具有距离的峰可能是由于脂肪酸链的并排堆叠引起的,且距离可以表明环的并排堆叠(上述引用的dorset(1987))。单层2型ce晶体中的主导相互作用是环-环和链-链(上述引用的ginsburgetal.(1984))。所述分子是反平行的。相对单层的酰基链是连结的(interlocked),但是彼此紧靠着松散堆叠,在各层之间形成界面。它们没有构成特定的“亚晶胞”结构(上述引用的gao&craven(1986)j.lipidres.27,1214-1221;das&de(2011))。就ce油酸酯而言,不饱和链以使所述链的线性度尽可能保持良好的方式弯曲(craven&guerina(1979)chem.phys.lipids29,91-98;上述引用的ginsburgetal.(1984))。观察到所述油酸酯链的广泛一致性,外部六个原子围绕顺式双键形成扭结区域(kinkregion)(上述引用的gao&craven(1986)。得出结论β-谷甾醇基油酸酯在“平衡”状态下形成双层结构。偏振光显微镜图5显示在10℃下回火72小时之后,β-谷甾醇基油酸酯的晶体网络。清楚地观察到晶体,其也是xrd结果所预期的。所述晶体是针状的,这也与ce油酸酯的情形相同(上述引用的das&de(2011))。所述针晶自身已经如同球晶一样结构化。球晶包含偏振交叉,其具有与偏振面平行的臂。对于ce,也观察到这些(lundberg(1975)chem.phys.lipids14,309-312)。球晶的直径在30至230μm的范围内。β-谷甾醇基油酸酯球晶主要是灰度着色的,而且微弱地显示一些黄色、橙色和蓝色。棕榈油与β-谷甾醇基油酸酯的掺合物差示扫描量热法棕榈油与β-谷甾醇基油酸酯的掺合物的熔融曲线显示在图6a和6b中。每次观察每个浓度的一个峰。从纯棕榈油到含有30%的β-谷甾醇基油酸酯的棕榈油,峰降低且峰最大值转移到较低温度。从含有30%的β-谷甾醇基油酸酯的棕榈油到含有40%的β-谷甾醇基油酸酯的棕榈油,峰似乎保持相同尺寸,但是显著地迁移至较低温度。从40%到60%β-谷甾醇基油酸酯的掺合物,在接近相同的温度下,峰大部分更尖锐且更大。从含有60%的β-谷甾醇基油酸酯的棕榈油到含有70%的β-谷甾醇基油酸酯的棕榈油,峰开始迁移回更高的温度,而峰大小没有任何变化。从70%的β-谷甾醇基油酸酯掺合物到80%的β-谷甾醇基油酸酯掺合物,峰变得更尖锐且更大,并转移到更高温度。从含有80%的β-谷甾醇基油酸酯的棕榈油到含有90%的β-谷甾醇基油酸酯的棕榈油,峰转移到更高温度,而峰大小没有任何明显变化。从含有90%的β-谷甾醇基油酸酯的棕榈油到100%β-谷甾醇基油酸酯,峰变得更尖锐且更大,且峰最大值增加。图7显示棕榈油与β-谷甾醇基油酸酯的掺合物在“平衡”下的峰最大值。所述峰最大值,对应于每个浓度的β-谷甾醇基油酸酯,为五个样品的峰最大值的平均值。直至加入20%的β-谷甾醇基油酸酯,峰最大值不会显著地降低。在加入超过20%的β-谷甾醇基油酸酯,在50%的浓度下,峰最大值降低至最小24.5℃±0.1℃。当随后提高β-谷甾醇基油酸酯的浓度时,峰最大值再次逐渐升高。如上提及的,在纯棕榈油和100%的β-谷甾醇基油酸酯之间没有观察到显著性差异,此外,对于含有10%、20%和90%的β-谷甾醇基油酸酯的棕榈油,这些峰的界限没有显著不同。图7也可以看作是二元棕榈油/β-谷甾醇基油酸酯体系的相位图中的液相线(marangoni&wesdorp(2013)pharmacol.res.61,193-199)。所述相位图显示共晶行为,因为在一些β-谷甾醇基油酸酯浓度下,峰最大值比纯棕榈油和纯β-谷甾醇基油酸酯的峰最大值更低。在50%的β-谷甾醇基油酸酯的浓度下得到的共晶最少。掺合物的共晶行为是由于固相的不相容性引起的(上述引用的dijkstraetal.(2007))。β-谷甾醇基油酸酯和棕榈油在固相中不可混溶的原因是由于分子结构的差异,其意味着它们不适合单晶形式(上述引用的dorset(1987);lidaetal.(2002)jaocs11,1137-1144;saadietal.(2011)journaloffoodsci.76,c21-c30)。当将熔融焓绘图为β-谷甾醇基油酸酯浓度的函数时(图8),观察到其降低直到30%的β-谷甾醇基油酸酯。在30%的β-谷甾醇基油酸酯的浓度下,熔融焓的降低达到最小值45.8j/g±1.7,然后再次逐渐增加。从70%的β-谷甾醇基油酸酯,达到平稳值,其与100%的β-谷甾醇基油酸酯的熔融焓没有显著不同。x-射线衍射图9和10显示在10℃下回火72小时之后,棕榈油与β-谷甾醇基油酸酯的掺合物的waxd和saxs图。在saxs中,β-谷甾醇基油酸酯的第一个峰特征从20%的β-谷甾醇基油酸酯向前可见。在waxd中,20%的β-谷甾醇基油酸酯曲线也趋向于具有位置2θ=6.76°的β-谷甾醇基油酸酯的峰。因此,β-谷甾醇基油酸酯已经从20%结晶,其也是通过dsc预期的。40%和60%的β-谷甾醇基油酸酯掺合物的saxs和waxd图清楚地显示了β-谷甾醇基油酸酯和棕榈油两者的峰。在高浓度的β-谷甾醇基油酸酯下,棕榈油继续形成晶体。除了典型的棕榈油和β-谷甾醇基油酸酯的峰之外,没有新的峰。β-谷甾醇基油酸酯和棕榈油分别彼此结晶,并且不是以单晶形式结晶。在所有浓度的β-谷甾醇基油酸酯下,棕榈油以β主要的多晶型物结晶。在所有掺合物中,β-谷甾醇基油酸酯的结晶形式也是相同的。对应于一个晶形的所有衍射峰的面积都将与该形式的量成比例,但是比例因子可以根据晶体结构变化。这意味着不同结晶形式的比例不能直接来源于在它们的相应峰下的相对表面积(surfaces)(shukatetal.(2012)j.thermalanal.calorimetry,108,153-161)。视觉观察到棕榈油峰的相对面积减小且β-谷甾醇基油酸酯峰的相对面积随β-谷甾醇基油酸酯的浓度增加而增加。可以看到随着β-谷甾醇基油酸酯的浓度增加,来自棕榈油的β主要的多晶型物的量降低,且β-谷甾醇基油酸酯晶体的量增加。偏振光显微镜图11显示与不同浓度的β-谷甾醇基油酸酯有关的显微镜照片。如已经从xrd结果显然的,棕榈油和β-谷甾醇基油酸酯分别结晶,且形成它们自身的晶体。在具有10%的β-谷甾醇基油酸酯的掺合物中,没有观察到β-谷甾醇基油酸酯晶体,而在具有20%的β-谷甾醇基油酸酯的掺合物中,观察到具有尺寸约16至42μm的明亮的、针状β-谷甾醇基油酸酯晶体紧靠着棕榈油晶体。在具有30%的β-谷甾醇基油酸酯的掺合物中,观察到最大的β-谷甾醇基油酸酯针状晶体,且具有约23至150μm的尺寸。从该浓度开始,β-谷甾醇基油酸酯晶体聚集在一起,尽管它们不会形成球晶。在具有40至90%的β-谷甾醇基油酸酯的掺合物中,β-谷甾醇基油酸酯的针状晶体较小,具有约7至25μm的尺寸,其没有比棕榈油晶体大多少。从80%的β-谷甾醇基油酸酯开始,棕榈油晶体在图像中不再能够清楚地区分。针状的β-谷甾醇基油酸酯晶体是非常亮的,且显示一些橙色和绿色。在较高浓度的β-谷甾醇基油酸酯下,β-谷甾醇基油酸酯的晶体似乎越来越将自身结构化成球晶。球晶的生长是过饱和度的函数,正如成核和生长过程一样(上述引用的marangoni&wesdorp(2013))。仅仅100%的β-谷甾醇基油酸酯被明确地发现是球状的。直至且包括90%的β-谷甾醇基油酸酯,球晶生长和排列的驱动力也可能太小。球晶生长是由于扩散不稳定性引起的,而且由于在生长前沿新的微晶的三种成核模式。球晶生长是二次成核过程(abeetal.(2002)liquidcrystals29,1503-1508;上述引用的marangoni&wesdorp(2013))。实施例2表2显示大量市售人造奶油产品的组成产品和产品包装信息的分析显示含有植物脂肪的所有产品都包含19-31g饱和的脂肪/100g脂肪,并且降低胆固醇的人造奶油包含15至41g/100g脂肪范围的植物甾醇/植物甾烷醇酯。表2.市售人造奶油产品的组成包含植物甾烷醇的产品用##指示。实施例3β-谷甾醇基油酸酯与菜籽油的掺合物的制备根据实施例1中描述的方法制备β-谷甾醇基油酸酯。掺合物由自制的β-谷甾醇基油酸酯(pe油酸酯)与菜籽油制成。所述掺合物的pe油酸酯的浓度为30、40和50%。pe油酸酯的纯度>99%(如通过薄层色谱确定的)。为了比较这些掺合物与现有人造奶油的脂肪级分的sfc特征,使用3种市售的人造奶油:benecoltm“bakkenensmeren”,beceloriginaltm和becelproactivtm。(这些人造奶油的组成概述在表2中)。根据上述引用的ryckeboschetal(2012)的方法确定所述pe油酸酯的脂肪酸组成。根据上述引用的ryckebosch(2012)方法分析pe油酸酯的甾醇组成。将人造奶油的代表性样品在80℃的烘箱中熔融。然后,将液体人造奶油溶于过量的乙醚中。通过加入无水na2so4除去水,并在定期搅拌下静置30分钟。通过经折叠过滤器过滤除去na2so4。将残余物用乙醚重复洗涤,直至黄色消失至明确地所有脂质都包含在滤液中。将滤液中的乙醚用旋转蒸发仪蒸发。脂肪提取的产率与人造奶油包装上声称的脂肪含量相当。也使用上述方法确定人造奶油的脂肪级分的脂肪酸组成,并与包装上的值进行比较。根据用于非稳定脂肪的aocs方法cd16b-93(直接法),由以下脂肪确定固体脂肪含量(sfc):在菜籽油中30、40、50%pe油酸酯的掺合物和脂肪级分beceloriginaltm、becelproactivtm和benecoltm。将脂肪在80℃下熔融30分钟,然后在0℃下保持过夜(16小时),接着在每个所选择的测量温度:10、20、30、35、40和45℃下保持60-65分钟。对于所有脂肪以3份进行sfc测定。将结果显示在表3和图12中。表3.pe油酸酯的脂肪酸含量该值显示三次测量的平均值。误差为0.2%。表4.pe油酸酯的甾醇组成甾醇含量(%)β-谷甾醇80.9β-谷甾烷醇12.9菜籽甾醇6.2该值显示三次测量的平均值。误差为0.2%。表5菜籽油中pe-油酸酯的不同组成和不同的市售人造奶油的固体脂肪含量(sfc)值(三次重复的平均值±标准偏差)样品30℃35℃benecoltm3.0±0.21.7±0.1beceloriginaltm3.5±0.31.8±0.5becelproactivtm3.5±0.41.5±0.130%pe-油酸酯2.7±0.12.0±0.040%pe-油酸酯4.0±0.12.8±0.250%pe-油酸酯5.3±0.14.1±0.0这些结果的表示也参见图12。基于sfc分析的结果,得出结论:与菜籽油的掺合物中pe油酸酯的最佳浓度是30%,因为该掺合物的sfc特征与市售人造奶油的sfc特征最接近。30%的pe油酸酯掺合物的脂肪酸特征与专利ep1011343b1中描述的最佳脂肪混合物的脂肪酸特征也非常类似(参见第12页表4,掺合物1和2)。基于这些数据的外推,具有25%的pe油酸酯的掺合物也适于制备人造奶油。经由dsc,测试了在具有pe-油酸酯的掺合物中液体脂肪种类的影响,但这证实对于热性质没有任何影响(结果没有显示)。因此,例如也可以使用葵花籽油代替菜籽油。在加入另一类型的脂肪(其充当硬浆)下,可以使用具有20%或更低浓度的pe油酸酯的掺合物。替代油酸,植物甾醇也可以用市售脂肪如橄榄油、高油酸葵花籽油、高油酸大豆油、高油酸红花油或高油酸芥花油进行酯化。由于pe油酸酯和市售可获得的高油酸油之间的脂肪酸特征有小的差异,sfc脂肪掺合特征则可能稍有不同。例如因为高油酸葵花籽油包含约10%的亚油酸和80%的油酸,所以预期脂肪掺合物的sfc特征稍低于具有pe油酸酯的掺合物的。对于包含约78%的油酸和13%的亚油酸的高油酸红花油,也是如此。在另一方面,由于橄榄油的脂肪酸组成中的饱和脂肪酸的百分比为约13%,以及高油酸大豆油的脂肪酸组成中的饱和脂肪酸的百分比为约9%,所以预期脂肪掺合物的sfc特征稍高于pe油酸酯掺合物的。这在下述实施例中得到证实。实施例4:作为质构剂的甾醇酯使用具有高油酸含量(至少70%)的两种不同种类的脂肪进行木甾醇的酯化:橄榄油和高油酸葵花籽油。如通过h-nmr确定的,所合成的甾醇酯的纯度大于99%。所述甾醇酯不包含游离甾醇,且仅包含非常少量的游离脂肪酸,如表6所示。通过由游离脂肪酸形成二甲基酰胺衍生物,随后用gc-fid分离和检测,进行总游离脂肪酸含量的测定,如gheysenetal.(foodchemistry2018,441-450)所述的。进行总游离脂肪酸的测定,一式三份。表6.不同甾醇酯的平均总游离脂肪酸含量与标准偏差表7.不同种类的甾醇酯、棕榈油和棕榈硬脂的脂肪酸组成根据上述引用的ryckeboschetal(2012)的方法确定。所述值显示三次测量的平均值。误差为0.2%。含有来源于高油酸葵花籽油和橄榄油的脂肪酸的甾醇酯的脂肪酸组成是高度不饱和的,二者都包含超过70%的油酸。相反,棕榈油和棕榈硬脂包含多得多的饱和脂肪酸。棕榈油中的饱和脂肪酸含量几乎为50%,且在棕榈硬脂中,其甚至上升至67%。表8.含有来源于高油酸葵花籽油和橄榄油的脂肪酸的甾醇酯的甾醇组成甾醇含量(%)β-谷甾醇75菜籽甾醇10其它15表9.甾醇酯、棕榈油和棕榈硬脂的脂肪含量(sfc)所述值显示三次重复的平均值±标准偏差。如上解释的,对于非稳定脂肪,根据aocs方法cd16b-93(直接法)测定sfc。这些数据也存在于图13中。在每个温度下,两种甾醇酯的sfc都高于棕榈油的。该结果是非常出人意料的,因为棕榈油包含比所述甾醇酯多得多的饱和脂肪酸。此外,直至20℃的温度,甾醇酯的sfc与棕榈硬脂的sfc类似,棕榈硬脂包含比棕榈油甚至更多的饱和脂肪酸。甾醇酯且特别是含有来源于高油酸葵花籽油的脂肪酸的甾醇酯的sfc特征,比棕榈硬脂的sfc特征更陡,特别是在20℃至30℃之间的温度范围中。这具有的好处是在高于37℃的温度下,甾醇酯的剩余sfc比棕榈硬脂的更低。含有来源于高油酸葵花籽油的脂肪酸的甾醇酯在40℃下已经几乎完全熔融,保证了在以任何浓度与液体脂肪的掺合物中没有任何蜡质口感。在高于37℃的温度下,含有来源于橄榄油的脂肪酸的甾醇酯的sfc高于含有来源于高油酸葵花籽油的脂肪酸的甾醇酯的sfc,可能是因为前者包含由甾醇的饱和脂肪酸酯组成的更高熔融的甾醇酯级分。由于含有来源于高油酸葵花籽油或橄榄油的脂肪酸的甾醇酯具有非常类似于常规硬浆(棕榈油和棕榈硬脂)的sfc特征,可以得出结论它们可以用于含有液体脂肪的掺合物中,作为常规硬浆的替代。使用装有100n测压元件和圆筒形探针(直径6mm)的质构仪(textureanalyzer)(lloydinstruments模型lf+),进行不同种类的甾醇酯与棕榈油和棕榈硬脂的结构分析。给具有直径30mm和高度70mm的塑料罐装满11.5g的样品。然后,将该样品在80℃下熔融30分钟,此后置于10℃的水浴中快速冷却。将样品保持在10℃下72小时,使它们处于动力学稳定状态。该回火之后,通过以10mm/min的恒定速度推动探针穿透样品至10mm的距离,获得样品的力-距离变形曲线。脂质的硬度定义为穿透样品所需要的最大力。表10:不同种类的甾醇酯、棕榈油和棕榈硬脂的硬度所述值显示四次重复的平均值±标准偏差。如通过单向anova结合tukey试验所证实的,上标中有不同字母的值显著不同。结果表明在10℃下,两种甾醇酯比棕榈油更硬几乎四倍。这是令人惊奇的结果,因为在10℃下,所述甾醇酯的sfc比棕榈油的sfc仅高几乎两倍。此外,两种甾醇酯的硬度都与棕榈硬脂的类似。因此,产生与高度饱和脂肪相同硬度的高度不饱和脂肪,其中一些之前还没有报道。实际上,该结果违反了脂肪结晶的所有当前“规则”。尽管它们的脂肪酸特征有差异,但是两种甾醇酯在10℃下的硬度并不是显著不同。这具有的好处是来源于高油酸葵花籽油的甾醇酯可以得到与来源于橄榄油的甾醇酯相同的硬度,但是具有的饱和脂肪酸的量更低。实施例5:根据本发明的包含质构剂的脂质掺合物(lipidblends)用具有不同重量比的甾醇酯和菜籽油和不含硬浆的不同种类的甾醇酯制备几种脂质掺合物。不同脂质掺合物的重量比显示如下。测定不同脂质掺合物和不同市售人造奶油的固体脂肪含量(sfc)。表11显示三次重复的平均值±标准偏差。如上解释的,对于非稳定脂肪,根据aocs方法cd16b-93(直接法)测定sfc。图14和15也显示包含分别来源于高油酸葵花籽油和橄榄油的甾醇酯的不同脂质掺合物的sfc特征。市售人造奶油的sfc特征也显示在图12中。表11:不同脂质掺合物和不同市售人造奶油的固体脂肪含量(sfc)所得到的sfc特征清楚表明脂质掺合物1至12可用于制备其中需要固体脂肪赋予最终食品结构的含脂质食品。通常,在每个温度下,包含含有来源于高油酸葵花籽油的脂肪酸的甾醇酯的脂质掺合物,具有比包含相同浓度的含有来源于橄榄油的脂肪酸的甾醇酯的脂质掺合物稍微更低的sfc。这是可预期的,因为相比于含有来源于橄榄油的脂肪酸的甾醇酯,含有来源于高油酸葵花籽油的脂肪酸的甾醇酯的脂肪酸组成包含更少的饱和脂肪酸。通过与市售人造奶油的sfc特征相比,可以得出结论:脂质掺合物2至9非常适用于普通餐用人造奶油和涂抹料。脂质掺合物1在可涂抹的餐用人造奶油和涂抹料中使用也可能太软。当在可涂抹的餐用人造奶油中使用时,脂质掺合物10至12将可能在口腔中引起蜡质回味,因为在高于30℃的温度下,在这些脂质掺合物中的sfc太高(miskandaretal.(2005)asiapacjclinnutr.14,387-395)。然而,这些脂质掺合物仍然可用于其他种类的人造奶油中,如例如酥饼用人造奶油(puffpastrymargarine),其中在高于37℃的温度下这种较高的sfc值不会引起不期望的口感。因此,可以得出结论,在可涂抹的餐用人造奶油中获得期望质地的典型浓度为20至35%的含有来源于橄榄油的脂肪酸的甾醇酯或25-45%的含有来源于高油酸葵花籽油的脂肪酸的甾醇酯。实施例6:包含富含油酸的甾醇酯的软餐用涂抹料的制备制备包含来自实施例4的不同种类的富含油酸的甾醇酯的软餐用涂抹料。制备具有典型配方的模型软餐用涂抹料,其在脂质相中包含液体油(例如,菜籽油)、富含油酸的甾醇酯和乳化剂(0.4%的甘油单酯和甘油二酯和0.2%的大豆卵磷脂)且在水相中包含1.5至2.5%的食盐和0.01%的防腐剂(例如山梨酸钾)。根据涂抹料的典型制备方法,首先,通过下述来制备脂质相:混合完全熔融的甾醇酯与液体油,同时加热,随后加入乳化剂。通过将所述盐和防腐剂溶于水中分别地制备水相。然后,在约43℃的温度下,通过混合所述脂质和所述水相制备乳液。任选地,将所述乳液巴氏杀菌以避免微生物污染。然后,使该乳液经过刮板式表面换热器(sshe),以诱发脂质结晶,且随后经过销工作单元(pin-worker),其中所述冷却的乳液完成其结晶,并且其中形成期望的人造奶油质地。最后,将所述人造奶油填装在桶中[miskandar(2005)asiapac.j.clin.nutr.,14,387–395]。通过人造奶油中脂质相的总量和按照所建议的植物甾醇的每日摄入范围,确定人造奶油中油相的甾醇酯浓度。制备具有不同脂质含量的四种人造奶油。表12显示不同涂抹料的脂质相的甾醇酯和菜籽油含量,其取决于总脂质含量。所述涂抹料的甾醇酯含量被设定的目标为20g/100g,其相当于甾醇含量12g/100g,并且当人造奶油消耗为20g/天时其确保了每日摄入2.4g的甾醇。例如,如果脂质相包含33%的甾醇酯,则由60%的脂质相组成的中等-脂肪人造奶油将提供足够高的每日植物甾醇剂量(如果每日消耗20g的人造奶油)。表12.不同涂抹料的脂质相的脂质含量与甾醇酯和菜籽油含量表13显示不同涂抹料的饱和脂肪酸含量,取决于用于甾醇酯合成的油种类,且考虑了涂抹料的脂质组成及甾醇酯和菜籽油的脂肪酸组成。注意到,所述涂抹料不含棕榈油且应当包含小于3.5g的饱和脂肪酸/100g产品,而目前市售的类似产品仍然包含7直至17g的饱和脂肪酸/100g产品。表13.不同涂抹料的饱和脂肪酸含量(%)用于甾醇酯合成的油的种类abcd橄榄油3.52.82.21.6高油酸葵花籽油3.12.51.91.2如在其它研究中经常进行的,首先,使用冰淇淋制造机小规模(约1l)制备涂抹料,所述冰淇淋制造机实际上是sshe、非常便宜、易于使用且能够优化配方[shah(2014)j.am.oilchem.soc.91,309–316;saadi(2012)foodchem.133,1485–1493;pande(2013)biocatal.agric.biotechnol.2,76–84.]。在4℃下储存一周之后,使用质构仪分析所制备的人造奶油的宏观特性如硬度和铺展性,并与市售人造奶油的相同性质进行比较[steen(2014)foodbioprocesstechnol.7,2855–2864]。考虑到获得的机械学见解(mechanisticinsights),所述涂抹料也接受热量分析和形态分析(使用x-射线和显微方法)。进一步,使用pnmr测定所述涂抹料的小滴尺寸。在下一步中,以中试规模(25l)制备涂抹料。使用中试工厂用于制备人造奶油具有的好处是它还包含紧挨着sshe的销工作单元(pin-worker)用于涂抹料制备。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1