覆膜支架及其制造方法与流程
本发明涉及医疗器械技术领域,特别涉及一种覆膜支架及其制造方法。
背景技术:
冠状动脉破裂、穿孔约占经皮冠状动脉介入治疗(PCI)的0.1%~2.5%左右,一旦发生后果严重,可引起急性心脏压塞,需紧急开胸止血,如处理不及时或处理不当甚至可以引起死亡,远期可以出现假性动脉瘤、冠状动脉心室瘘等。近年的临床研究结果发现药物洗脱支架(DES)植入,术后的支架贴壁不良是常见现象,因此支架释放后较常采用高压后扩张。随着新的PCI技术的发展和应用,介入医生处理越来越复杂的冠状动脉病变,如严重迂曲病变、严重钙化性病变,慢性闭塞性病变(CTO)介入治疗的开展。上述因素导致近年冠状动脉穿孔发生率有增加的趋势。
20世纪90年代初,随着冠状动脉介入治疗由单纯球囊扩张、金属支架本体至药物洗脱支架的进展,越来越多的患者从PCI中获益,然而在覆膜支架应用之前,超过半数的冠状动脉穿孔患者需紧急外科手术治疗。冠状动脉I型穿孔一般采取保守的治疗办法,静脉输入鱼精蛋白使活化凝血时间(ACT)<200s,该治疗方法可能会引起血小板聚集、支架血栓、过敏反应、心脏骤停、心肌梗死或其他不良反应4。II型以上穿孔可行球囊低压力扩张穿孔部位,但可造成病变远段血管血流阻断、心肌缺血坏死。因此,临床上急需一种安全、有效的覆膜支架。
覆膜支架是指金属支架本体内面或外面部分或完全覆盖膜性材料的人工体内移植物。早在19世纪80年代,Balko等学者就开展了覆膜支架的体外设计、研究,通过将支架本体外覆聚乙烯膜,经股动脉导入成功治疗了绵羊腹主动脉瘤。覆膜支架既保留了普通支架的支撑功能,又兼具膜性材料的特性,能有效地改善病变血管的异常血流动力学,处理很多普通支架所不能解决的病变,在血管畸形性病变和急慢性血管损伤等血管病变的治疗中得到广泛的应用。在冠状动脉病变中,覆膜支架作为一种具有特殊结构和功能的治疗手段,对传统的治疗手段(外科手术、传统支架治疗及药物治疗)是一种补充。
临床上曾用或在研的覆膜支架主要有:
1、聚四氟乙烯(PTFE)覆膜支架:(1)Jostent Graftmaster球囊扩张支架:唯一中国上市的冠状动脉覆膜支架(目前已停产),支架由双层316L不锈钢材料制成,两层支架中间镶嵌一层PTFE薄膜。由于PTFE薄膜具有较高的生物相容性,且具有较高的延伸率(薄膜可扩张4-5倍而不发生撕裂或收缩)。此外,这种高分子聚合物膜上的负电荷能抑制血栓蛋白在组织表面聚集,且能抑制血小板活动和血栓形成。多个临床研究及病例报告均表明Jostent Graftmaster支架可有效的治疗冠状动脉穿孔及冠状动脉瘤,尽管其还有许多临床问题(双层支架造成的支架输送性较差、支架内血栓、支架内再狭窄)尚未解决,曾经仍然是许多介入导管室必备的抢救器材。(2)Symbiot支架:由一个双层PTFE薄膜包绕在镍钛支架周围。Symbiot支架的特点是镍钛支架置于一个有孔的薄膨化聚四氟乙烯(ePTFE)多聚体膜内。设计意图为通过ePTFE膜和支架本体的扩张释放,以减少支架置入过程中的斑块或血栓引发的栓塞。Symbiot支架同样存在着支架输送系统较为坚硬,缺乏纵向柔顺性,难以通过弯曲的颅内血管等不足。STROMBOLI研究显示与金属支架本体对比,Symbiot支架在变性伴纤维化的桥血管病变的介入治疗中并没有取得更优的短期及长期临床获益,波士顿科学公司随后停止了该产品的进一步研发。(3)覆膜支架由钴基合金支架和聚四氟乙烯膜组成,支架结构由分节段的呈正弦波形的“n”形支撑杆组成,节段间通过2个非对称连接点连接,同时ePTFE膜厚度仅30μm-50μm,使得支架整体获得极佳的输送性及通过性。然而,由于中段被覆膜与金属支架大部游离,植入后由于血流冲击,病变部位的覆膜容易与支架分离,局部形似动脉瘤颈残留。目前临床上主要用于颅内动脉瘤的治疗。
2、心包覆膜支架:Over and under支架和Aneugraft支架(国内未上市),支架平台由激光旋磨的316L不锈钢材料构成,其表面由单层马心包膜(100μm)所覆盖。心包膜覆盖于支架本体主体部分,从而使支架与血管内膜贴合紧密,且在支架边缘下用聚丙烯缝合线缝合。单层金属支架平台的设计使得此类支架较之PTFE覆膜支架有着更为优越的输送性,在扭曲的血管段有较为良好的通过性,目前已在国外应用于颅内动脉瘤、冠状动脉瘤的治疗,但其长期有效性仍需大型临床随机研究的观察、验证。同时,由于此类支架需在灭菌的戊二醛溶液中进行保存,当支架离开戊二醛保存液需经过2次2min生理盐水冲洗,因此不能立即应用于术中。
3、自制自体静脉覆膜支架:自体静脉覆膜支架在冠状动脉穿孔治疗中已有应用,支架需由术者于术中进行组装,因而需要持续球囊扩张封闭穿孔部位以争取支架制作时间。组装支架所需的隐静脉、肘前静脉或头部浅静脉需经手术截取,并用缝合固定于金属支架本体(BMS)上。与人工材料相比,自体静脉材料有很多优点,如内膜光滑,弹性比较适合动脉管腔,壁薄、体积较小容易经导管输送,同时静脉壁有足够的强度抵抗动脉压力。然而,由于制作工序较为复杂,同时需手术截取部分静脉组织,因而未在临床广泛推广。
4、自制PTFE覆膜支架:由于目前国内市场上暂时没有冠状动脉脉专用覆膜支架(Jostent Graftmaster已停产),介入导管室在发生冠状动脉穿孔等急危重症又缺乏强有力的心外科支持时,只能选择自制覆膜支架,其原理与Jostent Graftmaster覆膜支架类似,即使用两个金属支架本体手工压握包夹一个相应直径及长度的支架球囊PTFE膜(三明治结构),有报道部分病例使用该器械成功挽救患者生命,但自制覆膜支架依然存在很多问题与不足,例如:支架整体外径较大降低支架整体输送性;手工压握的双层支架降低了支架的通过性,在通过穿孔部位时存在支架脱载的风险;病变部位术后存在多层金属支架成分加大了支架内血栓的发生机率。
除此以外,覆膜支架还广泛应用于动脉瘤的介入治疗。冠状动脉瘤是指冠状动脉的局限或弥漫性扩张,其直径为邻近正常冠状动脉段的至少1.5倍,其发病率大约为0.3%-4.5%,主要发生于男性,好发于右侧冠状动脉。近年来随着介入材料和介入技术的不断发展,血管内治疗已成为动脉瘤的首选治疗方法。血管内介入治疗以其微创的特点,也迅速为广大介入医师及动脉瘤患者所接受。这其中,覆膜支架植入是一种常用的手术方法。完全释放后的覆膜支架会覆盖病变血管,隔绝血管病变部位并形成新的血流通道,从而使动脉瘤丧失血液供应,达到治疗目的。传统的覆膜支架通过覆膜物理隔绝动脉瘤,但不能实现对动脉瘤的积极治疗,同时覆膜不可降解,导致覆膜永久存在,阻碍血管内皮化,存在血栓风险,需要进行长期抗血小板治疗。再者,覆膜支架在封堵动脉瘤瘤颈的同时,往往不可避免的封堵正常分支血管,造成分支血管供血区域缺血,导致一系列并发症的发生。
临床上除了采用植入覆膜支架外,还可选择:1、栓塞疗法,用于治疗存活心肌较少、直径较小血管,远端血管,完全闭塞血管,采用微弹簧圈、明胶海绵等将穿孔堵死,缺点是将血管直接封闭,导致病人该处持续心肌缺血。2、急诊外科手术修补,临床统计大约30%~40%的冠脉穿孔患者对于上述手术处理均无效果,需要对患者行外科手术,然而,由于患者在PCI手术中用了多种抗血栓药物,外科手术大出血风险极高,其手术期死亡率高达20%以上。
因此,上述处理措施均存在不同程度的不足之处,安全性最高的覆膜支架,在临床上应用也有诸多限制。需要有新的技术手段来进行弥补。
技术实现要素:
本发明的目的在于提供一种覆膜支架及其制造方法,以解决现有技术中的覆膜支架外形较大等问题。
为解决上述技术问题,本发明提供一种覆膜支架,所述覆膜支架包括支架本体及贴合在所述支架本体外的一覆膜,所述覆膜不完全覆盖所述支架本体的表面,以使所述覆膜支架不阻塞分支血管。
可选的,在所述的覆膜支架中,所述覆膜的材料为可降解高分子材料。
可选的,在所述的覆膜支架中,所述覆膜的材料为聚乳酸、聚乙醇酸、聚己内酯、聚三亚甲基碳酸酯和聚二恶烷酮中的一种或多种的共混物或共聚物。
可选的,在所述的覆膜支架中,所述支架本体在压握状态下,所述覆膜的厚度小于等于100μm;所述支架本体在扩张状态下,所述覆膜的厚度小于等于50μm。
可选的,在所述的覆膜支架中,所述覆膜上携带有药物。
可选的,在所述的覆膜支架中,所述支架本体的材料为可降解高分子材料或可降解金属材料或可降解合金材料,所述支架本体的降解速度比所述覆膜的降解速度慢。
可选的,在所述的覆膜支架中,所述支架本体两端的表面未覆膜。
本发明还提供一种覆膜支架,所述覆膜支架包括一覆膜区域以及未覆膜区域,所述未覆膜区域与一病变血管的分支血管位置相对应。
本发明还提供一种覆膜支架的制造方法,所述覆膜支架的制造方法包括:
获得一病变血管的分支血管数据;
根据所述病变血管的分支血管数据将覆膜管材套设于压握后的支架本体外以使所述支架本体表面形成一覆膜区域及未覆膜区域,所述未覆膜区域与所述病变血管的分支血管位置相对应。
本发明还提供一种覆膜支架的制造方法,所述覆膜支架的制造方法包括:
获得一病变血管的分支血管数据;
根据所述病变血管的分支血管数据将覆膜溶液涂覆于压握后的支架本体外以使所述支架本体表面形成一覆膜区域及未覆膜区域,所述未覆膜区域与所述病变血管的分支血管位置相对应。
可选的,在所述的覆膜支架的制造方法中,所述覆膜溶液中的溶质的浓度为1mg/ml~200mg/ml。
可选的,在所述的覆膜支架的制造方法中,所述覆膜溶液由可降解高分子材料溶解在亲水性有机溶剂中形成。
可选的,在所述的覆膜支架的制造方法中,所述覆膜溶液中的溶剂为丁酮、二甲基亚砜、氮酮、癸基甲基亚砜、吡咯烷酮、乙酸乙酯、乙酸甲酯、丙酮、乙醇、二甲基甲酰胺、四氢呋喃、二氧六环、油酸和丙二醇中的一种或多种混合。
可选的,在所述的覆膜支架的制造方法中,所述支架本体两端均为未覆膜区域。
在本发明提供的覆膜支架及其制造方法中,所述覆膜支架包括支架本体及贴合在所述支架本体外的一覆膜,由此可以使得所述覆膜支架具有较小的外形,进而提高所述覆膜支架的柔顺性;此外,所述覆膜不完全覆盖所述支架本体的表面,从而可以使所述覆膜支架不阻塞分支血管。进一步的,所述覆膜的材料为可降解高分子材料,由此可以促进覆膜支架内皮化,激化动脉瘤缩小,避免覆膜支架内血栓的形成,避免分支血管的堵塞,增加患者血流储备。更进一步的,本发明提供的覆膜支架的制造方法简单,因此可根据临床的不同需求在手术前进行制备,从而可以更加适配患者的情况并且也降低了医院的备货成本。
附图说明
图1是本发明实施例一的覆膜支架的制造方法的流程示意图;
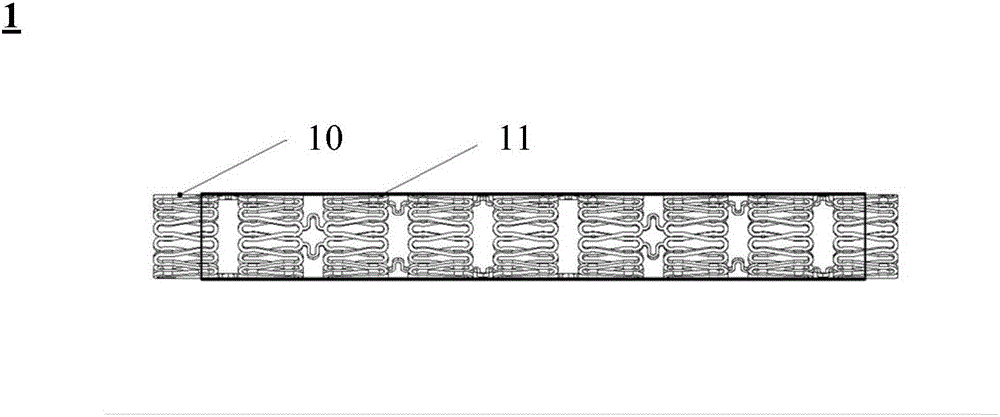
图2是本发明实施例一的一覆膜支架压握态下的主视示意图;
图3是本发明实施例一的一覆膜支架压握态下的剖视示意图;
图4是本发明实施例一的一覆膜支架扩张态下的主视示意图;
图5是本发明实施例一的一覆膜支架扩张态下的剖视示意图;
图6是本发明实施例一的另一覆膜支架的结构示意图;
图7是本发明实施例二的覆膜支架的制造方法的流程示意图。
具体实施方式
以下结合附图和具体实施例对本发明提出的覆膜支架及其制造方法作进一步详细说明。根据下面说明和权利要求书,本发明的优点和特征将更清楚。需说明的是,附图均采用非常简化的形式且均使用非精准的比例,仅用以方便、明晰地辅助说明本发明实施例的目的。特别的,由于各附图所要突出的内容不同,往往采用了不同的比例。
在本文中,不论是否明确指出,所有数值都被假定为可用术语“大约”进行修饰。在使用数值的上下文中,术语“大约”通常是指本领域的技术人员将认为等同于所引用的值(即,具有相同功能或结果)的一个值的范围。在许多情况下,术语“大约”可包括被四舍五入至最近的有效数字的数值。除非另有规定外,其他对术语“大约”的使用(即在除了使用数值以外的上下文中)可被假定为具有其普通和习惯定义,如可根据本说明书的上下文所理解的且与其保持一致。
在本文中,“近端”和“远端”是从使用该医疗器械的医生角度来看相对于彼此的元件或动作的相对方位、相对位置、方向,尽管“近端”和“远端”并非是限制性的,但是“近端”通常指该医疗设备在正常操作过程中靠近医生的一端,而“远端”通常是指首先进入患者体内的一端。
如在本说明书和所附权利要求中所使用的,单数形式“一”、“一个”以及“该”包括复数对象,除非内容另外明确指出外。如在本说明书和所附权利要求中所使用的,术语“或”通常是以包括“和/或”的含义而进行使用的,除非内容另外明确指出外。
【实施例一】
请参考图1,其为本发明实施例一的覆膜支架的制造方法的流程示意图。如图1所示,在本实施例一中,所述覆膜支架的制造方法具体包括:
首先,执行步骤S10:获得一病变血管的分支血管数据。在此主要包括分支血管相对于病变血管的位置,进一步还可包括病变血管的内径、分支血管的内径等数据。通过上述数据可使得制得的覆膜支架更好的适配患者的情况。
接着,执行步骤S11:根据所述病变血管的分支血管数据将覆膜管材套设于压握后的支架本体外以使所述支架本体表面形成一覆膜区域及未覆膜区域,所述未覆膜区域与所述病变血管的分支血管位置相对应。
在本申请实施例中,所述覆膜管材经过了灭菌处理。例如,所述覆膜管材可以通过电子束等辐射灭菌方法进行灭菌处理。
优选的,所述覆膜管材的材料为可降解高分子材料,例如,所述覆膜管材的材料为聚乳酸、聚乙醇酸、聚己内酯、聚三亚甲基碳酸酯和聚二恶烷酮中的一种或多种的共混物或共聚物。由此可以促进覆膜支架内皮化,激化动脉瘤缩小,避免覆膜支架内血栓的形成,避免分支血管的堵塞,增加患者血流储备。
较佳的,所述覆膜管材上携带有药物。例如,所述覆膜管材上携带有雷帕霉素、地塞米松、紫杉醇、依维莫司、阿司匹林、肝素、蛋白酶和/或水蛭素等功能性药物,从而减缓患者的炎症,促进血管内皮化和避免血管增生等。
较佳的,所述覆膜管材上已经开有孔洞或贯通区域,用于与病变血管的分支血管位置相对应。手术操作者可以根据临床手术中病变血管位置和长度以及病变血管上的分支血管的位置剪切覆膜管材的合适长度。
在本申请实施例中,所述支架本体的材料也可以为可降解高分子材料,在本申请的其他实施例中,所述支架本体的材料也可以为可降解金属材料或可降解合金材料。其中,所述支架本体的降解速度比所述覆膜(管材)的降解速度慢,由此,所述支架本体始终能够给所述覆膜(管材)以一定的支撑,防止覆膜堵塞分支血管或者影响侧枝循环。
在本申请实施例中,具体选用了直径为1.1mm,长度为28mm的支架本体;所选用的覆膜管材的内径为1.2mm,外径为1.26mm,长度为25mm,所选用的覆膜支架的材料为聚乳酸类材料。当然,在本申请的其他实施例中,可以根据具体需求选取不同规格的支架本体和覆膜管材,例如,所述支架本体的直径可以为1mm、1.05mm、1.15mm或者1.2mm等;所述覆膜管材的内径和外径可以相应调整,优选的,此时(所述支架本体在压握状态下),所述覆膜管材的厚度小于等于100μm。
进一步的,根据临床的使用情况,根据覆膜支架植入血管的位置、血管穿孔/破裂/动脉瘤和分支血管的相对位置等,使所述覆膜管材套设于所述支架本体的整体段、或近端、或远端、或中间段、或近端和中间段、或中间段和远端、或近端和远端等。较佳的,将所述覆膜管材套设于压握后的支架本体外后,所述支架本体两端露出于所述覆膜管材外,以使覆膜能覆盖血管穿孔、破裂和动脉瘤等病变,但又不堵塞分支血管。
优选的,通过专门的压握仪器对所述支架本体进行压握,以使得所述支架本体各处的受压均匀,从而实现所述覆膜管材与所述支架本体之间最佳的的贴合效果。
此外,所述支架本体也可通过手工进行压握,此时虽然会牺牲一点压握效果,即使得所述支架本体的各处的受压不够均匀,但是具有操作方便的优点,尤其适合手术前根据患者的不同情况制作覆膜支架。
通过上述工艺之后,便可得到覆膜支架,具体可参考图2至图6。所述覆膜支架1包括支架本体10及贴合在所述支架本体10外的一覆膜11,所述覆膜11不完全覆盖所述支架本体10的表面,以使所述覆膜支架1不阻塞分支血管。在图2至图5所示的覆膜支架1中,所述覆膜管材套设于所述支架本体的整体段,即所述支架本体10的整体段都贴合有覆膜11。在图6所示的覆膜支架1中,所示覆膜管材套设于所述支架本体的近端和远端,即所述支架本体10的近端和远端贴合有覆膜11。进一步的,所述支架本体10两端的表面未覆膜。即在本申请实施例中,所述覆膜支架1包括一覆膜区域以及未覆膜区域,所述未覆膜区域与一病变血管的分支血管位置相对应。
接着便可根据需要使用所述覆膜支架1。具体的可相应参考图6,在使用过程中,将所述覆膜支架1植入病变血管2中,在植入过程中,支架本体10进行扩张(其中,覆膜支架1扩张前的状态,即压握态,亦可参考图2和图3),此时,覆膜(管材)11随同支架本体10一同扩张变形(其中,覆膜支架1扩张后的状态,亦可参考图4和图5),在病变血管2中形成封闭的通道。由此,可有效封堵病变血管部位20(例如,血管穿孔和血管破裂),隔绝血管动脉瘤,使病变血管部位20血流恢复正常。请继续参考图6,在此,所示覆膜管材套设于所述支架本体的近端和远端,即所述支架本体10的中间段没有贴合覆膜11,同时所述支架本体10的中间段正好对应分支血管,由此可以更好的实现覆膜支架1不阻塞分支血管3。
在本申请实施例中,所述覆膜(管材)11的材料为可降解高分子材料,因此植入后,覆膜(管材)11逐渐发生降解,覆膜支架1发生内皮化。在病变血管的破裂和穿孔创面愈合,或动脉瘤愈合完成后,覆膜(管材)11逐渐降解消失,使得覆膜支架1梳理发生内皮化。
在本申请实施例中,优选的,所述支架本体10在压握状态下,所述覆膜(管材)11的厚度小于等于100μm;所述支架本体10在扩张状态下,所述覆膜(管材)11的厚度小于等于50μm。由此使得整个覆膜支架1的外形进一步减小,从而提高了所述覆膜支架1的柔顺性和通过性。同时,由于扩张后的覆膜(管材)11进一步变薄了,从而提高了所述覆膜(管材)11的降解速度,使得覆膜支架1尽早发生内皮化。
综上可见,在本发明实施例提供的覆膜支架及其制造方法中,所述覆膜支架包括支架本体及贴合在所述支架本体外的一覆膜,由此可以使得所述覆膜支架具有较小的外形,进而提高所述覆膜支架的柔顺性;此外,所述覆膜不完全覆盖所述支架本体的表面,从而可以使所述覆膜支架不阻塞分支血管。进一步的,所述覆膜的材料为可降解高分子材料,由此可以促进覆膜支架内皮化,激化动脉瘤缩小,避免覆膜支架内血栓的形成,避免分支血管的堵塞,增加患者血流储备。更进一步的,本发明提供的覆膜支架的制造方法简单,因此可根据临床的不同需求在手术前进行制备,从而可以更加适配患者的情况并且也降低了医院的备货成本。
【实施例二】
请参考图7,其为本发明实施例二的覆膜支架的制造方法的流程示意图。如图7所示,在本实施例二中,所述覆膜支架的制造方法具体包括:
首先,执行步骤S20:获得一病变血管的分支血管数据。在此主要包括分支血管相对于病变血管的位置,进一步还可包括病变血管的内径、分支血管的内径等数据。通过上述数据可使得制得的覆膜支架更好的适配患者的情况。
接着,执行步骤S21:根据所述病变血管的分支血管数据将覆膜溶液涂覆于压握后的支架本体外以使所述支架本体表面形成一覆膜区域及未覆膜区域,所述未覆膜区域与所述病变血管的分支血管位置相对应。
在此,所述覆膜溶液中的溶质为可降解高分子材料,例如,所述覆膜溶液中的溶质可以为乳酸、聚乙醇酸、聚己内酯、聚三亚甲基碳酸酯和聚二恶烷酮中的一种或多种。
较佳的,所述覆膜溶液中的溶剂为亲水性有机溶剂,例如,所述覆膜溶液中的溶剂为丁酮、二甲基亚砜、氮酮、癸基甲基亚砜、吡咯烷酮、乙酸乙酯、乙酸甲酯、丙酮、乙醇、二甲基甲酰胺、四氢呋喃、二氧六环、油酸和丙二醇中的一种或多种混合。
优选的,所述覆膜溶液中的溶质的浓度为1mg/ml~200mg/ml。更佳的,所述覆膜溶液中的溶质的浓度为5mg/ml~100mg/ml,由此可以使得所述覆膜溶液具有最佳的挂壁性能,从而易于后续喷涂于所述支架本体外。
在本申请实施例中,具体的,所述覆膜溶液采用如下方式配置而成:取重均分子量为15万,质量为700mg聚乙醇酸搅拌溶解在10ml丙酮中,得到浓度为70mg/ml的覆膜溶液备用。
此外,在本申请实施例中,所述支架本体的材料也可以为可降解高分子材料,在本申请的其他实施例中,所述支架本体的材料也可以为可降解金属材料或可降解合金材料。其中,所述支架本体的降解速度比所述覆膜的降解速度慢,由此,所述支架本体始终能够给所述覆膜以一定的支撑,防止覆膜堵塞分支血管或者影响侧枝循环。
在此,可通过加压超声的方式将覆膜溶液喷涂在支架本体的外表面。其中,在喷涂过程中,可控制喷涂段的长度和相对支架本体的喷涂位置,以使得得到的覆膜支架能覆盖血管穿孔、破裂和动脉瘤等病变,但又不堵塞分支血管。具体的,可以在所述支架本体的整体段、或近端、或远端、或中间段、或近端和中间段、或中间段和远端、或近端和远端等喷涂覆膜溶液,较佳的,所述支架本体的两端不喷涂覆膜溶液,即使得最后支架本体两端露出于覆膜外,也即所述支架本体两端均为未覆膜区域。
优选的,所述覆膜溶液的喷涂厚度为100μm内。从而使得所形成的覆膜支架具有较小的外形。
在本申请实施例中,优选沸点较低的溶剂,由此可以在覆膜溶液喷涂后,其中的溶剂尽快挥发,从而快速实现支架本体上贴合覆膜。
经过上述工艺后,便可得到覆膜支架,所述覆膜支架包括支架本体及贴合在所述支架本体外的一覆膜,所述覆膜不完全覆盖所述支架本体的表面,以使所述覆膜支架不阻塞分支血管。在此,所述覆膜由覆膜溶液经溶剂蒸发后而得到。
接着,便可使用制得的覆膜支架,具体可参考实施例一,本实施例二对此不再赘述。
上述描述仅是对本发明较佳实施例的描述,并非对本发明范围的任何限定,本发明领域的普通技术人员根据上述揭示内容做的任何变更、修饰,均属于权利要求书的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!