经血干细胞在制备治疗宫腔粘连的药物中的应用的制作方法
本发明属于生物医药领域,尤其涉及一种经血干细胞在制备治疗宫腔粘连的药物中的应用。
背景技术:
子宫内膜对维持女性生理特征和生育能力具有举足轻重的意义,它具有高度的再生能力和增殖活性,任何引起子宫内膜破坏的因素都可引起宫腔粘连。随着频繁的宫腔操作及宫腔镜手术的普及,子宫内膜损伤所致宫腔粘连(intrauterine adhesions,IUA)的发生率和检出率逐年增加,已成为女性继发性不孕的第二大原因。IUA是由于子宫内膜基底层损伤后形成纤维化瘢痕、修复障碍导致的宫腔部分或全部粘连闭塞,从而引起月经量少、闭经、不孕及反复流产等一系列并发症,也被定义为Asherman综合征。
目前治疗IUA的主要手段是采用宫腔镜手术分离粘连并置入粘连屏障包括宫内节育器、Foley气囊导尿管、透明质酸和羊膜等预防粘连复发,同时配合药物如雌激素、阿司匹林、中药治疗,以促进子宫内膜再生,恢复其生理功能,但疗效因人而异。尤其是中、重度粘连极易复发。此外,术后会出现不孕或多种妊娠并发症的情况。这类难治性宫腔粘连导致的不孕给患者身心及家庭带来极大痛苦。
近年,很多医学领域的研究人员进行宫腔粘连的临床研究,努力探索一种可以有效恢复患者子宫内膜再生能力的方法。大量研究表明子宫内膜存在干细胞,深入子宫基底层的损伤,会引起干细胞的丢失或功能异常,最终导致子宫内膜再生失败,因此干细胞移植治疗有望成为宫腔粘连患者更好的选择。目前,国内外已有研究报道应用骨髓干细胞移植治疗患者宫腔粘连或动物模型,患者在接受男性供者的骨髓间充质干细胞移植后,受者的子宫内膜中出现了Y染色体阳性的子宫内膜上皮细胞和基质细胞,提示骨髓间充质干细胞参与内膜的再生过程。但是,骨髓干细胞的主要缺憾是其获得存在侵袭性和创伤性,易引起患者的不适或感染;另外骨髓中直接分离出的干细胞比例较低,通过细胞培养,在有限次数的传代培养内获得足够数量的细胞也较困难,这在一定程度上限制了其应用。故亟需寻找更加安全、易获得、易扩增的干细胞才利于推广干细胞在宫腔粘连病症中的移植疗法。
目前,已报道了将干细胞-经血干细胞(menstrual blood stromal stem cells, MenSCs)用于治疗脑中风、下肢缺血、心肌梗死、肌营养不良、肠炎、卵巢早衰、败血症和糖尿病等多种动物模型。移植的MenSCs不同程度地促进了组织损伤修复,提高了动物的生存率或妊娠率。基于经血干细胞的优点,其有望应用于制备治疗宫腔粘连的药物,而至今为止未见相关报道。
技术实现要素:
针对上述问题,本发明提供了一种经血干细胞在制备治疗宫腔粘连的药物中的应用。该细胞存活率高,性状稳定,安全,易获得,易扩增,对宫腔粘连的治疗效果显著。
为实现上述目的,本发明提供一种经血干细胞在制备治疗宫腔粘连的药物中的应用。
所述的经血干细胞采用以下方法制备。
步骤1、经血干细胞的原代分离、培养:将提取的经血样本用PBS稀释,缓慢加至细胞分离液的上层,离心、分离单个核细胞层,弃去上清,细胞沉淀用完全培养液重悬,接种于细胞培养瓶,置于 5% CO2、37℃、饱和湿度的培养箱内培养。
步骤2、经血干细胞的传代:当细胞长满至80-90%,用0.25%胰蛋白酶消化传代,当细胞质回缩,细胞间隙增大后,应立即加入完全培养液终止消化;反复吹打瓶壁形成细胞悬液;将细胞悬液吸入离心管,离心,弃上清;沉淀用完全培养液调整细胞浓度,接种于培养瓶中;置37℃、5% CO2、饱和湿度的培养箱培养;培养代数2~3代。
所述的经血干细胞优选于患者经期中的经血干细胞。
所述的PBS稀释,按照与经血干细胞的体积比例为1:1进行稀释。
所述的完全培养液含10%人体血清或胎牛血清的DMEM-F12培养液,优选含10%人体血清。
本发明的有益效果。
本发明采用更加适用于内膜再生的干细胞-经血干细胞(menstrual blood stromal stem cells, MenSCs)。MenSCs是从女性月经血中分离、培养出来的新型成体干细胞。研究提示,MenSCs包含了脱落的子宫内膜干细胞和循环血液中的骨髓来源间充质干细胞。MenSCs具备间充质干细胞的所有特征,且极易扩增,在体外连续培养保持二倍体核型。它表达间充质干细胞的表面标记CD29、CD73、CD90和CD105,同时表达胚胎干细胞的多潜能性标记OCT-4。现有的研究已证实MenSCs可被诱导分化为多种组织细胞,包括神经细胞、成骨细胞、软骨细胞、脂肪细胞、肺上皮细胞、胰岛细胞和卵巢样细胞;MenSCs还可被成功诱导为多能干细胞(iPS),具有其自我更新、自我复制能力的多潜能性。基于经血干细胞自我更新能力强,易于获得,体外培养稳定,而且优选方案自体移植具备减少患者的精神和心理压力的优点;其在远期临床应用前景上远远超越骨髓间充质干细胞;经血干细胞药物的移植可对宫腔粘连患者进行内膜修复治疗。
附图说明
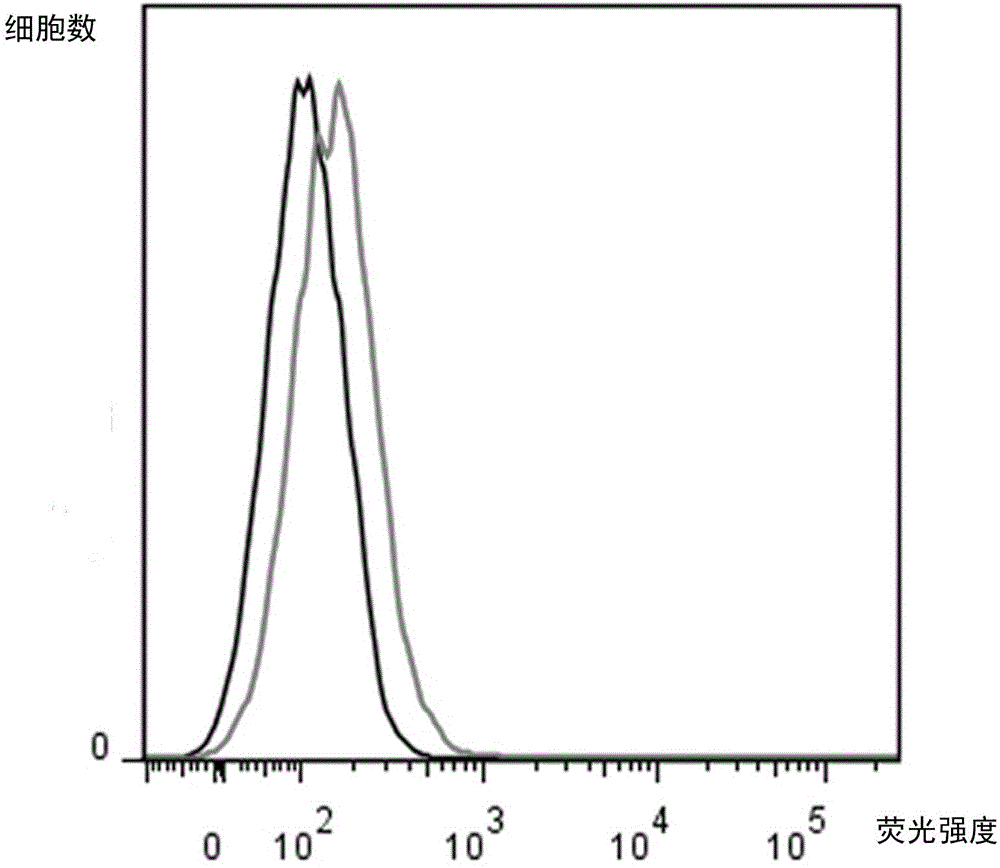
图1流式细胞术分析经血干细胞的表面标志(同型对照:黑色,特异性抗体:灰色);其中1-1为CD34、1-2为CD38、1-3为CD44、1-4为CD45、1-5为CD73、1-6为CD90、1-7为CD105和1-8为SSEA-4抗体。
图2患者接受MenSCs药物移植前、后子宫内膜厚度比较。
具体实施方式
下面结合具体实施例对本发明的内容做进一步说明。
实施例1。
出于人道主义角度考虑,患者更倾向于采集自体经血干细胞制备药物,治疗自身的宫腔粘连疾病。经血干细胞可以选择自体采取,进行药物的配制。
一、自体干细胞体外分离与培养。
1.所用设备,材料,试剂:超净工作台、CO2培养箱、倒置显微镜、离心机(采购于eppendorf公司)、恒温水浴箱(采购于JULABO公司)、B超机、细胞培养瓶、离心管(50 mL,15 mL)、吸管、5 mL注射器、人工授精导管、胚胎移植管、采血针、DMEM-F12培养液(采购于HyClone公司,货号:SH30023)、青霉素、链霉素(采购于SIGMA公司,货号:V900929)、0.25%胰蛋白酶(采购于SIGMA公司,货号:T4049)、磷酸盐缓冲液(PBS,采购于SIGMA公司HyClone公司,货号:SH30256)、样本密度分离液(采购于天津市灏洋生物制品科技有限责任公司,货号:HY2015)。
2.经血干细胞的原代分离、培养:(1)静脉血收集:患者月经来潮后第1天来院,用采血针取静脉血30 mL。采集的血液于4℃冰箱静置12 h后,3000 rpm离心处理10 min,取上层血清。将血清置于56℃恒温水浴箱中,经过30 min的灭活补体后,将得到血清于-20℃冰箱保存,备用。(2)月经血收集:患者在月经来潮后第2天来院,进入无菌手术室,截石位卧于手术台上,应用碘伏消毒阴道后,用5 mL注射器连接人工授精导管抽取月经血样本2-5 mL,全程严格执行无菌操作。(3)经血干细胞的分离培养:取经血样本1-5 mL,用等体积PBS稀释后,缓慢加至3mL样本密度分离液的上层,450 g离心处理25 min,分离细胞层。离心结束后分为3层,用吸管吸取中间层的单个核细胞,将所得到的细胞加至10 mLPBS中混匀,250 g离心处理20 min后,弃去上清,细胞沉淀用5 mL完全培养液(含10%自体血清、100 U/mL青霉素、100 μg/mL链霉素的DMEM-F12培养液)重悬,接种于培养瓶中置于 5% CO2、37℃饱和湿度的培养箱内培养约2周。每2-3 d全量更换为新鲜配制的5 mL完全培养液。培养过程中通过显微镜观察,可见经血干细胞为贴壁生长,呈短棒状或梭形,有较长的突起。
3.经血干细胞的传代:当细胞贴壁长满至80-90%,吸除培养瓶内旧培养液,加入PBS 2 mL,轻轻摇动培养瓶,以洗去残留在瓶内的培养液,吸弃 PBS,重复1次该操作过程。培养瓶内加入预热至37℃的0.25%胰蛋白酶2 mL,轻轻摇动培养瓶,使消化液0.25%胰蛋白酶流遍所有细胞表面,置于37℃培养箱孵育3 min。在倒置显微镜下观察,发现细胞质回缩,细胞间隙增大后,立即加入完全培养液2 mL终止消化。反复吹打瓶壁形成细胞悬液,将细胞悬液吸入离心管,1500rpm离心处理10 min,弃上清。沉淀用完全培养液调整细胞浓度为1×105/mL,接种于培养瓶中,每瓶5 mL,置37℃、5% CO2、饱和湿度的培养箱培养。培养代数2~3代,备用。
4.无菌试验:在细胞培养第4天,对细胞上清液作无菌试验,收集细胞培养上清液,进行细菌、真菌、内毒素及肝炎病毒检测。检测结果表明细胞上清液没有细菌和真菌生长、内毒素水平达到标准小于10pg/ml、肝炎病毒呈阴性,见表1。
表1经血干细胞培养上清液无菌性试验检测结果。
5.经血干细胞的表型鉴定:细胞药物移植当天,先将所有培养瓶中的细胞制成单细胞悬液。取1×106细胞与FITC或PE标记的CD34、CD38、CD44、CD45、CD73、CD90、CD105和SSEA-4抗体,置于4℃冰箱孵育30 min,用PBS清洗一遍,洗去未结合抗体。以相应的同型对照抗体作为阴性对照组。用FACS Canto流式细胞仪收集数据,用FACS Diva 软件分析,具体数据见图1和表2。
表2 FACS Diva 软件分析结果。
利用流式细胞术分析发现,经血干细胞低表达CD34、CD38、CD45和SSEA-4,高表达CD44、CD73、CD90和CD105。
二、自体经血干细胞药物给药方案。
(一)患者于取经血后第16 天来院进行干细胞药物移植(选择第16天原因:一方面是子宫内膜这个时间点最易接受移植,另一方面月经第2天开始培养细胞,正好培养2周后传代2-3代)。取消化传代培养所得的自体经血干细4×106/ml,用0.5mlPBS重悬至2×106/ml(重悬过程进行计数,此细胞数通过计数所得)。患者取膀胱截石位,为了细胞药物移植后更易种植在内膜中,先行轻度搔刮,B超引导下,将移植管的外管置入宫颈内口上方,将装有0.5 ml PBS重悬所得的自体MenSCs的内管送入到宫腔,将干细胞药物推注至子宫底部,卧床观察2 h。
(二)激素刺激内膜生长及胚胎移植:定期给予激素治疗刺激子宫内膜生长:首次取经血后,月经第5天开始口服雌激素-补佳乐4 mg/d,连用服用至药物移植当天,药物移植后补佳乐6 mg/d,连用21 d;如果B超检测子宫内膜厚度仍小于7 mm,给予黄体酮40 mg/日肌注,连用10天;下次月经3-5天开始重复上述激素治疗疗程。当在激素治疗周期,检测到子宫内膜厚度≥7 mm时,将其前期接受试管婴儿手术保存的冷冻胚胎解冻移植,黄体酮40 mg日两次肌注以支持黄体功能,继续口服补佳乐6 mg/d,移植14 d后,化验血绒毛膜促性腺激素(hCG)值。如果化验hCG阳性,移植28 d超声检查,随访至分娩;如果患者的输卵管通畅,当内膜厚度≥7 mm时,指导自然受孕。
三、典型病例。
对10个患者进行干细胞药物移植的效果进行统计,其中3例不符合病例入选标准,仅有7例可进行有效统计。
1.病例入选标准:(1)年龄20-40岁,存在月经周期;(2)确诊为单纯女方宫腔粘连导致的不孕患者;(3)已经过其他如雌孕激素人工周期治疗、节育环、阿斯匹林和中药治疗等,均无明显疗效;(4)签署知情同意书,同意经血干细胞药物移植治疗。
2.排除标准:患者存在(1)生殖系统结核;(2)其它慢性消耗性或出血性疾病,(3)子宫肌瘤;(4)子宫腺肌症;(5)输卵管积水未处理等子宫因素或影响胚胎着床的不孕因素。
7例患者均经宫腔镜证实有不同程度的宫腔粘连,超声检查内膜厚度均不大于4 mm,已经过各种药物及带宫内节育器等治疗无效。收集患者的月经血1-5 ml,成功分离出MenSCs,体外扩增后移植回子宫腔内,辅以激素治疗,超声监测子宫内膜的厚度均显著增长。5例增长至不小于7 mm,符合妊娠的条件,见图2和表3。
表3干细胞药物移植前后子宫内膜的厚度。
差异具有统计学意义(** p<0.01)。
其中,1例患者第二次干细胞移植后3个半月自然妊娠。其余4例患者治疗后接受解冻胚胎移植手术,1例两次胚胎移植后均为生化妊娠,1例妊娠但胚胎停滞,余下2例移植未妊娠。由此可以证实经血干细胞移植能够促进子宫内膜再生,帮助大多数宫腔粘连患者实现生育的愿望。
在患者宫腔粘连病症比较严重,出现月经量少、闭经等症状时,无法采集患者自身的月经血,患者可以选择预先采集的健康女性的月经血样本,进行药物的配置和移植治疗自身的病症。
上述实施例仅为说明本发明的技术构思及特点,其目的在于让本技术领域的人员了解本发明的内容并局限于此,并不能以此限制本发明的保护范围。凡根据本发明技术方案所作的等效变化,都应覆盖在本法的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!
- 从人胎盘羊膜制备羊膜间充质干细胞的方法及其应用与流程
- 一种脐疗贴的制备方法及应用与流程
- 一种干细胞制剂及其在制备治疗慢性肾炎的药物中的应用的制作方法与工艺
- 脐带间充质干细胞在制备治疗角膜损伤的干细胞制剂中的应用的制作方法与工艺
- 脐带间充质干细胞联合黄芪多糖在制备治疗高血糖和糖尿病肾病药物中的应用的制作方法与工艺
- 由脐带间充质干细胞制备CD34阳性细胞的方法与流程
- 基因重组干细胞制剂的制备方法及其在皮肤损伤修复、瘢痕抑制中的应用与流程
- 一种大规模制备人脐带间充质干细胞因子用诱导分泌培养基的制作方法与工艺
- 一种人母乳干细胞的制备方法及其应用与流程
- 间充质干细胞联合维生素E在制备肾脏组织细胞修复药物中的应用的制作方法与工艺