牛樟芝子实体萃取组合物的用途的制作方法
本发明为关于牛樟芝子实体萃取物的用途;具体而言,为用于治疗红血球和/或血小板低下。
背景技术:
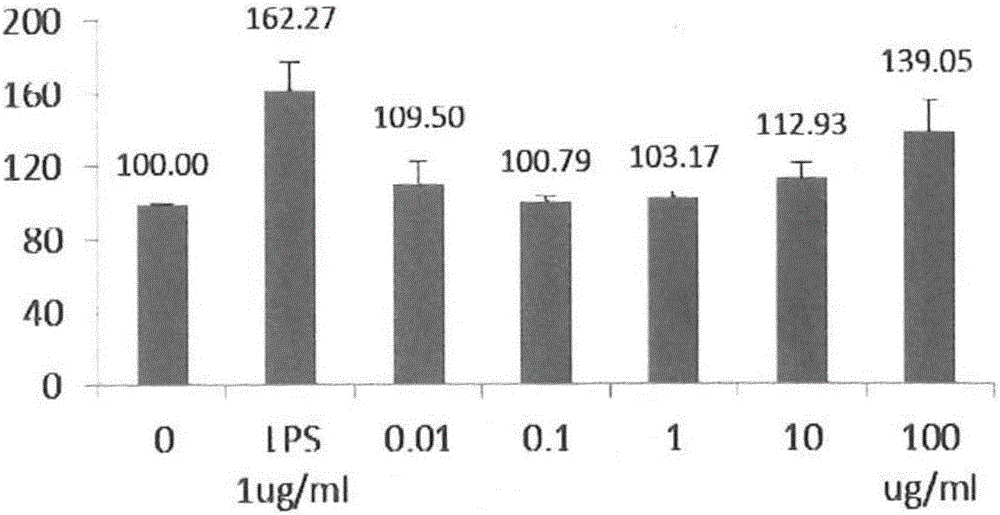
:在癌症治疗上,化学治疗药物的使用扮演相当重要的角色,然而化学治疗药物除了可毒杀癌细胞外,也对许多正常细胞产生毒害,而造成许多副作用。一般而言,癌细胞是生长分裂速度快速的细胞,化学治疗药物的毒杀机制通常与抑制细胞分裂相关,而体内许多正常的组织细胞的生长分裂速度也很快,因此化学治疗药物也会影响到这些细胞的生理功能,通常遭受化学治疗药物影响的细胞例如:骨髓造血细胞、消化道的表皮黏膜细胞、生殖系统的细胞、毛囊细胞。在前述易受化学治疗药物影响的细胞中,骨髓造血细胞为一种重要细胞,其为主要的造血组织,具有生长分裂快速的特性,依据骨髓造血细胞对化学治疗药物的感受度不同,在进行化学药物治疗时几乎都会出现程度不一的“骨髓抑制”副作用,其症状为白血球、红血球及血小板数降低;其中白血球数的降低使病患容易受到感染;红血球数降低则可能出现贫血,继而出现虚弱、疲倦等症状;血小板数降低则使病患凝血功能下降。现阶段临床上根据骨髓抑制的态样,而采不同的治疗机制,例如针对白血球降低,使用颗粒性巨噬细胞株刺激因子(granulocyte-macrophagecolony-stimulatingfactor,G-CSF);针对红血球降低则可服用铁剂,必要时需输血或给予红血球生成激素(EPO);针对血小板降低则需输血小板来治疗。然而前述处置如涉及血液制剂有安全性及供应上的考虑,红血球生成激素价格昂贵,使用颗粒性巨噬细胞株刺激因子也会引起许多副作用,包括骨头酸痛、肌肉酸痛、头痛、疲倦、恶心、呕吐、发烧、失眠等;在生化检验上,可以发现碱性磷酸酶升高、肝功能指数升高、以及尿酸升高;此外,还对肌肉骨骼系统、皮肤、呼吸系统、心脏血管系统、肾功能等产生影响。因此在癌症的化学药物治疗上仍须开发可妥善处理骨髓抑制副作用的药品。牛樟芝(Antrodiacinnamomea)为中国台湾特有真菌,属于真菌分类学中担子菌亚门(Basidiomycotina)、层菌纲(Hymenomycetes)、非褶菌目(Aphyllophorales)、多孔菌科(Polyporaceae)、薄孔菌属(Antrodia)的多年生菌类,仅生长于中国台湾特有牛樟树(Cinnamomumkanehirai)的中空芯材内壁,其子实体为一年生至多年生,呈鲜红色、橘红色或淡肉桂色,具有樟树香气。牛樟芝早期被中国台湾原住民视为解酒良药,具有解除宿醉的效果,含有三萜类化合物(Triterpenoids)、多醣体(Poly-saccharides)及β-葡聚糖(β-glucan)等成分,经广泛研究后,牛樟芝陆续证实具有抗B型肝炎病毒、抗癌、免疫调节、抗发炎、抗氧化、抗血管增生、降血压、降血脂、神经保护、抗菌、美白等功能。牛樟芝为一种真菌,其生长可分成菌丝、菌丝体、子实体、孢子体不同的阶段,其栽培成本、成分组成、成分含量各不相同。菌丝及菌丝体可利用液体发酵或固体培养栽培,其中液体发酵成本低廉,培养时间短,固体发酵则能获得与子实体外形相似的菌丝体,然而菌丝及菌丝体中所含的三萜类成分极低,在疗效上远不及子实体;子实体以往仅能在野外采集,价格昂贵且付出的生态成本极大,现已发展出椴木栽培,利用牛樟芝宿主牛樟树椴木为培养基栽培出子实体,为现今可与野外采集而得牛樟芝最相似、疗效最佳的方式。因牛樟芝子实体所含生理活性成分种类繁多,开发其疗效以扩大牛樟芝的应用仍为业界努力的目标。技术实现要素:本发明提供一种牛樟芝子实体萃取组合物的用途,其用于制造治疗红血球和/或血小板低下的药物,其中该牛樟芝子实体萃取组合物包含牛樟芝子实体的二氧化碳超临界流体萃取物。前述用途优选为用于制造治疗红血球和/或血小板低下并发白血球低下的药物或用于制造治疗红血球和/或血小板低下并发体重减轻的药物。本发明又提供一种治疗红血球和/或血小板低下的医药组合物,其包含治疗有效量的牛樟芝子实体萃取组合物,其中该牛樟芝子实体萃取组合物包含牛樟芝子实体的二氧化碳超临界流体萃取物。前述医药组合物优选用于治疗红血球和/或血小板低下并发白血球低下的或用于治疗红血球和/或血小板低下并发体重减轻。另一方面,前述的牛樟芝子实体萃取组合物另外包含芝麻萃取物。附图说明图1表示THP-1细胞给予不同浓度牛樟芝子实体萃取组合物(SR4)处理24小时后,对颗粒性巨噬细胞株刺激因子(granulocyte-macrophagecolony-stimulatingfactor)分泌的影响。图2表示THP-1细胞给予不同浓度牛樟芝子实体萃取组合物(SR4s)处理24小时后,对颗粒性巨噬细胞株刺激因子分泌的影响。具体实施方式本发明提供一种牛樟芝子实体萃取组合物的用途,其用于制造治疗红血球和/或血小板低下的药物,其中该牛樟芝子实体萃取组合物包含牛樟芝子实体的二氧化碳超临界流体萃取物。包含牛樟芝子实体萃取组合物的医药组合物可在一个体中治疗红血球和/或血小板低下,该医药组合物包含有效量的牛樟芝子实体萃取组合物及视需要的药学上可接受的载剂或赋形剂。参考以下对本发明的各态样、实例、及伴随相关描述的化学图式及表格的详细描述,可更容易地了解本发明。在揭示及描述本发明的用途及萃取物之前,应了解,除非由申请专利范围另外特别地指出,否则本发明不受限于特定制备方法、载剂或调配物、或将本发明化合物调配成用于局部、经口或非经肠施用的产物或组合物的特定模式,此为本领域技术人员非常清楚该事情是可以加以变化的。还应了解,本文所用的术语仅用于描述特定态样的目的而不旨在用于限制本发明的范围。除非另外指出,否则如本发明所用的以下术语应解释为具有以下含义。范围在本文中通常表述为“约”一个特定值和/或至“约”另一个特定值。当表述此类范围时,一种态样为包括一个特定值和/或至另一个特定值的范围。类似地,当通过使用字“约”表述为近似值时,应了解特定值可形成另一种态样。另外应了解,每一范围的各端点都有显著性,一端点与另一端点既有相关性,也彼此独立。“视情况”或“视情况地”是指随后所述的事件或状况可能发生或可能不发生,且该描述包括该事件或状况发生的情况及其未发生的情况。举例而言,“视情况包含药剂”是指该药剂可能存在或可能不存在。必须指出,除非上下文另外清楚规定,否则如本说明书及随附权利要求书中所用的单数形式“一”及“该”包括复数个所指标的物。因此,除非上下文另外需要,否则单数术语应包括复数且复数术语应包括单数。如本文所用的术语“个体”表示任何动物,优选为哺乳动物,且更优选为人类。个体的实例包括人类、非人类灵长类动物、啮齿动物、天竺鼠、兔、绵羊、猪、山羊、母牛、马、狗及猫。术语如本文所提供的化合物的“有效量”是指该化合物的量足以提供对所需功能(诸如基因表现、蛋白质功能或诱导特定类型的反应)的所需调节。如下文所指出,确切的需要量将在个体之间有变化,此视个体的疾病病况、身体状况、年龄、性别、物种及体重、组合物的特性及配方等而定。给药方案可经调整以诱导最佳治疗反应。举例而言,可每日施用若干分次剂量,或可依治疗情形的紧急程度按比例减少剂量。因此,很难指定确切的“有效量”。然而,本领域技术人员使用常规实验即可确定适当的有效量。如本文所用的术语“治疗”表示逆转、减轻或改善此术语所适用的病症或病状、或该病症或病状之一或多种症状,或抑制其进展。如本文所用的术语“载剂”或“赋形剂”是指自身并不为治疗剂,而是用作用于将治疗剂传递至个体的载剂和/或稀释剂和/或佐剂或媒剂,或添加至调配物中以改善调配物的处理或储存性质或允许或有助于组合物的剂量单位形成适于经口施用的剂量单位(诸如胶囊或锭剂)的任何物质。适合的载剂或赋形剂为了解制造医药调配物或食品的技术人员所熟知。载剂或赋形剂可包括(举例而言但不限于)缓冲剂、稀释剂、崩解剂、黏合剂、黏着剂、湿润剂、聚合物、润滑剂、滑动剂、为遮蔽或抵消不良味道或气味而添加的物质、调味剂、染料、芳香剂及为改善组合物的外观而添加的物质。可接受的载剂或赋形剂包括柠檬酸盐缓冲剂、磷酸盐缓冲剂、乙酸盐缓冲剂、碳酸氢盐缓冲剂、硬脂酸、硬脂酸镁、氧化镁、磷酸及硫酸的钠盐及钙盐、碳酸镁、滑石、明胶、阿拉伯胶、海藻酸钠、果胶、糊精、甘露糖醇、山梨糖醇、乳糖、蔗糖、淀粉、明胶、纤维素物质(诸如烷酸的纤维素酯及纤维素烷基酯)、低熔点蜡、可可脂、胺基酸、尿素、醇类、抗坏血酸、磷脂、蛋白质(例如血清白蛋白)、乙二胺四乙酸(EDTA)、二甲亚砜(DMSO)、氯化钠或其他盐、脂质体、甘露糖醇、山梨糖醇、甘油或粉末、聚合物(诸如聚乙烯吡咯啶酮、聚乙烯醇及聚乙二醇)、及其他药学上可接受的物质。载剂不应破坏治疗剂的药理学活性,且在以足以传递治疗量的药剂的剂量施用时应无毒性。优选地,该牛樟芝子实体萃取组合物包含于一种组合物中。根据本发明的组合物优选为食品组合物或医药组合物。该牛樟芝子实体萃取组合物可在食品制造过程中,添加于常用的食品组合物中(也即可食用的食品或饮品或其前驱物)。几乎所有的食品组合物都可添加根据本发明的该牛樟芝子实体萃取组合物。可添加根据本发明的该牛樟芝子实体萃取组合物的食品组合物包含,但不限于糖果、烘焙食品、冰淇淋、乳制品、甜品及风味小点、小吃、肉类替代产品、快餐食品、汤类、面食、面条、罐头食品、冷冻食品、干制食品、冷藏食品、油脂、婴儿食品、软食物、或面包涂酱或其混合物。本发明的医药组合物可通过本发明领域中已知的任何方法局部或全身施用,包括但不限于通过肌肉内、皮内、静脉内、皮下、腹膜内、鼻内、经口、黏膜或外部途径施用。适当的施用途径、调配方法及施用时程可由本领域技术人员来决定。在本发明中,医药组合物可根据相应施用途径以多种方式调配,诸如液体溶液、悬浮液、乳液、糖浆、锭剂、丸剂、胶囊、持续释放调配物、散剂、颗粒、安瓿、注射液、输注液、套组、软膏、洗剂、擦剂、乳膏或其组合。在必要时,其可经灭菌或与任何药学上可接受的载剂或赋形剂混合,其中有许多药学上可接受的载剂或赋形剂已为本领域技术人员所知。本文中所称的“牛樟芝子实体萃取组合物”一词是指包含牛樟芝子实体萃取物的组合物,特定地为包含牛樟芝子实体的二氧化碳超临界流体萃取物。本发明所称的“牛樟芝”为中国台湾特有真菌,属真菌分类学中担子菌亚门(Basidiomycotina)、层菌纲(Hymenomycetes)、非褶菌目(Aphyllophorales)、多孔菌科(Polyporaceae)、薄孔菌属(Antrodia)的多年生菌类,其学名为Antrodiacinnamomea、Ganodermacomphoratum、Antrodiacamphorata或Taiwanofunguscamphoratus。本发明所称的“牛樟芝子实体”是指牛樟芝产生的多细胞有性产孢结构,其上附有产孢的子囊、担子等构造,子实体是牛樟芝生活史中的有性阶段,为一年生至多年生,呈鲜红色、橘红色或淡肉桂色,具有樟树香气。根据本发明的牛樟芝子实体可自牛樟树采集而得或自牛樟树椴木培养而得,优选地,为自牛樟树椴木培养而得。根据本发明的该牛樟芝子实体的二氧化碳超临界流体萃取物是指以二氧化碳超临界流体萃取牛樟芝子实体所得的萃取物。超临界流体是指当超过临界温度及临界压力以上,气体与液体的性质会趋近于类似,最后会达成一个均匀相(homogenous)的流体状态。超临界流体类似气体具有可压缩性,兼具有类似液体的流动性,可用于萃取,也有商用的超临界流体萃取设备可供使用,例如NATEX、SEPAREX、UHDE及台超科都提供有商用的超临界流体萃取设备,其型号规格一般都以萃取槽能处理的容量表示,自500g至2000kg可供选择,可依所需选取合适的超临界流体萃取设备。在本发明的一个具体实施例中,该牛樟芝子实体的二氧化碳超临界流体萃取物的萃取压力为约150bar至约1000bar;优选为约200bar至约800bar;更优选为约350bar至约600bar。在本发明的一个具体实施例中,该牛樟芝子实体的二氧化碳超临界流体萃取物的萃取温度为约25℃至约80℃;优选为约35℃至约70℃;更优选为约40℃至约65℃。在本发明的一个具体实施例中,该牛樟芝子实体的二氧化碳超临界流体萃取物的二氧化碳流量为约20kg/h至约70kg/h;优选为约30kg/h至约60kg/h;尤其优选为约35kg/h至约55kg/h。在本发明的一个具体实施例中,该牛樟芝子实体的二氧化碳超临界流体萃取物的萃取时间为约40分钟至约120分钟;优选为约50分钟至约100分钟。在本发明的一个具体实施例中,该牛樟芝子实体的二氧化碳超临界流体萃取物为在共溶剂的存在下进行萃取,该共溶剂例如约1%至约10%的95%乙醇。在本发明的一个具体实施例中,该牛樟芝子实体的二氧化碳超临界流体萃取物的萃取中,牛樟芝子实体与二氧化碳超临界流体的重量比例为约10:1至约1:10;优选为约5:1至约1:5;更优选为约3:1至1:3。在本发明的一个优选的具体实施例中,该牛樟芝子实体先粉碎为小块,更优选地,将小块搅碎为粉末。切块和/或搅碎的方式为本领域技术人员所熟知。优选地,该超临界流体萃取方法进一步包含一浓缩步骤。在一个优选的具体实施例中,该牛樟芝子实体的二氧化碳超临界流体萃取物是在二氧化碳超临界流体萃取后,以一模拟移动床(SimulatedMovingBed,简称SMB)及碳18固体吸附剂浓缩,并收集亨利常数为2.8以上的组份。根据本发明的模拟移动床,是根据牛樟芝活性成分的极性特性(亨利常数H),将该牛樟芝的活性成分分离并浓缩,其实施方式如中国台湾专利第I487531号中“浓缩步骤”所述,其相关内容以引用方式并入本文。根据本发明的红血球和/或血小板低下是指任何原因所引起的红血球和/或血小板低下,例如先天性或后天性所引起,或是因其他疾病、药物所引起。在本发明的一个优选的具体实施例中,该红血球和/或血小板低下是因药物导致的红血球和/或血小板低下;优选地,该药物为治疗肿瘤且具有骨髓抑制副作用的药物,例如治疗癌症的化学治疗药物。本发明所称的“化学治疗药物”是指抑制癌细胞分裂的药物。本发明所称的“骨髓抑制”是指因使用化学治疗药物,而使骨髓造血细胞正常生理状况受影响的一种副作用,其症状包含白血球、红血球和/或血小板数降低。在本发明的具体实施例中,该肿瘤包含但不限于恶性淋巴瘤、Wilm's氏瘤、头颈部鳞状细胞癌、骨癌、骨转移型病变的高血钙症或睪丸癌。在本发明的具体实施例中,该药物包含但不限于苯丁酸氮芥(Chlorambucil)、阿糖胞苷(Cytarabine)、更生霉素(Dactinomycin)、博来霉素(Bleomycin)、普卡霉素(Pilcamycin)、依托泊苷(Etoposide)、亚硝基脲(nitrosourea)或环磷酰胺(cyclophosphamid);优选为环磷酰胺。在本发明的一个优选的具体实施例中,该牛樟芝子实体萃取组合物另外包含芝麻萃取物。本发明所称的“芝麻”又称胡麻、脂麻、油麻,为胡麻科胡麻属植物,其学名为Sesamumindicum,优选地,是指芝麻植株的种子。本发明所称的“芝麻萃取物”是指将芝麻种子的活性成分萃取所得的混合物,其萃取方法包含但不限于溶剂萃取、超临界流体萃取、热萃取、固相萃取,优选为超临界流体萃取,更优选为二氧化碳超临界流体萃取。在本发明的一个优选的具体实施例中,该芝麻萃取物为芝麻素(sesamin),本发明所称的“芝麻素”是指芝麻中脂溶性抗氧化群芝麻木酚素(lignans)的成份。根据本发明的芝麻与牛樟芝可分别萃取再合并为该牛樟芝子实体萃取组合物,例如分别制备芝麻萃取物及牛樟芝子实体的二氧化碳超临界流体萃取物,再视需要添加载剂/赋形剂制得该牛樟芝子实体萃取组合物。在本发明的一个优选的具体实施例中,该芝麻萃取物及牛樟芝子实体的二氧化碳超临界流体萃取物的混合重量比例为约1:3至约3:1;更优选为约1:2至约2:1。另一方面,根据本发明的芝麻与牛樟芝子实体可合并共同使用二氧化碳超临界流体萃取,再视需要添加载剂/赋形剂制得该牛樟芝子实体萃取组合物。在本发明的一个优选的具体实施例中,该芝麻及牛樟芝子实体的混合重量比例为约1:3至约3:1;更优选为约1:2至约2:1。优选地,根据本发明的该牛樟芝子实体萃取组合物可治疗红血球和/或血小板低下并发白血球低下,以全方位治疗骨髓抑制的副作用,并改善熟知使用颗粒性巨噬细胞株刺激因子时,虽提高周边血内中性球、单核球及淋巴球数目,但却降低血色素和血小板数目的问题,也避免使用颗粒性巨噬细胞株刺激因子所引起的副作用。在本发明的具体实施例中,该治疗红血球和/或血小板低下并发白血球低下包含但不限于促进白血球总数增加、促进颗粒性白血球数增加、促进嗜中性球数增加、促进淋巴球数增加、促进单核球数增加、增加颗粒性巨噬细胞株刺激因子(granulocyte-macrophagecolony-stimulatingfactor)分泌。另一方面,根据本发明的该牛樟芝子实体萃取组合物可治疗红血球和/或血小板低下并发体重减轻。由于癌症病患几乎都合并体重减轻,根据本发明的该牛樟芝子实体萃取组合物可在治疗骨髓抑制的同时一并治疗体重减轻,从而更广泛地辅助癌症化学药物的治疗。在本发明的BALB/c小白鼠动物实验模型中,针对牛樟芝子实体萃取组合物对环磷酰胺(CTX)诱发的骨髓抑制副作用进行功效测试,实验小鼠在第0天依体重分别以IP腹腔注射方式给予化学治疗药CTX300mg/kg,诱发实验动物产生骨髓抑制的模型﹔牛樟芝子实体萃取组合物则分别在第1天到第4天开始以口服(PO)方式施用测试物质。结果显示施用CTX其化学治疗药毒性会造成各组小鼠在第4天红血球数目降至低点,而口服牛樟芝子实体萃取组合物则可提升红血球数目达1.19倍,在第7天也持续提升红血球数目达1.23倍;另一方面,施用CTX在第7天会使小鼠血小板数目显著性下降,相较于第0天,CTX会造成血小板数目下降约为50%﹔管喂不同浓度的牛樟芝子实体萃取组合物具有保护血小板数目的能力。针对白血球低下而言,当小鼠施用单一剂量的CTX(300mg/kg),会使得小鼠的白血球数目在第4天显著性下降至最低点﹔在第7天白血球数目则开始上升。针对此两个观察点(Day4、Day7)进行分析,管喂牛樟芝子实体萃取组合物的各组小鼠白血球数目也都在第4天降至最低点(白血球下降比例范围约为86.7~91.5%)﹔各组小鼠在第0天施用CTX后都在第7天白血球数目开始上升。CTX组白血球在第7天上升约3倍,牛樟芝子实体萃取组合物处理下具有显著促进白血球数目增加的趋势。进一步分析牛樟芝子实体萃取组合物次族群颗粒性白血球、嗜中性球、单核球及淋巴球血球变化的影响评估。结果显示,在第0天施用单一剂量的CTX(300mg/kg),会造成小鼠在第4天的颗粒性白血球、嗜中性球数目降至最低点﹔在第7天可观察到颗粒性白血球数目开始上升﹔而测试物牛樟芝子实体萃取组合物具有2倍的显著性促进颗粒性白血球上升的能力;另一方面,在第7天牛樟芝子实体萃取组合物可提升嗜中性球数目达2.93倍;另外,施用化学治疗药CTX也会在第4天造成淋巴球、单核球数目显著性减少,同时也发现在第7天口服牛樟芝子实体萃取组合物可提升淋巴球数目达2.49倍;在单核球数目的表现,牛樟芝子实体萃取组合物在第7天其有促使单核球上升的潜力。针对体重减轻而言,施用单一剂量的CTX(300mg/kg)的各组小鼠,和空白组相较之下,施用CTX的小鼠在第三天其体重开始下降(约10%左右的降幅)﹔而管喂牛樟芝子实体萃取组合物的小鼠则观察到体重回升,因此本发明的牛樟芝子实体萃取组合物可治疗体重低下。针对增加颗粒性巨噬细胞株刺激因子分泌而言,以LPS诱发单核球细胞产生细胞激素GM-CSF,作为正控制组。利用此测试平台,探讨牛樟芝子实体萃取组合物对于细胞激素GM-CSF生成量的影响,用ELISA将所测得的O.D.450nm吸光值转换成百分比,以THP-1细胞株本身分泌的GM-CSF生成量当作100%,正控制组则因THP-1细胞通过LPS刺激其细胞激素GM-CSF生成量平均约可增加1.6倍,当THP-1细胞处理不同浓度的测试样品牛樟芝子实体萃取组合物,发现随着牛樟芝子实体萃取组合物浓度增加,其GM-CSF生成量也相对增加。由此结果发现,测试物牛樟芝子实体萃取组合物的浓度与GM-CSF生成量呈现剂量效应(dose-dependent)的关系,高浓度100μg/ml的牛樟芝子实体萃取组合物约可诱发GM-CSF生成量增加约1.3倍。以下的非限制性的实例有助于本领域技术人员实施本发明。这些实例不应视为过度地限制本发明。本领域技术人员可在不背离本发明的精神或范围的情况下对本文所讨论的实施例进行修改及变化,而仍属于本发明的范围。实施例牛樟芝子实体萃取组合物牛樟芝子实体的二氧化碳超临界萃取物(SR4)取105克的牛樟芝子实体,破碎成颗粒大小约为5毫米见方的颗粒,置于超临界流体萃取设备的萃取槽中,设定该萃取槽的内部压力为350bar,内部温度为50℃,辅溶剂为95%乙醇,并以每分钟3毫升的速率进料,其中牛樟芝子实体与二氧化碳超临界流体的重量比例为20:80至40:60,二氧化碳超临界流体量为35至55kg/h),由于该牛樟芝萃取液呈膏状,其中仍包含有95%乙醇,另以温度设定为30~35℃烘箱将该膏状牛樟芝萃取液中的乙醇去除,以便进行后续的浓缩步骤。浓缩步骤为以模拟移动床作为一种连续进料式的纯化平台,对该牛樟芝萃取液中不同亨利常数的成份进行群组分离;本实例模拟移动床的固定相(Stationaryphase,简称SP)为碳18管柱,本实例的移动相(Mobilephase,简称MP)为水及甲醇的混合液,该水含有0.05%的醋酸,以该移动相溶解该牛樟芝萃取物,该水及甲醇的重量比例优选为20:80至40:60,该水及甲醇更优选的重量比例为22:78,使该移动相的选择因子(Selectivefactor)为大于1.3,能够更有效地分离出不同极性特性的组份A及组份B。本实施例的模拟移动床包含至少三分离区域,其依序为α、β及γ区域,其中该α区域的后端设有一第一出料口Oα(称作Extractoutlet),该γ区域的后端设有一第二出料口Oγ(称作Raffinateoutlet),该进料口I(称作Feedinlet)则设于该β及γ区域之间。该三分离区域α、β及γ分别由二管柱c组成,该三分离区域的管柱c相互连通,该管柱c内填充该固定相,特别地该固定相的颗粒间具有孔隙供该移动相通过,并使该移动相朝同一方向依序流经该α、β及γ区域的管柱c内,该固定相则以一进料口切换装置在一进料口切换时间Tsw后改变该进料口I在该三分离区域的相对位置,使该固定相相对该移动相朝另一方向模拟移动。根据模拟移动床的三角理论,所欲分离组份包括:亨利常数为2.8以上的组份A及亨利常数为2.8以下的组份B,各三分离区域α、β及γ中,该组份A的净质量通量FA及该组份B的净质量通量FB符合表1的条件,使该组份A往该区域α移动,该组份B往该区域γ移动,且各该三分离区域α、β及γ的流速比值n(各分离区域α、β及γ的流速比值分别为nα、nβ及nγ)为与所欲分离组份的极性(即组份A的亨利常数为HA,组份B的亨利常数为HB)相关,各流速比值nα、nβ及nγ应符合如表1的条件,其中,各组份的亨利常数H为根据公式Ⅰ计算而得,T0为不被固定相吸附的物质流经管柱的滞留时间(T0=1.71),Tr为欲分离组份的滞留时间,ε为本实例所使用管柱的孔隙度(0.412)。表1:本实例各分离区域的净质量通量F、流速比值n与亨利常数H的条件设定区域αβγ净质量通量FFB>0;FA>0FB>0;FA<0FB>0;FA<0流速比值nnα>HA>HBHA>nβ>HBHA>nγ>HB本实例的模拟移动床由一液泵(HITACHIL-2130)进行加压,使移动相在各区域的管柱内朝向同一方向流动,设定本实例的进料口切换时间Tsw,以模拟该固定相朝向与该移动相流向相反的条件,并以第2表所示的条件分离该牛樟芝萃取物,并在该第一出料口Oα获得该亨利常数为2.8以上的组份A,该第二出料口Oγ获得该亨利常数为2.8以下的组份B,即为牛樟芝子实体的二氧化碳超临界萃取物(SR4)。牛樟芝子实体萃取组合物(SR4s)包含牛樟芝子实体的二氧化碳超临界萃取物及芝麻萃取物取250克的芝麻,置于超临界流体萃取设备的萃取槽中,设定该萃取槽的内部压力为350bar,内部温度为50℃,辅溶剂为95%乙醇,并以每分钟3毫升的速率进料,其中芝麻与二氧化碳超临界流体的重量比例为50:91,由于该芝麻萃取液呈膏状,其中仍包含有95%乙醇,另以温度设定为30~35℃烘箱将该膏状芝麻萃取液中的乙醇去除,以制得芝麻萃取物。将前述所得的芝麻萃取物与牛樟芝子实体的二氧化碳超临界萃取物(SR4)依重量比7:9调配,以获得牛樟芝子实体萃取组合物(SR4s)。牛樟芝子实体萃取组合物的疗效试验材料与方法[动物模型]以化学治疗药物环磷酰胺(CTX)施用BALB/c公鼠(mouse),使动物产生因化学治疗药物诱发的骨髓抑制,观察受试物质是否改善由化学治疗药物所产生的骨髓抑制作用。[试验方法]实验动物以口服(PO)方式施用受试物,主要分析其白血球及次族群颗粒性白血球、淋巴球、红血球及血小板数目的变化。[试验物质]前述所制得的牛樟芝子实体的二氧化碳超临界萃取物(SR4)及牛樟芝子实体萃取组合物(SR4s)。[实验设计]试验药品及配置化学治疗药CTX(SigmaChemicalCo.CASNumber:6500-19-2(StLouis,MO,USA))、颗粒性巨噬细胞株刺激因子(G-CSF,Filgrastim,Cat.08502A,KirinBreweryCo.Ltd.,Japan)。CTX加入生理食盐水配置终浓度为45mg/mL作为腹腔注射(IP)剂型,每只小鼠每公斤体重施用300mg。测试物SR4s、SR4分别溶于DMSO(Dimethylsulfoxide,购自sigma),其浓度为125mg/mL﹔各组测试物浓度为12.5mg/mL以二次水稀释十倍终浓度为1.25mg/mL的口服试剂,每公斤体重为10mg/Kg。实验动物饲养及分组本试验的实验动物为BALB/c小白鼠:6-8周大,雄性,所有动物购自乐斯科生物科技股份有限公司,饲育于25±2℃,湿度范围40-70%,12小时光照/黑暗交替,其饮水不限制。购入后给予小鼠一周的适应期,秤重后以随机分组方式,让各组间的平均体重无差异,动物共分十二组每组五只。化学治疗药CTX与测试物质实验设计实验小鼠于第0天依体重分别以IP腹腔注射方式施用化学治疗药CTX300mg/kg,诱发实验动物产生骨髓抑制的模型﹔各试验组SR4s、SR4则分别在第1天到第4天开始以口服(PO)方式施用测试物质。试验过程中,每隔三天秤重并记录观察小鼠的体重变化﹔在第0、4及7天进行采血并观察血项变化。血液学分析将实验动物徒手固定以脸颊采血(Lancet,facialveininMice)方式,利用采血针扎进小鼠面部的下颌骨的后面,以离心管收集流出的血液,采得足够的血量后以无菌纱布压住出血口10-30sec进行止血。将已收集的小鼠周边微量血轻拍摇匀,取出20μL的血液,并由细胞稀释液进行五倍稀释后,通过XT-1800i血液分析仪(SYSMEX)进行血液细胞定量检测。结果SR4s、SR4治疗CTX诱发的红血球及血小板数目低下如表1及表2所示,施用CTX其化学治疗药毒性会造成各组小鼠在第4天红血球数目降至低点,而口服SR4s可提升红血球数目达1.19倍,SR4可提升红血球数目达1.18倍,在第7天也持续提升红血球数目,口服SR4s可提升红血球数目达1.17倍,SR4可提升红血球数目达1.23倍。施用单一剂量的CTX(300mg/kg)对于小鼠的血小板数目的影响。如表2所示,施用CTX在第7天会使小鼠血小板数目显著性下降,相较于第0天,CTX会造成血小板数目下降约为50%﹔管喂不同浓度的测试物SR4s、SR4各组都具有保护血小板数目的潜力,尤其以测试物SR4对于保护血小板数目的能力表现最佳。表1:第4天的血液分析结果表2:第7天的血液分析结果SR4s、SR4治疗CTX诱发的白血球及其次族群颗粒性白血球、嗜中性球、单核球及淋巴球数目降低由表1及2结果发现,当小鼠施用单一剂量的CTX(300mg/kg),会使得小鼠的白血球数目在第4天显著性下降至最低点﹔在第7天白血球数目则开始上升。针对此两个观察点(Day4、Day7)进行分析,管喂测试物SR4s、SR4的各组小鼠白血球数目也都在第4天降至最低点(白血球下降比例范围约为86.7~91.5%)﹔各组小鼠在第0天施用CTX后都在第7天白血球数目开始上升。由结果得知,CTX组白血球在第7天上升约3倍,测试物SR4s、SR4处理下具有显著性促进白血球数目增加的趋势(血球上升分别为7、5倍)。进一步分析测试物SR4s、SR4对次族群颗粒性白血球、嗜中性球、单核球及淋巴球血球变化的影响评估。由表1及2结果显示,在第0天施用单一剂量的CTX(300mg/kg),会造成小鼠在第4天的颗粒性白血球、嗜中性球数目降至最低点﹔在第7天可观察到颗粒性白血球数目开始上升﹔而测试物SR4s具有2倍的显著性促进颗粒性白血球上升的能力;另一方面,在第7天口服SR4可提升嗜中性球数目达2.93倍,SR4s可提升嗜中性球数目达1.99倍。另外,施用化学治疗药CTX也会在第4天造成淋巴球、单核球数目显著性减少,在第7天口服SR4可提升淋巴球数目达2.49倍;在单核球数目的表现,测试物SR4s在第7天其有促使单核球上升的潜力。SR4s、SR4治疗CTX诱发的体重减轻试验动物施用化学治疗药对体重的影响,结果显示,施用单一剂量的CTX(300mg/kg)的各组小鼠,和空白组相较之下,施用CTX的小鼠在第三天其体重开始下降(约10%左右的降幅),因而单一剂量的CTX(300mg/kg)其化学治疗药的毒性会造成试验动物小鼠体重有下降趋势﹔而管喂测试物SR4的小鼠则观察到体重回升,因此本发明的牛樟芝子实体萃取组合物可治疗体重低下。牛樟芝子实体萃取组合物的增加颗粒性巨噬细胞株刺激因子功效实验材料与方法[实验材料]细胞株:THP-1细胞株[ATCC-TIB-202]。细胞培养及实验相关所需试剂:RPMI-1640培养基、胎牛血清(fetalcalfserum,FCS)及2-巯基乙醇(2-mercaptoethanol)。脂多醣(lipopolysaccharide﹔LPS,购自Sigma)、HumanGM-CSFELISAkit(Biolegend)等。[试验方法]THP-1细胞株培养:THP-1细胞是一种悬浮性-人类单核球急性白血癌细胞株(humanmonocyticleukemiacellline),培养在RPMI培养基含10%FCS及2-巯基乙醇,培养在37℃、5%CO2的培养箱内。约每2-3天更换一次培养基溶液,当培养瓶内细胞长满约8成,则进行继代培养(subculture)。实验时,以Vi-cell细胞计数器计算细胞数量,再取适当细胞数目进行实验。实验材料制备SR4、SR4s都溶于DMSO,浓度为125mg/ml,存放于4℃备用,使用时再稀释至所需的浓度。LPS的配制(浓度为10mg/ml),将LPS溶于1xPBS,分装后储存于-20℃备用。实验时,再稀释至所需的浓度。利用THP-1细胞作为平台进行细胞激素GM-CSF的测试THP-1细胞4×105个/孔,种至12孔盘,培养六小时后,分为控制组(0μg/ml)、LPS组(1μg/ml)及实验组(分别加入各种不同浓度的药物处理,0.01,0.1,1,10,100μg/ml),各做三重复,在37℃、5%CO2的培养箱内,培养24小时。次日,将细胞从培养箱取出,离心(1000rpm,5分钟,4℃),收集细胞上清液,并利用GM-CSFELISAkit测其细胞内所释放的细胞激素GM-CSF的含量。人类GM-CSFELISA检测利用HumanGM-CSFELISA试剂盒(Biolegend)进行细胞激素GM-CSF分析。先于96孔盘上涂覆捕捉抗体100μl/孔,4℃静置12-16小时﹔次日,将反应剂及待测样品置于室温中,回温备用﹔将先前已涂覆的96孔盘以清洗缓冲液进行清洗,并进行阻断200μl/孔,室温静置1小时,再以清洗缓冲液进行清洗﹔配置标准溶液分别为500,250,125,62.5,31.2,15.6,7.8pg/ml﹔再将待测样品和已系列稀释的标准溶液分别加入96孔盘,室温静置2小时﹔清洗后,加入侦测抗体,室温静置1小时﹔清洗后,加入100μl/孔的受质溶液(着色反应剂A+B),在室温下避光反应30分钟,再加入终止溶液终止反应。以ELISA读取仪测其O.D.450nm的吸光值,并将所测得的O.D.值利用其标准曲线的R-squared,以内插法计算其细胞激素GM-CSF的浓度。结果以LPS诱发单核球细胞产生细胞激素GM-CSF,作为正控制组。利用此测试平台,探讨测试样品SR4s、SR4对于细胞激素GM-CSF生成量的影响,其结果示于图1及图2。利用ELISA将所测得的O.D.450nm吸光值转换成百分比,以THP-1细胞株本身分泌的GM-CSF生成量当作100%,正控制组则因THP-1细胞经由LPS刺激其细胞激素GM-CSF生成量平均约可增加1.6倍,当THP-1细胞处理不同浓度的测试样品SR4s,发现随着SR4s浓度增加,其GM-CSF生成量也相对增加。由此结果发现,测试物SR4s的浓度与GM-CSF生成量呈现剂量效应(dose-dependent)的关系,高浓度100μg/ml的SR4s约可诱发GM-CSF生成量增加约1.3倍。上述实施例仅为说明本发明的原理及其功效,而非限制本发明。本领域技术人员对上述实施例所做的修改及变化仍不违背本发明的精神。本发明的权利范围应如权利要求书所列。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1