一种抑制阿霉素心脏毒性的中药组合物及其制备方法与流程
本发明属于中药组合物
技术领域:
,具体涉及一种抑制阿霉素心脏毒性的中药组合物及其制备方法。
背景技术:
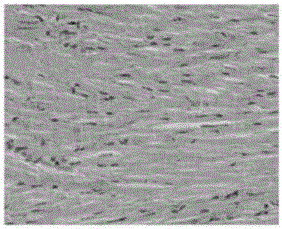
:阿霉素是蒽环类抗生素,自20世纪60年代发现并应用于多种癌症的治疗,现在仍然是最有效的抗癌药物之一。适用于恶性淋巴瘤、乳腺癌、肺癌、卵巢癌、骨及软组织肉瘤等多种肿瘤。但由于严重的心脏毒性,其临床应用受到一定影响。近年来,对阿霉素心脏毒性的研究较多,阿霉素中毒分为急性毒性、亚急性毒性和慢性毒性。急性中毒发生于单次使用或一个疗程后,常见症状有低血压、心律失常、心脏功能不全等,偶尔可发生心肌梗死。因此,寻找可以有效解除阿霉素心脏毒性的物质已经成为目前亟待解决的问题,但目前尚缺乏有效预防和治疗方法。植物化学研究表明,附子生物碱是附子中的有效组分、干姜挥发油和姜辣素类化合物是干姜中的有效组分、甘草黄酮和总皂苷是甘草中的有效组分。四逆汤通过用附子生物碱、干姜挥发油、姜辣素类化合物、甘草黄酮、甘草皂苷五大类组分、多途经、整合调节机制发挥抑制阿霉素心脏毒性的作用,具有高度复杂性和整体性。但传统的四逆汤中药方剂配伍目前尚停留在中药饮片的配伍,成分庞杂繁复,药效物质基础不明确,难于质量控制。四逆汤抑制阿霉素心脏毒性的各组方药材有效部位的功效各有不同和侧重,用有效部位的配伍代替全方,既具备中药整体的作用特点,同时降低了其复杂性,便于药物的质量控制。因此,提供更加方便有效的抑制阿霉素心脏毒性的有效部位复方组合物具有重要的临床意义。技术实现要素:本发明所要解决的技术问题在于针对上述现有技术的不足,提供了一种用于抑制阿霉素心脏毒性的中药组合物。该中药组合物能有效的抑制阿霉素心脏毒性,对患者治疗肿瘤的同时能够减轻阿霉素对心脏产生的副作用,解决了目前患者服用阿霉素的同时带来的低血压、心律失常、心脏功能不全,甚至心肌梗死等副作用。为解决上述技术问题,本发明采用的技术方案是:一种抑制阿霉素心脏毒性的中药组合物,其特征在于,由以下质量百分数的有效成分制成:附子生物碱提取物30%~42%、干姜挥发油提取物1%~3%、干姜姜辣素类化合物提取物24%~28%、甘草黄酮提取物15%~22%和甘草皂苷提取物15%~22%。上述的一种抑制阿霉素心脏毒性的中药组合物,其特征在于,由以下质量百分数的有效成分制成:附子生物碱提取物32%~40%、干姜挥发油提取物2%、干姜姜辣素类化合物提取物24%~26%、甘草黄酮提取物16%~20%和甘草皂苷提取物16%~20%。上述的一种抑制阿霉素心脏毒性的中药组合物,其特征在于,由以下质量百分数的有效成分制成:附子生物碱提取物36%、干姜挥发油提取物2%、干姜姜辣素类化合物提取物26%、甘草黄酮提取物18%和甘草皂苷提取物18%。上述的一种抑制阿霉素心脏毒性的中药组合物,其特征在于,所述附子生物碱提取物中附子生物碱的质量百分含量为30%~50%,所述干姜挥发油提取物中干姜挥发油的质量百分含量为90%~99%,所述干姜姜辣素类化合物提取物中姜辣素类化合物的质量百分含量为60%~80%,所述甘草黄酮提取物中甘草黄酮的质量百分含量为30%~60%,所述甘草皂苷提取物中甘草皂苷的质量百分含量为40%~60%。另外,本发明还提供了一种制备如上述抑制阿霉素心脏毒性的中药组合物的方法,该方法包括以下步骤:步骤一、附子生物碱提取物的制备:步骤101、取附子炮制品,粉碎后加入体积百分含量为50%的乙醇溶液,在温度为100℃的水浴中回流提取2~3次,每次提取3h,合并前后2~3次的提取液,得到混合液;每次提取过程中所述乙醇溶液的用量为所述附子炮制品质量的7~9倍;步骤102、向步骤101中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克附子炮制品;步骤103、离心除去步骤102中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱上端,静置吸附1h后,采用去离子水洗脱,弃去洗脱液,再采用5倍柱体积的70%乙醇洗脱,收集洗脱液,浓缩后,采用真空干燥后得到附子生物碱提取物;所述乙醇溶液中乙醇的体积百分含量为70%;步骤二、干姜挥发油提取物的制备:采用CO2超临界萃取制备干姜挥发油,取干姜粗粉,以体积百分含量为95%的乙醇溶液为夹带剂,在温度为40℃,压力为30MPa的条件下萃取1h,得棕黄色乙醇溶液,减压回收乙醇后,经无水硫酸钠干燥,得具有特殊浓郁香味的棕黄色干姜挥发油;所述夹带剂的质量为干姜粗粉质量的1.5~2倍;步骤三、干姜姜辣素类化合物提取物制备:采用乙醇渗漉法制备干姜姜辣素类化合物提取物,取干姜粗粉,装入渗滚筒中,装完后先向筒内加入4倍干姜粗粉质量的乙醇冷浸2h后,再加入8倍干姜粗粉质量的体积百分含量为85%的乙醇溶液,然后以5mL/(kg·min)的渗漉速度渗漉,收集渗漉液,减压液浓缩至干,即得干姜姜辣素类化合物提取物;步骤四、甘草黄酮提取物制备:步骤401、称取甘草,粉碎后加入乙醇中,在温度为100℃的水浴中回流提取2次,每次提取2h,得提取液,然后合并前后2次的提取液,得到混合液,每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的6倍;步骤402、将步骤401中所述混合液离心后,减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤403、将步骤402中所述浓缩液加至过D101大孔树脂柱上端,先用6倍体积的纯水洗脱除杂,再用5倍体积的乙醇洗脱,收集洗脱液,将洗脱液减压浓缩,再加至HZ915聚酰胺树脂柱,用5倍体积的乙醇洗脱,收集洗脱液,减压浓缩后干燥,得到甘草黄酮提取物;步骤五、甘草皂苷提取物制备:步骤501、称取甘草,然后粉碎后加入体积百分含量为70%的乙醇溶液,在温度为100℃的水浴中回流提取2次,每次2h,合并前后2次的提取液,得到混合液;每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的8倍;步骤502、向步骤501中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤503、离心除去步骤502中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱的上端,用6倍体积的百分数为30%的乙醇溶液除杂,再用5倍体积的体积百分含量为50%的乙醇洗脱,收集洗脱液,减压浓缩后,得到甘草皂苷提取物;步骤六、将步骤一中制备得到的附子生物碱提取物、步骤二中制备得到的干姜挥发油提取物、步骤三中制备得到的干姜姜辣素类化合物提取物、步骤四中制备的甘草黄酮提取物和步骤五中制备的甘草皂苷提取物混合,得到用于抑制阿霉素心脏毒性的中药组合物。上述的方法,其特征在于,步骤101中每次提取过程中所述乙醇溶液的用量为所述附子炮制品质量的8倍。上述的方法,其特征在于,步骤二中所述夹带剂的质量为干姜粗粉质量的1.5倍。本发明与现有技术相比具有以下优点:1、本发明的中药组合物中附子生物碱、干姜挥发油、姜辣素类化合物、甘草黄酮、甘草皂苷五大类组分、多途经、整合调节机制发挥抑制阿霉素心脏毒性的作用,具有高度复杂性和整体性,并且对机体的心肌组织代谢正常。2、本发明制备的中药组合物抑制阿霉素心脏毒性的药效不仅优于传统中药的汤剂,且服用方便,质量稳定可控,可长期保存。3、本发明制备附子生物碱提取物、干姜挥发油提取物、干姜姜辣素类化合物提取物、甘草黄酮提取物和甘草皂苷提取物的方法简单,得到的有效成分的纯度较高,并且方法易于操作。下面通过附图和实施例对本发明的技术方案作进一步的详细说明。附图说明图1是本发明实施例1步骤一中制备的附子生物碱有效组分的高效液相色谱分析谱图。图2是本发明实施例1步骤二中干姜挥发油提取物的气相色谱-质谱分析谱图。图3是本发明实施例1步骤三中制备的干姜姜辣素类化合物提取物的高效液相色谱分析谱图。图4是本发明实施例1步骤四中制备的甘草黄酮提取物的高效液相色谱分析谱图。图5是本发明实施例1步骤五中制备的甘草皂苷提取物的高效液相色谱分析谱图。图6是本发明实施例1制备的中药组合物对阿霉素心脏毒性的药效试验中正常对照组SD大鼠在400倍光镜下观察组织形态学照片。图7是本发明实施例1制备的中药组合物对阿霉素心脏毒性的药效试验中阿霉素模型组SD大鼠在400倍光镜下观察组织形态学照片。图8是本发明实施例1制备的中药组合物对阿霉素心脏毒性的药效试验中阿霉素+传统中药水煎组SD大鼠在400倍光镜下观察组织形态学照片。图9是本发明实施例1制备的中药组合物对阿霉素心脏毒性的药效试验中阿霉素+中药组合物组SD大鼠在400倍光镜下观察组织形态学照片。图10是本发明实施例1制备的中药组合物对阿霉素心脏毒性的药效试验中心肌组织代谢物气相色谱质谱的指纹图谱。图11是本发明实施例1制备的中药组合物对阿霉素心脏毒性的药效试验中正常对照组和阿霉素模型组经过主成分分析的得分图。图12是本发明实施例1制备的中药组合物对阿霉素心脏毒性的药效试验中正常对照组与阿霉素模型组之间的S-plot图。具体实施方式实施例1本实施例中抑制阿霉素心脏毒性的中药组合物由以下质量百分数的有效成分制成:附子生物碱提取物36%、干姜挥发油提取物2%、干姜姜辣素类化合物提取物26%、甘草黄酮提取物18%和甘草皂苷提取物18%;该制备方法包括以下步骤:步骤一、附子生物碱提取物的制备:步骤101、取1000g附子炮制品,粉碎后加入体积百分含量为50%的乙醇溶液,在温度为100℃的水浴中回流提取,每次提取3h,合并前后2次的提取液,得到混合液;2次提取过程中所述乙醇溶液的用量为所述附子炮制品质量的8倍;步骤102、向步骤101中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克附子炮制品;步骤103、离心除去步骤102中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱上端,静置吸附1h后,采用去离子水洗脱,弃去洗脱液,再采用5倍柱体积的70%乙醇洗脱,收集洗脱液,浓缩后,采用真空干燥后得到附子生物碱提取物;所述乙醇溶液中乙醇的体积百分含量为70%;步骤二、干姜挥发油提取物的制备:采用CO2超临界萃取制备干姜挥发油,取干姜粗粉,以体积百分含量为95%的乙醇溶液为夹带剂,在温度为40℃,压力为30MPa的条件下萃取1h,得棕黄色乙醇溶液,减压回收乙醇后,经无水硫酸钠干燥,得具有特殊浓郁香味的棕黄色干姜挥发油;所述夹带剂的质量为干姜粗粉质量的1.5倍;步骤三、干姜姜辣素类化合物提取物制备:采用乙醇渗漉法制备干姜姜辣素类化合物提取物,取干姜粗粉,装入渗滚筒中,装完后先向筒内加入4倍干姜粗粉质量的乙醇冷浸2h后,再加入8倍干姜粗粉质量的体积百分含量为85%的乙醇溶液,然后以5mL/(kg·min)的速度渗漉,收集渗漉液,减压液浓缩至干,即得干姜姜辣素类化合物提取物;步骤四、甘草黄酮提取物制备:步骤401、称取甘草,粉碎后加入乙醇中,在温度为100℃的水浴中回流提取2次,每次提取2h,得提取液,然后合并前后2次的提取液,得到混合液,每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的6倍;步骤402、将步骤401中所述混合液离心后,减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤403、将步骤402中所述浓缩液加至过D101大孔树脂柱上端,先用6倍体积纯水洗脱除杂,再用5倍体积的乙醇洗脱,收集洗脱液,将洗脱液减压浓缩,再加至HZ915聚酰胺树脂柱,用5倍体积的乙醇洗脱,收集洗脱液,减压浓缩后干燥,得到甘草黄酮提取物;所述甘草黄酮提取物中甘草黄酮的质量百分含量为30%~60%;步骤五、甘草皂苷提取物制备:步骤501、称取甘草,然后粉碎后加入体积百分含量为70%的乙醇溶液,在温度为100℃的水浴中回流提取2次,每次2h,合并前后2次的提取液,得到混合液;每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的8倍;步骤502、向步骤501中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤503、离心除去步骤502中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱的上端,用6倍体积的百分数为30%的乙醇溶液除杂,再用5倍体积的体积百分含量为50%的乙醇洗脱,收集洗脱液,减压浓缩后,得到甘草皂苷提取物;步骤六、将步骤一中制备得到的附子生物碱提取物、步骤二中制备得到的干姜挥发油提取物、步骤三中制备得到的干姜姜辣素类化合物提取物、步骤四中制备的甘草黄酮提取物和步骤五中制备的甘草皂苷提取物混合,得到用于抑制阿霉素心脏毒性的中药组合物。一、对本实施例中步骤一制备的附子生物碱提取物的成分进行分析:(1)附子生物碱提取物中附子生物碱含量测定:称取步骤一中制备的附子生物碱提取物的固体粉末0.1003g,加乙醇5ml溶解,调PH至10~11,氯仿萃取2次,每次10ml,取氯仿层挥干,残渣加5mL乙醇使其溶解,精密加入15mL硫酸滴定液(硫酸滴定液的摩尔浓度为0.01mol·L-1)、15mL水与3滴甲基红指示液,用氢氧化钠滴定液(氢氧化钠滴定液的摩尔浓度为0.02mol·L-1)滴定至黄色。以1mL硫酸滴定液(硫酸滴定液的摩尔浓度为0.01mol·L-1)相当于12.9mg的乌头(乌头按化学式C34H47NO11计)计算,0.1g附子生物碱提取物中总生物碱的含量为48.096mg。(2)附子生物碱提取物中苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱的含量分析:样品制备:精密称取自制的生物碱有效组分0.1005g,溶于10mL甲醇,超声30min,离心,取上清液,加甲醇定容至10mL,过0.22μm的有机膜,得供试品溶液备用。高效液相色谱(HPLC)条件:色谱柱为WatersTerraC18柱(3.0mm×100mm,3.5μm),流动相:乙腈:5mM醋酸铵水溶液,梯度见表1,流速0.5ml/min;检测波长235nm,柱温25℃,进样量5μL。表1附子生物碱组分的洗脱条件时间乙腈5mM醋酸铵水溶液015%85%10min26%74%20min30%70%25min30%70%图1为本实施例步骤一中制备的附子生物碱有效组分的高效液相色谱分析谱图(HPLC图谱),经HPLC测定生物碱组分中苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱含量分别为48.15mg·g-1,26.71mg·g-1,8.87mg·g-1,并且没有检测到毒性非常强的单酯型的新乌头碱、乌头碱和次乌头碱。二、对本实施例步骤二中制备的干姜挥发油提取物的分析:样品制备:吸称取本实施例步骤二中制备的干姜挥发油提取液10μL,用乙醚定容至10mL备用,得供试品溶液备用。气相色谱-质谱(GC-MS)分析条件:色谱柱为TR-35MS石英毛细管柱(30m×0.25mm×0.25μm);进样口温度:250℃。程序升温:起始温度60℃,3℃/min升至80℃,保持10min,3℃/min升至140℃,保持15min,6℃/min升至270℃,保持10min;载气:高纯氦气,流速1.0mL/min。质谱电子轰击源(EI);离子源温度:250℃;接口温度:280℃;电子能量:70eV;质量扫描方式:全部扫描范围:10~400amu。进样量1μL。图2是本实施例步骤二中制备的干姜挥发油提取物的气相色谱-质谱分析谱图,从谱图上分析可知,其中相对含量最高的3种成分分别为α-姜烯、α-金合欢烯和β-倍半菲兰烯,分别占挥发油提取物质量的32.24%、14.98%和13.39%。三、对本实施例步骤三中制备的干姜姜辣素类化合物提取物的分析:(1)姜辣素类化合物含量测定:称取本实施例步骤三中制备的干姜姜辣素类化合物提取物粉末0.1029g,用乙醇溶解,定容至1000ml,作为供试品溶液。以香草醛作对照标准,以2.001作为香草醛质量换算姜辣素类化合物质量的换算系数(姜辣素类化合物中6,8,10-姜酚的混合平均分子量为304.46,香草醛分子量为152.15,即304.46/152.15=2.001),在278nm波长处,采用紫外分光光度法测定姜辣素类化合物类的化合物含量为787.54mg·g-1。(2)干姜姜辣素类化合物提取物中6-姜酚的含量测定:样品制备:精密称取自制的干姜姜辣素类化合物提取0.1012g,溶于10mL甲醇,超声30min,离心,取上清液,加甲醇定容至100mL,过0.22μm的有机膜,得供试品溶液备用;HPLC条件:色谱柱为AgilentZORBAXSB-C18柱(4.6mm×150mm,5μm);流动相:甲醇-水(60:40),流速:1.0mL/min;检测波长:282nm,柱温:30℃;进样量:10μL。图3是本实施例步骤三中制备的干姜姜辣素类化合物提取物的高效液相色谱分析谱图(HPLC谱图),由HPLC谱图测定干姜姜辣素类化合物提取物中6-姜酚的含量为152.28mg·g-1。四、对本实施例步骤四中制备的甘草酮提取物进行分析:(1)甘草黄酮的含量测定:称取自制甘草黄酮粉末0.2012g,用甲醇溶解,定容至100mL,作为供试品溶液。精确吸取提取液0.5ml,加3ml蒸馏水,5%亚硝酸钠溶液0.5mL放置6min,加10%硝酸铝溶液0.5mL混匀后放置6min,加5%氢氧化钠2.5mL混匀,放置15min后蒸馏水定容至10mL。以相应溶剂为空白,以芦丁为对照品,在波长510nm处,采用紫外分光光度法测定甘草黄酮含量为550.67mg·g-1。(2)甘草黄酮提取物中甘草苷的含量测定:样品制备:精密称取自制的甘草黄酮提取物0.1024g,溶于10mL甲醇,超声30min,离心,取上清液,加甲醇定容至100mL,过0.22μm的有机膜,得供试品溶液备用。HPLC条件:色谱柱为AgilentZORBAXSB-C18柱(4.6mm×150mm,5μm);流动相:乙腈-0.5%醋酸水(20:80),流速:1.0mL/min;检测波长:276nm,柱温:30℃;进样量:10μL。图4是本实施例步骤四中制备的甘草黄酮提取物的高效液相色谱分析谱图(HPLC谱图),由HPLC测定甘草黄酮提取物中甘草苷的含量为320.33mg·g-1,甘草苷是甘草黄酮中的一种有效成分,说明甘草黄酮提取物中甘草黄酮中的有效成分含量较高。五、对本实施例步骤五中制备的甘草皂苷提取物进行分析:(1)甘草皂苷含量测定:称取本实施例步骤五中制备的甘草皂苷提取物粉末0.5002g,置于100mL圆底烧瓶中,精密加入质量浓度为1%的氨水50mL,回流提取60min,过滤,除去滤液,残渣用1%氨水溶解并转移至25mL量瓶,加水稀释至刻度,作为供试品溶液。精密吸取供试品溶液0.2mL,置于10mL具塞试管中,70℃水浴挥发溶剂,加入5%的香草醛-冰醋酸溶液0.2mL,再加入高氯酸0.8mL,摇匀,于55℃水浴中加热20min,立即取出用流水冷却至室温,加入冰醋酸5ml稀释,摇均。以甘草酸为对照品,在560nm波长处,采用紫外分光光度法测定甘草皂苷物含量为535.33mg·g-1。甘草皂苷提取物中甘草酸的含量测定:样品制备:精密称取自制的甘草皂苷有效组分0.1102g,溶于10mL甲醇,超声30min,离心,取上清液,加甲醇定容至100mL,过0.22μm的有机膜,得供试品溶液备用。HPLC条件:色谱柱为AgilentZORBAXSB-C18柱(4.6mm×150mm,5μm);流动相:乙腈-2%醋酸溶液(37:63),流速:1.0mL/min;检测波长:254nm,柱温:30℃;进样量:10μL。图5是本实施例步骤五中制备的甘草皂苷提取物的高效液相色谱分析谱图,HPLC测定甘草皂苷提取物中甘草酸的含量为318.92mg·g-1,甘草酸为甘草皂苷中的一种成分,对于阿霉素心脏毒性具有很好的疗效,说明甘草皂苷提取物中甘草皂苷中的有效成分含量较高。六、本实施例制备的中药组合物对阿霉素心脏毒性的药效试验1.实验方法SD大鼠48只(中国人民解放军第二军医大学动物中心),重量80~220g。大鼠被随机分为四组:正常对照组(标记为A组)、阿霉素模型组(标记为B组)、阿霉素+传统中药水煎组(标记为C组)、阿霉素+中药组合物组(标记为D组),每组12只。阿霉素模型组、阿霉素+传统中药水煎组、阿霉素+中药组合物组的大鼠,在两周内腹腔注射6次盐酸阿霉素(每kg体重给2.5mg盐酸阿霉素),其累积给药量达到15mg/kg/B.W.。阿霉素+传统中药水煎组和阿霉素+中药组合物组,在第一次注射盐酸阿霉素后的连续14天内,分别灌服给四逆汤水提物和中药组合物,阿霉素+传统中药水煎组给药剂量为5g/kg四逆汤水提物,阿霉素+中药组合物组给药剂量为50mg/kg中药组合物。对于健康对照组和阿霉素模型组,每次灌服等量蒸馏水。在第15天,眼眶取血进行生物化学指标的测定,采血后进行血流动力学评估,血流动力学评估之后,处死大鼠,立即取心脏,每组中4只大鼠心脏分离左心室,立即置于4%多聚甲醛中固定用于HE染色的分析。每组其余8只大鼠心脏,立即置于液氮中,冻存用于药效的代谢组学评价。阿霉素+中药组合物组中的重要有效组分组合物是由本发明实施例1制备得到的中药组合物,阿霉素+传统中药水煎组中传统中药水煎组的药物是由附子、干姜和甘草加水煎煮制得。2.观测指标(1)血清肌酸激酶(CK),肌酸激酶-MB同工酶(CK-MB)和乳酸脱氢酶(LDH)的含量测定将采集实验各组大鼠的血样,置于干燥试管内,经高速离心分离血清,-20℃冰箱保存。用本酶联免疫法测定血清肌酸激酶(CK),肌酸激酶-MB同工酶(CK-MB)和乳酸脱氢酶(LDH)的浓度。结果见表2。表2各组大鼠血清肌酸激酶(CK),肌酸激酶-MB同工酶(CK-MB)和乳酸脱氢酶(LDH)含量的比较分组CK(U/L)CK-MB(U/L)LDH(U/L)A组984.8±187.51012.6±484.1722.7±190.4B组2487.1±390.3**3179.8±780.3**1723.2±490.7**C组1538.3±392.5#2493.4±414.9#1308.9±318.2#D组1128.4±422.7#1767.5±523.7#1045.6±434.5#注:与正常对照组比较**p<0.01,与阿霉素模型组比较#p<0.05如表2所示,与正常对照组比,阿霉素模型组的血清肌酸激酶(CK),肌酸激酶-MB同工酶(CK-MB)和乳酸脱氢酶(LDH)显著升高(P<0.01),提示阿霉素引起心肌损坏。C组、D组可显著降低阿霉素引起的大鼠血清中血清肌酸激酶(CK),肌酸激酶-MB同工酶(CK-MB)和乳酸脱氢酶(LDH)(P<0.05),表明传统中药水煎液和中药组合物可以减轻阿霉素引起的心肌坏死,并且实验数据表明中药组合物对这些指标的降低效果明显优于传统中药水煎液。(2)血流动力学评估两周后,当完成最后一次给药,各组的动物都用戊巴比妥钠(50mg/kg/B.W.,i.p.)麻醉,右侧颈总动脉插入一根微量血压探头连接一台血压检测仪(SPR407,MillarInstrumentsInc.,美国)记录动脉压。然后,探头通过右侧颈总动脉插入左心室中,记录左心室收缩压(LVSP),左心室舒张压末期(LVEDP),最大升压速率(+dP/dtmax)和最大减压速率(-dP/dtmax)表3各组大鼠的血流动力学参数测定值注:与正常对照组比较**p<0.01,与阿霉素模型组比较#p<0.05如表2所示,与正常对照组比,阿霉素模型组的左心室收缩压(LVSP)、压力增加的最大速率(+dp/dt的最大值)和最大减压速率(-dp/dt的最大值)显著下降(P<0.01),左心室舒张压末期(LVEDP)显著升高(P<0.01),提示阿霉素引起严重的心脏毒性作用。C组、D组可显著升高阿霉素引起的大鼠左心室收缩压(LVSP)、压力增加的最大速率(+dp/dt的最大值)和最大减压速率(-dp/dt的最大值)(P<0.05),降低左心室舒张压末期(LVEDP)(P<0.05),表明传统中药水煎液和中药组合物可以减轻阿霉素引起的心脏毒性,并且实验数据表明中药组合物组对这些指标的回调作用优于传统中药水煎组。(3)HE染色心肌病理形态学评价完成血流动力学评估,将大鼠开胸留取心脏标本,每组中的4只大鼠心脏,分离左心室,于4℃的4%多聚甲醛中固定。24h后取心肌标本,常规取材、脱水、石蜡包埋,沿左室长轴线每隔1mm横断面切取数张5μm厚的组织切片,常规HE染色。400倍光镜下观察组织形态学变化结果见图6、图7、图8和图9。左心室HE染色的病理切片显示,与正常对照组(A组)相比,阿霉素造模后,心肌束的排列紊乱,心肌细胞受损明显,包括出血和坏死。给予四逆汤水煎液、中药组合物组治疗后,心肌细胞的损伤明显得到改善。(4)心肌组织代谢组学评价中药组合物对阿霉素心脏毒性作用完成血流动力学评估,将大鼠开胸留取心脏标本,每组中的8只大鼠心脏,立即置于液氮中冻存,采用代谢组学方法对其药效进行进一步的评价。①心肌组织样品处理:50mg的心脏组织加入200μL生理盐水匀浆,然后4℃下13000rpm离心15min,100μL上清加入5μL1mg/mL核糖醇作内标,加入4倍体积(400μL)的冰提取液(甲醇:乙腈:丙酮=1:1:1),涡旋30s,4℃超声抽提10min,4℃13000rpm离心15min,取上清300μL转移到玻璃管,氮气吹干,衍生化前50℃烘干15min。衍生化:75μL15μg/μL的甲氧胺吡啶溶液,涡旋5min,70℃烘箱放置1h;75μLMSTFA(内含质量百分含量为1%的三甲基氯硅烷),涡旋5min,室温1h;加入200μL正庚烷涡旋30s,4000rpm离心10min,取上清200μL至样品瓶,进样1.0μL。②心肌组织样品的气相色谱-质谱(GC-MS)分析:采用Thermo-FinniganTraceDSQ气质联用仪(ThermoElectronCorporation)。进样量1.0μL,TR-5MS毛细管柱(30m×250μm×0.25μm)、载气为氦气,柱流速为1mL/min,进样口温度为260℃;接口温度为260℃;离子源温度为200℃;四级杆温度150℃,EI离子源70eV;采用全扫描模式,m/z:60-600;程序升温条件:70℃保持4min,以4℃/min升至220℃,然后8℃/min升至310℃后保持10min。图10展示了某一心肌组织样本1次进样分析后得到的心肌组织代谢物气相色谱质谱的指纹图谱,横向坐标表示出峰时间,纵向坐标表示峰的强度。③阿霉素心脏毒性生物标志物的筛选与鉴定:原始数据经ThermoXconvert软件转换为通用的NetCDF格式,转换后的数据进一步通过XCMS数据处理软件,对各组大鼠心肌组织样本代谢指纹图谱数据进行去噪音、质谱峰提取、反卷积处理、峰排列、对齐、合并、峰合并后开始列表去噪音、缝隙填补处理,得到各个峰的峰面积以及质量数和保留时间等数据。根据A组和B组谱图的差异性比较,应用SIMCA-P统计软件(Version11.0)进行主成分分析(PCA)和偏最小二乘判别分析(PLS-DA),并选择变量重要性因子对分类贡献最大的检测离子,这些检测离子对应的代谢物可被认为是阿霉素心脏毒性的生物标志物。图11为正常对照组和阿霉素模型组经过主成分分析(PCA)的得分图,图中每个点代表一个样本,表明了阿霉素模型组和正常对照组之间差异明显。进一步使用SMICA-P统计软件(Version11.0)中偏最小二乘法-判别分析(PLS-DA)将阿霉素模型组和正常对照组分成两组进行分析,得到S-Plot图(图12),S-Plot图能够鲜明的突显出两组间差异最大的化合物,即右上角和左上角的点(灰框内的变量点)是置信度和贡献度双高的化合物,这些检测离子贡献度最大,可被认为阿霉素引起心脏毒性的生物标志物,可用于评价四逆汤的药效;对筛选出的标志物,使用NISTdatabase匹配进行化合物结构的鉴定,再结合标准品比对进行进一步鉴别的确证,最终对筛选出的标志物进行结构鉴定。表4给出了鉴定的10种标示物。表4阿霉素模型组和正常对照组的关系研究中涉及的重要化合物及其在不同组中变化情况注:与正常对照组比较**p<0.01,与阿霉素模型组比较#p<0.05阿霉素造模后,心肌组织中丙氨酸、甘氨酸、苹果酸、脯氨酸、谷氨酰胺、苯丙氨酸、硬脂酸和胆固醇的水平明显高于正常对照组(P<0.01),而缬氨酸、异亮氨酸的水平明显低于正常对照组。④基于阿霉素心脏毒性生物标志物的药效学评价:由于10种阿霉素心肌病的生物标志物已经通过上述代谢组学技术研究得到,可见,利用这些标志物作为监测指标进一步研究中药组合物的治疗作用是合理的。我们对标志物在不同组的相对峰面积进行了方差分析。结果如表4所示,与阿霉素模型组相比,除硬脂酸和胆固醇两种代谢物以外,四逆汤水煎液和中药组合物组对10种标志物中的8种具有明显的回调作用(P<0.05),并且中药组合物组回调作用更显著。实施例2本实施例中抑制阿霉素心脏毒性的中药组合物由以下质量百分数的有效成分制成:附子生物碱提取物32%、干姜挥发油提取物1%、干姜姜辣素类化合物提取物28%、甘草黄酮提取物20%和甘草皂苷提取物19%;该制备方法包括以下步骤:步骤一、附子生物碱提取物的制备:步骤101、取1000g附子炮制品,粉碎后加入体积百分含量为50%的乙醇溶液,在温度为100℃的水浴中回流提取,每次提取3h,合并前后2次的提取液,得到混合液;2次提取过程中所述乙醇溶液的用量为所述附子炮制品质量的8倍;步骤102、向步骤101中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克附子炮制品;步骤103、离心除去步骤102中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱上端,静置吸附1h后,采用去离子水洗脱,弃去洗脱液,再采用5倍柱体积的70%乙醇洗脱,收集洗脱液,浓缩后,采用真空干燥后得到附子生物碱提取物;所述附子生物碱提取物中附子生物碱的质量百分含量为30%~50%;所述乙醇溶液中乙醇的体积百分含量为70%;所述附子生物碱提取物中附子生物碱的质量百分含量为30.4%;步骤二、干姜挥发油提取物的制备:采用CO2超临界萃取制备干姜挥发油,取干姜粗粉,以体积百分含量为95%的乙醇溶液为夹带剂,在温度为40℃,压力为30MPa的条件下萃取1h,得棕黄色乙醇溶液,减压回收乙醇后,经无水硫酸钠干燥,得具有特殊浓郁香味的棕黄色干姜挥发油;所述夹带剂的质量为干姜粗粉质量的1.5倍;所述干姜挥发油提取物中干姜挥发油的质量百分含量为97%;步骤三、干姜姜辣素类化合物提取物制备:采用乙醇渗漉法制备干姜姜辣素类化合物提取物,取干姜粗粉,装入渗滚筒中,装完后先向筒内加入4倍干姜粗粉质量的乙醇冷浸2h后,再加入8倍干姜粗粉质量的体积百分含量为85%的乙醇溶液,然后以5mL/(kg·min)的速度渗漉,收集渗漉液,减压液浓缩至干,即得干姜姜辣素类化合物提取物;所述干姜姜辣素类化合物提取物中姜辣素类化合物的质量百分含量为75.3%;步骤四、甘草黄酮提取物制备:步骤401、取甘草粉碎后加入乙醇中,在温度为100℃的水浴中回流提取2次,每次提取2h,得提取液,然后合并前后2次的提取液,得到混合液,每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的6倍;步骤402、将步骤401中所述混合液离心后,减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤403、将步骤402中所述浓缩液加至过D101大孔树脂柱上端,先用6倍体积纯水洗脱除杂,再用5倍体积的乙醇洗脱,收集洗脱液,将洗脱液减压浓缩,再加至HZ915聚酰胺树脂柱,用5倍体积的乙醇洗脱,收集洗脱液,减压浓缩后干燥,得到甘草黄酮提取物;所述甘草黄酮提取物中甘草黄酮的质量百分含量为42.5%;步骤五、甘草皂苷提取物制备:步骤501、称取甘草,然后粉碎后加入体积百分含量为70%的乙醇溶液,在温度为100℃的水浴中回流提取2次,每次2h,合并前后2次的提取液,得到混合液;每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的8倍;步骤502、向步骤501中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤503、离心除去步骤502中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱的上端,用6倍体积的百分数为30%的乙醇溶液除杂,再用5倍体积的体积百分含量为50%的乙醇洗脱,收集洗脱液,减压浓缩后,得到甘草皂苷提取物;所述甘草皂苷提取物中甘草皂苷的质量百分含量为47.36%;步骤六、将步骤一中制备得到的附子生物碱提取物、步骤二中制备得到的干姜挥发油提取物、步骤三中制备得到的干姜姜辣素类化合物提取物、步骤四中制备的甘草黄酮提取物和步骤五中制备的甘草皂苷提取物混合,得到用于抑制阿霉素心脏毒性的中药组合物。经测试,本实施例制备的中药组合物能有效地抑制阿霉素心脏毒性,并且心肌组织代谢正常。实施例3本实施例中抑制阿霉素心脏毒性的中药组合物由以下质量百分数的有效成分制成:附子生物碱提取物42%、干姜挥发油提取物3%、干姜姜辣素类化合物提取物24%、甘草黄酮提取物15%和甘草皂苷提取物16%;该制备方法包括以下步骤:步骤一、附子生物碱提取物的制备:步骤101、取1000g附子炮制品,粉碎后加入体积百分含量为50%的乙醇溶液,在温度为100℃的水浴中回流提取,每次提取3h,合并前后2次的提取液,得到混合液;2次提取过程中所述乙醇溶液的用量为所述附子炮制品质量的8倍;步骤102、向步骤101中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克附子炮制品;步骤103、离心除去步骤102中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱上端,静置吸附1h后,采用去离子水洗脱,弃去洗脱液,再采用5倍柱体积的70%乙醇洗脱,收集洗脱液,浓缩后,采用真空干燥后得到附子生物碱提取物;所述附子生物碱提取物中附子生物碱的质量百分含量为30%~50%;所述乙醇溶液中乙醇的体积百分含量为70%;所述附子生物碱提取物中附子生物碱的质量百分含量为38.7%;步骤二、干姜挥发油提取物的制备:采用CO2超临界萃取制备干姜挥发油,取干姜粗粉,以体积百分含量为95%的乙醇溶液为夹带剂,在温度为40℃,压力为30MPa的条件下萃取1h,得棕黄色乙醇溶液,减压回收乙醇后,经无水硫酸钠干燥,得具有特殊浓郁香味的棕黄色干姜挥发油;所述夹带剂的质量为干姜粗粉质量的1.5倍;所述干姜挥发油提取物中干姜挥发油的质量百分含量为95%;步骤三、干姜姜辣素类化合物提取物制备:采用乙醇渗漉法制备干姜姜辣素类化合物提取物,取干姜粗粉,装入渗滚筒中,装完后先向筒内加入4倍干姜粗粉质量的乙醇冷浸2h后,再加入8倍干姜粗粉质量的体积百分含量为85%的乙醇溶液,然后以5mL/(kg·min)的速度渗漉,收集渗漉液,减压液浓缩至干,即得干姜姜辣素类化合物提取物;所述干姜姜辣素类化合物提取物中姜辣素类化合物的质量百分含量为72.3%;步骤四、甘草黄酮提取物制备:步骤401、称取甘草,粉碎后加入乙醇中,在温度为100℃的水浴中回流提取2次,每次提取2h,得提取液,然后合并前后2次的提取液,得到混合液,每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的6倍;步骤402、将步骤401中所述混合液离心后,减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤403、将步骤402中所述浓缩液加至过D101大孔树脂柱上端,先用6倍体积纯水洗脱除杂,再用5倍体积的乙醇洗脱,收集洗脱液,将洗脱液减压浓缩,再加至HZ915聚酰胺树脂柱,用5倍体积的乙醇洗脱,收集洗脱液,减压浓缩后干燥,得到甘草黄酮提取物;所述甘草黄酮提取物中甘草黄酮的质量百分含量为59.6%;步骤五、甘草皂苷提取物制备:步骤501、称取甘草,然后粉碎后加入体积百分含量为70%的乙醇溶液,在温度为100℃的水浴中回流提取2次,每次2h,合并前后2次的提取液,得到混合液;每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的8倍;步骤502、向步骤501中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤503、离心除去步骤502中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱的上端,用6倍体积的百分数为30%的乙醇溶液除杂,再用5倍体积的体积百分含量为50%的乙醇洗脱,收集洗脱液,减压浓缩后,得到甘草皂苷提取物;所述甘草皂苷提取物中甘草皂苷的质量百分含量为59.8%;步骤六、将步骤一中制备得到的附子生物碱提取物、步骤二中制备得到的干姜挥发油提取物、步骤三中制备得到的干姜姜辣素类化合物提取物、步骤四中制备的甘草黄酮提取物和步骤五中制备的甘草皂苷提取物混合,得到用于抑制阿霉素心脏毒性的中药组合物。经测试,本实施例制备的中药组合物能有效地抑制阿霉素心脏毒性,并且心肌组织代谢正常。实施例4本实施例中抑制阿霉素心脏毒性的中药组合物由以下质量百分数的有效成分制成:附子生物碱提取物40%、干姜挥发油提取物2%、干姜姜辣素类化合物提取物26%、甘草黄酮提取物17%和甘草皂苷提取物15%;该制备方法包括以下步骤:步骤一、附子生物碱提取物的制备:步骤101、取1000g附子炮制品,粉碎后加入体积百分含量为50%的乙醇溶液,在温度为100℃的水浴中回流提取,每次提取3h,合并前后2次的提取液,得到混合液;2次提取过程中所述乙醇溶液的用量为所述附子炮制品质量的8倍;步骤102、向步骤101中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克附子炮制品;步骤103、离心除去步骤102中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱上端,静置吸附1h后,采用去离子水洗脱,弃去洗脱液,再采用5倍柱体积的70%乙醇洗脱,收集洗脱液,浓缩后,采用真空干燥后得到附子生物碱提取物;所述附子生物碱提取物中附子生物碱的质量百分含量为30%~50%;所述乙醇溶液中乙醇的体积百分含量为70%;所述附子生物碱提取物中附子生物碱的质量百分含量为41.7%;步骤二、干姜挥发油提取物的制备:采用CO2超临界萃取制备干姜挥发油,取干姜粗粉,以体积百分含量为95%的乙醇溶液为夹带剂,在温度为40℃,压力为30MPa的条件下萃取1h,得棕黄色乙醇溶液,减压回收乙醇后,经无水硫酸钠干燥,得具有特殊浓郁香味的棕黄色干姜挥发油;所述夹带剂的质量为干姜粗粉质量的1.5倍;所述干姜挥发油提取物中干姜挥发油的质量百分含量为95%;步骤三、干姜姜辣素类化合物提取物制备:采用乙醇渗漉法制备干姜姜辣素类化合物提取物,取干姜粗粉,装入渗滚筒中,装完后先向筒内加入4倍干姜粗粉质量的乙醇冷浸2h后,再加入8倍干姜粗粉质量的体积百分含量为85%的乙醇溶液,然后以5mL/(kg·min)的速度渗漉,收集渗漉液,减压液浓缩至干,即得干姜姜辣素类化合物提取物;所述干姜姜辣素类化合物提取物中姜辣素类化合物的质量百分含量为60.23%;步骤四、甘草黄酮提取物制备:步骤401、称取甘草,粉碎后加入乙醇中,在温度为100℃的水浴中回流提取2次,每次提取2h,得提取液,然后合并前后2次的提取液,得到混合液,每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的6倍;步骤402、将步骤401中所述混合液离心后,减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤403、将步骤402中所述浓缩液加至过D101大孔树脂柱上端,先用6倍体积纯水洗脱除杂,再用5倍体积的乙醇洗脱,收集洗脱液,将洗脱液减压浓缩,再加至HZ915聚酰胺树脂柱,用5倍体积的乙醇洗脱,收集洗脱液,减压浓缩后干燥,得到甘草黄酮提取物;所述甘草黄酮提取物中甘草黄酮的质量百分含量为50.13%;步骤五、甘草皂苷提取物制备:步骤501、称取甘草,然后粉碎后加入体积百分含量为70%的乙醇溶液,在温度为100℃的水浴中回流提取2次,每次2h,合并前后2次的提取液,得到混合液;每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的8倍;步骤502、向步骤501中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤503、离心除去步骤502中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱的上端,用6倍体积的百分数为30%的乙醇溶液除杂,再用5倍体积的体积百分含量为50%的乙醇洗脱,收集洗脱液,减压浓缩后,得到甘草皂苷提取物;所述甘草皂苷提取物中甘草皂苷的质量百分含量为55.13%;步骤六、将步骤一中制备得到的附子生物碱提取物、步骤二中制备得到的干姜挥发油提取物、步骤三中制备得到的干姜姜辣素类化合物提取物、步骤四中制备的甘草黄酮提取物和步骤五中制备的甘草皂苷提取物混合,得到用于抑制阿霉素心脏毒性的中药组合物。经测试,本实施例制备的中药组合物能有效地抑制阿霉素心脏毒性,并且心肌组织代谢正常。实施例5本实施例中抑制阿霉素心脏毒性的中药组合物由以下质量百分数的有效成分制成:附子生物碱提取物37%、干姜挥发油提取物1%、干姜姜辣素类化合物提取物25%、甘草黄酮提取物22%和甘草皂苷提取物15%;该制备方法包括以下步骤:步骤一、附子生物碱提取物的制备:步骤101、取1000g附子炮制品,粉碎后加入体积百分含量为50%的乙醇溶液,在温度为100℃的水浴中回流提取,每次提取3h,合并前后2次的提取液,得到混合液;2次提取过程中所述乙醇溶液的用量为所述附子炮制品质量的8倍;步骤102、向步骤101中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克附子炮制品;步骤103、离心除去步骤102中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱上端,静置吸附1h后,采用去离子水洗脱,弃去洗脱液,再采用5倍柱体积的70%乙醇洗脱,收集洗脱液,浓缩后,采用真空干燥后得到附子生物碱提取物;所述附子生物碱提取物中附子生物碱的质量百分含量为30%~50%;所述乙醇溶液中乙醇的体积百分含量为70%;所述附子生物碱提取物中附子生物碱的质量百分含量为49.8%;步骤二、干姜挥发油提取物的制备:采用CO2超临界萃取制备干姜挥发油,取干姜粗粉,以体积百分含量为95%的乙醇溶液为夹带剂,在温度为40℃,压力为30MPa的条件下萃取1h,得棕黄色乙醇溶液,减压回收乙醇后,经无水硫酸钠干燥,得具有特殊浓郁香味的棕黄色干姜挥发油;所述夹带剂的质量为干姜粗粉质量的1.5倍;所述干姜挥发油提取物中干姜挥发油的质量百分含量为99%;步骤三、干姜姜辣素类化合物提取物制备:采用乙醇渗漉法制备干姜姜辣素类化合物提取物,取干姜粗粉,装入渗滚筒中,装完后先向筒内加入4倍干姜粗粉质量的乙醇冷浸2h后,再加入8倍干姜粗粉质量的体积百分含量为85%的乙醇溶液,然后以5mL/(kg·min)的速度渗漉,收集渗漉液,减压液浓缩至干,即得干姜姜辣素类化合物提取物;所述干姜姜辣素类化合物提取物中姜辣素类化合物的质量百分含量为62.3%;步骤四、甘草黄酮提取物制备:步骤401、称取甘草,粉碎后加入乙醇中,在温度为100℃的水浴中回流提取2次,每次提取2h,得提取液,然后合并前后2次的提取液,得到混合液,每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的6倍;步骤402、将步骤401中所述混合液离心后,减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤403、将步骤402中所述浓缩液加至过D101大孔树脂柱上端,先用6倍体积纯水洗脱除杂,再用5倍体积的乙醇洗脱,收集洗脱液,将洗脱液减压浓缩,再加至HZ915聚酰胺树脂柱,用5倍体积的乙醇洗脱,收集洗脱液,减压浓缩后干燥,得到甘草黄酮提取物;所述甘草黄酮提取物中甘草黄酮的质量百分含量为30.2%;步骤五、甘草皂苷提取物制备:步骤501、称取甘草,然后粉碎后加入体积百分含量为70%的乙醇溶液,在温度为100℃的水浴中回流提取2次,每次2h,合并前后2次的提取液,得到混合液;每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的8倍;步骤502、向步骤501中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤503、离心除去步骤502中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱的上端,用6倍体积的百分数为30%的乙醇溶液除杂,再用5倍体积的体积百分含量为50%的乙醇洗脱,收集洗脱液,减压浓缩后,得到甘草皂苷提取物;所述甘草皂苷提取物中甘草皂苷的质量百分含量为59.8%;步骤六、将步骤一中制备得到的附子生物碱提取物、步骤二中制备得到的干姜挥发油提取物、步骤三中制备得到的干姜姜辣素类化合物提取物、步骤四中制备的甘草黄酮提取物和步骤五中制备的甘草皂苷提取物混合,得到用于抑制阿霉素心脏毒性的中药组合物。经测试,本实施例制备的中药组合物能有效地抑制阿霉素心脏毒性,并且心肌组织代谢正常。实施例6本实施例中抑制阿霉素心脏毒性的中药组合物由以下质量百分数的有效成分制成:附子生物碱提取物35%、干姜挥发油提取物2%、干姜姜辣素类化合物提取物25%、甘草黄酮提取物16%和甘草皂苷提取物22%;该制备方法包括以下步骤:步骤一、附子生物碱提取物的制备:步骤101、取1000g附子炮制品,粉碎后加入体积百分含量为50%的乙醇溶液,在温度为100℃的水浴中回流提取,每次提取3h,合并前后2次的提取液,得到混合液;2次提取过程中所述乙醇溶液的用量为所述附子炮制品质量的8倍;步骤102、向步骤101中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克附子炮制品;步骤103、离心除去步骤102中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱上端,静置吸附1h后,采用去离子水洗脱,弃去洗脱液,再采用5倍柱体积的70%乙醇洗脱,收集洗脱液,浓缩后,采用真空干燥后得到附子生物碱提取物;所述附子生物碱提取物中附子生物碱的质量百分含量为30%~50%;所述乙醇溶液中乙醇的体积百分含量为70%;所述附子生物碱提取物中附子生物碱的质量百分含量为45.6%;步骤二、干姜挥发油提取物的制备:采用CO2超临界萃取制备干姜挥发油,取干姜粗粉,以体积百分含量为95%的乙醇溶液为夹带剂,在温度为40℃,压力为30MPa的条件下萃取1h,得棕黄色乙醇溶液,减压回收乙醇后,经无水硫酸钠干燥,得具有特殊浓郁香味的棕黄色干姜挥发油;所述夹带剂的质量为干姜粗粉质量的1.8倍;所述干姜挥发油提取物中干姜挥发油的质量百分含量为90%;步骤三、干姜姜辣素类化合物提取物制备:采用乙醇渗漉法制备干姜姜辣素类化合物提取物,取干姜粗粉,装入渗滚筒中,装完后先向筒内加入4倍干姜粗粉质量的乙醇冷浸2h后,再加入8倍干姜粗粉质量的体积百分含量为85%的乙醇溶液,然后以5mL/(kg·min)的速度渗漉,收集渗漉液,减压液浓缩至干,即得干姜姜辣素类化合物提取物;所述干姜姜辣素类化合物提取物中姜辣素类化合物的质量百分含量为78.9%;步骤四、甘草黄酮提取物制备:步骤401、称取甘草,粉碎后加入乙醇中,在温度为100℃的水浴中回流提取2次,每次提取2h,得提取液,然后合并前后2次的提取液,得到混合液,每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的6倍;步骤402、将步骤401中所述混合液离心后,减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤403、将步骤402中所述浓缩液加至过D101大孔树脂柱上端,先用6倍体积纯水洗脱除杂,再用5倍体积的乙醇洗脱,收集洗脱液,将洗脱液减压浓缩,再加至HZ915聚酰胺树脂柱,用5倍体积的乙醇洗脱,收集洗脱液,减压浓缩后干燥,得到甘草黄酮提取物;所述甘草黄酮提取物中甘草黄酮的质量百分含量为55.67%;步骤五、甘草皂苷提取物制备:步骤501、称取甘草,然后粉碎后加入体积百分含量为70%的乙醇溶液,在温度为100℃的水浴中回流提取2次,每次2h,合并前后2次的提取液,得到混合液;每次提取过程中所述乙醇溶液的体积为粉碎后甘草体积的8倍;步骤502、向步骤501中所述混合液中加入乙醇,使混合液中乙醇的体积百分含量达到90%,然后静置至固液分离,将下层的固体杂质除去,并将上层液体减压浓缩,得到浓缩液,其中每毫升浓缩液中含有1克甘草;步骤503、离心除去步骤502中所述浓缩液中含有的不溶物质后,再加至D-101大孔树脂柱的上端,用6倍体积的百分数为30%的乙醇溶液除杂,再用5倍体积的体积百分含量为50%的乙醇洗脱,收集洗脱液,减压浓缩后,得到甘草皂苷提取物;所述甘草皂苷提取物中甘草皂苷的质量百分含量为40.5%;步骤六、将步骤一中制备得到的附子生物碱提取物、步骤二中制备得到的干姜挥发油提取物、步骤三中制备得到的干姜姜辣素类化合物提取物、步骤四中制备的甘草黄酮提取物和步骤五中制备的甘草皂苷提取物混合,得到用于抑制阿霉素心脏毒性的中药组合物。经测试,本实施例制备的中药组合物能有效地抑制阿霉素心脏毒性,并且心肌组织代谢正常。以上所述,仅是本发明的较佳实施例,并非对本发明作任何限制。凡是根据发明技术实质对以上实施例所作的任何简单修改、变更以及等效变化,均仍属于本发明技术方案的保护范围内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1