移植用介质的制作方法
本发明涉及视网膜色素上皮(rpe)细胞的悬浮化剂、悬浮于该悬浮化剂中的含有rpe细胞的组合物、包括将rpe细胞悬浮于该悬浮化剂中的操作的含有rpe细胞的组合物的制造方法等。
背景技术:
视网膜色素上皮(rpe)细胞在视网膜的最外层作为伴随着色素的一层上皮细胞组织存在,对于维持掌管视觉的眼球视网膜的功能担负极为重要的作用。作为其代表性的功能,可以举出由吞噬功能造成的视网膜视细胞外节的新生、由特异性地存在于视细胞外节的作为感光蛋白的视物质的循环及各种细胞因子的分泌造成的作为rpe相邻组织的视细胞及血管膜的保护效果等。因而已知,rpe细胞因老化或其基因异常等而导致功能不全或与之相伴的变性甚至细胞死亡,由此引起老年性黄斑变性症(amd)及stargardt病等黄斑变性症或视网膜色素变性症(rp)等严重的视网膜变性。特别是,amd是引起老年人的中心视力的降低、失明的眼病,在包括将要迎来空前的老龄化社会的日本在内的发达国家中成为重要的社会问题。现在,针对amd的治疗方法一般是属于对症疗法的抗体药的眼内施用,还没有确立有效的治疗方法,因此希望开发出取代它的根治疗法。此外,对于stargardt病及rp迄今为止还没有确立任何有效的治疗方法。
近年来,作为针对amd、rp的新的治疗方法,补充或置换从多能干细胞分化诱导出的rpe细胞的细胞移植治疗引人关注,因此rpe细胞作为细胞治疗用移植材料的有效利用受到期待。例如,ocatatherapeutics公司(原advancedcelltechnology(act)公司)正在推进使用了人胚胎性干细胞(es细胞)来源的rpe细胞的有关老年性黄斑变性症(amd)及stargardt病的临床研究(非专利文献1)。日本国也报告过,在2014年实施了将人工多能干细胞(ips细胞)来源的rpe细胞膜片移植给渗出型amd患者的手术,作为世界首例的ips细胞移植治疗受到很大关注,现在治疗过程也很顺利。
现在,在rpe细胞的移植中,有(1)将所制备的rpe细胞膜片或向支架材料中接种rpe细胞而制备的带有支架的rpe细胞膜片从形成于视网膜中的切口移植到视网膜色素上皮的变性或缺损部位的方法;和(2)将rpe细胞悬浮液注入相同的部位的方法。由于移植用细胞的培养需要以gmp水平实施,因此在前者的情况下,要在rpe细胞膜片的制造后从细胞制备中心(cpc;cellprocessingcenter)运送到进行移植手术的设施(医院)。另一方面,在后者的情况下,例如在ocatatherapeutics公司的临床试验中,将cpc中制造并冷冻保存了的rpe细胞运送到医院,在医院中解冻,并在悬浮于移植用介质中后立即带入手术室而实施移植。从可以将细胞以冷冻状态从cpc运送到医院这一点考虑,认为后者的便利性更高。
然而,无法否定因实施冷冻-解冻处理而引起对移植细胞的损伤的可能性。以往,移植到局部的终末分化细胞、组织一般是通过生物体间移植、不包括冷冻工序的制造来提供。在不得已移植经过冷冻保存的细胞的情况下,担心因冷冻-解冻工序而造成细胞、组织的结构的损伤和功能降低。在实现局部的细胞移植治疗的方面,移植冷冻保存细胞的功能降低是大的课题,然而对于因移植刚刚解冻后的rpe细胞而造成的对治疗效果的影响,迄今为止没有进行过研究。
已知泊洛沙姆188(聚氧乙烯(160)聚氧丙烯(30)二醇)通过修复物理、化学地损伤了的细胞膜而显示出细胞保护效果,迄今为止,已经提出过若干有关肌营养不良症、心力衰竭、神经变性疾病、电损伤等疾病的治疗、移植等医疗应用中的作为细胞膜密封剂的泊洛沙姆188的使用的专利及专利申请(非专利文献2)。例如,austen等人公开过将脂肪抽吸时损伤了的脂肪组织的细胞膜用泊洛沙姆188密封的方法(专利文献1)。他们还公开过通过将冷冻保存细胞在泊洛沙姆188的存在下解冻来提高冷冻保存细胞的生存率的方法(专利文献2)。
然而,对于rpe细胞的移植、冷冻保存了的rpe细胞解冻时的泊洛沙姆188的使用,迄今为止还没有进行过报告。
现有技术文献
专利文献
专利文献1:日本专利第5795961号公报
专利文献2:日本特表2012-533620号公报
非专利文献
非专利文献1:schwartzetal.,lancet,379:713-720(2012)
非专利文献2:moloughneyetal.,recentpat.biotechnol.,6(3):200-211(2012)
技术实现要素:
发明所要解决的问题
本发明的目的在于,提供适合用于黄斑变性症、视网膜色素变性症(rp:retinitispigmentosa)等视网膜变性疾病的治疗的rpe细胞的使用的rpe细胞的悬浮化剂及悬浮于该悬浮化剂中的含有rpe细胞的组合物,另外,提供包括将rpe细胞悬浮于该悬浮化剂中的工序的适合移植的含有rpe细胞的组合物的制造方法等。
用于解决问题的方法
本发明人等在为了达成上述目的而反复进行深入研究的过程中发现,如果向解冻后添加的移植用介质(悬浮化剂)中添加泊洛沙姆188,则冷冻保存rpe细胞解冻后的生存率及回收率提高。
在使用了es细胞来源的rpe细胞的针对黄斑变性症的治疗试验中,将冷冻保存了的rpe细胞解冻后立即移植(上述非专利文献1),然而本发明人等根据上述的结果想到,在解冻后立即移植rpe细胞的情况下,是否会因细胞的生存率的降低、状态的恶化而损害移植效果(例如视细胞保护效果),使用作为视网膜变性模型的rcs(royalcollegeofsurgeons)大鼠,在将rpe细胞解冻后立即移植的情况下、解冻后培养一定期间后移植的情况下,比较了视细胞保护效果,结果显而易见,后者显示出更高的视细胞保护效果。
因而,本发明人等为了防止刚刚解冻后的rpe细胞的视细胞保护效果的降低而进行了深入研究,其结果是,在向移植用介质中添加了泊洛沙姆188的情况下,rpe细胞即使在刚刚解冻后,也显示出与培养一定期间后相比同等或在其以上的高的视细胞保护效果。该结果显示,通过使用泊洛沙姆,即使在将冷冻保存了的rpe细胞解冻后不在cpc内暂时培养,而以冷冻保存的状态将rpe细胞运送到医院内,在解冻后立即实施移植,也可以获得高的移植效果。
此外,本发明人等对于泊洛沙姆188向移植用介质中的添加是否不仅有助于解冻后的rpe细胞的生存率、移植效果,而且还有助于从解冻到移植的各种工序期间的rpe细胞的损失的减少(细胞回收率的提高)进行了试验。其结果是,显而易见,通过从刚刚解冻后的稀释、清洗工序的工序起,使用含有泊洛沙姆188的介质作为悬浮化剂,对于解冻后的细胞的损失、由离心分离工序造成的细胞的损失、通过移植用设备时的细胞的损失均可以减少。
本发明人等基于这些见解发现,含有泊洛沙姆188的悬浮化剂的作为移植用介质的使用在rpe细胞的移植治疗中,对于移植方案的简化、迅速化、以及移植效果的改善及均一化、乃至成本削减而言有用,从而完成了本发明。
即,本发明提供如下所示的内容。
[1]一种视网膜色素上皮(rpe)细胞的悬浮化剂,其为含有泊洛沙姆、和医药上容许用作眼内灌注液或清洗液的介质而成。
[2]根据[1]记载的悬浮化剂,其中,所述介质为经过调整的汉克斯平衡盐溶液或氧化型谷胱甘肽眼内灌注液或清洗液。
[3]根据[1]或[2]记载的悬浮化剂,其中,泊洛沙姆的浓度为0.001%(w/v)~0.1%(w/v)。
[4]根据[1]或[2]记载的悬浮化剂,其中,泊洛沙姆的浓度为0.01%(w/v)~0.1%(w/v)。
[5]根据[1]~[4]中任一项记载的悬浮化剂,其用于将冷冻保存了的rpe细胞不进行培养地移植。
[6]根据[1]~[5]中任一项记载的悬浮化剂,其用于在解冻后8小时以内移植。
[7]根据[1]~[6]中任一项记载的悬浮化剂,其为rpe细胞的保护剂。
[8]根据[1]~[7]中任一项记载的悬浮化剂,其在解冻后直至移植前的任意的工序中使用,抑制该工序前后的rpe细胞数的减少。
[9]一种移植用医药组合物,其为含有rpe细胞及泊洛沙姆而成。
[10]根据[9]记载的医药组合物,其中,在含有泊洛沙姆的医药上容许用作眼内灌注液或清洗液的介质中悬浮有rpe细胞。
[11]根据[10]记载的医药组合物,其中,所述介质为经过调整的汉克斯平衡盐溶液或氧化型谷胱甘肽眼内灌注液或清洗液。
[12]根据[10]或[11]记载的医药组合物,其中,所述介质中的泊洛沙姆的浓度为0.001%(w/v)~0.1%(w/v)。
[13]根据[10]或[11]记载的医药组合物,其中,所述介质中的泊洛沙姆的浓度为0.01%(w/v)~0.1%(w/v)。
[14]根据[9]~[13]中任一项记载的医药组合物,其中,rpe细胞为从冷冻保存状态解冻后1小时以内的细胞,并且医药组合物在制备后8小时以内被移植给对象。
[15]根据[9]~[14]中任一项记载的医药组合物,其中,与不含有泊洛沙姆的情况相比rpe细胞的生存率提高。
[16]根据[9]~[15]中任一项记载的医药组合物,其中,与不含有泊洛沙姆的情况相比rpe细胞的回收率提高。
[17]一种含有rpe细胞的组合物的制造方法,该制造方法包括使rpe细胞在含有泊洛沙姆的医药上容许用作眼内灌注液或清洗液的介质中悬浮的工序。
[18]根据[17]记载的方法,其中,所述介质为经过调整的汉克斯平衡盐溶液或氧化型谷胱甘肽眼内灌注液或清洗液。
[19]根据[17]或[18]记载的方法,其中,所述介质中的泊洛沙姆的浓度为0.001%(w/v)~0.1%(w/v)。
[20]根据[17]或[18]记载的方法,其中,所述介质中的泊洛沙姆的浓度为0.01%(w/v)~0.1%(w/v)。
[21]根据[17]~[20]中任一项记载的方法,其中,rpe细胞为从冷冻保存状态解冻后1小时以内的细胞,并且含有rpe细胞的组合物为在制备后8小时以内被移植给对象的移植用医药组合物。
[22]根据[17]~[21]中任一项记载的方法,其中,与不含有泊洛沙姆的情况相比rpe细胞的生存率提高。
[23]根据[17]~[22]中任一项记载的方法,其中,与不含有泊洛沙姆的情况相比rpe细胞的回收率提高。
[24]根据[9]~[16]中任一项记载的医药组合物,其用于保护视细胞。
[25]根据[1]~[8]中任一项记载的悬浮化剂,其中,所述泊洛沙姆为泊洛沙姆188。
[26]根据[9]~[16]、[24]中任一项记载的医药组合物,其中,所述泊洛沙姆为泊洛沙姆188。
[27]根据[17]~[23]中任一项记载的方法,其中,所述泊洛沙姆为泊洛沙姆188。
发明效果
根据本发明,通过使用泊洛沙姆,可以提高冷冻保存了的rpe细胞的解冻后的生存率及回收率。由于该效果在常温下也长时间持续,因此在制备移植用的细胞悬浮液后能够实现常温下的保存、运送。
另外,通过使用泊洛沙姆,即使将冷冻保存了的rpe细胞在解冻后立即移植,也显示出与移植解冻后培养一定期间的rpe细胞的情况同等以上的视细胞保护效果,因此可以将rpe细胞以冷冻了的状态从cpc运送到医院,在医院内解冻后立即进行移植,能够实现移植方案的简化、移植实施前的时间的缩短。
此外,由于通过使用泊洛沙姆,可以减少从解冻到移植的各工序中的rpe细胞数的损失、使细胞数均一化,因此可以削减为了确保足够移植的细胞数而应该准备的rpe细胞数,另外,由于每次移植的移植细胞的生存率、细胞数的波动减少,因此可以实现治疗效果的均一化、从防止损伤细胞的施用的观点考虑的安全性的提高。
附图说明
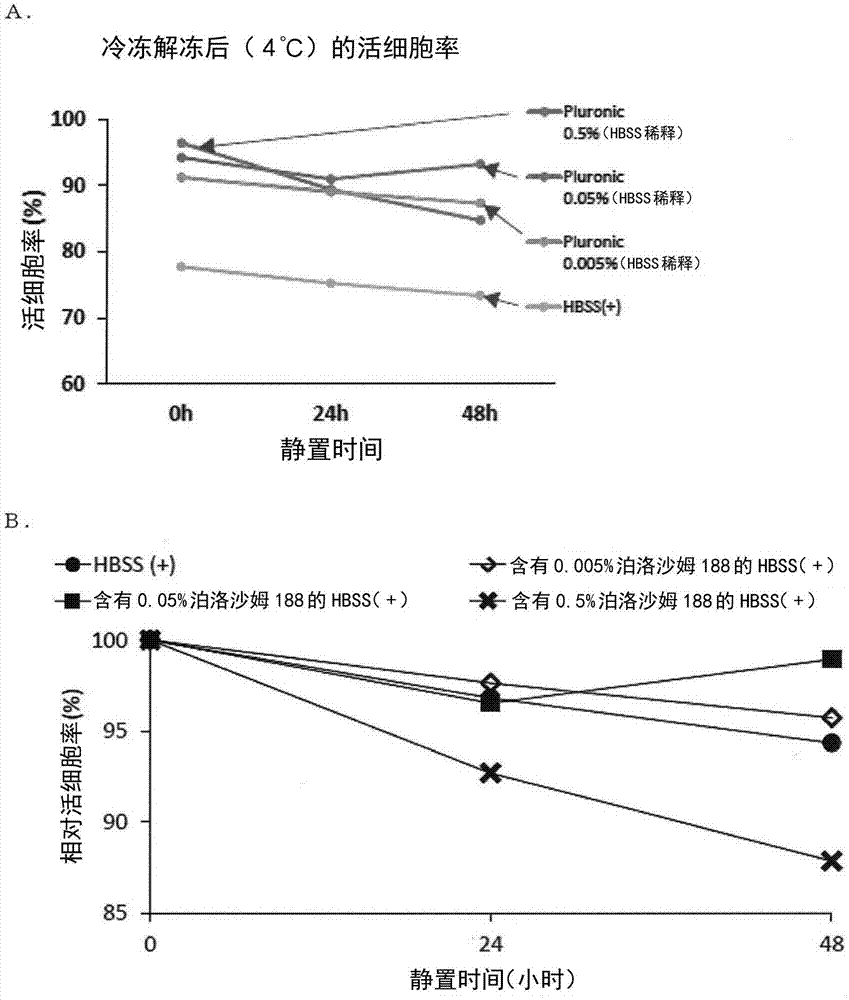
图1是表示各种浓度的泊洛沙姆188对冷冻解冻后在4℃静置到48小时的rpe细胞的生存率产生的效果的图。
图2是表示0.05%(w/v)泊洛沙姆188对冷冻解冻后在室温或4℃静置6小时的rpe细胞的生存率产生的效果的图。
图3是表示各种浓度的泊洛沙姆188对冷冻解冻后在室温静置到8小时的rpe细胞的生存率产生的效果的图。
图4是表示将刚刚解冻后或解冻后培养14天后的rpe细胞仅悬浮于介质(bss)中或悬浮于添加有0.05%(w/v)泊洛沙姆188的介质中后移植到rcs大鼠中时的视细胞保护效果的图。
图5是表示泊洛沙姆188对解冻时的rpe细胞回收率产生的效果的图。
图6是表示泊洛沙姆188对供移植的细胞悬浮液制备工序中的rpe细胞回收率产生的效果的图。
具体实施方式
本发明提供含有泊洛沙姆、和医药上容许用作眼内灌注液或清洗液的介质而成的视网膜色素上皮(rpe)细胞的悬浮化剂。另外,本发明提供含有rpe细胞及泊洛沙姆而成的移植用医药组合物。
(a)视网膜色素上皮(rpe)细胞
本说明书中所谓“视网膜色素上皮(rpe)细胞”,是指构成视网膜色素上皮的上皮细胞及其前体细胞。对于是否为视网膜色素上皮细胞,例如可以通过细胞标记物(rpe65、cralbp、mertk、best1等)的表达、细胞的形态(细胞内的黑色素沉着、多边形且扁平的上皮样的细胞形态、多边形的肌动蛋白束的形成等)等来确认。另外,所谓视网膜色素上皮细胞的前体细胞,是指确定了分化诱导为视网膜细胞的方向的细胞,对于是否为该前体细胞,可以通过细胞标记物(mitf(色素上皮细胞、色素上皮前体细胞)、pax6(色素上皮前体细胞)、rx(视网膜前体细胞)、otx2(视网膜前体细胞)、rpe65(色素上皮细胞)、best1(色素上皮细胞))的表达等来确认。另外,视网膜色素上皮细胞的功能评价例如可以以细胞因子(vegf、pedf等)的分泌能力、吞噬能力等为指标来确认。这些功能评价及确认工序只要是本领域技术人员,就可以设定适当的条件来实施。
rpe细胞可以由拥有rpe细胞的任意动物得到,也可以通过从多能干细胞等利用本身公知的方法进行分化诱导来得到。作为rpe细胞,例如可以举出从多能干细胞分化诱导出rpe细胞的细胞。作为多能干细胞,只要是具有能够分化为存在于生物体中的所有细胞的多能性、并且还兼具增殖能力的干细胞,就没有特别限定,例如包含胚胎性干细胞(es细胞)、通过核移植而得的克隆胚胎来源的胚胎性干细胞(ntes细胞)、精子干细胞(gs细胞)、胚胎性生殖细胞(eg细胞)、人工多能干细胞(ips细胞)、培养成纤维细胞或骨髄干细胞来源的多能性细胞(muse细胞)等。优选多能干细胞为es细胞及ips细胞。多能干细胞的来源没有特别限制,例如可以举出报告过下述的任意一种多能干细胞的建立的任意的动物、优选为哺乳动物、更优选为人、小鼠、大鼠等。
es细胞是来源于受精卵的8细胞期、作为桑葚胚后的胚胎的囊胚的内部细胞块的胚胎来源的干细胞,且具有分化为构成成体的所有细胞的能力、所谓的分化多能性、和基于自我复制的增殖能力。es细胞在1981年发现于小鼠中(m.j.evansandm.h.kaufman(1981),nature292:154-156),其后,在人、猴等灵长类中也建立了es细胞株(j.a.thomsonetal.(1998),science282:1145-1147:j.a.thomsonetal.(1995),proc.natl.acad.sci.usa,92:7844-7848:j.a.thomsonetal.(1996),biol.reprod.,55:254-259:j.a.thomsonandv.s.marshall(1998),curr.top.dev.biol.,38:133-165)。
es细胞可以通过从对象动物的受精卵的囊胚中取出内部细胞块、并在成纤维细胞的饲养细胞上培养内部细胞块来建立。另外,利用继代培养的细胞的维持可以使用添加有白血病抑制因子(leukemiainhibitoryfactor(lif))、碱性成纤维细胞生长因子(basicfibroblastgrowthfactor(bfgf))等物质的培养液来进行。对于人及猴的es细胞的建立和维持的方法,例如记载于usp5,843,780:thomsonja,etal.(1995),procnatl.acad.sci.usa.92:7844-7848;thomsonja,etal.(1998),science.282:1145-1147;h.suemorietal.(2006),biochem.biophys.res.commun.,345:926-932;m.uenoetal.(2006),proc.natl.acad.sci.usa,103:9554-9559;h.suemorietal.(2001),dev.dyn.,222:273-279:h.kawasakietal.(2002),proc.natl.acad.sci.usa,99:1580-1585;klimanskayai,etal.(2006),nature.444:481-485等中。
ips细胞是可以通过将特定的初始化因子以dna或蛋白质的形态导入体细胞来制作的具有与es细胞大致同等的特性、例如分化多能性和基于自我复制的增殖能力的体细胞来源的人工的干细胞(k.takahashiands.yamanaka(2006)cell,126:663-676:k.takahashietal.(2007),cell,131:861-872:j.yuetal.(2007),science,318:1917-1920:nakagawa,m.等人,nat.biotechnol.26:101-106(2008);国际公开wo2007/069666)。
本说明书中使用的称作“体细胞”的术语是指除去卵子、卵母细胞、es细胞等生殖系列细胞或分化全能性细胞以外的所有动物细胞(优选为包括人在内的哺乳动物细胞)。在体细胞中,非限定性地包含胎儿(幼仔)的体细胞、新生儿(幼儿)的体细胞、以及成熟了的健全或疾病性的体细胞的任意一种,另外,包含初代培养细胞、继代细胞、以及株化细胞的任意一种。具体而言,体细胞例如可以例示出(1)神经干细胞、造血干细胞、间充质干细胞、牙髓干细胞等组织干细胞(体性干细胞)、(2)组织前体细胞、(3)淋巴细胞、上皮细胞、内皮细胞、肌肉细胞、成纤维细胞(皮肤细胞等)、毛细胞、肝细胞、胃粘膜细胞、肠细胞、脾细胞、胰细胞(胰外分泌细胞等)、脑细胞、肺细胞、肾细胞及脂肪细胞等分化了的细胞等。
初始化因子可以由以下物质构成:es细胞中特异性地表达的基因、其基因产物或non-codingrna或者对于es细胞的未分化维持起到重要的作用的基因、其基因产物或non-codingrna、或者低分子化合物。作为初始化因子中所含的基因,例如可以例示出oct3/4、sox2、sox1、sox3、sox15、sox17、klf4、klf2、c-myc、n-myc、l-myc、nanog、lin28、fbx15、eras、ecat15-2、tcl1、beta-catenin、lin28b、sall1、sall4、esrrb、nr5a2、tbx3或glis1等,这些初始化因子可以单独使用,也可以组合使用。作为初始化因子的组合,可以例示出wo2007/069666、wo2008/118820、wo2009/007852、wo2009/032194、wo2009/058413、wo2009/057831、wo2009/075119、wo2009/079007、wo2009/091659、wo2009/101084、wo2009/101407、wo2009/102983、wo2009/114949、wo2009/117439、wo2009/126250、wo2009/126251、wo2009/126655、wo2009/157593、wo2010/009015、wo2010/033906、wo2010/033920、wo2010/042800、wo2010/050626、wo2010/056831、wo2010/068955、wo2010/098419、wo2010/102267、wo2010/111409、wo2010/111422、wo2010/115050、wo2010/124290、wo2010/147395、wo2010/147612、huangfud,etal.(2008),nat.biotechnol.,26:795-797、shiy,etal.(2008),cellstemcell,2:525-528、eminlis,etal.(2008),stemcells.26:2467-2474、huangfud,etal.(2008),natbiotechnol.26:1269-1275、shiy,etal.(2008),cellstemcell,3,568-574、zhaoy,etal.(2008),cellstemcell,3:475-479、marsona,(2008),cellstemcell,3,132-135、fengb,etal.(2009),natcellbiol.11:197-203、r.l.judsonetal.,(2009),nat.biotech.,27:459-461、lyssiotisca,etal.(2009),procnatlacadsciusa.106:8912-8917、kimjb,etal.(2009),nature.461:649-643、ichidajk,etal.(2009),cellstemcell.5:491-503、hengjc,etal.(2010),cellstemcell.6:167-74、hanj,etal.(2010),nature.463:1096-100、malip,etal.(2010),stemcells.28:713-720、maekawam,etal.(2011),nature.474:225-9.中记载的组合。
作为从es细胞分化诱导rpe细胞的方法,例如可以举出sdia法(pnas,99:1580-1585,2002)、sfeb法(nat.biotechnol.,26:215-224,2008)等,然而并不限定于这些方法。另外,从ips细胞也可以利用相同的方法分化诱导rpe细胞(例如neurosci.lett.,458:126-131,2009:plosone,8:409-412,2011)。或者,也可以使用wo2015/053375、wo2015/053376、wo2015/125941、wo2017/043605等中记载的方法。
作为本说明书中的rpe细胞,具体而言可以举出人es细胞或从人ips细胞分化诱导出的rpe细胞。
适用本发明的悬浮化剂的、或者本发明的医药组合物中所含的rpe细胞优选为从被冷冻保存的状态解冻后1小时以内、20分钟以内、或刚刚解冻后的rpe细胞。如上所述地制备的rpe细胞被依照本身公知的方法冷冻保存,在即将向本发明的悬浮化剂中悬浮前得到解冻。作为rpe细胞的冷冻保存法,例如可以举出如下的方法等,即,将rpe细胞回收到离心管等中,将细胞离心而颗粒化后,加入包含冷冻保护剂的冷冻保存液而悬浮,将该悬浮液加入冷冻保存管中,在-80℃的冰箱中冷冻后,在气相或液相的氮罐中保存,然而并不限定于此。作为冷冻保护剂,例如可以适当地使用dmso、甘油、抗冻蛋白、抗冻糖蛋白等。
冷冻保存了的rpe细胞的解冻方法也可以使用该技术领域中周知的方法(例如参照freshneyri,cultureofanimalcells:amanualofbasictechnique,4thedition,2000,wiley-liss,inc.,chapter19)。优选在约37℃的热水浴中急速解冻。在使用dmso之类的细胞毒性强的冷冻保护剂的情况下,最好在解冻后立即用适当的稀释剂将dmso浓度稀释到不对细胞造成不良影响的程度,最好通过利用离心分离除去上清液而除去具有毒性的冷冻保护剂等。作为稀释剂,例如可以使用含有血清或不含血清的培养基,此外还可以使用生理盐水、pbs,另外也优选使用本发明的悬浮化剂中的医药上容许用作眼内灌注液或清洗液的介质。
(b)泊洛沙姆(英文:poloxamer)
本申请说明书中所谓“泊洛沙姆”,是以下述结构式表示的三嵌段共聚物:
[化1]
作为泊洛沙姆,例如可以举出泊洛沙姆124、泊洛沙姆188、泊洛沙姆237、泊洛沙姆407,优选为泊洛沙姆188、泊洛沙姆237,更优选为泊洛沙姆188。
泊洛沙姆188(式中,a=80、b=30。)被作为医药品添加物用于稳定(化)剂、表面活性剂、润滑剂、增溶(化)剂、基剂、粘合剂、悬浮(化)剂、涂布剂、湿润剂、乳化剂、粘稠剂、赋形剂、分散剂、崩解剂、溶解辅助剂等用途中,可以安全地使用。
泊洛沙姆188可以利用本身公知的方法来制造。另外,泊洛沙姆188例如以pluronic(注册商标)f68(basf)、pluronicf6810%(100×)(thermofisherscientific(原lifetechnologies))、plonon(注册商标)#188p(日油)等商品名销售。
对于本发明的悬浮化剂、或本发明的医药组合物的介质中所含有的泊洛沙姆、例如泊洛沙姆188的浓度,只要是足以保护rpe细胞、特别是从冷冻保存中解冻了的rpe细胞、抑制细胞的损伤或细胞死亡(rpe细胞保护效果)、改善由rpe细胞带来的视细胞保护效果(防止减少)、且/或防止从解冻到移植的各种工序中的rpe细胞数的损失的浓度,就没有特别限制,然而优选为0.001%(w/v)~0.1%(w/v),更优选为0.01%(w/v)~0.1%(w/v)(例如0.01%(w/v)~小于0.1%(w/v)、0.01%(w/v)~0.09%(w/v)、0.08%(w/v)、0.07%(w/v)、0.06%(w/v)或0.05%(w/v)等)。如果考虑为了防止冷冻保存了的脂肪组织“解冻时”的细胞死亡而必需的泊洛沙姆188的浓度为0.1至2%(w/v)或其以上(上述专利文献2),则令人惊奇的发现是,通过在“解冻后”添加小于0.1%(w/v)的低浓度的泊洛沙姆,可以实现优异的rpe细胞保护效果。
(c)医药上容许用作眼内灌注液或清洗液的介质
作为本发明的悬浮化剂及本发明的医药组合物中所含有的“医药上容许用作眼内灌注液或清洗液的介质”,只要是在医药上容许将在该介质中悬浮rpe细胞而得的悬浮液向疾病部位、即黄斑变性症或视网膜色素变性症的视网膜下视网膜色素上皮的变性或缺损部位直接注入的液体,就没有特别限制,例如可以适当地选择缓冲剂、等渗剂、粘性基剂、螯合剂、ph调节剂、抗氧剂等、并在不对rpe细胞的生存率造成影响的范围中含有。
作为缓冲剂,例如可以举出磷酸缓冲剂、硼酸缓冲剂、柠檬酸缓冲剂、酒石酸缓冲剂、乙酸缓冲剂、氨基酸等。
作为等渗剂,可以举出山梨醇、葡萄糖、甘露醇等糖类、甘油、丙二醇等多元醇类、氯化钠等盐类、硼酸等。
作为粘性基剂,可以举出聚乙烯基吡咯烷酮、聚乙二醇、聚乙烯醇等水溶性高分子、羟乙基纤维素、甲基纤维素、羟丙基甲基纤维素、羧甲基纤维素钠等纤维素类等。
作为螯合剂,可以举出乙二胺四乙酸钠、柠檬酸等。
作为ph调节剂,例如可以举出氢氧化钠、氢氧化钾、碳酸钠、碳酸氢钠、硼酸或其盐(硼砂)、盐酸、柠檬酸或其盐(柠檬酸钠、柠檬酸二氢钠等)、磷酸或其盐(磷酸氢二钠、磷酸二氢钾等)、乙酸或其盐(乙酸钠、乙酸铵等)、酒石酸或其盐(酒石酸钠等)等。
作为抗氧剂,例如可以举出谷胱甘肽、亚硫酸氢钠、干燥亚硫酸钠、焦亚硫酸钠、生育酚等。
本发明的剂的ph通常被调整为约5.0~约8.5,优选调整为约7.0~约8.0,可以优选进行使用了膜滤器等的过滤灭菌等灭菌处理。
在本发明的优选的一个实施方式中,对于“医药上容许用作眼内灌注液或清洗液的介质”,可以使用经过调整的汉克斯平衡盐溶液(hbss)或氧化型谷胱甘肽眼内灌注液或清洗液。作为经过调整的hbss,可以举出不含酚红的hbss(-)(400mg/lkcl、8g/lnacl、350mg/lnahco3、60mg/lkh2po4、47.9mg/l无水na2hpo4、1g/ld-葡萄糖;以下也简称为“hbss(-)”。)、不含酚红的hbss(+)(向hbss(-)中添加了140mg/l无水cacl2、100mg/lmgcl2·6h2o、100mg/lmgso4·7h2o的溶液;以下也简称为“hbss(+)”。)等。另外,作为经过调整的氧化型谷胱甘肽眼内灌注液或清洗液,可以举出bssplus(注册商标)眼内灌注液0.0184%(日本alcon)(以下也简称为“bss”。)等。
(d)本发明的悬浮化剂、本发明的医药组合物
本发明的悬浮化剂可以通过向上述(c)的医药上容许用作眼内灌注液或清洗液的介质中添加适当量的泊洛沙姆(例:泊洛沙姆188)来制备。
本发明的医药组合物可以通过使上述的rpe细胞悬浮于本发明的悬浮化剂中来制备。
如上所述,在本发明的优选的一个实施方式中,利用本发明的悬浮化剂悬浮、作为本发明的医药组合物制备的rpe细胞是从冷冻保存状态刚刚解冻后的细胞。冷冻保存了的rpe细胞在被利用上述的方法解冻后,最好立即由适当的稀释剂稀释,并利用离心分离进行清洗。此处作为稀释剂,除了可以如上所述地使用生理食盐水、pbs以外,还可以使用上述(c)的医药上容许用作眼内灌注液或清洗液的介质(例如hbss(+)、bss等)。在该稀释剂中可以包含、也可以不包含泊洛沙姆(例:泊洛沙姆188),然而为了抑制由离心分离造成的清洗工序中的rpe细胞的损伤、细胞死亡,防止操作中的细胞数的损失,优选向稀释剂中添加泊洛沙姆188。即,在一个实施方式中,通过利用包含泊洛沙姆(例:泊洛沙姆188)的医药上容许用作眼内灌注液或清洗液的介质进行稀释、清洗工序,可以观察到rpe细胞的保护效果、或rpe细胞的损伤或细胞死亡的抑制效果,rpe细胞的回收率得到改善。因而,包括在包含泊洛沙姆(例:泊洛沙姆188)的医药上容许用作眼内灌注液或清洗液的介质中悬浮rpe细胞的工序的rpe细胞的保护方法、rpe细胞的损伤或细胞死亡的抑制方法、或rpe细胞的回收率的改善方法也是本发明的范畴。作为泊洛沙姆的添加浓度,同样优选例示出本发明的悬浮剂中的泊洛沙姆的浓度范围。稀释、清洗工序可以在室温至约37℃进行,也可以在约4℃的冷却下进行。清洗操作可以仅进行1次,也可以反复进行2至数次。
通过将稀释、清洗了的rpe细胞再悬浮于本发明的悬浮化剂中,可以制成本发明的医药组合物、即含有rpe细胞的组合物。本发明的医药组合物中的rpe细胞为从冷冻保存状态解冻后1小时以内、更优选为20分钟以内的细胞。对于本发明的医药组合物中的rpe细胞的密度,只要在向疾病部位、即黄斑变性症、视网膜色素变性症的视网膜色素上皮的缺损部位注入的悬浮液(例如50~500μl、优选为100~300μl)中含有治疗上有效的量的rpe细胞,就没有特别限制,例如可以以达到100~20000细胞/μl、优选为1000~10000细胞/μl的细胞密度的方式悬浮。在使用了es细胞来源rpe细胞的针对黄斑变性症的试药中,以最终达到333细胞/μl的方式在bss中悬浮活rpe细胞,并将该细胞悬浮液150μl(活rpe细胞的总数为50000细胞)注入黄斑部(上述非专利文献1),配合有泊洛沙姆(例:泊洛沙姆188)的本发明的医药组合物与仅在介质(例如bss)中悬浮rpe细胞的情况相比,可以保护rpe细胞,显著地抑制rpe细胞的损伤及细胞死亡,并且可以显著地防止用于稀释、清洗的离心分离工序、接下来的该医药组合物的再悬浮、通过移植医药组合物时的移植用设备(注射器等)时的细胞的损失,因此可以减少使与以往方法同等量的活rpe细胞到达移植部位所需的起始rpe细胞数,从而可以削减移植所必需的rpe细胞的制备所需的成本、时间。
本发明的医药组合物通过将冷冻保存了的rpe细胞在刚刚解冻后悬浮于本发明的悬浮化剂中,即使在4℃静置至少48小时以上、在常温静置至少8小时以上,也不会降低rpe细胞的生存率。该结果意味着具有如下的优点,即,在将cpc中冷冻保存了的rpe细胞解冻、作为移植用制剂制备后,可以在冷藏或常温下运送到实施移植的医院,可以消除运送时的麻烦,并且可以在到达医院后立即实施移植。即,作为一个实施方式,通过将冷冻保存了的rpe细胞在刚刚解冻后悬浮于本发明的悬浮化剂中,可以在解冻后48小时以内、优选在8小时以内将rpe细胞移植给对象患者。
因而,包括以下工序的rpe细胞向患者的移植方法也是本发明的范畴:
(1)将冷冻保存了的rpe细胞解冻的工序、
(2)将经过解冻的rpe细胞悬浮于本发明的悬浮液中的工序、以及
(3)将(2)中得到的包含rpe细胞的悬浮液在解冻后48小时以内、优选在8小时以内向患者的眼组织施用的工序。
另一方面,本发明的医药组合物即使在将冷冻保存了的rpe细胞刚刚解冻后悬浮于本发明的悬浮化剂中,然后立即用于移植,也显示出与将解冻了的细胞培养一定期间后移植的情况同等或其以上的高的视细胞保护效果。即,作为一个实施方式,可以在将冷冻保存了的rpe细胞解冻后不进行恢复培养地移植。即,以在解冻后不包括培养rpe细胞的工序为特征的上述向患者的移植方法也是本发明的范畴。
此处,由rpe细胞带来的所谓“视细胞保护效果”,是指通过rpe细胞的移植而维持视细胞的生存、保护视网膜功能并使之正常化的效果。
在使用了es细胞来源rpe细胞的针对黄斑变性症的治疗试验中,在不包含泊洛沙姆的bss中悬浮刚刚解冻后的rpe细胞,不经过培养工序而直接用于移植(上述非专利文献1),取得了一定的治疗效果。该以往方法中rpe细胞的视细胞保护效果显著地降低的可能性高的新问题、和通过在悬浮化剂中配合泊洛沙姆(例:泊洛沙姆188)而解决该问题的方法在本发明中同时提出。该新问题可以说促使对以往实施的如下的简易移植方案重新思考,即,出于提高由rpe细胞带来的治疗效果(视细胞保护效果)的目的,从cpc以冷冻保存了的状态将rpe细胞运送到医院,在医院内解冻后立即移植rpe细胞。本发明证实,通过添加泊洛沙姆188,即使将刚刚解冻后的rpe细胞用于移植,也可以获得与将培养一定期间后的rpe细胞移植的情况同等的治疗效果,由此显示,能够没有损害治疗效果地实施以往所示的简易移植方案。即,利用本发明,可以实现简便并且有效的rpe细胞的移植治疗。
本发明的医药组合物通过使用包括适当的注射器及针头的的移植用设备(例如medone0(注册商标)、polytip(注册商标)、cannula25g/38g等),向例如具有黄斑变性症(例如萎缩型及渗出型老年性黄斑变性症、stargardt病)、视网膜色素变性症等视网膜疾病的哺乳动物(例如人、小鼠、大鼠等、优选为人)的视网膜下注入,就可以进行移植。本发明的医药组合物通过添加泊洛沙姆(例:泊洛沙姆188),而提高移植用设备内的流动性,可以显著地减少注入时残留于该设备内的rpe细胞数。因此,能够正确地设定移植用量,在临床研究以及治疗试验及认可后的临床使用中可以正确地实施用量依赖性的治疗效果的评价判定,可以对再生医疗等产品的实用化做出大的贡献。
以下给出实施例而对本发明进一步具体说明,然而本发明并不受它们的任何限定。
[实施例]
实施例1.由泊洛沙姆188带来的rpe细胞保护效果的验证
继时性地测定在以各种浓度含有已知有细胞保护效果的泊洛沙姆188的hbss(+)中悬浮的rpe细胞以细胞悬浮液的状态保存时的活细胞率,由此验证了泊洛沙姆188对rpe细胞的保护效果。
将被进行冷冻保存(stem-cellbanker(注册商标)gmpgrade)的rpe细胞(1120c7ips细胞来源rpe细胞;ips细胞提供方:国立大学法人京都大学)在37±2℃解冻,利用台盼蓝染色法测定活细胞数及活细胞率,以达到1.5×105细胞/管的细胞数的方式进行了分注。然后,进行离心分离(200g、4分钟、室温),除去上清液。向其中添加含有0%(w/v)、0.005%(w/v)、0.05%(w/v)、0.5%(w/v)的浓度的泊洛沙姆188的hbss(+)450μl并进行再悬浮,将所得的rpe细胞悬浮液在4℃静置,继时性地测定出活细胞率。含有泊洛沙姆188的hbss(+)是将pluronicf-68、10%(100x)(thermofisherscientific(原lifetechnologies))用hbss(+)稀释而制备(以下的所有实施例中都利用相同的方法进行含有泊洛沙姆188的介质的制备)。将刚刚制备悬浮液后设为0小时,在24小时后、48小时后的各测定时刻实施取样,利用台盼蓝染色法测定出活细胞率。
将结果表示于图1中。图1a是将活细胞率的变动以测定值绘制的图,图1b是以刚刚制备悬浮液后(0小时后)的活细胞率的值为100%、以相对值显示4℃静置后的活细胞率的变动的图。与悬浮于未调制hbss(+)中的情况相比,悬浮于含有0.005%(w/v)、0.05%(w/v)泊洛沙姆188的hbss(+)中的rpe细胞的活细胞率的降低得到抑制,直至4℃静置48小时(图1a)。另一方面,与悬浮于未调制hbss(+)中的情况相比,悬浮于含有0.5%(w/v)泊洛沙姆188的hbss(+)中的rpe细胞的活细胞率降低的倾向大,没有抑制活细胞率降低(图1b)。根据这些结果发现,泊洛沙姆188的添加浓度0.005%(w/v)及0.05%(w/v)抑制活细胞率降低。此外,泊洛沙姆188的添加浓度0.5%(w/v)无法抑制活细胞率降低。暗示出在该浓度下,显现出由表面活性剂的细胞膜增溶作用造成的细胞损伤性。
然后,考虑到在临床现场是在室温进行rpe细胞悬浮液制备操作,出于评价悬浮于未调制bss或含有0.05%(w/v)泊洛沙姆188的bss中的rpe细胞悬浮液在室温及4℃的保存稳定性的目的,进行了以下的实验。
将被冷冻保存的rpe细胞(1120c7ips细胞来源rpe细胞;ips细胞提供方:国立大学法人京都大学)在37±2℃解冻并用bss稀释、清洗,利用台盼蓝染色法测定活细胞数及活细胞率,以达到3×106细胞/管的细胞数的方式进行分注。然后,进行离心分离(200g、4分钟、室温),除去上清液。向其中添加未调制bss或含有0.05%(w/v)泊洛沙姆188的bss1ml并进行再悬浮,将所得的rpe细胞悬浮液在室温或4℃静置,6小时后使用nucleocounter(注册商标)nc-200(制造商:chemometec)测定出活细胞率。
将结果表示于图2中。与悬浮于未调制bss中的情况相比,悬浮于含有泊洛沙姆188的bss中的rpe细胞的活细胞率在室温及4℃都保持为高活细胞率,直至静置6小时后。另外显示,悬浮于含有泊洛沙姆188的bss中的rpe细胞悬浮液的保存稳定性在室温及4℃静置时直至6小时后没有变化。因而显而易见,在室温下也可以观察到泊洛沙姆188对rpe细胞的保护效果。如果使用含有泊洛沙姆188的bss作为移植用介质,则在易于控制温度的室温条件下,在院内cpc等特殊环境并且在远距离地区制备、保存或运送rpe细胞悬浮液时也有效。
此外,出于针对泊洛沙姆188对rpe细胞的保护效果详细地验证有效浓度的目的,进行了以下的实验。
将被冷冻保存的rpe细胞(ff-i01ips细胞来源rpe细胞:ips细胞提供方:国立大学法人京都大学)在37±2℃解冻并用hbss(+)稀释、清洗,使用nucleocounter(注册商标)nc-200(制造商:chemometec)测定活细胞数及活细胞率,以达到1×106细胞/管的细胞数的方式进行分注。然后,进行离心分离(200g、4分钟、室温),除去上清液。添加含有0%(w/v)、0.001%(w/v)、0.005%(w/v)、0.01%(w/v)、0.05%(w/v)、0.1%(w/v)的浓度的泊洛沙姆188的hbss(+)1ml并进行再悬浮,将所得的rpe细胞悬浮液在室温下静置,继时性地测定活细胞率。在刚刚制备悬浮液后、2小时后、4小时后、8小时后的各测定时刻实施取样,使用nucleocounter(注册商标)nc-200(制造商:chemometec)测定活细胞率。
与悬浮于未调制hbss(+)中的情况相比,悬浮于含有泊洛沙姆188的hbss(+)中的rpe细胞的活细胞率在进行了试验的所有泊洛沙姆188浓度下,都保持为高活细胞率,直至室温静置8小时(图3)。在泊洛沙姆188的浓度为0.01%(w/v)~0.1%(w/v)时,显示出特别高的活细胞率。根据这些结果发现,作为移植用介质,泊洛沙姆188的rpe细胞保护效果的合适浓度为0.01%(w/v)~0.1%(w/v)。由此,在不需要特别条件的通常的院内制备时的环境下,可以在被认为对于制备后的从制备场所的移动、运送及移植时的眼科手术而言所必需的足够的时间中稳定地保持rpe细胞的活细胞率,不会损失作为rpe细胞制剂的品质,安全地供移植使用。另外,如果使用本移植用介质,则在院内cpc等特殊环境并且在远距离地区制备rpe细胞悬浮液、在常温下保存或运送时也有效。
实施例2.使用了rcs大鼠的视细胞保护效果试验
利用作为视网膜变性大鼠模型的rcs大鼠的视网膜下移植后的视网膜视细胞保护效果,评价了由有无解冻后的培养工序及有无泊洛沙姆188向移植用介质中的添加造成的对使用了人ips细胞来源rpe细胞的细胞悬浮液的有效性的效果的差别。
受试动物:使用了3周龄的rcs(royalcollegeofsurgeons)大鼠(提供方:cleajapan,inc.)。rcs大鼠是作为表现系具有自然发病视网膜变性的大鼠,作为视网膜色素变性症及老年性黄斑变性症的模型动物,在证实对这些疾病的有效性的试验系中广泛地使用。
受试物质:使用如下得到的物质作为受试物质,即,将在即将移植前解冻了的rpe细胞(1120c7ips细胞来源rpe细胞;ips细胞提供方:国立大学法人京都大学)不经过培养地使用不同的2种移植用介质(bssplus500眼内灌注液0.0184%(日本alcon;以下记作bss)、含有0.05%(w/v)泊洛沙姆188的bss)作为悬浮液制备的物质(受试物质-1a及-1b),或在移植前在rpe细胞制造设施中解冻复苏后培养14天,将其保持未冷冻状态地使用不同的2种移植用介质(含有泊洛沙姆188的bss、bss)作为悬浮液制备的物质(受试物质-2及-3)。
受试物质-1a:用bss悬浮解冻rpe细胞
受试物质-1b:用含有泊洛沙姆188的bss悬浮解冻rpe细胞
受试物质-2:用含有泊洛沙姆188的bss悬浮培养rpe细胞
受试物质-3:用bss悬浮培养rpe细胞
移植方法:将盐酸氯胺酮(25mg/ml;supriyalifescienceltd.)与塞拉嗪(10mg/ml;拜耳药品株式会社)的9:2(容量比)混合液以2.0ml/kg实施肌肉内给药,进行麻醉后,点入散瞳剂(mydrinp滴眼液、参天制药株式会社),使之散瞳。确认散瞳后,用benoxyl滴眼液0.4%(参天制药株式会社)实施眼球的表面麻醉后,用由含有0.1%碘伏的生理盐水形成的消毒液对眼球表面及眼睑进行消毒。消毒液立即由生理盐水从眼球冲掉。消毒后,点上scopisol滴眼液(千寿制药株式会社),将进行了酒精消毒、并用生理盐水清洗了的unicon公司制隐形眼镜放在眼球上,在显微镜下,使用针(33g)在眼球上开孔,使用hamilton注射器(10μl)及针(33g)向视网膜下注入受试物质或介质。注入结束后将阿替美唑盐酸盐(antisedan;5.0mg/ml、orionpharma)进行了肌肉内施用(0.72ml/kg)。对于伪处理眼球,进行除了注入操作以外与介质及受试物质施用眼球相同的操作。
病理学的检查(标本制作):将眼球及视神经用superfix(仓敷纺织株式会社)固定。在解剖检查日的第三天不进行水洗,用密闭式自动固定包埋装置进行处理。进行了薄切。
检查方法:各个体以最低1只(介质组、伪处理组、无处置组各为1只眼,受试物质施用组各为10只眼)的标本观察了视神经乳头、视神经。视细胞残留数是对视网膜区域进行4等分(移植侧前方、移植侧后方、非移植侧前方及非移植侧后方),对各区域的每个载玻片将外颗粒层的视细胞残留的最大数计分化,继而算出各区的最大数的平均值。
【表1】
试验组构成
将结果表示于图4中。在使用bss作为移植用介质的情况下,视细胞层残留数(onlscore)与bss施用组相比,培养rpe细胞的悬浮液(受试物质-3)施用组显示出明显高的值。然而,与bss施用组相比,解冻rpe细胞的悬浮液(受试物质-1a)施用组显示出高值的倾向,然而没有显著性差别。该结果显示,被移植的rpe细胞具有视细胞保护效果,对于该效果,与解冻rpe细胞相比,培养rpe细胞的一方更高。另一方面,在使用含有泊洛沙姆188的bss作为移植用介质的情况下,视细胞层残留数(onlscore)与含有泊洛沙姆188的bss施用组相比,解冻rpe细胞的悬浮液(受试物质-1b)及培养rpe细胞的悬浮液(受试物质-2)施用组显示出明显且显著高的值。更令人惊奇的是,解冻rpe细胞的悬浮液(受试物质-1b)施用组与培养rpe细胞的悬浮液(受试物质-2)施用组相比显示出高值倾向。
根据该结果发现,通过使用含有泊洛沙姆188的bss作为移植用介质,解冻rpe细胞与培养rpe细胞的视细胞保护效果同等,或者反而比其更好。通过使用含有泊洛沙姆188的bss作为移植用介质,在每次移植使用时,能够省略将冷冻解冻细胞培养14天的工序、以及接在其后的剥离、回收培养细胞、作为细胞悬浮液制备、运送该细胞悬浮液的一连串工序和其间的用于保持品质性能稳定的一切试验。如果考虑各个临床现场、院内制备等环境、技术的变量,则难以在院内将冷冻细胞解冻后培养一定期间,然而通过使用本方法,即使将在制造单位(cpc)进行了冷冻制剂化的细胞医药品在医疗现场解冻后立即使用,也可以提供保持、发挥与培养细胞同等或在其以上的视细胞保护功能的细胞。
实施例3.由泊洛沙姆188添加带来的对解冻时的细胞回收率的影响
验证了由作为将冷冻保存细胞解冻时使用的移植用介质的未调制hbss(+)或含有0.05%(w/v)泊洛沙姆188的hbss(+)造成的对解冻后的细胞回收率的影响。
将制剂后被冷冻保存的rpe细胞(qhji01ips细胞来源rpe细胞:ips细胞提供方:国立大学法人京都大学)在37±2℃解冻,用未调制hbss(+)或含有0.05%(w/v)泊洛沙姆188的hbss(+)悬浮。然后,进行离心分离(200g、4分钟、室温),除去上清液。分别用相同的未调制hbss(+)或含有泊洛沙姆188的hbss(+)再悬浮,使用nucleocounter(注册商标)nc-200(制造商:chemometec)或台盼蓝染色法测定出活细胞数及死细胞数。对以2×107cells/vial冷冻保存了的细胞的活细胞、死细胞算出以2×107cells为100%时的回收率及损失细胞的比率。
将结果表示于图5中。使用nucleocounter(注册商标)nc-200(制造商:chemometec)测定活细胞数及死细胞数时,用未调制hbss(+)再悬浮的样品的解冻后的回收率为活细胞60.50%、死细胞2.10%、损失细胞37.40%。另一方面,用含有0.05%(w/v)泊洛沙姆188的hbss(+)再悬浮的样品的解冻后的回收率为活细胞79.10%、死细胞1.55%、损失细胞19.35%。使用台盼蓝染色法测定活细胞数及死细胞数时,用未调制hbss(+)再悬浮的样品的解冻后的回收率为活细胞45.5%、死细胞2.75%、损失细胞51.75%。另一方面,用含有0.05%(w/v)泊洛沙姆188的hbss(+)再悬浮的样品的回收率为活细胞87.50%、死细胞7.50%、损失细胞5.00%。
根据这些结果证实,经过冷冻保存的rpe细胞被解冻时受到大的损害,从而使作为活细胞的回收率降低,损失细胞的比率升高。然而发现,通过在刚刚解冻后,将rpe细胞悬浮于含有0.05%(w/v)泊洛沙姆188的hbss(+)中,可以大幅度降低损失细胞的比率。通过使用含有0.05%(w/v)泊洛沙姆188的hbss(+)而减轻细胞的损失,该做法除了具有可以严密地控制冷冻保存制剂的细胞数的产业上的优点以外,还会促成对每个患者的必需细胞数的确保、负担费用的减轻。
实施例4.由泊洛沙姆188添加带来的对供移植用的细胞悬浮液制备工序中的细胞回收率的影响
作为移植用介质,制备出在未调制hbss(+)或含有0.05%(w/v)泊洛沙姆188的hbss(+)中悬浮有rpe细胞的细胞悬浮液。对该细胞悬浮液进行离心分离,除去上清液后测定活细胞数、死细胞数,算出rpe细胞的回收率,由此验证了由泊洛沙姆188添加带来的对细胞回收率的影响。
将解冻后用移植用介质清洗了1次的rpe细胞(qhji01ips细胞来源rpe细胞:ips细胞提供方:国立大学法人京都大学)用与前一工序相同的未调制hbss(+)或含有0.05%(w/v)泊洛沙姆188的hbss(+)悬浮。使用nucleocounter(注册商标)nc-200(制造商:chemometec)或台盼蓝染色法测定活细胞数,将rpe细胞悬浮液以达到1×106细胞/管的细胞数的方式进行分注。然后,作为离心分离前的细胞数,使用nucleocounter(注册商标)nc-200(制造商:chemometec)或台盼蓝染色法测定出活细胞数及死细胞数。进行离心分离(200g、4分钟、室温),除去上清液。用未调制hbss(+)或含有泊洛沙姆188的hbss(+)再悬浮。然后,作为离心分离后的细胞数,使用nucleocounter(注册商标)nc-200(制造商:chemometec)或台盼蓝染色法测定出活细胞数及死细胞数。以离心分离前的活细胞数为100%,算出离心分离后的细胞的回收率。
将结果表示于图6中。使用nucleocounter(注册商标)nc-200(制造商:chemometec)测定活细胞数及死细胞数时,用未调制hbss(+)再悬浮的样品的回收率为活细胞54.23%、死细胞2.36%、损失细胞43.41%。另一方面,用含有0.05%(w/v)泊洛沙姆188的hbss(+)再悬浮的样品的回收率为活细胞98.42%、死细胞1.03%、损失细胞0.55%。使用台盼蓝染色法测定活细胞数及死细胞数时,用未调制hbss(+)再悬浮的样品的回收率为活细胞74.80%、死细胞15.45%、损失细胞9.75%。另一方面,用含有0.05%(w/v)泊洛沙姆188的hbss(+)再悬浮的样品的回收率为活细胞86.60%、死细胞5.36%、损失细胞8.04%。
根据这些结果,通过向移植用介质中添加泊洛沙姆188,使由细胞悬浮液制备工序中的离心分离操作造成的死细胞数、或损失细胞的比率大幅度减少,证实活细胞的回收率的改善。由此,不仅可以减少由细胞悬浮液制备的操作环境、例如使用设备、以及依赖于操作人的细胞的解冻、清洗、以及悬浮液中的细胞数计测的手法等的波动造成的细胞伤害的影响,确保有效的细胞数,还可以正确地掌握细胞数,因此能够使临床现场中的供移植用的细胞悬浮液的制备操作稳定化。
实施例5.rpe细胞通过移植用设备(medone(注册商标)polytip(注册商标)cannula25g/38g)效率的改善
作为移植用介质,制备出在未调制bss、或含有0.05%(w/v)泊洛沙姆188的bss中悬浮有rpe细胞的细胞悬浮液。测定通过移植用设备后的活细胞数,由此评价了细胞悬浮液的移植用设备通过效率。
制备出用未调制bss或含有0.05%(w/v)泊洛沙姆188的bss悬浮了的rpe细胞(ff-i01ips细胞来源rpe细胞:ips细胞提供方:国立大学法人京都大学)悬浮液。然后,作为通过移植用设备前的细胞,使用nucleocounter(注册商标)nc-200(制造商:chemometec)测定出活细胞数。采集通过移植用设备后的细胞悬浮液,使用nucleocounter(注册商标)nc-200(制造商:chemometec)测定出活细胞数。以通过移植用设备前的活细胞数作为初始值(100%),算出通过移植用设备后的活细胞数的比率,评价了移植用设备通过效率。
将结果表示于表2中。用未调制bss再悬浮了的样品的通过移植用设备前的活细胞数为1.26×106细胞/ml/管(初始值),通过移植用设备后的活细胞数为1.08×106细胞/ml/管(通过效率85.7%)。另一方面,用含有0.05%(w/v)泊洛沙姆188的bss再悬浮了的样品的通过移植用设备前的活细胞数为1.48×106细胞/ml/管(初始值),通过移植用设备后的活细胞数为1.45×106细胞/ml/管(通过效率98.0%)。
[表2]
根据这些结果,通过使用含有0.05%(w/v)泊洛沙姆188的bss作为移植用介质,rpe细胞悬浮液在移植用设备内的流动性提高,证实了在移植用设备内被捕获的细胞数的减少、以及移植用设备通过效率的改善。此前,在供移植用的细胞数与通过移植用设备后的细胞数中存在15%左右的偏离。然而,显而易见,通过添加泊洛沙姆188,使该偏离大幅度减少。由此,对因通过移植用设备而造成的移植细胞的活细胞率降低的担心得到缓解。另外,能够正确地设定移植用量,在临床研究以及治疗试验及认可后的临床使用中可以正确地实施用量依赖性的治疗效果的评价判定,可以对再生医疗等制品的实用化做出大的贡献。
产业上的可利用性
包含泊洛沙姆(例:泊洛沙姆188)的本发明的悬浮化剂起到改善冷冻保存了的rpe细胞解冻后的生存率的效果、改善在刚刚解冻后将rpe细胞用于移植时的视细胞保护效果的效果、以及防止从解冻至移植的各种工序中的细胞的损失的效果。因而,包含悬浮于本发明的悬浮化剂中的rpe细胞的本发明的医药组合物的处置便利,并且治疗效果也优异,在以黄斑变性症为首的视网膜疾患的移植治疗中极为有用。
本申请以在日本申请的特愿2016-131171(申请日:2016年6月30日)为基础,将其内容全都包含于本说明书中。
- 还没有人留言评论。精彩留言会获得点赞!