一种双载多西紫杉醇和黄酮类化合物的聚合物纳米粒及其制备方法与流程
本发明涉及药物研发领域,具体涉及一种以纳米材料为载体的抗肿瘤药物。
背景技术
多烯紫杉醇(docetaxel,dtx)是由欧洲红豆杉叶中的提取物进一步合成的紫衫烷类广谱抗肿瘤药物。近年来,大量研究报告证实了dtx对乳腺癌、肺癌、头颈癌、肉质瘤、非小型细胞癌、前列腺癌等恶性肿瘤具有较好的作用。
由于dtx存在低水溶性和不稳定性,现今主流的做法是将其搭载到具有两性亲和能力的纳米材料上,纳米材料的疏水侧结合并包裹dtx;纳米材料的亲水侧基团负责与体液接触,具有较好的生物相容性,实现其运输功能。纳米材料还能减少体循环中药物的非靶向释放,从而保证高载药量和肿瘤治疗中的有效药物浓度。
但是只有正确的材料才能提升药物本身的治疗效果,yu等的研究(journalofdrugtargeting,2007,15(4):279-284)就发现,抗癌药多柔比星搭载到peg-pla材料后并未能显著提升多柔比星的抗癌效果。因此,合适的纳米材料关系到药物的功效。
dtx还存在着耐药性的问题,通过多种药物的协同作用有望解决该问题。专利cn107913249a公开了几种含有dtx和一些中药单体的组合,它们可以一定程度上降低肿瘤细胞的耐药性,但其程度尚不能满足人们的需求。
技术实现要素:
为了解决上述问题,本发明提供了一种双载多西紫杉醇和天然黄酮化合物(漆黄素、木犀草素、山奈酚)的聚合物纳米粒。
本发明抗肿瘤的组合物,它包括如下重量配比的组分:多西紫杉醇10~25份,黄酮14~25份。
优选地,所述组合物包括如下重量配比的组分:多西紫杉醇10份,黄酮14份。
优选地,所述黄酮为漆黄素、木犀草素或山奈酚。
本发明还提供了一种双载多西紫杉醇和黄酮类化合物的聚合物纳米粒,其特征在于:它由以下重量配比的原料制成:多西紫杉醇10~25份,黄酮14~25份,peg-pcl两嵌段聚合物材料50~500份,水20~50份。
所述原料还包含水溶性乳化剂50~125份。
它由以下重量配比的原料制成:多西紫杉醇5份,黄酮7份,peg-pcl两嵌段聚合物材料100份,水溶性乳化剂25份,水10份。
所述黄酮为漆黄素、木犀草素或山奈酚;
和/或,所述peg-pcl两嵌段聚合物材料中,peg与pcl的嵌段摩尔比为1:1、1:2或1:4;
和/或,所述水溶性乳化剂为泊洛沙姆f127或聚乙烯醇中的一种。
本发明还提供了一种前述聚合物纳米粒的方法,其特征在于:
(1)peg-pcl溶于二氯甲烷或乙酸乙酯,多西紫杉醇和黄酮溶于无水乙醇,混合前述溶液,在旋转蒸发仪中形成薄膜层;
(2)步骤(1)中的薄膜溶解于磷酸缓冲液中,并用超声波使其混合均匀;
(3)用微孔滤膜过滤,冷冻干燥得固体粉末。
步骤(1)中的旋转蒸发仪设定温度是35-50℃,优选为45℃;
和/或,步骤(2)中的磷酸缓冲液浓度0.01m,ph值为7.4,温度50-75℃;
和/或,步骤(3)中的微孔滤膜孔径为0.45微米。
本发明还提供了一种制备前述聚合物纳米粒的方法,其特征在于:包括以下步骤:
1)peg-pcl溶于二氯甲烷或乙酸乙酯,多西紫杉醇和黄酮溶于无水乙醇,混合前述溶液,作为有机相;
2)泊洛沙姆f127或聚乙烯醇溶于超纯水中,作为水相;
3)在超声乳匀分散仪乳化条件下,将1)中有机相缓慢滴加入2)中水相,乳化形成乳液;
4)使用旋转蒸发仪除去3)中乳液的有机溶剂,制得载药纳米乳液,并于4℃保存。
步(3)的乳化条件为5000-15000rpm;
和/或,步骤4)的旋转蒸发仪设定温度是32-45℃,优选为37℃。
本发明还提供了一种制备前述聚合物纳米粒的方法,其特征在于:包括以下步骤:
(1-1)peg-pcl溶于二氯甲烷或乙酸乙酯,多西紫杉醇和黄酮溶于无水乙醇,混合前述溶液,作为有机相;
(1-2)泊洛沙姆f127或聚乙烯醇溶于超纯水中,作为水相;
(1-3)在高压均质机工作条件下,将(1-1)所述有机相倒入(1-2)所述水相中,连续均质化1-5分钟,循环1-6次得到初乳;
(1-4)使用旋转蒸发仪除去(1-3)中乳液的有机溶剂,制得载药纳米乳液,并于4℃保存。
步骤(1-3)所述工作条件为:20-50rpm,10-30mpa;
和/或,步骤(4)所述旋转蒸发仪设定温度为32-50℃,优选为40℃。
本发明还提供了前述聚合物纳米粒在制备治疗肿瘤的药物中的用途。
本发明所制得的空白纳米粒粒径在50-200nm,所制得的双载药聚合物纳米粒的粒径为70-300nm,粒径分布均匀;多西紫杉醇和黄酮化合物的载药率分别在3-6%与4-8%,包封率分别在80-95%与75-90%,稳定性良好。
本发明所制得的纳米粒在tem电镜下显示出完整、独立、分散均均的类球形粒子,平均粒径小于300nm,zeta电位在-10mv-0mv。
本发明所用的两亲性聚合物纳米材料利用其疏水性内核包裹疏水性药物多西紫杉醇与黄酮化合物,其亲水性外壳作为隐形功能的基团,能够减少纳米粒被网状内皮吞噬系统的识别与清除作用,从而延长在体内作用时间。
本发明所制得的双载药纳米粒,具有显著的缓释效果,能够在体内保持较高的血药浓度,持续作用于肿瘤细胞,达到治疗效果,且对正常组织器官的损伤非常少,且所载药物黄酮包括漆黄素、木樨草素、山萘酚),与多西紫杉醇用于抗瘤可以发挥协同增效作用,应用前景优良。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
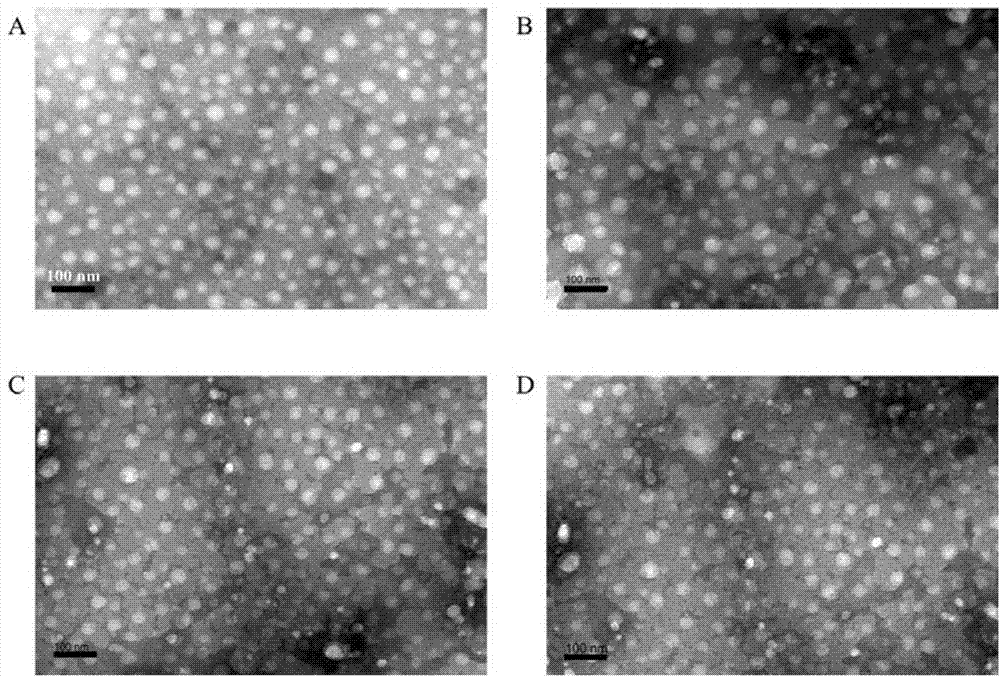
图1a是空白聚合物纳米粒tem电镜图;1b双载多西紫杉醇和漆黄素纳米粒的tem电镜图;1c是双载多西紫杉醇和木犀草素纳米粒的tem电镜图;1d是双载多西紫杉醇和山奈酚纳米粒的tem电镜图。
图2是双载多西紫杉醇和各种黄酮类化合物的聚合物纳米粒(材料嵌段比为1:1)的水合平均粒径以及zeta电位分布图。
图3是双载多西紫杉醇和各种黄酮类化合物的聚合物纳米粒(材料嵌段比为1:2)的水合平均粒径以及zeta电位分布图。
图4是双载多西紫杉醇和各种黄酮类化合物的聚合物纳米粒(材料嵌段比为1:4)的水合平均粒径以及zeta电位分布图。
图5a是双载多西紫杉醇和漆黄素的聚合物纳米粒的体外释放曲线;5b是双载多西紫杉醇和木犀草素的聚合物纳米粒的体外释放曲线;5c是双载多西紫杉醇和山奈酚的聚合物纳米粒的体外释放曲线。
图6是双载多西紫杉醇和各种黄酮化合物的聚合物纳米粒的体外抗肿瘤细胞活性图。
图7是双载多西紫杉醇和各种黄酮化合物的聚合物纳米粒的体内肿瘤生长抑制图。
具体实施方式
下面结合附图及优选实施例对本发明作进一步详细说明,应当理解,优选实施例仅用于说明和解释本发明,并不限定本发明。
实施例1一种双载多西紫杉醇和漆黄素的纳米粒的制备方法
称取peg-pcl(1:1,mw:10k)50.0mg溶于5ml乙酸乙酯,5mg漆黄素和4mg多西紫杉醇溶于2ml无水乙醇,并将两种溶液混合转移到圆底烧瓶内,在旋转蒸发仪下工作条件(45℃,50rpm,30min)下形成薄膜层;量取5mlpbs溶液(0.01m,ph7.4,65℃)溶解薄膜,并用超声分散纳米粒使其均匀分散在水溶液中;然后经0.45μm微孔滤膜过滤,冷冻干燥得固体粉末。其水合平均粒径图如图2a所示。
实施例2一种双载多西紫杉醇和木犀草素的纳米粒的制备方法
称取peg-pcl(1:1,mw:20k)200.0mg溶于3ml乙酸乙酯,20.0mg木樨草和16mg多西紫杉醇溶于2ml无水乙醇,并将两种溶液混合为有机相备用;称取50.0mg泊洛沙姆f127溶于20ml超纯水中作为水相备用;在t25探头超声乳匀分散仪乳化条件(9600rpm/min)下将有机相缓慢滴加入水相中,连续工作10min。将乳化好的乳液转移至圆底烧瓶内,使用旋转蒸发仪进行减压抽滤(37℃,60rpm,15min),除去有机溶剂,制得载药纳米乳液,并于4℃条件保存。其水合平均粒径图如图2b所示。
实施例3一种双载多西紫杉醇和漆黄素的纳米粒的制备方法
称取peg-pcl(1:2,mw:15k)200.0mg溶于3ml二氯甲烷,14.0mg漆黄素与10.0mg多西紫杉醇分别溶于1ml无水乙醇,并将两种溶液混合为有机相备用;称取50.0mg聚乙烯醇溶于20ml超纯水中作为水相备用;在t25探头超声乳匀分散仪乳化条件(9600rpm/min)下将有机相缓慢滴加入水相中,连续工作10min。将乳化好的乳液转移至圆底烧瓶内,使用旋转蒸发仪进行减压抽滤(37℃,60rpm,15min),除去有机溶剂,制得载药纳米乳液,并于4℃条件保存。其水合平均粒径图如图3a所示。
实施例4一种双载多西紫杉醇和山奈酚的纳米粒的制备方法
按照比例称取125.0mg泊洛沙姆f127于50ml超纯水中,室温搅拌2h使之充分溶解,制备成水相待用;取5ml二氯甲烷溶解500.0mgpeg-pcl(1:2,mw:30k)聚合物材料,25.0mg山奈酚与25.0mg多西紫杉醇共溶于5ml无水乙醇,作为有机相待用;在高压均质机工作条件下(35rpm,20mpa),将有机相倒入50ml水相中,连续均质乳化2min,循环三次得到初乳。将初乳转移至圆底烧瓶内,使用旋转蒸发仪进行减压抽滤(40℃,60rpm,20min),除去有机溶剂,制得载药纳米乳液,并于4℃条件保存。其水合平均粒径图如图3b所示。
实施例5一种双载多西紫杉醇与木犀草素的纳米粒的制备方法
称取peg-pcl(1:4,mw:25k)200.0mg溶于3ml二氯甲烷,14.0mg木犀草素与10.0mg多西紫杉醇分别溶于1ml无水乙醇,并将两种溶液混合为有机相备用;称取50.0mg聚乙烯醇溶于20ml超纯水中作为水相备用;在t25探头超声乳匀分散仪乳化条件(9600rpm/min)下将有机相缓慢滴加入水相中,连续工作10min。将乳化好的乳液转移至圆底烧瓶内,使用旋转蒸发仪进行减压抽滤(37℃,60rpm,15min),除去有机溶剂,制得载药纳米乳液,并于4℃条件保存。其水合平均粒径图如图4a所示。
实施例6一种双载多西紫杉醇与漆黄素的纳米粒的制备方法
称取peg-pcl(1:4,mw:25k)200.0mg溶于3ml二氯甲烷,14.0mg漆黄素与10.0mg多西紫杉醇分别溶于1ml无水乙醇,并将两种溶液混合为有机相备用;称取50.0mg聚乙烯醇溶于20ml超纯水中作为水相备用;在t25探头超声乳匀分散仪乳化条件(9600rpm/min)下将有机相缓慢滴加入水相中,连续工作10min。将乳化好的乳液转移至圆底烧瓶内,使用旋转蒸发仪进行减压抽滤(37℃,60rpm,15min),除去有机溶剂,制得载药纳米乳液,并于4℃条件保存。其水合平均粒径图如图4b所示。
实施例7一种双载多西紫杉醇和山奈酚的纳米粒的制备方法
按照比例称取125.0mg泊洛沙姆f127于50ml超纯水中,室温搅拌2h使之充分溶解,制备成水相待用;量取5ml二氯甲烷溶解500.0mgpeg-pcl(1:4,mw:25k)聚合物材料,25.0mg山奈酚与25.0mg多西紫杉醇共溶于5ml无水乙醇,作为有机相待用;在高压均质机工作条件下(35rpm,20mpa),将有机相倒入50ml水相中,连续均质乳化2min;循环三次得到初乳。将初乳转移至圆底烧瓶内,使用旋转蒸发仪进行减压抽滤(40℃,60rpm,20min),除去有机溶剂,制得载药纳米乳液,并于4℃条件保存。其水合平均粒径图如图4c所示。
以下通过实验例的方式对本发明的技术效果做进一步说明。下述实验例均使用实施例3得到的双载多西紫杉醇和山奈酚的纳米粒。
实验例1一种双载多西紫杉醇和山奈酚的纳米粒的性质测定
1.形态观察
取双载药物的纳米粒溶液少量滴于铜网上,自然干燥后,于tem下观察,为球形粒子,粒径在40-60nm之间,结果见图1。
2.粒径与zeta电位
取双载药物的纳米粒溶液少量,用纯水稀释40倍后置于zetasizernanos90型malvern激光粒度仪下检测其粒径(见图2a),用原乳液测其zeta电位;测得水合平均粒径为106.20±2.29nm,zeta电位为-0.876±0.259。
3.包封率与载药率的测定
3.1紫外分光光度法测量黄酮类化合物的药物含量
分别配制2-12μg/ml系列浓度梯度的漆黄素)乙醇溶液,以乙醇为对照样品,使用紫外分光光度仪进行全波长扫描,在最大吸收波长353±1nm处建立漆黄素(的标准曲线。量取2ml冻干双载药纳米粒溶液于以1ml乙醇溶解后,在高速冷冻离心机(4℃,15000rpm/min,30min)中冷冻离心;用1ml乙醇洗涤离心管底沉淀物,在相同条件下离心,合并各次上清液,稀释20倍,使用紫外分光光度仪测量其最大吸收光度,对应漆黄素的标准曲线,算得漆黄素含量为4.36±0.19%。
3.2高效液相色谱法测量多西紫杉醇的药物含量
精密称量多西紫杉醇标准品称取于10ml容量瓶中,先用少许乙醇溶解并用乙腈定容。配置至浓度为1mg/ml的多西紫杉醇母液。精密量取称取多西紫杉醇母液,分别置于10个10ml的量瓶中,加入甲醇稀释至刻度,配制成(1,5,10,20,40,80,160,320,500,1000μg/ml)系列浓度梯度的多西紫杉醇标准溶液。以纯水为流动相a,乙腈为流动相b,梯度洗脱(见表2-1),平行进样3次,进样量为每次20μl,流速为1ml/min;在254nm波长处采用高效液相法测定峰面积a,建立浓度-峰面积(c-a)标准曲线方程(见图4)。取1ml冻干双载药纳米粒用4ml甲醇萃取,稀释20倍后,测定其峰面积a,通过标准曲线方程计算双载药纳米系统中多西紫杉醇的含量为4.28±0.27%。
4.体外释放实验
在ph为7.45的释放介质中,对0.5h,1h,2h,4h,8h,24h,48h,72h,96h,120h,144h,168h各个时间点的对药物溶出液进行含量检测,计算并制得体外溶出释放曲线(见图5)。在游离多西紫杉醇与双载多西紫杉醇和黄酮类化合物的聚合物纳米粒的释放比较中,可以明显看出游离的药物释放速率高于被纳米载体装载的药物,整个双载药物聚合物纳米粒呈现出更为缓慢释放的效果,药物持续释放时间大于168h。
实验例2体外肿瘤细胞抑制试验
采用mtt染色法测量载药纳米粒对乳腺癌细胞株(4t1,mda-mb-231)的存活率,以评估双载药制剂对肿瘤细胞的抑制作用。
经mtt法检测,细胞存活率-浓度曲线计算其ic50值(见图6)。与游离药物作用相比,多西紫杉醇纳米粒在24小时表现出略高的ic50值,在药物与细胞共孵育48h和72h后,多西紫杉醇纳米粒对两种细胞系的ic50值均与游离紫杉醇接近;而在48小时共培养后,对乳腺癌4t1细胞的半数抑制浓度(ic50),双载多西紫杉醇和漆黄素的纳米粒为6.72±0.46μg/ml;双载多西紫杉醇和木樨草素的纳米粒为5.03±0.22μg/ml;双载多西紫杉醇和山奈酚的纳米粒为8.45±1.03μg/ml。
对乳腺癌mda-mb-231细胞的半数抑制浓度(ic50),双载多西紫杉醇和漆黄素的纳米粒为9.21±0.65μg/ml;双载多西紫杉醇和木樨草素的纳米粒为8.32±1.02μg/ml;双载多西紫杉醇和山奈酚的纳米粒为12.14±1.25μg/ml。
结果显示出双载多西紫杉醇和黄酮类化合物的聚合物纳米粒对于乳腺癌细胞株(4t1)有更明显的抑制作用。
实验例3体内肿瘤生长抑制试验
1、实验方法
选用4t1乳腺癌皮下瘤模型,在接种第6天肿瘤生长至5*5mm2后,将荷瘤小鼠进行以下分组并进行相应的治疗方案(每组5只):生理盐水组,游离多西紫杉醇组,单载多西紫杉醇纳米粒组,双载多西紫杉醇和黄酮的纳米粒组(包括双载紫杉醇-漆黄素纳米粒组,双载紫杉醇-木樨草素纳米粒组,双载紫杉醇-山奈酚纳米粒组)。在第6、7、8天,连续通过尾静脉注射给药三次(每组每次给药剂量按照10mg/kg多西紫杉醇计算)。
2、实验结果
双载药纳米粒对4t1乳腺癌皮下瘤模型的治疗效果:经18天治疗后观察,以荷瘤小鼠肿瘤体积的测量计算出其变化趋势。
如图7a所示,双载多西紫杉醇和黄酮的纳米粒组的肿瘤体积增加明显小于对照组(生理盐水)(p<0.01)。与游离多西紫杉醇给药组相比,双载多西紫杉醇和黄酮的纳米粒组的皮下瘤生长有明显减缓趋势(p<0.01),与单载多西紫杉醇给药组相比,双载多西紫杉醇和黄酮的纳米粒组的皮下瘤生长缓慢(p<0.05)。如图7b所示,在每个组的肿瘤的重量也显示双载多西紫杉醇和黄酮的纳米粒能够有效的抑制皮下4t1乳腺癌的生长(p<0.01)。
在前期研究中发现,单载漆黄素的纳米粒的抑瘤效果非常局限,在给药结束第10天后出现肿瘤复发生长(qianyang,jinfengliao,jianliang,xindeng,chaofenglong,chengshixie,xiaoxinchen,lanzhang,jinxinsun,jinrongpeng,bingyangchu,gangguo,fengluo,zhiyongqian*.anti-tumoractivityandsafetyevaluationoffisetin-loadedmethoxypoly(ethyleneglycol)-poly(ε-caprolactone)nanoparticles.journalofbiomedicalnanotechnology.2014,10(4):580-591.)
实验结果说明,本发明将黄酮(包括漆黄素、木樨草素、山萘酚)与多西紫杉醇联合使用,可以发挥协同增效的作用,抑瘤作用优良,采用纳米粒装载的方式可以有效递送这些药物,让它们在体内发挥作用。
本发明所制得的双载药纳米粒,具有显著的缓释效果,能够在体内保持较高的血药浓度,持续作用于肿瘤细胞,达到治疗效果,且对正常组织器官的损伤非常少,且所载药物黄酮包括漆黄素、木樨草素、山萘酚),与多西紫杉醇用于抗瘤可以发挥协同增效作用,应用前景优良。
- 还没有人留言评论。精彩留言会获得点赞!