一种抗体偶联药物的制备方法与流程
本发明属于生物医学领域,具体涉及一种抗体偶联药物的制备方法。
背景技术:
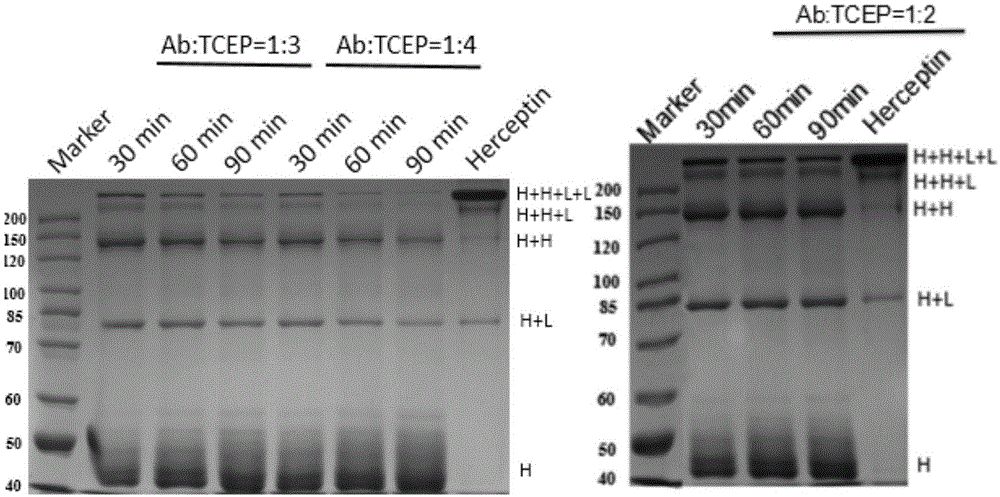
:人erbb2蛋白(简称erbb2,又称her2或p185)是一种糖蛋白,属于i型受体酪氨酸激酶家族中的表皮生长因子受体(erbb/her)家族。erbb2与肿瘤的发生发展密切相关,在多种癌症(如乳腺癌、肺癌、胰腺癌、卵巢癌)中都可以检测到erbb2原癌基因或erbb2的高表达。同时,erbb2还经常被用来作为一些肿瘤(如乳腺癌)重要的预后判定指标,erbb2高表达的肿瘤往往预后效果差。由此可见,erbb2已经成为肿瘤靶向治疗的重要靶点之一。肿瘤的靶向治疗是治疗肿瘤的一个重要手段。一个成功的策略是利用单克隆抗体特异性识别肿瘤细胞表面的抗原决定簇,从而靶向杀死癌细胞。据此,可以利用抗体靶向肿瘤细胞表面的erbb2来特异性的杀死肿瘤细胞。曲妥珠单抗(trastuzumab,商品名为herceptin)和帕妥珠单抗(pertuzumab,商品名perjeta)均为抗erbb2人源化单克隆抗体。“曲妥珠单抗与化疗联用”或“曲妥珠单抗与帕妥珠联用”均能有效治疗erbb2高表达的肿瘤(如乳腺癌)。但是,临床上曲妥珠单抗的治疗方法非常受限,且极易出现原发性或继发性肿瘤耐药性以及肿瘤异质性。因此,需要寻找erbb2高表达的肿瘤的新的治疗方法。将抗肿瘤的单克隆抗体通过化学修饰与小分子毒素偶联,得到抗体偶联药物(adc)。该抗体偶联药物既保留了抗体特异性识别肿瘤抗原的能力,又具有小分子毒素杀伤肿瘤细胞的毒性,因而日益成为抗肿瘤研发领域的热点。目前市售的抗体偶联药物仅有四种,分别为genentech的kadcyla(ado-曲妥珠单抗-emtansine;t-dm1)、seattlegenetics的adcetris(brentuximabvedutin)、辉瑞的mylotarg和besponsa。由于早期偶联技术不成熟的原因,这四种抗体偶联药物均有一定的局限性。以kadcyla(又称t-dm1)为例,t-dm1是曲妥珠单抗与dm1(一种美坦辛衍生物,微管抑制剂)通过一硫醚连接子(mcc)连接而成,主要用于治疗her2阳性的晚期乳腺癌。临床研究结果表明,与曲妥珠单抗(原裸抗)相比,t-dm1使her2阳性的晚期乳腺癌患者的生存期几乎翻倍,尽管二者的临床条件并不一样。但是,t-dm1采用的是赖氨酸偶联的方法,曲妥珠单抗的抗体表面存在大量(超过80个)赖氨酸,加之偶联反应的非选择性,因而偶联数目和位点具有极大的不确定性,导致生成的抗体偶联药物不均一,这给抗体偶联药物的纯化以及之后在体内的药代动力学带来了极大的挑战,在被fda批准时有一个黑框警告,提醒患者与卫生保健专业人员该药物可导致肝毒性、心脏毒性和死亡。这主要是脱落的dm1以及t-dm1进入体内降解释放出dm1引起的。monomethylauristatine(mmae)是一种人工合成的具有高毒性的微管蛋白抑制剂,其与海兔毒素类似都能抑制细胞分裂。mmae与maleimidocaproyl-dipeptide(valine-citrullineorvc)接头连接后,其毒性是阿霉素的10-1000倍。由于mmae毒性较高且无选择性,因此其不能作为药物单独进行癌症治疗。技术实现要素:本发明的目的在于抑制肿瘤细胞增殖。本发明首先保护一种抗体偶联药物的制备方法,可包括如下步骤:(1)将抗人erbb2单克隆抗体和还原剂混合,还原;(2)将完成步骤(1)的体系稀释2-4倍(如2-3倍、3-4倍、2倍、3倍或4倍),搅拌1-3h(如1-2h、2-3h、1h、2h或3h);(3)将完成步骤(2)的体系和vc-mmae混合,偶联。所述步骤(1)中,抗人erbb2单克隆抗体和还原剂的摩尔比可为1:(2-4)(如1:2、1:3、1:4、1:(2-3)或1:(3-4))。还原的时间可为30-60min(如30-40min、40-60min、30min、40min或60min)。所述还原剂可为tcep。所述步骤(1)中,抗人erbb2单克隆抗体和还原剂混合的体系(即还原体系)中,抗人erbb2单克隆抗体的浓度可为4.0-6.0mg/ml(如4.0-5.0mg/ml、5.0-6.0mg/ml、4.0mg/ml、5.0mg/ml或6.0mg/ml)。所述步骤(2)中,所述“将完成步骤(1)的体系稀释2-4倍(如2-3倍、3-4倍、2倍、3倍或4倍)”可为将完成步骤(1)的体系用ph7.2-7.6、0.005-0.015m的pbs缓冲液(如ph7.2-7.4、0.005-0.01m的pbs缓冲液、ph7.4-7.6、0.01-0.015m的pbs缓冲液、ph7.2、0.005m的pbs缓冲液、ph7.4、0.01m的pbs缓冲液或ph7.6、0.015m的pbs缓冲液)稀释2-4倍(如2-3倍、3-4倍、2倍、3倍或4倍)。所述步骤(3)中,vc-mmae和所述完成步骤(2)的体系中已还原的抗人erbb2单克隆抗体的摩尔比可为(5-7):1(如(5-6):1、(6-7):1、5:1、6:1或7:1)。偶联的时间可为1-2h(如1-1.5h、1.5-2h、1h、1.5h或2h)。所述步骤(3)中,完成步骤(2)的体系和vc-mmae混合的体系(即偶联体系)中,已还原的抗人erbb2单克隆抗体的浓度可为2.0-3.0mg/ml(如2.0-2.5mg/ml、2.5-3.0mg/ml、2.0mg/ml、2.5mg/ml或3.0mg/ml)。上述任一所述制备方法还可包括步骤(4):将完成步骤(3)的体系进行脱盐。所述步骤(4)具体可为:将完成步骤(3)的体系上样至琼葡糖凝胶g25ff柱,然后用ph7.2-7.6、0.005-0.015m的pbs缓冲液(如ph7.2-7.4、0.005-0.01m的pbs缓冲液、ph7.4-7.6、0.01-0.015m的pbs缓冲液、ph7.2、0.005m的pbs缓冲液、ph7.4、0.01m的pbs缓冲液或ph7.6、0.015m的pbs缓冲液)洗脱,过柱后溶液即为制备的抗体偶联药物。本发明还保护上述任一所述的制备方法制备的抗体偶联药物。所述抗体偶联药物的dar可为4.00-5.00(如4.00-4.50、4.50-5.00、4.00、4.50或5.00)。在本发明的一个实施例中制备的抗体偶联药物hk02-mmae的dar具体可为4.07。本发明还保护上述任一所述的抗体偶联药物的应用,可为a1)-a5)中的至少一种:a1)抑制肿瘤细胞增殖;a2)抑制肿瘤生长;a3)治疗和/或预防癌症;a4)制备抗肿瘤药物;a5)制备肿瘤细胞增殖抑制剂。上述应用中,所述肿瘤细胞可为jimt-1、skbr3、nci-n87、hcc1954、mda-mb-453和kpl-4中的至少一种。上述应用中,所述肿瘤可为移植瘤。所述移植瘤具体可为jimt-1移植瘤。上述应用中,所述癌症可为乳腺癌和/或胃癌。所述乳腺癌可为herceptin耐药的乳腺癌或herceptin敏感的乳腺癌。实验证明,本发明提供的抗体偶联药物和t-dm1均可抑制skbr3、nci-n87、hcc1954、mda-mb-453和kpl-4的增殖,且抑制效果基本一致;与t-dm1相比,jimt-1用抗体偶联药物处理后,生长抑制率显著提高,即本发明提供的抗体偶联药物抑制jimt-1增殖的效果显著高于t-dm1。本发明具有重要的应用价值。附图说明图1为还原条件优化。图2为偶联反应优化。图3为偶联条件的优化。图4为抗体偶联药物hk02-mmae纯度和偶联情况的检测。图5为抗体偶联药物hk02-mmae抑制肿瘤细胞增殖。图6为jimt-1移植瘤的生长曲线。图7为小鼠体重变化曲线。具体实施方式以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。下述实施例中人erbb2蛋白的genebank登录号为x03363。抗人erbb2单克隆抗体为安徽安科生物工程(集团)股份有限公司的产品。vc-mmae粉末为上海皓元医药股份有限公司的产品。蛋白酶抑制剂complete为roche公司的产品。辣根过氧化物酶标记的羊抗人igg为thermo公司的产品。cck-8显色试剂为东仁化学科技(上海)有限公司的产品。琼葡糖凝胶g25ff柱为博格隆生物技术有限公司的产品。pb缓冲液为hyclone公司的产品。下述实施例中,通过sec-hplc高效液相色谱法测定抗体偶联药物的纯度。具体测定条件为:hplc系统:waterse2695hplc操作系统;检测器:紫外吸光度计(测定波长:280nm);色谱柱:日本东曹株式会社的tosohtskgelg3000sw(7.8×300,p/n0008541);柱温:室温;流动相:含0.15mnacl和3%(v/v)异丙醇的pb缓冲液;流速:0.5ml/min;上样量:20μl(浓度为1mg/ml)。下述实施例中,抗体偶联药物中每一个抗体分子平均药物偶联数可以用紫外分光光度计法进行测定,也可以用疏水高效液相色谱法(hic-hplc)进行测定。hic-hplc测定的具体条件为:hplc系统:waterse2695hplc操作系统;检测器:紫外吸光度计(测定波长:280nm);色谱柱:waters的watersproteinpakhireshic(4.6×100mm);柱温:室温;流动相a:含1.0m(nh4)2so4和5%(v/v)异丙醇的pb缓冲液;流动相b:含5%(v/v)异丙醇的pb缓冲液;流速:0.5ml/min;上样量:20μl(浓度为1mg/ml);洗脱条件:0-15min,流动相中a液的体积百分含量由100%匀速降至0%,b液的体积百分含量由0%匀速升至100%;15-20min,b液;20-35min,流动相中a液的体积百分含量由0%匀速升至100%,b液的体积百分含量由100%匀速降至0%。hic-hplc测定的数据分析:不同的抗体偶联上的小分子化药的数量是不一样的,进而导致其疏水性质不同,进行hic-hplc分析后,抗体偶联药物会根据其偶联上化药的数量,分散成不同的峰,不同的峰对应偶联了不同数量的药物;对所有产生的峰进行积分分析,计算峰面积和峰权重(峰权重=峰面积百分比×药物数量),进而计算每个抗体的平均药物偶联数(dar),dar=∑(weightedpeakarea)/100实施例1、抗体偶联药物hk02-mmae的制备及条件优化一、还原条件优化1、取琼葡糖凝胶g25ff柱,先用5个柱体积的ph7.4、0.01m的pbs缓冲液平衡,再将抗人erbb2单克隆抗体(即裸抗)上样,然后用1个柱体积的含2mmedta的ph7.4、0.01m的pbs缓冲液洗脱,得到纯化抗体溶液。2、完成步骤1后,取纯化抗体溶液,sds-page检测纯化抗体的纯度。结果表明,纯化抗体溶液为电泳纯。3、完成步骤1后,取纯化抗体溶液,采用bca法测定浓度。4、将含10-50mmol/ltcep和1mmedta的水溶液和1ml纯化抗体溶液(浓度为5mg/ml)混合,得到混合液。混合液中,纯化抗体和tcep的摩尔比为1:2、1:3或1:4。5、取混合液,室温搅拌30min、60min或90min。6、将完成步骤5的混合液上样至琼葡糖凝胶g25ff柱,然后用1个柱体积的含2mmedta的ph7.4、0.01m的pbs缓冲液洗脱(目的为脱盐),收集过柱后溶液。过柱后溶液中含有已还原的纯化抗体。7、完成步骤6后,将过柱后溶液和herceptin(即裸抗)进行非还原型sds-page(浓缩胶为8%的聚丙烯酰胺凝胶,分离胶为10%的聚丙烯酰胺凝胶,样品缓冲液不含巯基乙醇,上样量为8μg),根据h-h以及h-l之间二硫键的还原情况,获得最佳还原条件。实验结果见图1(h为重链,l为轻链,marker为蛋白marker,herceptin为裸抗)。结果表明,纯化抗体和tcep的摩尔比为1:2时,仍然有大量的纯化抗体未被还原(未被还原的纯化抗体将会与adc之间产生抗原结合的竞争);纯化抗体和tcep的摩尔比为1:3、还原时间为30min或60min时,纯化抗体和tcep的摩尔比为1:4、还原时间为30min时,纯化抗体基本被还原,适宜偶联反应。选择最佳还原条件进行后续实验。最佳还原条件为纯化抗体和tcep的摩尔比为1:3、还原时间为30min或60min。二、偶联反应优化本发明的发明人经过大量实验发现,还原后的纯化抗体脱盐去除tcep后再进行接下来的偶联反应会使得整个抗体偶联药物的制备过程更为复杂,可以通过稀释反应体系减慢抗体的还原过程,从而将还原后的抗体直接进行接下来的偶联。1、将含10-50mmol/ltcep和1mmedta的水溶液和1ml纯化抗体溶液(浓度为5mg/ml)混合,得到混合液。混合液中,纯化抗体和tcep的摩尔比为1:2、1:3或1:4。2、取混合液,室温搅拌30min、60min或90min。3、将完成步骤2的混合液用ph7.4、0.01m的pbs缓冲液稀释2倍、3倍或4倍,然后室温搅拌2h。4、将完成步骤3的混合液、步骤1得到的混合液、完成步骤2的混合液和herceptin(即裸抗)进行sds-page。sds-page结果见图2(a为纯化抗体和tcep的摩尔比为1:3、室温搅拌30min,b为纯化抗体和tcep的摩尔比为1:3、室温搅拌60min,c为纯化抗体和tcep的摩尔比为1:4、室温搅拌30min,marker为蛋白marker,herceptin为裸抗,control为步骤1得到的混合液,nodilution为完成步骤2的混合液,1/2dilution为完成步骤2的混合液稀释2倍,1/3dilution为完成步骤2的混合液稀释3倍,1/4dilution为完成步骤2的混合液稀释4倍)。结果表明,对完成步骤2的混合液进行稀释可以减慢反应的进行,稀释倍数越高则反应越慢。后续实验选择对完成步骤2的混合液稀释2倍。三、偶联条件的优化和抗体偶联药物hk02-mmae的制备1、将含10-50mmol/ltcep和1mmedta的水溶液和1ml纯化抗体溶液(浓度为5mg/ml)混合,得到混合液。混合液中,纯化抗体和tcep的摩尔比为1:3。2、取混合液,室温搅拌30min或60min(还原时间)。3、将完成步骤2的混合液用ph7.4、0.01m的pbs缓冲液稀释2倍,然后室温搅拌2h。4、取vc-mmae粉末,加入dmso溶解,得到vc-mmae溶液。5、将完成步骤3的混合液和vc-mmae溶液混合(vc-mmae和已还原的纯化抗体的摩尔比为6:1),室温搅拌1h或2h(偶联时间)。6、将完成步骤5的反应体系上样至琼葡糖凝胶g25ff柱,然后用1个柱体积的ph7.4、0.01m的pbs缓冲液洗脱(目的为脱盐),收集过柱后溶液。过柱后溶液即为抗体偶联药物hk02-mmae。将完成步骤3的混合液室温搅拌1h,然后上样至琼葡糖凝胶g25ff柱,然后用1个柱体积的ph7.4、0.01m的pbs缓冲液洗脱(目的为脱盐),收集过柱后溶液。过柱后溶液即为hk02(作为对照)。通过检测抗体偶联药物hk02-mmae和hk02中每一个抗体分子平均药物偶联数,确定最佳的偶联条件。实验结果见表1,部分hic-hplc测定图谱见图3(a为hk02-mmae30-1,b为hk02-mmae30-2,c为hk02-mmae60-1,d为hk02-mmae60-2),hk02-mmae30-1表示还原时间为30min、偶联时间为1h,hk02-mmae30-2表示还原时间为30min、偶联时间为2h,hk02-mmae60-1表示还原时间为60min、偶联时间为1h,hk02-mmae60-2表示还原时间为60min、偶联时间为2h。结果表明,最佳偶联条件为:vc-mmae和已还原的纯化抗体的摩尔比为6:1,已还原的纯化抗体的浓度为2.5mg/ml,将完成步骤2的混合液用ph7.4、0.01m的pbs缓冲液稀释2倍,还原时间为60min,偶联时间为1h。表1裸抗偶联数2偶联数3偶联数4偶联数5偶联数6偶联数8偶联数>8darhk02100.0————————hk02-mmae30-17.3537.17—46.05———9.43—hk02-mmae30-28.0537.25—42.360.219.812.32—3.2hk02-mmae60-11.6618.41—46.950.7720.2311.99—4.5hk02-mmae60-21.7515.92.4352.03———25.84—注:“—”表示积分无法得到完整峰形,故无法计算。采用紫外分光光度计法测定最佳偶联条件下获得的抗体偶联药物hk02-mmae的浓度,然后-80℃保存。实施例2、抗体偶联药物hk02-mmae的放大生产按照如下生产条件进行抗体偶联药物hk02-mmae的放大生产(约200mg):还原条件:纯化抗体的浓度为5mg/ml,纯化抗体和tcep的摩尔比为1:3,室温;偶联条件:vc-mmae和已还原的纯化抗体的摩尔比为6:1,已还原的纯化抗体的浓度为2.5mg/ml,还原时间为60min,偶联时间为1h,将完成还原步骤的混合液用ph7.4、0.01m的pbs缓冲液稀释2倍。检测抗体偶联药物hk02-mmae的纯度和每一个抗体分子平均药物偶联数。检测抗体偶联药物hk02-mmae的纯度的结果见图4中a和表2。结果表明,抗体偶联药物hk02-mmae的纯度为95%以上。表2保留时间(min)面积(微伏*秒)面积(%)高度(微伏)第1个峰13.700701861.541395第2个峰15.824448801498.46120917检测抗体偶联药物hk02-mmae每一个抗体分子平均药物偶联数的结果见图4中b和表3。结果表明,裸抗的出峰时间为7.911min,dar为0,裸抗组分低于10%;之后分别在8.942、10.644、12.084、13.713、16.271、17.678min出峰,依次对应的dar为1、2、3、4、6和8,对应的峰面积分别为4.03、0.70、22.02、1.06、44.06、20.78、7.26,最终计算获得的dar值为4.07。结果表明,裸抗的出峰时间为7.911min,dar为0;之后分别在8.942、10.644、12.084、13.713、16.271、17.678min出峰,依次对应的dar为1、2、3、4、6和8,对应的峰面积分别为4.03、0.70、22.02、1.06、44.06、20.78、7.26,最终计算获得的dar值为4.07。表3保留时间(min)面积(微伏*秒)面积(%)高度(微伏)第1个峰7.9112179784.039955第2个峰8.942574030.701941第3个峰10.644197860822.0278520第4个峰12.0842569461.066035第5个峰13.713382837944.06107697第6个峰16.271191382620.7847983第7个峰17.6786705817.2620871实施例3、elisa检测抗体偶联药物hk02-mmae对抗原(人erbb2蛋白)的亲和力t6-17细胞(记载于如下文献中:王弦,谢小强,曹亮等.t6-17细胞培养上清中肿瘤蛋白p185的表达.细胞与分子免疫学杂志,2008,24(10):1018-1019)为向nih3t3细胞(小鼠胚胎成纤维细胞)转入人erbb2基因的稳转细胞株,其细胞膜表面高表达人erbb2蛋白。细胞裂解液:含150mmnacl、1%(v/v)triton-100和4mm蛋白酶抑制剂complete的ph7.5、50mmtris-hcl缓冲液。洗涤液(ph7.4)(即pbst缓冲液):向蒸馏水中加入kh2po40.2g、na2hpo412h2o2.9g、nacl8g、kcl0.2g和tween-200.05%(体积百分比),定容至1l。待测抗体为抗体偶联药物hk02-mmae或抗人erbb2单克隆抗体。1、用胰酶消化处于对数生长期的t6-17细胞,然后用含10%(v/v)fbs的dmem培养基重悬,1000rpm/min离心5min,收集沉淀。2、完成步骤1后,将细胞裂解液中加入步骤1收集的沉淀中,得到裂解体系;裂解体系中,t6-17细胞的浓度为1×107个/ml。3、完成步骤2后,将所述裂解体系冰上裂解20min,然后12000rpm/min离心15min,收集上清2。4、取elisa板(nunc公司的产品),每孔加入100μl包被液(1体积份上清2和999体积份ph9.6、50mm碳酸盐缓冲液混合而成),然后用封口膜封好,4℃、50rpm包被过夜,然后弃上清,用洗涤液洗涤,拍干。5、完成步骤4后,加入含10g/lbsa的pbst缓冲液,用封口膜封好,37℃、60rpm封闭1h,然后弃上清,用洗涤液洗涤,拍干。6、完成步骤5后,向elisa板每孔加入100μl待测抗体稀释液(浓度为2μg/ml、0.5μg/ml、0.125μg/ml、0.03125μg/ml、0.0078125μg/ml、0.001953125μg/ml、0.000488μg/ml或0.000122μg/ml,用含10g/lbsa的pbst缓冲液稀释),用封口膜封好,室温震荡孵育1h;然后弃上清,用洗涤液洗涤,拍干。每个浓度重复2个孔。7、完成步骤6后,每孔加入100μl辣根过氧化物酶标记的羊抗人igg(工作浓度为1:8000,用含10g/lbsa的pbst缓冲液稀释),室温孵育1h;然后弃上清,用洗涤液洗涤,拍干。8、完成步骤7后,每孔加入opd底物显色3-5min,最后用浓度为1m的h2so4水溶液终止反应,用bio-tekelx-800酶标仪检测od490nm值。以待测抗体稀释液的浓度为横坐标,相应的od490nm值为纵坐标,绘制反应曲线;然后采用4参数logistic拟合方法作图,获得ic50值。实验结果见表4。结果表明,抗人erbb2单克隆抗体和抗体偶联药物hk02-mmae与抗原的亲和力无显著差异。表4抗人erbb2单克隆抗体抗体偶联药物hk02-mmaeic50(μg/ml)0.049220.03651实施例4、抗体偶联药物hk02-mmae抑制肿瘤细胞增殖本实施例涉及的肿瘤细胞株的名称、癌症类型、培养基、培养条件和来源具体见表5。表5待测抗体为抗体偶联药物hk02-mmae或t-dm1(genentech公司的产品)。1、用胰酶消化体外培养的肿瘤细胞株,然后用培养基重悬,得到肿瘤细胞重悬液。2、完成步骤1后,取96孔细胞培养板,每孔接种100μl肿瘤细胞重悬液,置于培养箱培养24h,以使肿瘤细胞充分贴壁。3、完成步骤2后,每孔加入含有不同浓度待测抗体的培养基(共10个浓度,药物稀释浓度即梯度视细胞生长情况而定,每个浓度做3个平行孔),置于培养箱继续培养72h。4、完成步骤3后,弃培养基,每孔加入100μl显色培养基(由1体积份cck-8显色试剂和9体积份培养基混合而成),在37℃、5%co2的条件下显色,然后用bio-tekelx-800酶标仪检测od490nm值。该od490nm值即为给药孔od490nm值。利用graphpad软件,采用四参数回归法对数据进行处理。部分实验结果见图5(herceptin-mmae为抗体偶联药物hk02-mmae)。5、按照步骤1-4的方法,将3中的“含有不同浓度待测抗体的培养基”替换为培养基(不含待测抗体),其它步骤均不变,得到对照孔od490nm值。然后计算肿瘤细胞株生长抑制率。肿瘤细胞株生长抑制率=(对照孔od490nm值-给药孔od490nm值)/对照孔od490nm值×100%。结果表明,skbr3、nci-n87、hcc1954、mda-mb-453和kpl-4分别用抗体偶联药物hk02-mmae和t-dm1处理后,生长抑制率均无显著差异,即抗体偶联药物hk02-mmae和t-dm1均可抑制skbr3、nci-n87、hcc1954、mda-mb-453和kpl-4的增殖,且抑制效果基本一致;与t-dm1相比,jimt-1用抗体偶联药物hk02-mmae处理后,生长抑制率显著提高,即抗体偶联药物hk02-mmae抑制jimt-1增殖的效果显著高于t-dm1。实施例5、抗体偶联药物hk02-mmae治疗jimt-1移植瘤的疗效balb/c小鼠为北京维通利华试验动物有限公司的产品。1、取32只6-8周龄、体重为20-30g的balb/c小鼠,在腋下接种0.1mljimt-1细胞液(接种量为5×106个细胞/只),然后正常饲养。2、完成步骤1后,取肿瘤(即jimt-1移植瘤)体积为200mm3左右的balb/c小鼠24只,随机分成g1、g2和g3三组(每组8只),然后进行如下处理:g1组:腹腔注射生理盐水;注射体积同g2组t-dm1的体积;g2组:腹腔注射t-dm1(genentech公司的产品);注射剂量为10mg/kg;g3组:腹腔注射抗体偶联药物hk02-mmae;注射剂量为10mg/kg。3、完成步骤2后,分别与实验第4天、第11天、第14天、第18天、第21天、第25天和第28天测量肿瘤块的长径(a)和短径(b),然后得到肿瘤体积。肿瘤体积=a×b2/2。以balb/c小鼠腋下接种jimt-1的时间为横坐标,肿瘤体积为纵坐标,绘制jimt-1移植瘤的生长曲线。jimt-1移植瘤的生长曲线见图6。结果表明,抗体偶联药物hk02-mmae可以抑制jimt-1移植瘤的生长,药效显著高于t-dm1。以balb/c小鼠腋下接种jimt-1的时间为横坐标,体重为纵坐标,绘制小鼠体重变化曲线。小鼠体重变化曲线见图7。结果表明,在10mg/kg的给药剂量下,抗体偶联药物hk02-mmae并未表现出明显的毒性。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1