厄他培南钠在制备防治牛传染性鼻气管炎药物中的应用的制作方法
本发明涉及医药领域,具体涉及厄他培南钠在制备防治牛传染性鼻气管炎药物中的应用。
背景技术:
公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
牛传染性鼻气管炎(infectiousbovinerhinotracheitis,ibr)又称坏死性鼻炎、红鼻病,是由牛传染性鼻气管炎病毒(infectiousbovinerhinotracheitisvirusibrv)引起的一种急性、热性、接触性传染病,以高热、呼吸困难、流鼻汁、上呼吸道及气管、黏膜发炎等为特征。20世纪50年代早期,美国科罗拉多州某些牧场首次出现以鼻气管炎为症状的传染性牛病,1955年首次报道了该病的临床症状。我国于20世纪70年代首次在进口种牛中鉴定并分离获得,牛传染性鼻气管炎病毒可导致持续性感染,世界动物卫生组织(oie)将该病列为b类疾病,也是我国进境动物必检疾病之一。
目前牛传染性鼻气管炎病毒有效的疫苗是灭活疫苗和弱毒疫苗,但存在免疫抑制与潜伏感染等问题。灭活苗免疫后个体无法与自然感染个体进行鉴别诊断,因此会给根除ibr带来一定的障碍。传统弱毒苗存在毒力返强现象,存在一定的安全隐患。最重要的是牛传染性鼻气管炎病毒为胞内增殖病毒,灭活疫苗不能清除体内的病毒,只能预防。基于防控的难点和免疫的限制,研发能抑制和杀灭牛传染性鼻气管炎病毒的药物成为众多研究者的热点之一。
技术实现要素:
本发明提供厄他培南钠化合物在抑制和杀灭牛传染性鼻气管炎病毒中的应用,厄他培南钠化合物能够有效地抑制牛传染性鼻气管炎病毒的增殖,对细胞的毒性较小,具有开发成抗牛传染性鼻气管炎药物的前景。
本发明所述化合物厄他培南钠(cas号:153832-38-3,其化学名称为:(1r,5s,6s,8r,2s*,4s*)-2-[2-[3-羧基-苯基氨基-甲酰基]-吡咯烷基-4-硫代]-6-(1-羟乙基)-1-甲基碳青霉烯-3-甲酸单钠盐,结构式如式(i)所示)是一种新型长效1-β-甲基碳青霉烯抗生素,它具有广泛的抗菌谱包括常见的有氧和厌氧细菌和超广谱β-内酰胺酶的生物。本发明提供了厄他培南钠在制备抑制和/或杀灭牛传染性鼻气管炎病毒的药物中的应用,该应用是首次公开,与已知的临床用药用途不同。
本发明建立了牛传染性鼻气管炎病毒在细胞水平上药物筛选体系。确定了厄他培南钠对mdbk细胞的半数毒性浓度(cc50)大于100μm,对牛传染性鼻气管炎病毒的半数有效浓度(ec50)为1.779μm,厄他培南钠对牛传染性鼻气管炎病毒的治疗指数大于56.21。
本发明还提供了根据病毒的致病机制,分别采用不同时间点给药实验以及先加药后加病毒、先加病毒后加药、病毒预先作用的3种不同作用方式进行了体外抗病毒抑制试验。
具体地,本发明具有如下所示的技术方案:
在本发明的第一方面,本发明提供了厄他培南钠或包含厄他培南钠的组合物或其制剂在制备预防和/或治疗牛传染性鼻气管炎药物中的应用。
根据本发明,“预防和/或治疗”的概念表示任一适用于治疗牛传染性鼻气管炎病毒相关疾病的措施,或者对于这种表现的疾病或所表现出来的症状进行预防性治疗,或者避免这种疾病的复发,例如在结束了治疗时间段之后的复发或对已经发作的疾病的症状进行治疗,或预先介入性的防止或抑制或减少该类疾病或症状的发生。
在本发明的第二方面,厄他培南钠或包含厄他培南钠的组合物或其制剂在制备抗牛传染性鼻气管炎病毒的药物中的应用。
在本发明的第三方面,厄他培南钠或包含厄他培南钠的组合物或其制剂在制备抑制和/或杀灭牛传染性鼻气管炎病毒的药物中的应用。
在本发明的第四方面,厄他培南钠或包含厄他培南钠的组合物或其制剂在制备抑制牛传染性鼻气管炎病毒增殖的药物中的应用。
在本发明的第五方面,厄他培南钠或包含厄他培南钠的组合物或其制剂在制备阻断牛传染性鼻气管炎病毒复制的药物中的应用。
在本发明的第六方面,厄他培南钠或包含厄他培南钠的组合物或其制剂在制备抑制牛传染性鼻气管炎病毒增殖的药物中的应用。
在本发明的第七方面,厄他培南钠或包含厄他培南钠的组合物或其制剂在制备阻断牛传染性鼻气管炎病毒吸附的药物中的应用。
在本发明的第八方面,厄他培南钠或包含厄他培南钠的组合物或其制剂在制备抑制牛传染性鼻气管炎病毒吸附的药物中的应用。
在本发明的意义上,本发明所述的药物表示一种物质,其所含有的厄他培南钠对牛传染性鼻气管炎病毒具有明显的抑制和/或杀灭作用,并主要作用于牛传染性鼻气管炎病毒生活周期的多个阶段,可以实现对牛传染性鼻气管炎病毒的直接杀灭、可以阻断或抑制牛传染性鼻气管炎病毒对细胞的吸附、可以阻断或抑制牛传染性鼻气管炎病毒的复制,尤其具有特别优异的阻断或抑制牛传染性鼻气管炎病毒复制的效果。
本发明所述制剂包括厄他培南钠的制剂或包含厄他培南钠的组合物的制剂。
本发明所述包含厄他培南钠的组合物为以厄他培南钠作为组成成分的组合物、以厄他培南钠为活性成分的组合物、以厄他培南钠为主要活性成分的组合物或者以厄他培南钠为唯一活性成分的组合物。
根据本发明,不仅公开了厄他培南钠在制备抗牛传染性鼻气管炎药物中的应用、在制备抗牛传染性鼻气管炎病毒的药物中的应用、在制备抑制和/或杀灭牛传染性鼻气管炎病毒的药物中的应用、在制备抑制牛传染性鼻气管炎病毒增殖的药物中的应用、在制备阻断牛传染性鼻气管炎病毒复制的药物中的应用、在制备抑制牛传染性鼻气管炎病毒增殖的药物中的应用、在制备阻断牛传染性鼻气管炎病毒吸附的药物中的应用,以及在制备抑制牛传染性鼻气管炎病毒吸附的药物中的应用,而且还公开了施用厄他培南钠与其它至少一种药物活性成分的组合时,可以增强这种作用。作为其它药物活性成分的替代或补充,厄他培南钠还可以与其它非药物活性成分组合使用。
本发明的又一具体实施方式中,提供一种抗牛传染性鼻气管炎的药物组合物,所述药物组合物由厄他培南钠与至少一种其它药物活性成分和/或至少一种其它非药物活性成分构成。
本发明化合物或含有它的药物组合物可以单位剂量形式给药。给药剂型可以是厄他培南钠的常规剂型,尤其比如冻干粉针剂等,或者其他适宜于厄他培南钠的剂型,液体剂型例如乳剂剂型、胶体类、真溶液类、微粒剂型、混旋剂型;其他常规剂型例如片剂、胶囊、滴丸、气雾剂、丸剂、粉剂、溶液剂、混悬剂、乳剂、颗粒剂、栓剂、包合物、填埋剂、贴剂、擦剂等。
本发明的药物组合或药物制剂中还可以含有与厄他培南钠相适宜的本领域常用的载体,载体在药物组合物中的含量可以是1wt%-98wt%,通常大约占到80wt%。为方便起见,局部麻醉剂,防腐剂,缓冲剂等可直接溶于载体中。
口服液可以制成悬浮液、溶液、乳浊液、糖浆,也可以制成干品,用前补充适宜的溶剂或其它合适的媒质。这种液体制剂可以包含常规的添加剂,如悬浮剂、乳化剂或非水载体(可能包含可食用油)、防腐剂。如需要可添加调味剂或着色剂。口服片剂和胶囊可以含有与厄他培南钠相容的赋形剂如粘合剂、填充剂、崩解剂或可接受的增润剂。片剂可以用制药学上公知的方法包衣。
根据本发明的上述应用,厄他培南钠对牛传染性鼻气管炎病毒的半数有效浓度(ec50)为1.779μm;厄他培南钠对牛传染性鼻气管炎病毒的治疗指数大于56.21。
根据本发明的实施方式,厄他培南钠在药物浓度安全范围内,随着浓度的升高,抑制或杀灭效果随之提升。本发明所述的药物在浓度安全范围内即指药物在抑制或杀灭牛传染性鼻气管炎病毒时,对牛传染性鼻气管炎病毒的易感细胞没有伤害。
本发明的具体实施方式中,厄他培南钠可以取不低于半数有效浓度(ec50)的药物浓度,比如不低于1.779μm;当然,当厄他培南钠与其他具有抑制和/或杀灭或者协助抑制和/或杀灭牛传染性鼻气管炎病毒等与本发明上述相同应用的药物或活性成分联合使用时,其药物浓度理论上可以低于上述有效浓度,但也不排除特殊的例外情况。
厄他培南钠对牛传染性鼻气管炎病毒的易感细胞毒性较低,比如mdbk细胞的半数毒性浓度(cc50)大于100μm,在将其制备为药物的应用中,在未接触或未被牛传染性鼻气管炎病毒感染的状况下使用该药物可在接触或被牛传染性鼻气管炎病毒感染后起到对牛传染性鼻气管炎病毒的抑制作用。如本发明图3所示,在先给药后感染牛传染性鼻气管炎病毒病毒的情况下(对应图3中的-2h),其具有与其他给药时间相当地对牛传染性鼻气管炎病毒的抑制作用。因此,厄他培南钠能够较好的起到对牛传染性鼻气管炎病毒引起的牛传染性鼻气管炎起到较好的预防和治疗作用。
以及,厄他培南钠对牛传染性鼻气管炎病毒的作用呈现多位点、多环节性,在本发明的药物体外研究中可以发现(如实施例4和5),不同给药时间包括感染病毒前给药、感染病毒后给药以及感染病毒的同时给药三种给药时间,和不同作用方式包括先加药后加病毒、先加病毒后加药、药物和病毒预先作用三种作用方式,通过不同时间给药发现厄他培南钠对牛传染性鼻气管炎病毒均有明显的抑制作用;而通过不同作用方式给药发现厄他培南钠与牛传染性鼻气管炎病毒直接接触(或称为预先作用)可实现对牛传染性鼻气管炎病毒的直接杀伤作用(ec50=1.377μm,图4);将牛传染性鼻气管炎病毒加入到已加好厄他培南钠(即与细胞预先作用后)的细胞中,厄他培南钠对牛传染性鼻气管炎病毒具有吸附阻断作用(ec50=1.953μm,图5),将厄他培南钠加入到已加好毒液(即与细胞预先作用后)的细胞中,厄他培南钠对牛传染性鼻气管炎病毒具有复制阻断作用(ec50=0.7902μm,图6)。
附图说明
以下,结合附图来详细说明本发明的实施方案,其中:
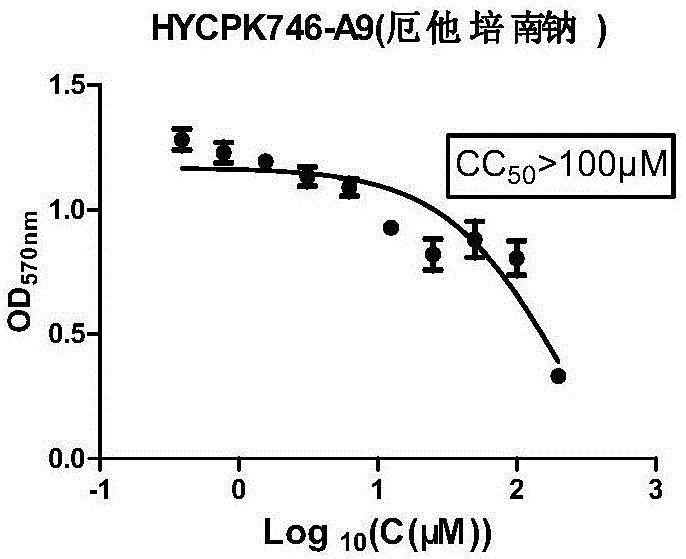
图1显示为实施例2中厄他培南钠对mdbk细胞的半数细胞毒性浓度(cc50);
图2显示为实施例3中厄他培南钠对牛传染性鼻气管炎病毒的半数有效浓度(ec50);
图3显示为实施例4中厄他培南钠不同时间点给药(40μm)对牛传染性鼻气管炎病毒抑制的效果图;
图4显示为实施例5中厄他培南钠对牛传染性鼻气管炎病毒直接杀伤作用效果图;
图5显示为实施例5中厄他培南钠对牛传染性鼻气管炎病毒吸附阻断作用效果图;
图6显示为实施例5中厄他培南钠对牛传染性鼻气管炎病毒复制阻断作用效果图。
具体实施方式
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明方法中。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径获得。以下实施例中所称药物如无其他说明均指厄他培南钠。文中所述的较佳实施方法与材料仅作示范之用。
实施例1病毒tcid50的测定
将mdbk细胞(山东省农业科学院奶牛研究中心保存)消化后以每孔1×105个/ml的细胞密度接种到96孔细胞培养板中,放入37℃,5%co2的细胞培养箱中培养成单层细胞后,弃去孔内细胞生长液,将牛传染性鼻气管炎病毒(山东省农业科学院奶牛研究中心保存)连续10倍稀释的病毒稀释液(稀释度分别为10-1~10-10)接种于长满单层细胞的96孔板,每孔100μl,放入37℃、5%co2的培养箱中继续培养,并逐日观察细胞的细胞病变效应(cpe)情况,以及详细记录细胞病变孔数。同时设置正常细胞对照组和空白对照组,每组设8个重复,待不再继续发生细胞病变时判定结果。细胞病变孔是以上的细胞发生病变对应的细胞孔,并按karber法计算病毒tcid50。
表1、ibrv-f9的tcid50
注:tcid50,tissuecultureinfectivedose,半数组织培养感染剂量,又称50%组织细胞感染量;即指能在培养板孔或试管内引起半数细胞病变或死亡(cytopathiceffect,cpe)所需的病毒量。
结果:在显微镜下的形态学观察发现48h时不同浓度的病毒稀释液均造成了细胞病变,细胞的折光性发生改变,单层结构被破坏,细胞出现圆缩坏死,逐渐呈拉网状并形成空泡,有的细胞裂解脱落成碎片状,5天后各孔的细胞病变不再继续,统计出不同浓度的cpe孔数,并计算出不同浓度的cpe比率,并按karber法计算牛传染性鼻气管炎病毒的tcid50值:
lgtcid50=l-d(s-0.5)
(l:最高稀释度的对数;d:稀释度对数之间的差;s阳性孔比率总和)
lgtcid50=l-d(s-0.5)=-1-1×(5.5-0.5)=-6
tcid50=10-6/0.1ml
即将该病毒稀释106接种100μl可使50%的细胞发生病变。
实施例2厄他培南钠对mdbk细胞的毒性实验:
mdbk细胞是牛传染性鼻气管炎病毒的易感细胞。因此,首先检测厄他培南钠对mdbk细胞的细胞毒性,具体实验步骤如下:
(1)在96孔板内接种100μl细胞(mdbk5000个/孔)。
(2)培养约12h后,进行下一步加药分析。弃去培养基,每孔加100μl含不同药物浓度(以50μm为起始浓度,按两倍梯度依次稀释得到25μm,12.5μm,6.25μm,3.125μm等9个浓度)的2%fbsdmem,每个浓度做3个平行。同时对照孔:加100μl含0.9%dmso的2%fbsdmem培养基。调零孔:不铺细胞。
(3)在37℃,5%co2条件下培养48h后,弃去孔内的培养基。用100μlpbs洗涤两遍,排除药物对mtt反应的影响。每孔再补加100μldmem培养基+10μlmtt。
(4)37℃,5%co2条件下继续培养4h后,每孔加入100μlformazan溶解液。37℃,5%co2继续孵育,直至formazan紫色结晶完全溶解。
(5)在570nm测定吸光值。将0.9%dmso处理的细胞的a570nm设为100%细胞对照。
(6)分析数据,利用graphpadprism5计算厄他培南钠的半数细胞毒性浓度(cc50)值。其结果如图1所示。
结果:厄他培南钠出现剂量依赖关系,即随着药物浓度的增加,则表现出细胞病变较为明显。经统计学分析,确定厄他培南钠半数中毒浓度为大于100μm。
实施例3厄他培南钠对牛传染性鼻气管炎病毒的抑制实验:
(1)在96孔板的每个孔中接种1×104个mdbk细胞,37℃,5%co2培养箱中过夜培养;
(2)弃去培养基,每孔加入100μl100tcid50的牛传染性鼻气管炎病毒病毒稀释液(用2%fbsdmem细胞长满后加入病毒稀释液,按照50μm初始浓度,两倍浓度梯度稀释加药,5%co2培养箱中培养;
(3)48h后,按cck-8试剂盒说明书操作,用酶标仪测定450nm处的od值。
(4)分析数据,病毒抑制率(%)=(药物处理组d450nm值-病毒对照组d450nm值)/(正常细胞对照组d450nm值-病毒对照组d450nm值)×100%,用graphpadprism5软件得化合物的半数有效浓度(ec50)值。其结果如图2所示。然后按公式ti=cc50/ec50,计算相应的治疗指数ti值。
结果:通过cck-8试剂盒检测细胞活力,可以计算出药物对牛传染性鼻气管炎病毒的有效抑制率。从结果可以看出,厄他培南钠在安全浓度范围内,其有效抑制率随着药物浓度的增加而增大,呈一定的量效关系。通过分析软件,对牛传染性鼻气管炎病毒的半数有效浓度(ec50)为1.779μm。厄他培南钠对牛传染性鼻气管炎病毒的治疗指数大于56.21。
实施例4作用机制的初步研究
通过不同的给药时间,即对应的时刻是先给药后感染病毒(0h之前)、先感染病毒后给药(0h之后)、病毒和药物同时加入细胞(0h)三个时间点,将待测化合物加入到接种了牛传染性鼻气管炎病毒的mdbk细胞中,进而初步判断厄他培南钠的作用时期。具体实验步骤如下:
(1)在96孔板的每个孔中接种1×104个mdbk细胞,37℃,5%co2培养箱中培养。
(2)根据已测得的相关药物的药效学评价结果,确定实验所需药物的浓度,并用维持培养基把药物稀释至所需浓度。
(3)细胞过夜培养后,将96孔板中第二列三个复孔的细胞上清吸走,用磷酸缓冲液清洗细胞2遍。然后加入50μl的待测药物,记为-2h。
(4)2h后,将其他孔的细胞上清全部吸走,将稀释好的牛传染性鼻气管炎病毒稀释液加到第2-11列的每孔中,每孔加样体积为50μl。同时在第3列的三个复孔中加入50μl相应待测物,此刻记为0h。
(5)以后每隔一定时间在下一列的三个复孔中加入相应待测化合物,标记好相应时间。以第11列的mdbk细胞作为病毒对照组。
(6)培养48h后,进行od值测定。分析数据,得出结论,给药浓度为40μm时的结果如图3所示。
结果:从不同时间点给药实验结果分析可知,厄他培南钠在病毒感染细胞-2h~8h时加药,对病毒有明显的抑制作用,说明厄他培南钠对牛传染性鼻气管炎病毒呈现出多位点、多环节的作用。
实施例5化合物不同时间加入对牛传染性鼻气管炎病毒复制的影响
我们对厄他培南钠进行了进一步的作用机制研究。分别采用先加药后加病毒、先加病毒后加药、药物和病毒预先作用的3种不同作用方式进行了体外抗病毒抑制试验。
(1)药物对病毒的直接杀伤作用
将等量的100tcid50病毒液与不同浓度的药物稀释液(以50μm为起始浓度,按两倍梯度依次稀释得到25μm,12.5μm,6.25μm,3.125μm等9个浓度)混合均匀置于37℃、5%co2培养箱中预先作用4h后,加入长成单层的96孔细胞培养板中,每个药液梯度100μl/孔,培养箱中作用2h,弃去上清液,加细胞维持液继续培养。本试验同时设置正常细胞对照组、病毒对照组和空白对照组,每个浓度设3个重复,48h进行细胞活力检测,用graphpadprism5软件得化合物的ec50。
结果:厄他培南钠与牛传染性鼻气管炎病毒预先作用的给药方式下,各浓度的试验加药组细胞病变较病毒对照组轻微,细胞的变圆、脱落、空泡化等病理现象有所减轻,通过分析软件,厄他培南钠对牛传染性鼻气管炎病毒的作用效果如图4所示。从图中可以看出,在这种作用式下,厄他培南钠对牛传染性鼻气管炎病毒表现出一定的抑制作用,并且药物在安全浓度范围内,其有效抑制率随着药物浓度的增加而增大,呈一定的量效关系。表明厄他培南钠对牛传染性鼻气管炎病毒具有一定的直接灭活的作用,图4示出了-4小时(即药物与病毒先作用4h再加入细胞中)时厄他培南钠对牛传染性鼻气管炎病毒的ec50值为1.377μm。
(2)药物对牛传染性鼻气管炎病毒吸附的阻断作用
按每孔个的细胞密度将消化好的细胞接种到孔板中,待长成单层细胞后弃去上清液,将不同浓度的药物稀释液每个药液梯度100μl/孔,加入长成单层的96孔细胞培养板中,培养箱中预先作用4h后,弃去上清液,用pbs洗两遍,加入等量的100tcid50病毒液置于37℃、5%co2培养箱中培养。本试验同时设置正常细胞对照组、病毒对照组和空白对照组,每个浓度设3个重复,48h后进行细胞活力检测,并计算该作用方式下不同浓度药物的抗病毒有效率。
结果:采用先加药后加病毒的给药方式下,各浓度的试验加药组细胞病变较病毒对照组轻微,细胞的变圆、脱落、空泡化等病理现象有所减轻,通过分析软件,厄他培南钠对牛传染性鼻气管炎病毒的作用效果如图5所示。从图中可以看出,在这种作用式下,厄他培南钠对牛传染性鼻气管炎病毒表现出一定的抑制作用,并且药物在安全浓度范围内,其有效抑制率随着药物浓度的增加而增大,呈一定的量效关系。表明厄他培南钠对牛传染性鼻气管炎病毒具有一定的吸附阻断作用,图5示出了0小时(即药物先与细胞作用4h后再加入病毒)时厄他培南钠对牛传染性鼻气管炎病毒的ec50值为1.953μm。
(3)药物对牛传染性鼻气管炎病毒复制的阻断作用
按每孔个的细胞密度将消化好的细胞接种到孔板中,待长成单层细胞后弃去上清液,将等量的100tcid50病毒液加入长成单层的96孔细胞培养板中,置于37℃、5%co2培养箱中预先作用2h后,然后弃去上清液,pbs将细胞洗2遍,然后加入不同浓度的药物稀释液,每个药液梯度100μl/孔,本试验同时设置正常细胞对照组、病毒对照组和空白对照组,每个浓度设3个重复,置于37℃、5%co2培养箱中培养,48h后进行细胞活力检测,分析数据,得出结论。
结果:采用先加病毒后加药的给药方式下,各浓度的试验加药组细胞病变较病毒对照组轻微,细胞的变圆、脱落、空泡化等病理现象有所减轻,通过分析软件,厄他培南钠对牛传染性鼻气管炎病毒的作用效果如图6所示。从图中可以看出,在这种作用式下,厄他培南钠对牛传染性鼻气管炎病毒表现出一定的抑制作用,并且药物在安全浓度范围内,其有效抑制率随着药物浓度的增加而增大,呈一定的量效关系。表明厄他培南钠对牛传染性鼻气管炎病毒具有一定的复制阻断作用,图6示出了2小时(即药物先与细胞作用2h后再加入病毒)时厄他培南钠对牛传染性鼻气管炎病毒的ec50值为0.7902μm。
本发明应用实施例以牛肾细胞(mdbk)为载体,在细胞致病模型上,采用先加药后加病毒、先加病毒后加药、病毒预先作用再加药物的3种不同作用方式进行了体外抗病毒抑制研究。发现厄他培南钠的新型抗病毒作用,对牛传染性鼻气管炎病毒有一定的抑制作用,且呈现出多位点、多环节的作用。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!