一种三维打印结合生物三维打印技术制备肌腱方法与流程
本发明属于生物三维打印技术领域,具体涉及一种三维打印结合生物三维打印技术制备肌腱方法。
背景技术:
肌腱损伤是最常见的运动损伤之一,也是临床软组织损伤中的常见类型,目前的治疗方法存在着一定的局限性或不足,支架与种子细胞共同对受损组织的再生进行引导和对再生组织的结构进行控制,是决定人工肌腱是否能用于临床治疗的关键;
目前,制备肌腱支架主要包括以纤维束支架,编织类支架,针织类支架,静电纺丝纳米纤维支架等几类,然而上述方法制备的肌腱支架,在修复中种子细胞的黏附、定植效率低下,难以达到对损伤组织进行快速修复的效果,而且,所获肌腱支架在体内易与周围组织黏连,影响肌腱康复后的正常功能的恢复。
技术实现要素:
为解决上述背景技术中提出的问题。本发明提供了一种三维打印结合生物三维打印技术制备肌腱方法,具有有利于肌腱修复和正常功能丰富的特点。
为实现上述目的,本发明提供如下技术方案:一种三维打印结合生物三维打印技术制备肌腱方法,其制备方法为:
s1、种子细胞的培养;
s2、肌腱支架的制备;
s3、细胞涂层的制备。
优选的,所述s1步骤中种子细胞的培养,肌腱干细胞以含10%胎牛血清的dmem培养基培养于孵箱中,骨髓干细胞和脂肪干细胞以含10%胎牛血清、结缔组织生长因子ctgf25ng/ml、抗坏血酸25um的α-mem培养基培养于孵箱中。
优选的,所述s1步骤中所用的孵箱内含有5%co2,其孵箱内的温度为37℃。
优选的,所述s2步骤中肌腱支架的制备步骤包括s21、模型的建立:使用三维打印软件建立打印模型,为单层或多层长方形状,并保存,等待下一步骤;
s22、材料的制备:量取适量的生物高分子材料,等待下一步骤;
s23、设备的准备:调校熔融静电纺丝三维打印设备的打印参数,将步骤s22的生物高分子材料置入熔融静电纺丝三维打印设备的料筒内部,启动设备进行熔融静电纺丝三维打印获得肌腱支架,等待下一步骤;
优选的,所述s23步骤中打印设备的打印参数为,打印头直径为150-400μm,打印温度为120-200℃,打印过程中料筒气压为600-1000kpa,熔融纺丝负高压模块电压为-2-10kv,打印结构由打印路径控制,打印路径为0/90°、0/60°和0/60/120°。
优选的,所述s3步骤中细胞涂层的制备步骤包括s31、模型的建立:使用三维打印软件建立打印模型,为单层或多层长方形状,并保存。
s32、材料的准备:量取适量的无菌天然材料与种子细胞混合,得到含细胞凝胶,然后取部分含细胞凝胶与适量的润滑相关物质混合。
s33、细胞涂层的打印:将三维打印设备消毒,设定打印参数;
s34、将步骤s32中的含细胞凝胶加入至三维打印设备的料筒内部,以纳米纤维膜接收,启动打印程序,使纳米纤维膜获得细胞涂层,将s32中的含润滑物质的细胞凝胶加入至三维打印设备的料筒,同样打印参数进行打印,打印于细胞涂层旁相邻区域,使用适当方法对凝胶进行交联。
优选的,所述s33步骤中的打印参数为,三维打印设备的打印头直径为150-400μm,打印温度为18-37℃,打印过程中料筒气压为600-1000kpa,打印结构由打印路径控制,打印路径为0/90°、0/60°和0/60/120°。
优选的,其制备方法还包括s4、纳米纤维膜-细胞涂层的处理。
优选的,所述s3步骤中纳米纤维膜-细胞涂层的处理步骤包括将s34步骤中获得的具细胞涂层纳米纤维膜进行卷曲,并使得具有润滑相关物质的细胞涂层位于外层,获得人工肌腱,呈卷曲结构圆柱状,长度为2-10cm,直径为2-10mm。
与现有技术相比,本发明的有益效果是:
本发明,该三维打印结合生物三维打印技术,易于控制纤维直径,得到肌腱支架,并通过生物三维打印技术在其表面打印得到润滑细胞涂层,使其本身便含有大量定植的种子细胞,利于细胞增殖、分化和分泌基质,且具有良好润滑性能,该制作方法简单方便,更好地仿生天然肌腱组织形态、细胞成分及润滑性能,利于肌腱修复及正常功能恢复。
附图说明:
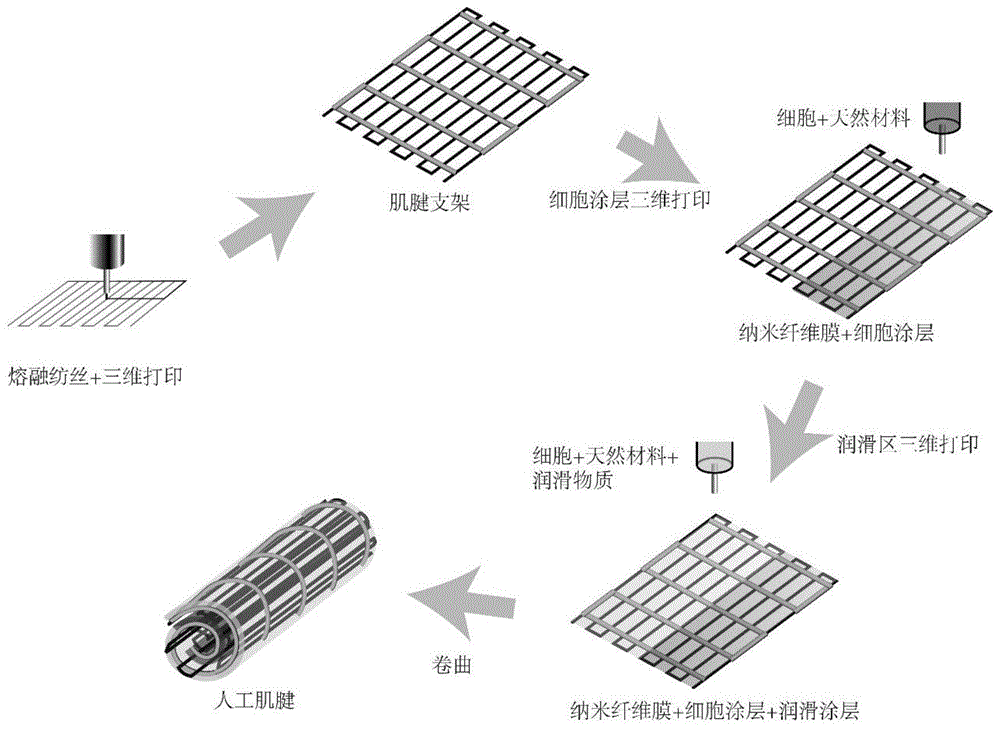
图1为本发明人工肌腱的流程示意图;
图2为本发明对照实验的数据示意图;
图3为本发明qrt-pcr检测的结果示意图;
图4为本发明应力应变曲线示意图;
图5为本发明摩擦系数对照实验图。
具体实施方式
下面将结合附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明提供以下技术方案:一种三维打印结合生物三维打印技术制备肌腱方法,其制备方法为:
s1、种子细胞的培养;
s2、肌腱支架的制备;
s3、细胞涂层的制备。
具体的,所述s1步骤中种子细胞的培养,肌腱干细胞以含10%胎牛血清的dmem培养基培养于孵箱中,骨髓干细胞和脂肪干细胞以含10%胎牛血清、结缔组织生长因子ctgf25ng/ml、抗坏血酸25um的α-mem培养基培养于孵箱中。
具体的,所述s1步骤中所用的孵箱内含有5%co2,其孵箱内的温度为37℃。
具体的,所述s2步骤中肌腱支架的制备步骤包括s21、模型的建立:使用三维打印软件建立打印模型,为单层或多层长方形状,并保存,等待下一步骤;
s22、材料的制备:量取适量的生物高分子材料,等待下一步骤;
s23、设备的准备:调校熔融静电纺丝三维打印设备的打印参数,将步骤s22的生物高分子材料置入熔融静电纺丝三维打印设备的料筒内部,启动设备进行熔融静电纺丝三维打印获得肌腱支架,等待下一步骤;
具体的,所述s23步骤中打印设备的打印参数为,打印头直径为150-400μm,打印温度为120-200℃,打印过程中料筒气压为600-1000kpa,熔融纺丝负高压模块电压为-2-10kv,打印结构由打印路径控制,打印路径为0/90°、0/60°和0/60/120°。
具体的,所述s3步骤中细胞涂层的制备步骤包括s31、模型的建立:使用三维打印软件建立打印模型,为单层或多层长方形状,并保存。
s32、材料的准备:量取适量的无菌天然材料与种子细胞混合,得到含细胞凝胶,然后取部分含细胞凝胶与适量的润滑相关物质混合。
s33、细胞涂层的打印:将三维打印设备消毒,设定打印参数;
s34、将步骤s32中的含细胞凝胶加入至三维打印设备的料筒内部,以纳米纤维膜接收,启动打印程序,使纳米纤维膜获得细胞涂层,将s32中的含润滑物质的细胞凝胶加入至三维打印设备的料筒,同样打印参数进行打印,打印于细胞涂层旁相邻区域,使用适当方法对凝胶进行交联。
具体的,所述s33步骤中的打印参数为,三维打印设备的打印头直径为150-400μm,打印温度为18-37℃,打印过程中料筒气压为600-1000kpa,打印结构由打印路径控制,打印路径为0/90°、0/60°和0/60/120°。
具体的,其制备方法还包括s4、纳米纤维膜-细胞涂层的处理。
具体的,所述s3步骤中纳米纤维膜-细胞涂层的处理步骤包括将s34步骤中获得的具细胞涂层纳米纤维膜进行卷曲,并使得具有润滑相关物质的细胞涂层位于外层,获得人工肌腱,呈卷曲结构圆柱状,长度为2-10cm,直径为2-10mm。
实施例1
(1)将高分子材料聚己内酯置入熔融静电纺丝三维打印设备的料筒内部,调校熔融静电纺丝三维打印设备的工艺参数:打印头直径为200μm,打印温度为180℃,打印过程中料筒气压为600-1000kpa,熔融纺丝负高压模块电压为-3kv,打印结构由打印路径控制,打印路径为0/90°,启动设备进行熔融静电纺丝三维打印获得肌腱支架。
(2)将肌腱干细胞与10g海藻酸钠凝胶混合,加入到三维打印机的料筒内,打印温度设置为37℃,打印头直径均为200μm,层高为200μm,料筒气压为800kpa。打印路径设置为0/90°,对所得的纳米纤维膜表面进行打印,启动打印程序,打印单层长方形支架,长度为3cm,宽度为1cm。
(3)将肌腱干细胞、细胞因子bmp7与10g海藻酸钠凝胶混合,加入到三维打印机的料筒内,打印温度设置为18-37℃,打印头直径均为200μm,层高为200μm,料筒气压为800kpa,打印路径设置为0/90°,在所得的纳米纤维膜表面,与打印区域相邻区域进行打印,启动打印程序,打印单层长方形支架,长度为2cm,宽度为1cm,最终得到具有润滑性能细胞涂层的纳米纤维膜。
(4)将纳米纤维膜沿着宽边进行卷曲,得到圆柱形人工肌腱,其长度为5cm,直径为8mm,具体流程如图1。
实施例2
将所得人工肌腱,放入培养箱中培养,以普通静电纺丝得到的纳米纤维膜,表面种植肌腱干细胞为对照组作对比,分别培养1、3、5、7和9天后,利用mtt法检测肌腱支架中的肌腱细胞活力,结果图如2所示,显示熔融静电纺丝三维打印结合生物三维打印技术得到的肌腱支架上的肌腱细胞具有良好的增殖行为,细胞活力较好,且较对照组增殖行为更加显著。
实施例3
将得到的肌腱支架进行qrt-pcr检测,将所得具有润滑性能细胞涂层的人工肌腱,放入培养箱中培养,以所得的肌腱支架以及单层的普通静电纺丝膜表面种植肌腱干细胞作对比,分别培养7天后,进行qrt-pcr检测,结果图如3所示,显示两组具有细胞涂层肌腱支架上的肌腱细胞肌腱相关产物(coli、coliii、scx、tnmd)表达明显较多,同时具有润滑性能细胞涂层的肌腱支架黏附相关产物(vinculin)表达明显较少。
实施例4
将上述实施例1中得到的肌腱支架放置于万能测试机上进行力学拉伸测试,应力应变曲线如图4所示,结果显示该支架最大的断裂应力为177.433mpa,力学性能较好。
实施例5
将到的人工肌腱支架放置于摩擦系数测试机上进行摩擦学测试,以不含润滑物质的人工肌腱作为对照,结果如图5所示,结果显示该人工肌腱摩擦系数明显小于对照组。
最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!