硅钨酸盐及其制备方法和应用与流程
本发明涉及属于医药化学技术领域,具休涉及一种硅钨酸盐及其制备方法和抗真菌的应用。
背景技术:
病原菌感染严重威胁人类健康。随着艾滋病、糖尿病及恶性肿瘤患者等免疫受损人群的不断增多,广谱抗生素、皮质类固醇、化疗药物的大量应用,器官、骨髓移植,侵入性技术的开展,真菌感染的发病率显著增加。免疫受损人群深部真菌感染的发生率约为11%-40%,病死率超过40%。念珠菌属引起的感染占院内真菌血行感染的四分之三,已成为美国院内导管相关性血流感染的第四大病因。系统性真菌感染患者的一年总生存率很低,一般小于20%。目前,临床上常用的治疗真菌感染的药物主要有咪唑类、多烯类、制霉素等,但一些新发现的真菌均对这些药物固有耐药。如克柔念珠菌、部分光滑念珠菌及土曲霉等真菌均对氟康唑天然耐药,而葡萄牙念珠菌、尖端赛多孢霉等真菌对两性霉素b固有耐药。总体来说,抗真菌药的现状是种类少、毒副作用大、价格高、耐药增多,开发具有新作用靶点或机制的抗菌剂和改造原有抗菌剂是解决耐药菌耐药性的主要方法。总体来说,抗真菌药的现状是种类少、毒副作用大、价格高、耐药增多,因此高效、低毒、廉价的抗真菌药亟待开发。
多金属氧酸盐(poms)的药物活性研究始于上世纪七十年代初,迄今报道具有各种药物活性的poms200余种,主要集中在抗病毒和抗肿瘤两方面。抗菌活性研究得较少,抗真菌研究更少,仅有日本的yamase小组进行了多酸抗细菌(肺炎链球菌和金黄色葡萄球菌)研究,国内开展了为数不多的农业食品方面的抗真菌研究,目前国内外尚无多酸抗人类病原真菌的研究。
技术实现要素:
本发明的目的是为解决抗真菌药种类少、毒副作用大、价格高、耐药增多的问题,而提供硅钨酸盐及其制备方法和应用。
硅钨酸盐,它的化学式为:k13[ce(siw11o39)2]·17h2o或k13[eu(siw11o39)2]·25h2o。
硅钨酸盐的制备方法,它包括:15克h4siw12o40·25h2o晶体溶于150ml蒸馏水中,于65℃水浴中边搅拌边加入过量的同温稀土硝酸铈或稀土硝酸铕,并逐滴加入醋酸钾-冰醋酸缓冲液,调至ph值为4-5,过滤,滤液置于0-3℃,待转变成八面体晶体后,重结晶三次得到纯净的晶体k13[ce(siw11o39)2]·17h2o或k13[eu(siw11o39)2]·25h2o,置于干燥器保存。
硅钨酸盐k13[ce(siw11o39)2]·17h2o或k13[eu(siw11o39)2]·25h2o在制备抗真菌药物的应用;
所述的真菌为白色念珠菌c.albicans、光滑念珠菌c.glabrata、热带念珠菌c.tropicalis、克柔念珠菌c.krusei、近平滑念珠菌c.parapsilosis或新型隐球菌cryptococcusneoformans。
硅钨酸盐k13[ce(siw11o39)2]·17h2o提高氟康唑抗白色念珠菌c.albicans活性的用途。
本发明提供了硅钨酸盐,它的化学式为:k13[ce(siw11o39)2]·17h2o或k13[eu(siw11o39)2]·25h2o,它是15克h4siw12o40·25h2o晶体溶于150ml蒸馏水中,于65℃水浴中边搅拌边加入过量的同温稀土硝酸盐,并逐滴加入醋酸钾-冰醋酸缓冲液,调至ph值为4-5,过滤,滤液置于0-3℃,待转变成八面体晶体后,重结晶三次得到纯净的晶体;获得10余种硅钨酸盐;其中k13[ce(siw11o39)2]·17h2o和k13[eu(siw11o39)2]·17h2o,具有较好的抗真菌活性和较低的毒性,硅钨酸盐k13[ce(siw11o39)2]·17h2o和氟康唑具有协同作用,可以提高氟康唑抗白色念珠菌c.albicans活性。
附图说明
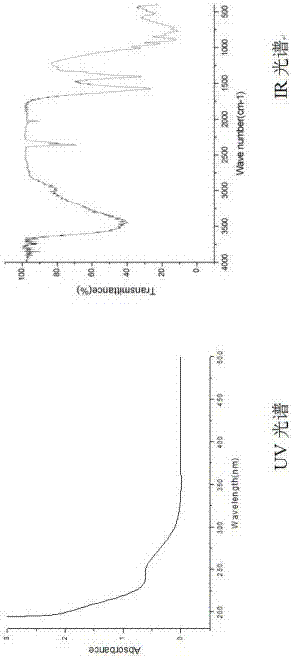
图1是合成化合物的紫外光谱(uv);
图2是合成化合物的红外光谱(ir);
图3是透射电镜下的c.albicans27(×3k)a.对照组b.siw-5mic浓度用药组;
图4是峰面积为纵坐标,麦角固醇标准品浓度为横坐标,标准曲线;
图5系统性念珠菌感染小鼠的生存率;
图6系统性念珠菌感染小鼠的pas染色病理(×200)a.感染组,b.10mg/kgflc,c.100mg/kgsiw-5,d.50mg/kgsiw-5,e.25mg/kgsiw-5。
具体实施方式
本发明的目的是硅钨酸盐表现出较好的抗真菌活性,是通过如下实施例完成。
实施例1:硅钨酸盐的制备
硅钨酸盐k13[ce(siw11o39)2]·17h2o的合成(siw-5):
1)、首先将15克h4siw12o40·25h2o晶体溶于150ml蒸馏水中,于65℃水浴中边搅拌边加入稍多于理论计算量的同温稀土硝酸铈,并逐滴加入醋酸钾-冰醋酸缓冲液,调ph值为4-5,趁热过滤,滤液置于0-3℃,待转变成八面体晶体后,重结晶三次得到纯净的晶体产品siw-5,置于干燥器保存。
2)k13[eu(siw11o39)2]·25h2o(siw-10)的合成:
首先将15克h4siw12o40·25h2o晶体溶于150ml蒸馏水中,于65℃水浴中边搅拌边加入稍多于理论计算量的同温稀土硝酸铕,并逐滴加入醋酸钾-冰醋酸缓冲液调ph值为4-5,趁热过滤,滤液置于0-3℃,待转变成八面体晶体后,重结晶三次得到纯净的晶体产品siw-10,置于干燥器保存。
3)硅钨酸盐检测
用紫外光谱(uv)和红外光谱(ir)如图1和图2。可以看出siw-5和siw-10在200~300nm及700~1100cm-1范围内出现了多酸化合物的特征峰,说明所合成的化合物保持了母体多酸化合物的结构。
实施例2:培养基配制
1)、pda培养基:将39gpda粉末加入1000ml纯化水,115℃、30min加热溶解,通过高压灭菌,待培养基温度降到50℃左右时,倒入灭菌的培养皿中制成平板,将菌株的分离、保存。
2)、pdb培养基:24gpdb粉末加入1000ml纯化水,115℃、30min加热溶解,通过高压灭菌,待培养分装于15ml离心管中保存备用,将菌株的增菌、活化。
3)、rpmi-1640液体培养基:10.4grpmi-1640粉末和34.53gmops,加入900ml无菌蒸馏水,轻轻搅拌至溶解,用1mnaoh在25℃下,调节ph值至7.0,定容至1000ml,用0.22μm微孔滤膜过滤除菌,无菌瓶分装,-20℃保存备用。
实施例3菌株复活
向冻干菌株管中加入0.2mlpdb液基,充分悬浮,制成菌悬液,取0.1ml液体分别于pda平板及斜面培养基上35°c、湿度60%进行菌株的活化。
实施例4硅钨酸盐的抗真菌活性菌悬液制备
1、活性菌悬液:用含有0.5%tween-80的;0.9%无菌生理盐水制备受试菌悬液,用血细胞计数板将其浓度调至菌悬液浓度为1~3×106cfu/ml(0.5麦氏单位),作为原液-20℃保存备用;药敏试验时,用rpmi1640将液基稀释1000倍,至菌悬液浓度为1~3×103cfu/ml。
2、药物贮存液的配制:用无菌去离子水将硅钨酸盐粉末配成终浓度为20480μg/ml,用无菌去离子水将flc粉末配成终浓度为2560μg/ml;分装1.5ml无菌离心管,置-20℃储藏备用。
3、体外药敏试验
按照美国国家临床试验室标准化委员会(clsi)颁布的微量稀释法进行药物敏感性实验。
微量药敏板的制备:
1)用rpmi1640液作稀释液将待测硅钨酸盐贮存液作10级倍比稀释,将硅钨酸盐的起始浓度定为1024μg/ml,终止浓度定为2μg/ml;以上各药浓度均为2倍应试药物浓度,对应加在无菌的96孔微量培养板中,从第1孔至第10孔浓度由高到低,每孔100μl;第11孔加不含药物rpmi1640液100μl,第12孔加200μl。
2)用微量移液器从第1孔至第11孔,每孔分别加入100μl菌悬液,第12孔不加;第1孔至第10孔药物终浓度为512μg/ml至1/ml,第11孔作为生长对照孔,第12孔作为空白对照孔。
3)、用rpmi1640液作稀释液将flc贮存液作10级倍比稀释,使flc起始浓度为64μg/ml,终止浓度为0.125μg/ml。
实施例5最低抑菌浓度(mic)的判定
1)、将接种后的药敏板置微量振荡板上振荡5min,均匀混合后,培养24h,观察受试菌生长情况,接种后的药敏板置微量振荡板上振荡5min,均匀混合后,培养24h,观察受试菌生长情况,并读取结果,在不搅动的情况下与对照孔标准比较进行结果;待测硅钨酸盐flc;取浊度显著减低为mic检测值。在10余种硅钨酸盐中,只有2种硅钨酸盐siw-5和siw-10表现出了较好的抗真菌活性和较低的毒性,siw-5和siw-10均具有较好的抗真菌活性,siw-5的抗真菌活性略高于siw-10(见表1)。
表1硅钨酸盐最小抑菌浓度(μm)
所用受试菌白色念珠菌(c.albicans)、光滑念珠菌(c.glabrata)、热带念珠菌(c.tropicalis)、克柔念珠菌(c.krusei)、近平滑念珠菌(c.parapsilosis)、新型隐球菌(cryptococcusneoformans)均保藏于公共卫生学院卫生检验教研室的耐药菌株。
实施例6联合抑菌实验
用微量棋盘稀释法分级抑菌浓度指数(fractionalinhibitoryconcentrationindex,fici)实验,选择白色念珠菌c.albicans27、c.albicans36、c.albicans37、c.albicans59,分别检测siw-5和氟康唑对各菌株联合用药的fici,研究siw-5和氟康唑联合应用的抗真菌效果。
fici是其为联合用药时甲药mic/单独应用甲药时mic和联合应用乙药时mic/单独应用乙药时为mic。
fici指数判读标准:当fici指数小于0.5时,两种药物为协同作用;当fici指数为0.5~1时,两种药物为相加作用;当fici指数大于l且小于2时,两种药物为无关作用;当fici指数大于2时,两种药为拮抗作用。
siw-5和氟康唑对c.albicans27、c.albicans36、c.albicans37、c.albicans59的fici均在0.5~1,因此二药联合为相加作用。
实施例7将mic浓度的siw-5作用于白色念珠菌后透射电镜观察其结构
将mic浓度的siw-5作用于白色念珠菌c.albicanshl27,未用药的作为对照组,35°c培养24h,离心后用pbs洗三次,去上清,然后进行透射电镜样品制备。
透射电镜样品制备步骤:
1)、4%戊二醛固定,4℃;
2)、pbs缓冲液漂洗3次,每次10-45min;
3)、锇酸固定,2h,4℃;
4)、蒸馏水漂洗3次,每次15min;
5)、梯度脱水:50%70%80%95%乙醇各1次,每次10min95%乙醇和95%丙酮1:1混合脱水,10min;100%丙酮2次,每次20min;环氧丙烷置换丙酮1次,20min;
6)、预浸透:环氧丙烷和包埋剂(spi-pon812)1:1混合,预浸透1h;
7)、浸透:包埋剂浸透3h;聚合:35℃,12h;45℃,12h;60℃,24h;超薄切片。超薄切片机型号:leicaemuc7;
8)、染色:醋酸双氧铀染色10min,蒸馏水冲洗;柠檬酸铅染色10min,蒸馏水冲洗;即可用透射电镜观察;透射电镜型号:hitachih-7650透射电镜观察可见;
9)、白色念珠菌细胞呈圆形或椭圆形,细胞壁质地致密,厚薄均匀、规则,细胞膜完整,胞质均匀。siw-5的mic浓度用药后的念珠菌与正常组相比,细胞较小,形状不规则,细胞壁厚薄不均,细胞膜不完整,轮廓不清,细胞质不均匀(如图3)。
实施例8念珠菌麦角固醇的高效液相分析(hplc)
1)、将2mic、mic、0.5mic浓度的siw-5作用于白色念珠菌c.albicanshl27,mic浓度的氟康唑作为阳性对照组,未用药的作为阴性对照组,35°c培养24h,离心后用pbs洗三次,去上清,各取0.5g湿菌,加皂化剂(新鲜配制的含15%naoh的90%乙醇溶液)6ml和pbs2.5ml,混匀,80°c水浴皂化1h。加石油醚6ml提取3次,提取液用水洗涤后,60°c水浴挥干,加色谱级甲醇使溶液体积为1ml/g湿菌。
2)、精确称取麦角固醇标准品25mg,用色谱级甲醇稀释,用25ml容量瓶定容,稀释成0.001,0.004,0.015,0.0625,0.25,1mg/ml,进行高效液相色谱检测,测得峰面积,绘制标准曲线。
3)、采用岛津高性能液相色谱仪lc-20ab,岛津glc18色谱柱(250mm×4.6mm,5μm),流动相为甲醇:水=97:3,流速1ml/min,柱温25°c,检测器为紫外/可见检测器,检测波长282nmuv。
以峰面积为纵坐标,麦角固醇标准品浓度为横坐标,绘制标准曲线(图4),线性回归方程:y=1357660x-291.14469(r2=0.99978)
4)、hplc得出,2mic、mic、0.5mic浓度的siw-5组的麦角固醇含量分别为0.06±0.01、0.15±0.02、0.25±0.01mg/ml,与对照组相比,减少了80.65%、51.61%、19.35%。氟康唑组麦角固醇含量为0.12±0.00mg/ml,减少了61.29%。可见,siw-5对麦角固醇的抑制作用随着药物浓度的增加而增强,因此,抑制细胞膜上麦角固醇的生物合成可能是siw-5抗真菌的作用机制之一。
实施例9:急性毒性实验
1)、将70只icr小鼠随机分为7组,每组10只,雌雄各半。实验前禁食,但不禁水。给受试化合物前禁水。siw-5用无菌水溶解,6个受试组分别以1300、1400、1500、1600、1700、1800mg/kg灌胃一次,对照组给无菌水。染毒后观察动物的一般状况,中毒症状和死亡情况,观察14天。用bliss法计算半数致死剂量ld50。
2)、ld50为1651.5mg/kg,ld50的95%可信限范围为1539.6mg/kg~1926.5mg/kg,按who急性毒性分级,属低毒化合物。染毒后,动物短时间内状态不佳,呈应激反应。但经2小时左右逐渐恢复。活动自如,饮食正常。其余未见异常表现。
实施例8:体内药效学实验
1)、在感染前第3天和第1天,用150mg/kg环磷酰胺腹腔注射balb/c小鼠(18-22g),并在感染后第3、6、9天注射150mg/kg环磷酰胺维持免疫抑制状态。免疫抑制的小鼠尾静脉注射2×105cfu/0.1ml白色念珠菌c.albicanshl27。染菌后24h,分别腹腔注射100、50、25mg/kgsiw-5作为高、中、低药物剂量组,腹腔注射10mg/kg氟康唑作为阳性药物组,各治疗组每天给药一次,连续给药7d,每个治疗组14只,雌雄各半。感染组10只,雌雄各半,每天腹腔注射一次无菌水,连续7d。各组连续监测15天,以生存率、pas染色病理观察及肾脏匀浆培养真菌菌落计数(logcfu/g肾脏)评价siw-5体内药效。
2)、注射无菌水的感染组在6d内全部死亡,中位生存期为5d;15d后,10mg/kg氟康唑和100mg/kgsiw-5组分别存活70%和60%;50mg/kg和25mg/kgsiw-5组的中位生存期分别为7d和6d(图5)。
3)、感染组肾组织严重破坏,有大量真菌孢子和菌丝浸润;25mg/kg和50mg/kgsiw-5组的菌丝和孢子分别呈轻度和中度减少;100mg/kgsiw-5和10mg/kg氟康唑组真菌细胞很少,大部分以孢子的形式存在(图6)。25mg/kg、50mg/kg、100mg/kgsiw-5及10mg/kg氟康唑组的肾脏匀浆菌落计数依次减少,与感染组之间有统计学差异(p<0.05)(表2)。
- 还没有人留言评论。精彩留言会获得点赞!