二次电池正极活性材料前体的制备方法和利用该方法的制备装置与流程
本发明涉及一种二次电池正极活性材料前体的制备方法和利用该方法的制备装置。更具体地,本发明涉及一种二次电池正极活性材料前体的制备方法和实现该制备方法的制备装置,所述制备方法包括共沉淀滤液再利用工艺。
背景技术:
随着科学技术的飞速发展,近年来市面上不仅出现了各种电子产品和通信设备,还出现了需要大容量存储装置的电动车辆,对它们的动力源二次电池的需求正在迅速增长。
通常,用于制备二次电池正极活性材料前体的最先进的技术是利用共沉淀法的技术。为了共沉淀反应,将niso4、coso4、mnso4以适当的比例混合而成的高浓度金属溶液与naoh和nh4oh一起注入反应器,以形成核并长时间反应,从而获得具有一定粒径的前体。
共沉淀法利用连续搅拌釜反应器(cstr,continuousstirredtankreactor)、库爱特-泰勒连续反应器、间歇式(batch)反应器等,根据ph、温度、搅拌条件,前体的形状或粒度、形貌会改变。通常,如果需要大量生产前体,就利用连续搅拌釜反应器来生产,而如果要求前体品质,就使用间歇式反应器。
通常,在基于共沉淀法的反应中,为了克服根据镍、钴、锰等金属离子ph值的共沉淀速度之差,加入氨作为螯合剂,但是根据ph条件金属离子(特别是镍)与氨配位结合而溶出,因此溶液中会残留一定量的金属离子。此时,随着镍的溶出量增加,上清液会变成蓝色。对于这种溶出的镍,在共沉淀后通过压滤器(filterpress)过滤之后,还是会溶解在剩下的共沉淀滤液中,需要另进行废水处理,因此制备前体时成为导致原材料成本上升的因素。
通常,在共沉淀反应之后,对产物前体通过压滤器进行过滤,并经过2~3次水洗工艺后,再经过干燥过程。在此情况下,当生产1吨前体时,将会产生50吨废水(所消耗的水洗液包括在内),而废水中含有氨、溶出的金属离子、硫酸钠等,因此需要独立的废水处理设施,而且产生成本。大多数氨、溶出的金属离子、硫酸钠会残留在从共沉淀滤液过滤后剩下的溶液中,而水洗时产生的水洗液中含有微量的氨、硫酸钠等。在共沉淀滤液和水洗液等废水中,氨是利用硫酸等通过湿式洗涤器来清除,而金属离子是在重金属处理槽中通过催化剂析出和沉淀,剩下的进行废水处理。
在现有技术或文献中,连续搅拌釜反应器、库爱特-泰勒连续反应器、间歇式反应器等是已知的,但是没有提出一种共沉淀工艺,可以提高共沉淀工艺中溶出的金属离子的收率,并且减少废水产生量或者再利用共沉淀滤液。
技术实现要素:
技术问题
本发明要解决的技术问题是提供一种方法,在制备二次电池正极活性材料前体时,再利用反应中产生的共沉淀滤液中含有的金属离子,并提高共沉淀反应时的收率以及大幅减少废水产生量。
技术方案
根据本发明的一个实施例的二次电池正极活性材料前体的制备方法可包括将共沉淀反应后生成的共沉淀滤液转移到共沉淀滤液储罐的步骤、使所述共沉淀滤液通过滤器以去除金属氢氧化物的步骤、将所述去除金属氢氧化物的共沉淀滤液与硫酸或硝酸进行反应以去除所述去除金属氢氧化物的共沉淀滤液中的氨并生成硫酸铵或硝酸铵的步骤、将所述去除金属氢氧化物和氨的共沉淀滤液冷却结晶化以析出硫酸钠的步骤、将所述析出的硫酸钠过滤以从所述去除金属氢氧化物和氨的共沉淀滤液中分离出所述析出的硫酸钠的步骤、将所述从共沉淀滤液中分离出的硫酸钠进行干燥并将与所述硫酸钠分离的共沉淀滤液转移到循环浓缩罐的步骤、及将储存在所述循环浓缩罐内的所述共沉淀滤液升温至一定温度以供再利用并进行n2吹扫(purging)或鼓泡(bubbling)的步骤。
所述二次电池正极活性材料前体的制备方法还可包括将naoh加入所述共沉淀滤液储罐内的所述共沉淀滤液中以使所述共沉淀滤液的ph增加到11.8以上的步骤。
在所述二次电池正极活性材料前体的制备方法中,使所述共沉淀滤液通过滤器以去除金属氢氧化物的步骤中,所述金属氢氧化物可包括共沉淀滤液中残留的金属氢氧化物和naoh加入共沉淀滤液而重新生成的金属氢氧化物。
在所述二次电池正极活性材料前体的制备方法中,将所述去除金属氢氧化物的共沉淀滤液与硫酸或硝酸进行反应以去除所述去除金属氢氧化物的共沉淀滤液中的氨并生成硫酸铵或硝酸铵的步骤中,所述氨可以是nh3气体状态。
在所述二次电池正极活性材料前体的制备方法中,将所述去除金属氢氧化物和氨的共沉淀滤液冷却结晶化以析出硫酸钠的步骤中,可以将所述共沉淀滤液冷却至10℃。
在所述二次电池正极活性材料前体的制备方法中,所述将储存在循环浓缩罐内的共沉淀滤液升温至一定温度以供再利用的步骤中,所述温度可以是45℃以上。
在所述二次电池正极活性材料前体的制备方法中,所述共沉淀反应是将金属硫酸盐用蒸馏水溶解制备成金属溶液,再将所述金属溶液与naoh和nh4oh一起注入反应器进行反应,可以将去除所述氨时生成的所述硫酸铵重新溶解后使用以代替所述共沉淀反应的nh4oh。
根据本发明的一个实施例的二次电池正极活性材料前体的制备装置可包括:共沉淀滤液储罐,用于储存共沉淀反应后生成的共沉淀滤液;滤器,用于从所述共沉淀滤液中去除金属氢氧化物;去氨用膜接触器,用于从所述去除金属氢氧化物的共沉淀滤液中去氨;硫酸罐或硝酸罐,用于将与氨接触的硫酸或硝酸供应到所述去氨用膜接触器;冷却结晶罐,用于使所述去除金属氢氧化物和氨的共沉淀滤液冷却结晶化,以析出硫酸钠;过滤器,用于将所述析出的硫酸钠进行过滤,以从所述去除金属氢氧化物和氨的共沉淀滤液中分离出所述析出的硫酸钠;干燥器,用于将所述从共沉淀滤液中分离出的硫酸钠进行干燥;循环浓缩罐,用于储存与所述硫酸钠分离的共沉淀滤液;以及初始溶液制备罐,用于将储存在所述循环浓缩罐内的所述共沉淀滤液升温至一定温度以供再利用并进行n2吹扫或鼓泡。
在所述二次电池正极活性材料前体的制备装置中,通过向所述共沉淀滤液储罐内的所述共沉淀滤液加入naoh,可以将所述共沉淀滤液的ph增加到11.8以上。
在所述二次电池正极活性材料前体的制备装置中,所述滤器可以去除共沉淀滤液中残留的金属氢氧化物和naoh加入共沉淀滤液而重新生成的金属氢氧化物。
在所述二次电池正极活性材料前体的制备装置中,所述去氨用膜接触器中氨可以nh3气体状态存在。
在所述二次电池正极活性材料前体的制备装置中,所述冷却结晶罐可以将温度冷却至10℃。
在所述二次电池正极活性材料前体的制备装置中,所述初始溶液制备罐可以将储存的共沉淀滤液升温至45℃以上。
在所述二次电池正极活性材料前体的制备装置中,所述共沉淀反应是将金属硫酸盐用蒸馏水溶解制备成金属溶液,再将所述金属溶液与naoh和nh4oh一起注入反应器进行反应,所述制备装置还可包括硫酸铵供应罐,用于储存所述硫酸铵,将去除所述氨时生成的所述硫酸铵重新溶解后使用,以代替所述共沉淀反应的nh4oh。
发明效果
根据本发明的一个实施例的制备方法,用于制备二次电池正极活性材料前体等的共沉淀反应中产生的共沉淀滤液的成分中氨经过浓缩成硫酸铵或硝酸铵的过程被去除,而硫酸钠通过冷却结晶化析出,剩下的共沉淀滤液可得到再利用,重新用于形成金属溶液。因此,通过这样的共沉淀反应工艺,可以进一步生产出硫酸铵或硝酸铵、硫酸钠等副产物,可以使收率最大化。
此外,根据本发明的另一个实施例,可以提供二次电池正极活性材料前体的制备装置,该制备装置实现所述制备方法,包括再利用共沉淀反应中生成的共沉淀滤液的工艺。
附图说明
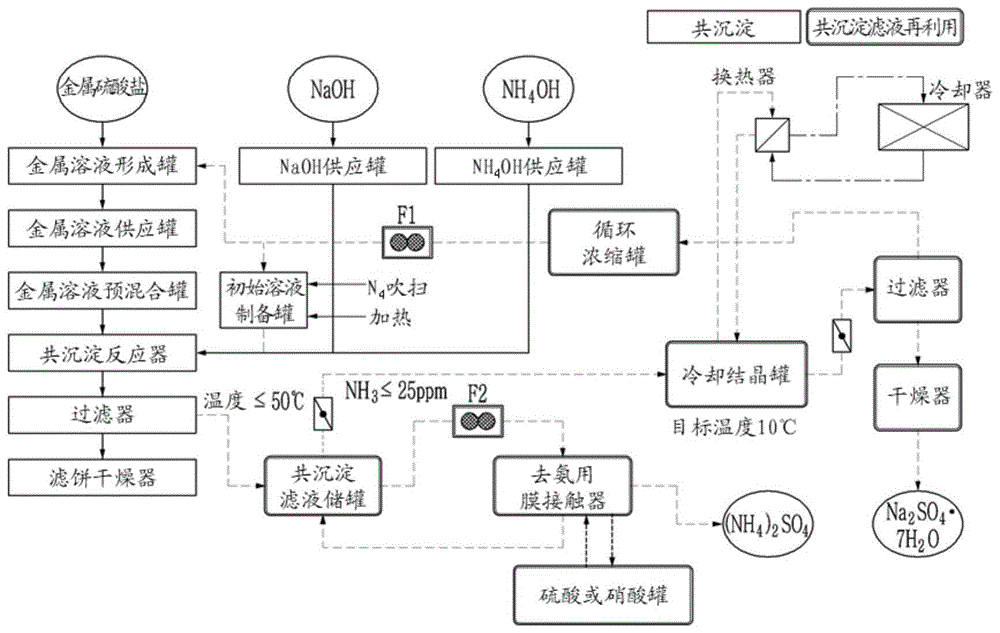
图1是根据本发明的一个实施例的包括共沉淀滤液再利用工艺的间歇式共沉淀法的示意图。
图2是示出根据温度的硫酸钠和硫酸镍的溶解度之差的曲线图。
图3是对根据本发明的一个实施例的制备方法的共沉淀滤液再利用工艺中析出的硫酸钠的成分进行分析的结果。
图4示出根据温度和ph的nh3/nh4+的比例。
图5示出根据本发明的一个实施例的去氨用膜片中氨以气体状态通过膜片与硫酸进行反应而浓缩成硫酸钠的反应。
图6是曲线图,示出了如果采用根据本发明的一个实施例的共沉淀法将共沉淀滤液循环使用几次,则循环超过一定次数时,将会析出一定量的硫酸钠。
图7是将根据本发明的一个实施例的共沉淀法中去氨用膜接触器内的工艺细化的示意图。
图8是根据本发明的又一个实施例的包括共沉淀滤液再利用工艺的间歇式共沉淀法的示意图,增加有硫酸铵供应罐,其用于重新溶解并准备供应通过膜片浓缩的硫酸铵以用作螯合催化剂。
图9是示出根据本发明的一个实施例的去氨用膜片中根据共沉淀滤液的流量、ph、温度的氨去除率的图。
图10是根据本发明的一个实施例的冷却结晶化步骤前共沉淀滤液中含有的成分和冷却结晶化后析出的硫酸钠成分的比较图。
图11是示出在50℃的等温状态下na2so4-niso4-h2o体系下可生成na2ni(so4)2·4h2o化合物的条件的na2ni(so4)2·4h2o等温溶解度图。
具体实施方式
在下文中,将参照附图描述本发明。然而,本发明能够以各种不同方式实施,因此不限于所述的实施例。
下面参照附图详细描述本发明的实施例。
图1是根据本发明的一个实施例的包括共沉淀滤液再利用工艺的间歇式共沉淀法的示意图。参照图1,为了常规共沉淀反应,将金属硫酸盐用蒸馏水溶解制备成混合有niso4、coso4、mnso4等的金属溶液,并将该金属溶液与naoh和nh4oh一起注入反应器进行共沉淀反应。对于现有的共沉淀反应,共沉淀反应后生成的前体在过滤步骤中通过压滤器被过滤,然后经过水洗过程,再经过干燥过程。此时,压滤器中过滤后残留的溶液和对用所述过滤器过滤出的前体进行水洗时使用的水洗溶液作为共沉淀滤液残留,而这样的共沉淀滤液中含有溶出的金属离子(镍、钴、锰)、5μm以下的微细金属氢氧化物(氢氧化镍、氢氧化钴、氢氧化锰)、na+、so42-、nh3等。在本发明的一个实施例中,将所述压滤器中过滤后残留的共沉淀滤液储存在共沉淀滤液储罐。此时,为了调整共沉淀滤液的na+、so42-的摩尔比,加入naoh使ph增加到11.8以上。如此调整ph的共沉淀滤液使其通过滤器f2,而滤器f2起到过滤共沉淀滤液中残留的微细金属氢氧化物和共沉淀滤液储罐中加入naoh时重新生成的金属氢氧化物的作用。将共沉淀滤液通过滤器f2进行过滤,从而起到过滤作用,以避免后续对硫酸钠进行冷却结晶化时金属氢氧化物或金属离子进入成为杂质。将经滤器f2去除金属氢氧化物的共沉淀滤液转移到去氨用膜接触器,使得以气体状态存在的nh3与稀硫酸或硝酸接触时,氨被去除作为副产物生成硫酸铵((nh4)2so4)。将通过去氨用膜接触器去氨的共沉淀滤液转移到冷却结晶罐中。转移到冷却结晶罐的共沉淀滤液冷却至10℃并析出硫酸钠。此时,为了冷却,使用换热器和冷却器。经由过滤器将析出的硫酸钠与共沉淀滤液分离后,将析出的硫酸钠在干燥器中进行干燥,而与析出的硫酸钠分离的共沉淀滤液经循环浓缩罐转移到初始溶液制备罐和金属溶液形成罐,以重新形成金属溶液。在所述初始溶液制备罐中,将共沉淀滤液升温至45℃,并实施n2吹扫(purging)或n2鼓泡(bubbling),以防止初始共沉淀反应时金属离子的氧化。
如果利用根据本发明的一个实施例的所述共沉淀滤液再利用工艺,则以镍为83%的ncm前体为例,可以从生产1吨前体时产生的共沉淀滤液中获得3.1吨左右的硫酸钠(na2so4·7h2o),当利用膜片和硫酸对氨进行浓缩时,作为副产物可以获得1.3吨左右的硫酸铵((nh4)2so4)。根据ph条件,在共沉淀滤液中会残留1000ppm以上的被氨等溶出的金属离子,这相当于加入的金属离子总量的0.1%至几个百分点。
图2是示出根据温度的硫酸钠(na2so4)和硫酸镍(niso4)的溶解度之差的曲线图,图中示出根据本发明的一个实施例的共沉淀滤液再利用步骤中,将去氨的共沉淀滤液冷却至10℃时,可以析出硫酸钠。
参照图3,图中示出对根据本发明的一个实施例的制备方法的共沉淀滤液再利用工艺中所述去氨的共沉淀滤液冷却至10℃而析出的硫酸钠的成分进行分析的结果,如图2所示,在10℃下硫酸镍的溶解度远高于硫酸钠的溶解度,因此可知硫酸镍等杂质没有进入析出的硫酸钠中。
通常,用于生产ncm前体的共沉淀反应之后,共沉淀滤液的温度为45℃以上,ph为11以上。此时,大多数是以nh3气体状态存在(参照图4)。在本发明的一个实施例中,共沉淀滤液中含有5000ppm以上的氨,当再利用共沉淀滤液时,为了在不影响共沉淀反应的情况下去除共沉淀滤液中含有的氨,使得以nh3气体状态存在的氨与硫酸或硝酸进行反应,从而浓缩成硫酸钠或硝酸钠进行去除。此时,所述nh3气体由以下的亨利定律(henry′slaw)以气体状态通过膜片并与硫酸或硝酸进行反应。
亨利定律(p=hx)
p=与溶液接触的气体的部分压力
h=气体的亨利比例常数
x=溶解于溶液中的气体的浓度
如图4所示,可知ph越高,去氨效率越高,而且共沉淀滤液的温度越高,去氨效率越高。因此,在本发明的一个实施例中,当共沉淀反应时,在48℃以上的温度下反应结束后,如果经压滤工艺共沉淀滤液的温度降低,则通过共沉淀滤液槽的加热器进行温度补偿。在共沉淀反应之后,共沉淀滤液的ph高达11以上。因此,当加入少量的naoh以调整na+和so42-的摩尔比时,ph会升高到11.8以上,由此去氨效率可以保持非常高的状态。
去氨的共沉淀滤液中na+和so42-、ni2+等是以离子状态存在。将这种共沉淀滤液冷却至10℃时,na+和so42-会以硫酸钠(na2so4·7h2o)水合物形式析出(参照图2),而溶解度以下的na+和so42-与ni2+一起残留在共沉淀滤液中。经所述步骤去氨且na+和so42-的浓度降低的共沉淀滤液形成金属溶液或者供应到初始溶液制备罐再用于共沉淀反应。参照图6,在重复几次根据本发明的一个实施例的制备工艺后,na+和so42-被浓缩,最终超过一定的循环次数再利用共沉淀滤液时,冷却结晶化后会析出一定量的硫酸钠,而循环的共沉淀滤液的na+和so42-离子浓度保持一定,因此共沉淀反应时工艺条件变得稳定。
图7是将根据本发明的一个实施例的共沉淀法中去氨用膜接触器内的工艺细化的示意图。
参照图7,当向膜接触器供应稀硫酸时,与氨气进行反应而生成硫酸铵,当供应稀硝酸时,与氨气进行反应而生成硝酸铵。此时,如前所述,在膜接触器中,硫酸或硝酸与共沉淀滤液分离的状态下只有nh3气体移动进行反应。对浓缩在硫酸储存槽中的硫酸铵测定密度,当浓缩到一定程度以上时,将其转移到硫酸铵储存槽。通过膜接触器中去氨的工艺大部分氨被去除后,利用换热器和冷却器将沉淀过滤槽内的共沉淀滤液冷却至10℃,冷却时共沉淀滤液中的na+和so42-会以硫酸钠水合物形式析出,析出量相当于饱和溶解度以下的量。析出的硫酸钠通过过滤与共沉淀滤液分离,剩下的共沉淀滤液储存到循环浓缩罐中。
储存的共沉淀滤液再次供应到初始溶液制备罐和金属溶液形成罐进行循环,当共沉淀滤液再利用工艺重复几次以上时,na+和so42-的浓度被浓缩。
参照图8可知,在图1所示的根据本发明的一个实施例的包括共沉淀滤液再利用工艺的间歇式共沉淀法中,可以增加共沉淀反应时代替氨加入重新溶解的通过膜片生成、浓缩的硫酸铵以用作螯合催化剂的步骤。
图9是示出根据本发明的一个实施例的去氨用膜片中根据共沉淀滤液的流量、ph、温度的氨去除率的图,由此可知共沉淀滤液的温度和ph越高,去氨效率越增加。
图10是根据本发明的一个实施例的冷却结晶化步骤前共沉淀滤液中含有的成分和冷却结晶化后析出的硫酸钠成分的比较图,由此可知析出的硫酸钠中几乎不包括共沉淀滤液中含有的镍、钴、锰等金属离子。
图11是示出在50℃的等温状态下na2so4-niso4-h2o体系下可生成na2ni(so4)2·4h2o化合物的条件的na2ni(so4)2·4h2o等温溶解度图,示出了根据本发明的一个实施例的共沉淀滤液再利用工艺中硫酸钠和硫酸镍化合物的生成可能性非常低。参照图11,初始条件是在50℃以上的温度下na2so4为17.78重量%,niso4为18.24重量%,h2o为63.98重量%的m点上生成na2so4和niso4化合物na2ni(so4)2·4h2o,如图10所示,根据本发明的一个实施例的共沉淀滤液中含有的硫酸镍的浓度非常低,因此几乎不存在图11的m点上形成的na2so4和niso4化合物形式。
上面描述了本发明的优选实施例,但是本发明的权利范围不限于上述实施例,所属领域的技术人员利用权利要求书中定义的本发明的基本概念所做的各种变形和改进形式也落入本发明的权利范围。
- 还没有人留言评论。精彩留言会获得点赞!