β-氨基羰基类化合物、其制备方法、药物组合物及其用途与流程
本发明属于药物化学领域。具体而言,本发明涉及一种通式I所示的新的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐,其制备方法,药物组合物及其作为二肽基肽酶IV(DPP-4)抑制剂的用途。该类化合物或其药物组合物作为DPP-4抑制剂可用于治疗II型糖尿病、高血糖症、肥胖症或胰岛素抵抗症。
背景技术:
糖尿病(diabetes)是由遗传因素、免疫功能紊乱、微生物感染及其毒素、自由基毒素、精神因素等等各种致病因子作用于机体导致胰岛功能减退、胰岛素抵抗等而引发的糖、蛋白质、脂肪、水和电解质等一系列代谢紊乱综合征,临床上以高血糖为主要特点,典型病例可出现多尿、多饮、多食、消瘦等表现,即“三多一少”症状。糖尿病(血糖)一旦控制不好会引发并发症,导致肾、眼、足等部位的衰竭病变,且无法治愈。
近年来,糖尿病的发病率逐年攀升,成为21世纪人类健康的主要威胁之一,其中II型糖尿病占90%以上。胰岛素抵抗和胰岛素分泌功能受损是II型糖尿病发病和病理过程之中的两个重要现象。目前临床上使用的降糖药物都存在不同程度的副作用和局限性:磺脲类和胰岛素类降糖药物增加体重并伴随低血糖风险;噻唑烷二酮类胰岛素增敏剂的代表药物——罗格列酮因可能增加糖尿病患者心血管疾病的风险,而在全球范围内退市或被限制使用;吡格列酮也在2011年标注膀胱癌风险;二甲双胍和α糖苷酶抑制剂则存在不同程度的消化道反应;胰岛素不能口服给药。DPP-4抑制剂因具有良好的血糖控制、低血糖发生风险小和不影响体重等优势已成为当下最热门的抗糖尿病药物。
目前,已有5个DPP-4抑制剂上市用于治疗糖尿病,它们分别是西他列汀(sitagliptin)、维达列汀(vildagliptin)、沙格列汀(saxagliptin)、阿格列汀(alogliptin)、利拉利汀(linagliptin)。
本发明的目的在于提供一种新的具有DPP-4抑制活性,可用于糖尿病及类似疾病的治疗或缓解性药物的化合物。
技术实现要素:
发明目的
本发明的一个目的是提供一种通式I所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐。
本发明的另一个目的是提供本发明提供的化合物的制备方法。
本发明的又一个目的是提供通式I所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐作为DPP-4抑制剂的用途,以及在制备治疗II型糖尿病、高血糖症、肥胖症或胰岛素抵抗症药物中的应用。
本发明的再一个目的是提供包含通式I所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐中的一种或多种的药物组合物。
本发明的再一个目的是提供一种治疗II型糖尿病、高血糖症、肥胖症或胰岛素抵抗症的方法。
技术方案
根据本发明的一个方面,提供了一种通式I所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐:
其中:
A选自C6-C10芳基、饱和或不饱和C3-C10环烃基、4-10元杂环基或4-10元杂芳基;所述杂环基或杂芳基含有1-4个选自N、S和O的杂原子;A优选为苯基、5~6元杂环基或5~6元杂芳基,更优选为苯基、吡啶基或环戊二烯基;
W为N、S、O或C1-C4直链烃基;
Q为N、S、O或C原子;
W与Q之间的虚线存在或不存在,存在时表示此处是不饱和键(如双键),不存在时表示此处是饱和键(单键),优选为不存在;
Y为N或CR7;
X为N或CR7;
R1、R2、R3和R4各自独立地为H;卤素;三氟甲基;羟基;硝基;腈基;羧基;-C(O)OC1-C10烷基;氨基;C1-C10烷氧基;C1-C10烷基;C1-C10烷酰基(即-C(O)C1-C10烷基);C1-C10烷酰氧基(即-OC(O)C1-C10烷基);磺酰基;C1-C10烷基磺酰基;C6-C10芳基;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C10烷基、氨基、C1-C10烷氧基、C1-C10烷基、C1-C10烷酰基、C1-C10烷酰氧基、磺酰基、C1-C10烷基磺酰基、C6-C10芳基、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷基、C1-C10烷氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、C1-C10烷酰基、磺酰基、C1-C10烷基磺酰基、苯基和苯甲基中的取代基取代;
R5和R6各自独立地为-(CH2)mR9;-(CH2)mCO(CH2)nR9;或-[(CH2)iO]jH,其中i=1~5的整数,j=1~3的整数,R9为H;卤素;羟基;硝基;氨基;腈基;羧基;-C(O)OC1-C10烷基;C1-C10烷酰基;C1-C10烷基磺酰基;C1-C10烷基;C2-C10烯基;C2-C10炔基;C3-C10环烷基;C3-C8内酰胺基;C1-C10烷氨基磺酰基;C1-C10烷氨酰基;C6-C10芳酰基;C1-C10烷氧基;C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16;C6-C10芳基;4-10元杂环基;4-10元杂芳基;4-10元杂环基或4-10元杂芳基并C3-C10环烃基;或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;上述氨基、-C(O)OC1-C10烷基、C1-C10烷酰基、C1-C10烷基磺酰基、C1-C10烷基、C2-C10烯基、C2-C10炔基、C3-C10环烷基、C3-C8内酰胺基、C1-C10烷氨基磺酰基、C1-C10烷氨酰基、C6-C10芳酰基、C1-C10烷氧基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C3-C10环烃基或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NR15R16、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;上述C6-C10芳基、C6-C10芳酰基和C6-C10芳基磺酰基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C10烷氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NR15R16、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基和C6-C10芳基C1-C10烷基中的取代基取代;
或者,R5和R6与它们相连的X共同构成氨基葡萄糖基;氨基酸残基;氨基酸酯残基;或氨基酰胺残基,且非必须地被一个或多个选自C1-C6烷基、C1-C6烷基取代的氨基、C1-C10烷酰基、苄基、苄氧羰基和叔丁氧羰基中的取代基取代;
或者,R5和R6与连接它们的X一起形成C6-C10芳基;C3-C10环烃基;C3-C10环烃基并C3-C10环烃基;C3-C10环烃基并C6-C10芳基;C6-C10芳基并C3-C10环烃基;4-10元杂环基;4-10元杂芳基;4-10元杂环基螺环;4-10元杂芳基螺环;4-10元杂环基或4-10元杂芳基并C3-C10环烃基;C3-C10环烃基并4-10元杂环基或4-10元杂芳基;4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;C6-C10芳基并4-10元杂环基或4-10元杂芳基;4-10元杂环基或4-10元杂芳基并C6-C10芳基;[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基];或者[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[C6-C10芳基];上述基团可非必须地被一个或多个R’取代,R’选自-(CH2)mR10;-(CH2)mCO(CH2)nR10;-(CH2)mO(CH2)nR10;-(CH2)mNHC(O)(CH2)nR10;和-(CH2)mNSO2(CH2)nR10;
其中,R10为氢、卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NH2、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或上述氨基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NH2、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NR15R16、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;
R15、R16各自独立地为H;C1-C10烷基;C3-C10环烷基;4-10元杂环基;4-10元杂芳基;或者R15、R16与连接它们的N原子一起形成4-10元杂环基;4-10元杂芳基;其中,所述C1-C10烷基、C3-C10环烷基、4-10元杂环基和4-10元杂芳基可非必须地被1个或多个卤素;羟基;腈基;氨基;C1-C10烷基;=O(氧代);=S(硫代);C1-C10烷氧基取代;
R7为-(CH2)mR11、-(CH2)mO(CH2)nR11或-(CH2)mNHR11;
其中,R11为H;卤素;硝基;腈基;羧基;-C(O)OC1-C10烷基;C2-C10烯基;C2-C10炔基;C1-C10烷酰基;C1-C10烷基磺酰基;氨基C1-C10烷酰基;C1-C10烷基;C6-C10芳基;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C10烷基、C2-C10烯基、C2-C10炔基、C1-C10烷酰基、C1-C10烷基磺酰基、氨基C1-C10烷酰基、C1-C10烷基、C6-C10芳基、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、C1-C10烷酰基、C1-C10烷基磺酰基、=O(氧代)、=S(硫代)和C1-C10烷基中的取代基取代;
R8为-(CH2)mR12、-(CH2)mO(CH2)nR12或-(CH2)mNHR12;
其中,R12为H;卤素;硝基;腈基;羧基;=O(氧代);=S(硫代);-C(O)OC1-C10烷基;C2-C10烯基;C2-C10炔基;C1-C10烷酰基;C1-C10烷基磺酰基;氨基C1-C10烷酰基;C1-C10烷基;Ph(CH2)m-;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C10烷基、C2-C10烯基、C2-C10炔基、C1-C10烷酰基、C1-C10烷基磺酰基、氨基C1-C10烷酰基、C1-C10烷基、Ph(CH2)m-、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、C1-C10烷酰基、C1-C10烷基磺酰基、=O(氧代)、=S(硫代)和C1-C10烷基中的取代基取代;
各个m和各个n各自独立地为0-5的整数;
q为0-4的整数。
X为CR7、Y为R7时,各R7可以相同也可以不同。
本发明中,未特别指出,各基团均可包括取代或未取代的形式,如对于C1-C10烷基而言,包括未取代或取代的C1-C10烷基,对于C6-C10芳基、C6-C10芳酰基、4-10元杂环基、4-10元杂芳基而言,包括未取代或取代的C6-C10芳基、C6-C10芳酰基、4-10元杂环基、4-10元杂芳基,其中,取代方式如通式I所示的化合物中所定义。
其中,除非特别指出,所述烷基包括直链、支链烷基;
所述C6-C10芳基为苯基、稠环芳基,所述芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C10烷氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NR15R16、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基和C6-C10芳基C1-C10烷基中的取代基取代;
所述芳酰基为被芳基取代的酰基,其中的芳基定义同前。
在一优选例中,通式I所示的β-氨基羰基类化合物具有以下一个或多个特征:
(1)A为C6-C10芳基、饱和或不饱和C3-C10环烃基、4-10元杂芳基;所述4-10元杂芳基含有1-4个选自N、S和O中的杂原子;
(2)R1、R2、R3和R4各自独立地为H、卤素、三氟甲基、羟基、硝基、腈基、羧基、氨基、C1-C10烷氧基、C1-C10烷基;
(3)R8为-(CH2)mR12、-(CH2)mO(CH2)nR12或-(CH2)mNHR12;其中,R12为H、卤素、Ph(CH2)m-、4-10元杂环基、=O(氧代)、=S(硫代)、C1-C10烷基;以上Ph(CH2)m-、4-10元杂环基、C1-C10烷基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷氧基、=O(氧代)、=S(硫代)、C1-C10烷基中的取代基取代;(在另一优选例中,所述4-10元杂环基为吲哚基或吡咯基);
(4)Y为N或CR7,其中,R7为-(CH2)mR11、-(CH2)mO(CH2)nR11或-(CH2)mNHR11;其中,R11为H、C6-C10芳基、4-10元杂环基、羧基、氨基C1-C10烷酰基、-C(O)OC1-C10烷基、卤素、硝基或4-10元杂芳基;上述C6-C10芳基、4-10元杂环基、氨基C1-C10烷酰基、-C(O)OC1-C10烷基、或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、=O(氧代)、=S(硫代)、C1-C10烷基、C1-C10烷氧基硝基、和氨基中的取代基取代;
m和n各自独立地为0-5的整数;
(5)X为N或CR7;其中,R7为-(CH2)mR11,其中,R11为H,m为0;
(6)R5和R6各自独立地为-(CH2)mR9;-(CH2)mCO(CH2)nR9;或-[(CH2)iO]jH,其中i=1~5的整数,j=1~3的整数,m和n各自独立地为0-5的整数;R9为H、C6-C10芳基、4-10元杂环基、C1-C10烷基、C2-C10烯基、4-10杂芳基、C1-C10烷酰基、C3-C8内酰胺基、4-10元杂环基或4-10元杂芳基并C3-C10环烃基、4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;
上述C6-C10芳基、4-10元杂环基、4-10杂芳基、C1-C10烷基、C2-C10烯基、C1-C10烷酰基、C3-C8内酰胺基、4-10元杂环基或4-10元杂芳基并C3-C10环烃基、4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自4-10元杂环基、腈基、羧基、C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、卤素、三氟甲基、-C(O)OC1-C10烷基、-C(O)NR15R16、-SO2NR15R16、-NR15R16、-NR15SO2R16、C1-C10烷基磺酰基、羟基中的取代基取代;
(7)R5和R6与它们相连的X共同构成氨基葡萄糖基;氨基酸残基;氨基酸酯残基;或氨基酰胺残基,且非必须地被一个或多个选自C1-C6烷基、C1-C6烷基取代的氨基、C1-C10烷酰基、苄基、苄氧羰基和叔丁氧羰基中的取代基取代;
(8)R5和R6与连接它们的X一起形成4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基、4-10元杂环基、C6-C10芳基并4-10元杂环基或4-10元杂芳基、C6-C10芳基、C3-C10环烃基、C3-C10环烃基并C3-C10环烃基、C3-C10环烃基并C6-C10芳基、C6-C10芳基并C3-C10环烃基、4-10元杂芳基、4-10元杂环基螺环、4-10元杂芳基螺环、4-10元杂环基或4-10元杂芳基并C3-C10环烃基、C3-C10环烃基并4-10元杂环基或4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]、或者[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[C6-C10芳基];上述基团可非必须地被一个或多个R’取代,R’选自-(CH2)mR10;-(CH2)mCO(CH2)nR10;-(CH2)mO(CH2)nR10;-(CH2)mNHC(O)(CH2)nR10;和-(CH2)mNSO2(CH2)nR10;其中,m和n各自独立地为0-5的整数;
R10为氢、卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NH2、、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或上述氨基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NH2、、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、、腈基、羧基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NR15R16、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;
R15、R16各自独立地为H;C1-C10烷基;C3-C10环烷基;4-10元杂环基;4-10元杂芳基;或者R15、R16与连接它们的N原子一起形成4-10元杂环基;4-10元杂芳基;其中,所述C1-C10烷基、C3-C10环烷基、4-10元杂环基和4-10元杂芳基可非必须地被1个或多个卤素;羟基;腈基;氨基;C1-C10烷基;=O(氧代);=S(硫代);C1-C10烷氧基取代;
在另一优选例中,通式I所示的β-氨基羰基类化合物还具有以下一个或多个特征:
(1)A为苯基、吡啶基或环戊二烯基;
(2)R1、R2、R3和R4各自独立地为H、卤素、三氟甲基、羟基、腈基、氨基、C1-C10烷基;
(3)W为CH;
(4)Q为C;
(5)R8为-(CH2)mR12;其中,R12为H、卤素、C1-C10烷基;q为0-4的整数;m为0-5的整数;
(6)Y为CR7,其中,R7为-(CH2)mR11,R11为H、卤素,m为0-5的整数。
在所述通式I中,通式I所示的化合物优选为通式IA所示的化合物:
其中,R1、R2、R3、R4、R5、R6、R8、X和q的定义同其在通式I中的定义;
R7为-(CH2)mR11、-(CH2)mO(CH2)nR11或-(CH2)mNHR11;
其中,R11为H;卤素;硝基;腈基;羧基;-C(O)OC1-C4烷基;C2-C4烯基;C2-C4炔基;C1-C4烷酰基;C1-C4烷基磺酰基;氨基C1-C4烷酰基;C1-C4烷基;C6-C10芳基;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C4烷基、C2-C4烯基、C2-C4炔基、C1-C4烷酰基、C1-C4烷基磺酰基、氨基C1-C4烷酰基、C1-C4烷基、C6-C10芳基、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、C1-C4烷酰基、C1-C4烷基磺酰基、=O(氧代)、=S(硫代)、C1-C4烷基中的取代基取代;
其中,m和n各自独立地为0-5的整数。
在所述通式I中,通式IA所示的化合物进一步优选为通式IB所示的化合物:
其中,
X为N或CR7;
R1、R2、R3和R4各自独立地优选为H;卤素;三氟甲基;羟基;硝基;腈基;羧基;-C(O)OC1-C4烷基;氨基;C1-C4烷氧基;C1-C4烷基;C1-C4烷酰基;C1-C4烷酰氧基;磺酰基;或C1-C4烷基磺酰基;上述-C(O)OC1-C4烷基、氨基、C1-C4烷氧基、C1-C4烷基、C1-C4烷酰基、C1-C4烷酰氧基、磺酰基或C1-C4烷基磺酰基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷基、C1-C4烷氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、C1-C4烷酰基、磺酰基、C1-C4烷基磺酰基、苯基和苯甲基中的取代基取代;
R5和R6各自独立地为-(CH2)mR9;-(CH2)mCO(CH2)nR9;或-[(CH2)iO]jH,其中i=1~5的整数,j=1~3的整数,R9为H;卤素;羟基;硝基;氨基;腈基;羧基;-C(O)OC1-C4烷基;C1-C4烷酰基;C1-C4烷基磺酰基;C1-C4烷基;C2-C4烯基;C2-C4炔基;C3-C10环烷基;C3-C8内酰胺基;C1-C4烷氨基磺酰基;C1-C4烷氨酰基;C6-C10芳酰基;C1-C4烷氧基;C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16;C6-C10芳基;4-10元杂环基;4-10元杂芳基;4-10元杂环基或4-10元杂芳基并C3-C8环烃基;或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;上述氨基、-C(O)OC1-C4烷基、C1-C4烷酰基、C1-C4烷基磺酰基、C1-C4烷基、C2-C4烯基、C2-C4炔基、C3-C10环烷基、C3-C8内酰胺基、C1-C4烷氨基磺酰基、C1-C4烷氨酰基、C6-C10芳酰基、C1-C4烷氧基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C3-C8环烃基或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C4烷氧基、-C(O)OC1-C4烷基、-C(O)NR15R16、C1-C4烷酰基、C1-C4烷基磺酰基、-SO2NR15R16、-NR15SO2R16、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;上述C6-C10芳基、C6-C10芳酰基和C6-C10芳基磺酰基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C4烷氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NR15R16、C1-C4烷酰基、C1-C4烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基和C6-C10芳基C1-C4烷基中的取代基取代;
或者,R5和R6与连接它们的X一起形成C6-C10芳基;C3-C10环烃基;C3-C10环烃基并C3-C10环烃基;C3-C10环烃基并C6-C10芳基;C6-C10芳基并C3-C10环烃基;4-10元杂环基;4-10元杂芳基;4-10元杂环基螺环;4-10元杂芳基螺环;4-10元杂环基或4-10元杂芳基并C3-C10环烃基;C3-C10环烃基并4-10元杂环基或4-10元杂芳基;4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;C6-C10芳基并4-10元杂环基或4-10元杂芳基;4-10元杂环基或4-10元杂芳基并C6-C10芳基;[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基];或者[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[C6-C10芳基];上述基团可非必须地被一个或多个R’取代,R’选自-(CH2)mR10;-(CH2)mCO(CH2)nR10;-(CH2)mO(CH2)nR10;-(CH2)mNHC(O)(CH2)nR10;和-(CH2)mNSO2(CH2)nR10;
其中,R10为氢、卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷氧基、C6-C10芳氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NH2、C1-C4烷酰基、C1-C4烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或上述氨基、C1-C4烷氧基、C6-C10芳氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NH2、、C1-C4烷酰基、C1-C4烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C4烷氧基、C6-C10芳氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NR15R16、C1-C4烷酰基、C1-C4烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;
R15、R16各自独立地为H;C1-C4烷基;C3-C10环烷基;4-10元杂环基;4-10元杂芳基;或者R15、R16与连接它们的N原子一起形成4-10元杂环基;4-10元杂芳基;其中,所述C1-C4烷基、C3-C10环烷基、4-10元杂环基和4-10元杂芳基可非必须地被1个或多个卤素;羟基;腈基;氨基;C1-C4烷基;=O(氧代);=S(硫代);C1-C4烷氧基取代;
R7为-(CH2)mR11、-(CH2)mO(CH2)nR11或-(CH2)mNHR11;
其中,R11为H;卤素;硝基;腈基;羧基;-C(O)OC1-C4烷基;C2-C4烯基;C2-C4炔基;C1-C4烷酰基;C1-C4烷基磺酰基;氨基C1-C4烷酰基;C1-C4烷基;C6-C10芳基;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C4烷基、C2-C4烯基、C2-C4炔基、C1-C4烷酰基、C1-C4烷基磺酰基、氨基C1-C4烷酰基、C1-C4烷基、C6-C10芳基、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、C1-C4烷酰基、C1-C4烷基磺酰基、=O(氧代)、=S(硫代)和C1-C4烷基中的取代基取代;
R8为-(CH2)mR12、-(CH2)mO(CH2)nR12或-(CH2)mNHR12;
其中,R12优选为H;卤素;硝基;腈基;羧基;=O(氧代);=S(硫代);-C(O)OC1-C4烷基;C2-C4烯基;C2-C4炔基;C1-C4烷酰基;C1-C4烷基磺酰基;氨基C1-C4烷酰基;C1-C4烷基;Ph(CH2)m-;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C4烷基、C2-C4烯基、C2-C4炔基、C1-C4烷酰基、C1-C4烷基磺酰基、氨基C1-C4烷酰基、C1-C4烷基、Ph(CH2)m-、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、C1-C4烷酰基、C1-C4烷基磺酰基、=O(氧代)、=S(硫代)和C1-C4烷基中的取代基取代;R12进一步优选为H;卤素;=O(氧代);C1-C4烷酰基;C1-C4烷基;Ph(CH2)m-;吲哚;二氢吲哚;吡咯;呋喃;噻吩;噻唑;咪唑;噁唑;异噁唑;吡唑;吡啶;吡嗪;嘧啶;哒嗪;吡喃;吲哚;或喹啉;R10更优选为H;卤素;=O(氧代);C1-C4烷基;苯基;苄基;吲哚;二氢吲哚;或吡咯;R12最优选为H;
m和n各自独立地优选为0-3的整数;最优选为0、1或2;q优选为0-2的整数。
在所述通式I、通式IA或通式IB所示的化合物中,
其中,在R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11和R12的定义中,优选地,
所述C1-C10烷基优选为甲基;乙基;丙基;异丙基;丁基;异丁基或叔丁基;
所述C6-C10芳基优选苯基;
所述C3-C10环烃基优选为以下基团:
所述C3-C10环烃基并C3-C10环烃基优选为以下基团:
所述C3-C10环烃基并C6-C10芳基或C6-C10芳基并C3-C10环烃基优选为以下基团:
所述4-10元杂环基或4-10元杂芳基含有1-4个选自N、S和O的杂原子,优选为以下基团:
所述4-10元杂环基螺环或杂芳基螺环优选为以下基团:
所述[4-10元杂环基或4-10元杂芳基]并[C3-C10环烃基]或者[C3-C10环烃基]并[4-10元杂环基或4-10元杂芳基]优选为以下基团:
所述[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]优选为以下基团:
所述[4-10元杂环基或4-10元杂芳基]并[C6-C10芳基]或者[C6-C10芳基]并[4-10元杂环基或4-10元杂芳基]优选为以下基团:
所述[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]优选为以下基团:
所述[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[C6-C10芳基]优选为以下基团:
上述各环可通过环上任意位置与其他基团相连,也可以在任意位置被如上所定义的取代基所取代。
在所述通式I中,通式IA或IB所示的化合物更进一步优选为通式IA-1、IA-2、IA-3、IA-5、IB-1、IB-2、IB-3或IB-5所示的化合物:
其中,Z为N原子或C原子;
R1、R2、R3和R4各自独立地更优选为H;F;Cl;Br;三氟甲基;羟基;腈基;氨基;C1-C4烷氧基;C1-C4烷基;或C1-C4烷酰基;最优选为H或卤素;
R1和R4最优选为H,R2和R3最优选为F;
R’为-(CH2)mR10;-(CH2)mCO(CH2)nR10;-(CH2)mO(CH2)nR10;-(CH2)mNHC(O)(CH2)nR10;或-(CH2)mNSO2(CH2)nR10;m优选为0-3的整数;最优选为0、1或2;
其中,所述R10更优选为氢、卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷氧基、苯氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NH2、C1-C4烷酰基、C1-C4烷基磺酰基、苯磺酰基、苯甲酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、苄基、=O(氧代)、=S(硫代)、苯基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或上述氨基、C1-C4烷氧基、苯氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NH2、C1-C4烷酰基、C1-C4烷基磺酰基、苯磺酰基、苯甲酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、苄基、=O(氧代)、=S(硫代)、苯基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C4烷氧基、C6-C10芳氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NR15R16、C1-C4烷酰基、C1-C4烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;
R15、R16各自独立地为H;C1-C4烷基;C3-C10环烷基;4-10元杂环基;4-10元杂芳基;或者R15、R16与连接它们的N原子一起形成4-10元杂环基;4-10元杂芳基;其中,所述C1-C4烷基、C3-C10环烷基、4-10元杂环基和4-10元杂芳基可非必须地被1个或多个卤素;羟基;腈基;氨基;C1-C4烷基;=O(氧代);=S(硫代);C1-C4烷氧基取代;
其中,通式IA-1或IB-1所示的化合物中,R’最优选为H;F;Cl;Br或三氟甲基,
或者通式I、通式IA或通式IB所示的化合物优选为通式IA-4或IB-4所示的化合物:
其中,R1、R2、R3和R4定义同其在通式IA-1中的定义;
R5和R6各自独立地为-(CH2)mR9;-(CH2)mCO(CH2)nR9;或-[(CH2)iO]jH,其中i=1~5的整数,j=1~3的整数,R9更优选为H;羟基;腈基;C2-C4烯基;C6-C10芳酰基;C6-C10芳基;4-10元杂环基;4-10元杂芳基;4-10元杂环基或4-10元杂芳基并C3-C8环烃基;或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;上述C2-C4烯基、C6-C10芳酰基、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C3-C8环烃基或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C4烷氧基、-C(O)OC1-C4烷基、-C(O)NR15R16、C1-C4烷酰基、C1-C4烷基磺酰基、-SO2NR15R16、-NR15SO2R16、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代。
在所述通式I所示的化合物中,特别优选的具体化合物包括以下化合物,或其互变异构体、对映体、消旋体或其药学上可接受的盐:
一类优选的具体化合物为实施例化合物1至实施例化合物378,或其互变异构体、对映体、消旋体或其药学上可接受的盐。
其中,所述药学上可接受的盐为所述化合物与选自以下的酸形成的盐:磷酸、苹果酸、乳酸、马来酸、盐酸、甲磺酸、硫酸、柠檬酸、酒石酸、乙酸或三氟乙酸,优选为磷酸盐、盐酸盐或三氟乙酸盐。
通式I所示的化合物可含有一个或多个手性中心,因此可存在立体异构体,即对映异构体、非对映异构体或其混合物。若通式I所示的化合物中含有链烯基或亚烯基,则还可以存在顺式(E)和反式(Z)异构现象。因此,本发明式I所示的化合物可以为单个异构体或各异构体的混合物。
利用常规工艺可以实现非对映异构体或顺式和反式异构体的分离,例如通式I所示的化合物或其适合的盐或衍生物的立体异构体的混合物的分步结晶、色谱或HPLC。通式I所示的化合物还可以这样制备:从对应的旋光纯中间体制备,或者利用适合的手性载体拆分对应的外消旋物,例如通过HPLC或者分步结晶由对应的外消旋物与适合的旋光活性酸或碱的反应所生成的非对映异构盐。
通式I所示的化合物可存在互变异构体的形式,而本发明包括了其混合物和单一的互变异构体。
本发明包括通式I所示的化合物的放射标记衍生物,这些衍生物适用于生物学研究。
本发明提供了通式I所示的化合物的药用盐,例如,与无机酸如盐酸、氢溴酸、氢碘酸、硫酸和磷酸,与有机羧酸或有机磺酸形成的无毒酸加成盐,优选磷酸、苹果酸、乳酸、马来酸、盐酸、甲磺酸、硫酸、柠檬酸、酒石酸、乙酸或三氟乙酸,更优选为磷酸盐、甲磺酸盐、盐酸盐或三氟乙酸盐。通式I所示的化合物还可与碱反应提供药用金属盐,特别是无毒碱金属盐(例如钠盐和钾盐)。
本发明包括通式I所示的化合物的任何前药形式。
本发明还包括通式I的化合物的可药用溶剂化物(例如水合物)。(这里是通式I的溶剂化物)
本发明也包括通式I所示的化合物的可药用氧化物,及其可药用盐和可药用溶剂化物。(这里是可药用氧化物的盐及溶剂化物)
本发明还包括通式I所示的化合物和各种盐的多种晶型。
本发明的另一个目的是提供通式I化合物的制备方法。
本发明通式1所示化合物可通过如下的方法制得,然而该方法的条件,例如反应物、溶剂、碱、所用化合物的量、反应温度、反应所需时间等不限于下面的说明。
通常,本发明方法包括在合适的惰性溶剂中,在合适的反应温度(如-80℃至回流温度,较佳地-20至回流温度)下,反应一段时间(如0.1-72小时,较佳地0.2-24小时)。此外,本发明化合物可以任选将在本说明书中描述的或本领域已知的各种合成方法组合起来而方便的制得。
典型地,本发明方法包括:
(1)方法一:
通式I化合物可以由通式II化合物经过还原氨化反应得到,
其中,A、R1、R2、R3、R4、R5、R6、R8、W、Q、Y和X的定义同其在通式I中的定义;
所述还原氨化反应可以在氨甲醇/乙酸铵、氰基硼氢化钠存在的条件下进行。
其中,通式II化合物可以通过通式III化合物与通式S化合物反应得到:
其中,A、R1、R2、R3、R4、R5、R6、R8、W、Q、Y和X的定义同其在通式I中的定义;R13为羟基、卤素、C1-C10烷氧基、C6-C10芳氧基或C1-C10烷酰氧基;
所述通式III化合物与通式S化合物的反应可以在碱性条件下进行;
其中,通式III化合物可以通过通式V化合物制备,或者通过通式IV化合物制备:
其中,A、R1、R2、R3、R4、W、Q和Y的定义同其在通式I中的定义;R13为卤素、C1-C10烷氧基、C6-C10芳氧基或C1-C10烷酰氧基。
其中,当通式III化合物通过通式V化合物制备时,通式V化合物可与丙二酸单烷基酯的钾盐进行缩合消除反应,得到产物通式III化合物;当通式III化合物通过通式IV化合物制备时,通式V化合物先与米氏酸在缩合剂存在下发生缩合反应得到通式IV化合物,然后通式IV化合物在酸性条件下进行开环脱羧反应得到产物通式III化合物;
通式V化合物可以由市场购买,或者参照下述式VA化合物的制备方法制备,
(2)方法二:
本发明还提供了通式I化合物的另一种制备方法,所述方法包括:
通式I化合物可以由通式VI化合物经过脱保护基反应得到,
其中,A、R1、R2、R3、R4、R5、R6、R8、W、Q、Y和X的定义同其在通式I中的定义;R14为氨基保护基,优选为苄氧羰基或叔丁氧羰基;
所述脱保护基的反应可以在酸性条件下进行,得到通式I化合物或通式I化合物的盐,该通式I化合物的盐在碱性条件下游离得到通式I化合物;
通式VI化合物可以通过通式VII化合物与通式S化合物制备得到:
其中,A、R1、R2、R3、R4、R5、R6、R8、W、Q、Y和X的定义同其在通式I中的定义;R14为氨基保护基,优选为苄氧羰基或叔丁氧羰基;
所述式VII化合物与通式S化合物经缩合反应或者酰化反应得到通式VI化合物,反应可以在碱性条件下进行,也可以在缩合剂存在条件下进行;
其中,通式VII化合物通过式III化合物经以下方法制备:
其中,A、R1、R2、R3、R4、R8、W、Q、Y和X的定义同其在通式I中的定义;R13为卤素、C1-C10烷氧基、C6-C10芳氧基或C1-C10烷酰氧基;R14为氨基保护基,优选为苄氧羰基或叔丁氧羰基;
上述通式III化合物进行还原氨化反应得到氨基物(通式IX化合物),然后通式IX化合物的氨基用保护基团保护得到通式VIII化合物,最后通式VIII化合物进行水解反应脱保护基得到产物通式VII化合物,还原氨化条件、脱保护基条件可参照方法一;
其中,通式III化合物的制备方法参见方法一,
(3)方法三:当R8为氧代或取代氨基时,可由R8=H的通式V化合物经官能团变换得到R8为氧代或取代氨基的通式V化合物,再参照方法一得到通式I化合物,
(4)方法四:通式I化合物还可以由其他通式I化合物经过官能团变换得到。
优选地,当通式I化合物中的A环为苯环时,通式IA化合物通过以下方法制备:
(1)方法一:
其中,通式IIIA化合物可以通过通式V化合物制备:
通式VA化合物可以由市场购买,或者由以下方法制备:
当R7为H时,通式VA化合物可由通式IXA化合物参照文献(J.Med.Chem.2003,46,399-408)方法制备得到通式XA化合物,通式XA化合物经羧基化得到式VA’化合物:
其中,通式IXA化合物可由市场购买得到;
当R7不为H时,通式VA化合物可由通式VA’化合物(R7=H)经酯化后与R7X反应制备得到通式XIA化合物后再水解制备通式VA化合物。其中,R7X中的X为卤素,
(2)方法二:
通式IA化合物可以通过通式IIIA化合物经以下步骤制备,具体制备方法同前述通式I化合物的制备方法(方法二);
其中通式IIIA化合物的制备方法同通式III化合物的制备方法,
(3)方法三:当R8为氧代或取代氨基时,可由R8=H的通式V化合物经官能团变换得到R8为氧代或取代氨基的通式V化合物,再参照方法一得到通式I化合物,
(4)方法四:通式I化合物还可以由其他通式I化合物经过官能团变换得到。
单一手性异构体的通式I化合物可通过以下方式制备:
(1)方法一:通式I化合物经过柱层析,分离非对映异构体,分别得到两对对映体,该对对映体再经手性制备柱拆分得到单一光学异构体的通式I化合物,
(2)方法二:或者,通式VIIIA化合物经手性制备柱拆分得到光学异构体通式VIIIA’化合物和式VIIIA”化合物,
通式VIIIA’化合物或通式VIIIA”化合物再与通式S化合物反应,得到单一手性的通式IA化合物,具体制备方法同前述通式I化合物的消旋体的制备方法。
本发明还包括将所述得到的通式I化合物在酸的有机溶剂中反应,得到其酸加成产物盐,其中所述的酸选自磷酸、苹果酸、乳酸、马来酸、盐酸、甲磺酸、硫酸、柠檬酸、酒石酸、乙酸或三氟乙酸,优选磷酸、盐酸或三氟乙酸。
本发明的还一目的是提供一种通式II、III、VI或VII所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐:
其中,
A选自C6-C10芳基、饱和或不饱和C3-C10环烃基、4-10元杂环基或4-10元杂芳基;所述杂环基或杂芳基含有1-4个选自N、S和O的杂原子;
W为N、S、O或C1-C4直链烃基;
Q为N、S、O或C原子;
W与Q之间的虚线存在或不存在,存在时表示此处是不饱和键,不存在时表示此处是饱和键,优选为不存在;
Y为N或CR7;
X为N或CR7;
R1、R2、R3和R4各自独立地为H;卤素;三氟甲基;羟基;硝基;腈基;羧基;-C(O)OC1-C10烷基;氨基;C1-C10烷氧基;C1-C10烷基;C1-C10烷酰基(即-C(O)C1-C10烷基);C1-C10烷酰氧基(即-OC(O)C1-C10烷基);磺酰基;C1-C10烷基磺酰基;C6-C10芳基;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C10烷基、氨基、C1-C10烷氧基、C1-C10烷基、C1-C10烷酰基、C1-C10烷酰氧基、磺酰基、C1-C10烷基磺酰基、C6-C10芳基、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷基、C1-C10烷氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、C1-C10烷酰基、磺酰基、C1-C10烷基磺酰基、苯基和苯甲基中的取代基取代;
R5和R6各自独立地为-(CH2)mR9;-(CH2)mCO(CH2)nR9;或-[(CH2)iO]jH,其中i=1~5的整数,j=1~3的整数,R9为H;卤素;羟基;硝基;氨基;腈基;羧基;-C(O)OC1-C10烷基;C1-C10烷酰基;C1-C10烷基磺酰基;C1-C10烷基;C2-C10烯基;C2-C10炔基;C3-C10环烷基;C3-C8内酰胺基;C1-C10烷氨基磺酰基;C1-C10烷氨酰基;C6-C10芳酰基;C1-C10烷氧基;C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16;C6-C10芳基;4-10元杂环基;4-10元杂芳基;4-10元杂环基或4-10元杂芳基并C3-C10环烃基;或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;上述氨基、-C(O)OC1-C10烷基、C1-C10烷酰基、C1-C10烷基磺酰基、C1-C10烷基、C2-C10烯基、C2-C10炔基、C3-C10环烷基、C3-C8内酰胺基、C1-C10烷氨基磺酰基、C1-C10烷氨酰基、C6-C10芳酰基、C1-C10烷氧基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C3-C10环烃基或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NR15R16、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;上述C6-C10芳基、C6-C10芳酰基和C6-C10芳基磺酰基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C10烷氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NR15R16、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基和C6-C10芳基C1-C10烷基中的取代基取代;
或者,R5和R6与它们相连的X共同构成氨基葡萄糖基;氨基酸残基;氨基酸酯残基;或氨基酰胺残基,且非必须地被一个或多个选自C1-C6烷基、C1-C6烷基取代的氨基、C1-C10烷酰基、苄基、苄氧羰基和叔丁氧羰基中的取代基取代;
或者,R5和R6与连接它们的X一起形成C6-C10芳基;C3-C10环烃基;C3-C10环烃基并C3-C10环烃基;C3-C10环烃基并C6-C10芳基;C6-C10芳基并C3-C10环烃基;4-10元杂环基;4-10元杂芳基;4-10元杂环基螺环;4-10元杂芳基螺环;4-10元杂环基或4-10元杂芳基并C3-C10环烃基;C3-C10环烃基并4-10元杂环基或4-10元杂芳基;4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;C6-C10芳基并4-10元杂环基或4-10元杂芳基;4-10元杂环基或4-10元杂芳基并C6-C10芳基;[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基];或者[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[C6-C10芳基];上述基团可非必须地被一个或多个R’取代,R’选自-(CH2)mR10;-(CH2)mCO(CH2)nR10;-(CH2)mO(CH2)nR10;-(CH2)mNHC(O)(CH2)nR10;和-(CH2)mNSO2(CH2)nR10;
其中,R10为氢、卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NH2、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或上述氨基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NH2、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C10烷氧基、C6-C10芳氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、-C(O)NR15R16、C1-C10烷酰基、C1-C10烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C10烷基、羟基C1-C10烷基、氨基C1-C10烷基、C6-C10芳基C1-C10烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;
R15、R16各自独立地为H;C1-C10烷基;C3-C10环烷基;4-10元杂环基;4-10元杂芳基;或者R15、R16与连接它们的N原子一起形成4-10元杂环基;4-10元杂芳基;其中,所述C1-C10烷基、C3-C10环烷基、4-10元杂环基和4-10元杂芳基可非必须地被1个或多个卤素;羟基;腈基;氨基;C1-C10烷基;=O(氧代);=S(硫代);C1-C10烷氧基取代;
R7为-(CH2)mR11、-(CH2)mO(CH2)nR11或-(CH2)mNHR11;
其中,R11为H;卤素;硝基;腈基;羧基;-C(O)OC1-C10烷基;C2-C10烯基;C2-C10炔基;C1-C10烷酰基;C1-C10烷基磺酰基;氨基C1-C10烷酰基;C1-C10烷基;C6-C10芳基;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C10烷基、C2-C10烯基、C2-C10炔基、C1-C10烷酰基、C1-C10烷基磺酰基、氨基C1-C10烷酰基、C1-C10烷基、C6-C10芳基、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、C1-C10烷酰基、C1-C10烷基磺酰基、=O(氧代)、=S(硫代)和C1-C10烷基中的取代基取代;
R8为-(CH2)mR12、-(CH2)mO(CH2)nR12或-(CH2)mNHR12;
其中,R12为H;卤素;硝基;腈基;羧基;=O(氧代);=S(硫代);-C(O)OC1-C10烷基;C2-C10烯基;C2-C10炔基;C1-C10烷酰基;C1-C10烷基磺酰基;氨基C1-C10烷酰基;C1-C10烷基;Ph(CH2)m-;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C10烷基、C2-C10烯基、C2-C10炔基、C1-C10烷酰基、C1-C10烷基磺酰基、氨基C1-C10烷酰基、C1-C10烷基、Ph(CH2)m-、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C10烷氧基、C1-C10烷酰氧基、-C(O)OC1-C10烷基、C1-C10烷酰基、C1-C10烷基磺酰基、=O(氧代)、=S(硫代)和C1-C10烷基中的取代基取代;
m和n各自独立地为0-5的整数,q选自0-4的整数;
R13为卤素、C1-C10烷氧基、C6-C10芳氧基或C1-C10烷酰氧基;
R14为氨基保护基,优选为苄氧羰基或叔丁氧羰基。
所述通式II、III、VI或VII所示的化合物优选为通式IIA、IIIA、VIA或VIIA化合物:
其中,R1、R2、R3、R4、R5、R6、R8、R12、R13、X和q的定义同其在通式II、III、VI或VII中的定义;
R7为-(CH2)mR11、-(CH2)mO(CH2)nR11或-(CH2)mNHR11;
其中,R11为H;卤素;硝基;腈基;羧基;-C(O)OC1-C4烷基;C2-C4烯基;C2-C4炔基;C1-C4烷酰基;C1-C4烷基磺酰基;氨基C1-C4烷酰基;C1-C4烷基;C6-C10芳基;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C4烷基、C2-C4烯基、C2-C4炔基、C1-C4烷酰基、C1-C4烷基磺酰基、氨基C1-C4烷酰基、C1-C4烷基、C6-C10芳基、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、C1-C4烷酰基、C1-C4烷基磺酰基、=O(氧代)、=S(硫代)和C1-C4烷基中的取代基取代;
其中,m和n各自独立地为0-5的整数。
所述通式IIA、IIIA、VIA或VIIA所示的化合物更优选为通式IIB、IIIB、VIB或VIIB所示的化合物:
X为N或CR7:
R1、R2、R3和R4各自独立地优选为H;卤素;三氟甲基;羟基;硝基;腈基;羧基;-C(O)OC1-C4烷基;氨基;C1-C4烷氧基;C1-C4烷基;C1-C4烷酰基;C1-C4烷酰氧基;磺酰基;或C1-C4烷基磺酰基;上述-C(O)OC1-C4烷基、氨基、C1-C4烷氧基、C1-C4烷基、C1-C4烷酰基、C1-C4烷酰氧基、磺酰基或C1-C4烷基磺酰基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷基、C1-C4烷氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、C1-C4烷酰基、磺酰基、C1-C4烷基磺酰基、苯基和苯甲基中的取代基取代。
R1、R2、R3和R4各自独立地更优选为H;卤素;羟基;腈基;氨基;C1-C4烷氧基;C1-C4烷基;或C1-C4烷酰基;最优选为H或卤素;
R5和R6各自独立地为-(CH2)mR9或-(CH2)mCO(CH2)nR9,其中,R9为H;卤素;羟基;硝基;氨基;腈基;羧基;-C(O)OC1-C4烷基;C1-C4烷酰基;C1-C4烷基磺酰基;C1-C4烷基;C2-C4烯基;C2-C4炔基;C6-C10芳酰基;C1-C4烷氧基;C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16;C6-C10芳基;4-10元杂环基;4-10元杂芳基;4-10元杂环基或4-10元杂芳基并C3-C8环烃基;或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;上述氨基、-C(O)OC1-C4烷基、C1-C4烷酰基、C1-C4烷基磺酰基、C1-C4烷基、C2-C4烯基、C2-C4炔基、C6-C10芳酰基、C1-C4烷氧基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C3-C8环烃基或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C4烷氧基、-C(O)OC1-C4烷基、-C(O)NR15R16、C1-C4烷酰基、C1-C4烷基磺酰基、-SO2NR15R16、-NR15SO2R16、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;R9更优选为H;羟基;腈基;C2-C4烯基;C6-C10芳酰基;C6-C10芳基;4-10元杂环基;4-10元杂芳基;4-10元杂环基或4-10元杂芳基并C3-C8环烃基;或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基;上述C2-C4烯基、C6-C10芳酰基、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C3-C8环烃基或者4-10元杂环基或4-10元杂芳基并4-10元杂环基或4-10元杂芳基可进一步被卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C4烷氧基、-C(O)OC1-C4烷基、-C(O)NR15R16、C1-C4烷酰基、C1-C4烷基磺酰基、-SO2NR15R16、-NR15SO2R16、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;
或者,R5和R6与连接它们的X一起形成C6-C10芳基;C3-C10环烃基;C3-C10环烃基并C3-C10环烃基;C3-C10环烃基并C6-C10芳基;C6-C10芳基并C3-C10环烃基;4-10元杂环基;4-10元杂芳基;4-10元杂环基螺环;4-10元杂芳基螺环;[4-10元杂环基或4-10元杂芳基]并[C3-C10环烃基];[C3-C10环烃基]并[4-10元杂环基或4-10元杂芳基];[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基];[C6-C10芳基]并[4-10元杂环基或4-10元杂芳基];[4-10元杂环基或4-10元杂芳基]并[C6-C10芳基];[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基];[4-10元杂环基或4-10元杂芳基]并[4-10元杂环基或4-10元杂芳基]并[C6-C10芳基];上述基团可非必须地被一个或多个R’取代,R’选自-(CH2)mR10;-(CH2)mCO(CH2)nR10;-(CH2)mO(CH2)nR10;-(CH2)mNHC(O)(CH2)nR10;和-(CH2)mNSO2(CH2)nR10;
其中,所述R10为氢、卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷氧基、C6-C10芳氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NH2、C1-C4烷酰基、C1-C4烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或上述氨基、C1-C4烷氧基、C6-C10芳氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NH2、C1-C4烷酰基、C1-C4烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、-NR15R16、腈基、羧基、C1-C4烷氧基、C6-C10芳氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NR15R16、C1-C4烷酰基、C1-C4烷基磺酰基、C6-C10芳基磺酰基、-SO2NR15R16、-NR15SO2R16、C6-C10芳酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、C6-C10芳基C1-C4烷基、=O(氧代)、=S(硫代)、C6-C10芳基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基和4-10元杂芳酰基中的取代基取代;所述R10更优选为卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷氧基、苯氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、-C(O)NH2、C1-C4烷酰基、C1-C4烷基磺酰基、苯磺酰基、-SO2NR15R16、-NR15SO2R16、苯甲酰基、C1-C4烷基、羟基C1-C4烷基、氨基C1-C4烷基、苄基、=O(氧代)、=S(硫代)、苯基、4-10元杂环基、4-10元杂芳基、4-10元杂环基或4-10元杂芳基并C6-C10芳基、4-10元杂环酰基、4-10元杂芳酰基或
R15、R16各自独立地为H;C1-C4烷基;C3-C10环烷基;4-10元杂环基;4-10元杂芳基;或者R15、R16与连接它们的N原子一起形成4-10元杂环基;4-10元杂芳基;其中,所述C1-C4烷基、C3-C10环烷基、4-10元杂环基和4-10元杂芳基可非必须地被1个或多个卤素;羟基;腈基;氨基;C1-C4烷基;=O(氧代);=S(硫代);C1-C4烷氧基取代;
R8为-(CH2)mR12、-(CH2)mO(CH2)nR12或-(CH2)mNHR12,
其中,R12优选为H;卤素;硝基;腈基;羧基;=O(氧代);=S(硫代);-C(O)OC1-C4烷基;C2-C4烯基;C2-C4炔基;C1-C4烷酰基;C1-C4烷基磺酰基;氨基C1-C4烷酰基;C1-C4烷基;Ph(CH2)m-;4-10元杂环基;或4-10元杂芳基;上述-C(O)OC1-C4烷基、C2-C4烯基、C2-C4炔基、C1-C4烷酰基、C1-C4烷基磺酰基、氨基C1-C4烷酰基、C1-C4烷基、Ph(CH2)m-、4-10元杂环基或4-10元杂芳基可非必须地被一个或多个选自卤素、三氟甲基、羟基、硝基、氨基、腈基、羧基、C1-C4烷氧基、C1-C4烷酰氧基、-C(O)OC1-C4烷基、C1-C4烷酰基、C1-C4烷基磺酰基、=O(氧代)、=S(硫代)和C1-C4烷基中的取代基取代;R12进一步优选为H;卤素;=O(氧代);C1-C4烷酰基;C1-C4烷基;Ph(CH2)m-;吲哚;二氢吲哚;吡咯;呋喃;噻吩;噻唑;咪唑;噁唑;异噁唑;吡唑;吡啶;吡嗪;嘧啶;哒嗪;吡喃;吲哚;或喹啉;R10更优选为H;卤素;=O(氧代);C1-C4烷基;苯基;苄基;吲哚;二氢吲哚;或吡咯;R12最优选为H;
m和n各自独立地优选为0-3的整数;最优选为0、1或2;q优选为0-2的整数;
R13为卤素、C1-C4烷氧基、C6-C4芳氧基或C1-C4烷酰氧基;
R14为氨基保护基,优选苄氧羰基或叔丁氧羰基。
根据本发明的又一方面,本发明提供了通式I所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐的用途,其作为DPP-4抑制剂的用途,和在制备用于治疗II型糖尿病、高血糖症、肥胖症或胰岛素抵抗症等疾病的药物中的用途。
根据本发明的再一方面,本发明还提供了一种包含治疗有效量的通式I所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐中的一种或多种的药物组合物,其可以作为DPP-4抑制剂,以及该组合物可以任选包含药学上可接受的载体或赋形剂。
在另一优选例中,式I所示的β-氨基羰基类化合物或其药学上可接受的盐在所述药物组合物中的剂量为1~500mg/天。
根据本发明的另一方面,本发明还提供了一种DPP-4抑制剂,其含治疗有效量的通式I所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐中的一种或多种,以及该抑制剂可以任选包含药学上可接受的载体或赋形剂。
该组合物由治疗有效量的一种或多种通式I所示的β-氨基羰基类化合物(或其可药用盐,或它们的可药用溶剂化物)与至少一种可药用辅料组成。药用辅料的选择因施用途径和作用特点而异,通常是填充剂、稀释剂、粘合剂、润湿剂、崩解剂、润滑剂、乳化剂、助悬剂等。式I化合物、其药学上可接受的盐或其溶剂化物在上述组合物中的所占的比例为总重量的0.1%~99.9%,优选1%~99%。
所述药学上可接受的载体是指药学领域常规的药物载体,例如:稀释剂,如水等;填充剂,如淀粉、蔗糖等;粘合剂,如纤维素衍生物、藻酸盐、明胶、聚乙烯吡咯烷酮;湿润剂,如甘油;崩解剂,如琼脂、碳酸钙和碳酸氢钠;吸收促进剂,如季铵化合物;表面活性剂,如十六烷醇;吸附载体,如高岭土和皂粘土;润滑剂,如滑石粉、硬脂酸钙和硬脂酸镁、和聚乙二醇等。另外,还可以在所述药物组合物中加入其它辅剂,如香味剂和甜味剂等。
本发明还提供了通式I所示的β-氨基羰基类化合物、其药学上可接受的盐或其溶剂化物的可药用的组合物的制备方法。通常将通式I所示的β-氨基羰基类化合物、其药学上可接受的盐或其溶剂化物与可药用辅料相混合,经常规的制备方法制成适于一定途径施用的形式(剂型)。剂型包括片剂、胶囊剂、颗粒剂、丸剂、溶液剂、混悬剂、乳剂、软膏、膜剂、霜剂、气雾剂、注射剂、栓剂等。优选片剂和胶囊剂。
本发明化合物的使用剂量一般为每天1~500mg,优选10~100mg,分单次或多次使用。但在必要时,可适当偏离上述剂量。专业人员可根据具体情况和专业知识,确定最佳剂量。这些情况包括疾病的严重程度、患者的个体差异、制剂的特性和给药途径等。
此外,本发明还提供了通式I所示的β-氨基羰基类化合物、其可药用盐或其溶剂化物,或其可药用的组合物作为人用药物的用途。
根据本发明的又一方面,本发明还提供了治疗治疗II型糖尿病、高血糖症、肥胖症或胰岛素抵抗症的方法,所述方法包括施用治疗有效量的通式I所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐中的一种或多种或者本发明的所述药物组合物给患者。
本发明提供的化合物或组合物可以口服、注射(静脉、肌肉、皮下和冠状动脉内)、舌下、经颊、经直肠、经尿道、经阴道、经鼻、吸入或局部途径施用。优选的途径是口服。用于口服时,可以将其制成常规的固体制剂,如片剂、粉剂、粒剂、胶囊等,或制成液体制剂,如水或油悬浮剂,或其它液体制剂,如糖浆等;用于肠外给药时,可将其制成注射用的溶液、水或油性悬浮剂等。
在另一优选例中,该化合物进一步与其他药物(抗糖尿病药物)联用。
根据本发明的再一方面,本发明提供了一种抑制二肽基肽酶IV催化活性的方法,该方法包括将所述的二肽基肽酶与通式I所示的β-氨基羰基类化合物或其互变异构体、对映体、消旋体或其药学上可接受的盐中的一种或多种接触。
本发明还提供了通式I所示的β-氨基羰基类化合物、其可药用盐或其溶剂化物,在制备DPP-4抑制剂的人用药物中的用途。
本发明利用分子对接技术评估设计的化合物对DPP-4的结合能力。在设计中参考了利用碎片生长技术获得的化合物结构,碎片生长采用了综合药物化学三维结构数据库(Comprehensive Medicinal Chemistry,CMC)的分子碎片及发明人收集的其他分子碎片从不同的片段起点进行延伸生长,并通过分子对接技术进行评估。计算结果表明本发明中的化合物具有较好的DPP-4抑制活性,与体外活性实验结果吻合。
体外活性实验结果表明,本发明中的化合物对DPP-4有不同程度的抑制作用;体外选择性实验结果表明,本发明中的化合物对DPP-8和DPP-9有较好的选择性;体内活性实验表明本发明部分化合物显著增强了小鼠口服葡萄糖耐量。
通式I所示的β-氨基羰基类化合物、其药学上可接受的盐或其溶剂化物具有DPP-4抑制活性,更重要的是,部分化合物具有比西他列汀更强的DPP-4抑制活性,更好的选择性,且在体内实验中具有明显的降糖作用。因此本发明提供的化合物可望在临床上表现出更佳的安全性和有效性,临床应用前景广阔。
附图说明
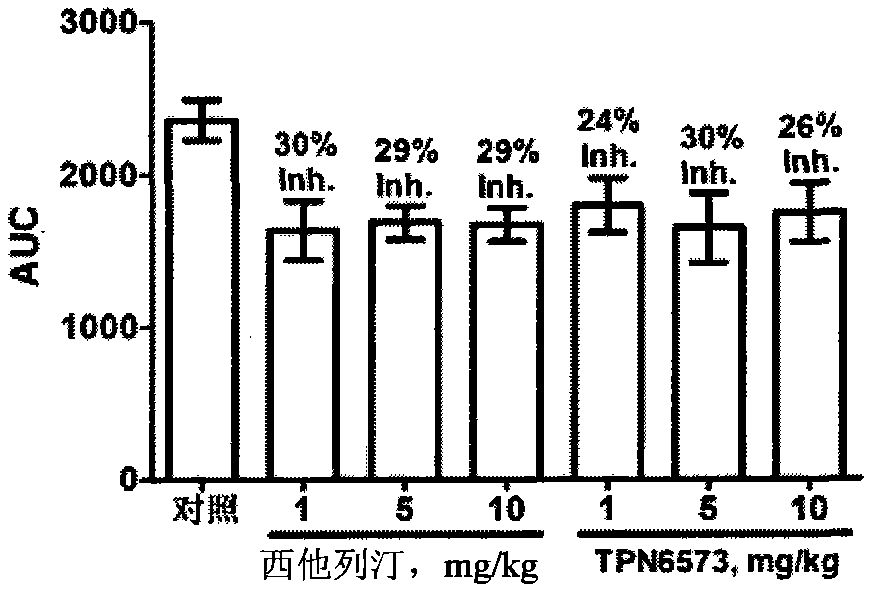
图1(a)和图1(b)为本发明实施例5制备的化合物的口服葡萄糖耐量实验结果图;其中Inh.为抑制(inhibition)。
图2(a)和图2(b)为本发明实施例5制备的化合物的小鼠急性毒性实验结果图。
具体实施方式
下列实施例进一步解释了本发明的化合物及其中间体的合成方法,但并不限制本发明的范围。1H NMR在Mercury-400或Mercury-300核磁共振波谱仪(Varian公司)上完成。常规缩写如下:s,单峰;d,双峰;t,三重峰;q,四重峰;m,多重峰;br,宽峰。
5,6-二氟-1-茚酮是以3.4-二氟苯甲醛为原料,参照文献(J.Med.Chem.2003,46,399-408)方法制备。化合物7-1以5,6-二氟-1-茚酮为原料,参照文献(ORG LETT.2007,9,2915-2918)方法制备。
制备例1:
5,6-二氟-1-茚酮(61g)溶于二氯甲烷,冰浴下加入碘化锌(3.54g),搅拌,滴加三甲基硅氰(183ml),氮气保护,逐渐升至室温,反应2h,二氯甲烷稀释反应液,饱和碳酸氢钠水溶液洗涤有机层,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩。
上步浓缩物溶于冰醋酸(100ml)中,加入氯化亚锡(200g),浓盐酸(100ml),油浴140℃,反应完全后,冷至室温,过滤,二氯甲烷洗去杂质,碱水层冰浴下,3N盐酸调PH=3,二氯甲烷萃取,洗涤有机层,浓缩,浓缩物溶于二氧六烷(100ml),加入40%氢氧化钾溶液,回流,反应完全后,冷至室温,乙酸乙酯/水分层,有机层5%氢氧化钠溶液洗涤,合并有机相,EA洗涤,水相用3N盐酸调pH=2,EA萃取,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩得39g化合物S-1。
1H NMR(300MHZ,CDCl3):δ7.22(1H,dd),7.01(1H,dd),4.02(1H,t),2.99-3.09(1H,m),2.81-2.93(1H,m),2.34-2.51(2H,m).
MS:m/e 197[M+H]-.
制备例2:
丙二酸单乙酯钾盐(81g)悬浮于乙腈(300ml)中,加入三乙胺(94ml),氯化镁(43g),室温搅拌两小时。化合物S-1(42g)悬浮于乙腈(150ml),加入CDI(52g),30min反应完全,加入到上述丙二酸单乙酯钾盐反应液中,反应完全后,加入1M HCl溶液至澄清,分层,蒸干上层,乙酸乙酯溶解;水层用乙酸乙酯萃取,合并乙酸乙酯层,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得46g化合物S-2。
1H NMR(300MHZ,CDCl3):δ7.09(1H,dd),7.02(1H,dd),4.19(2H,q),3.52(1H,s),2.94-3.06(1H,m),2.81-2.93(1H,m),2.27-2.51(2H,m),1.27(3H,t).
MS:m/e 267[M+H]-.
制备例3:
化合物S-2(20g)溶于甲醇(50ml),加入氨甲醇溶液(30ml),加入乙酸铵(16g),65℃下反应,2h反应完全,冷至室温,加入氰基硼氢化钠(9g),加入醋酸(3ml)调pH=5,反应过夜,次日蒸干溶剂,用二氯甲烷溶解,有机层依次用饱和NaHCO3溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得16.5g化合物S-3。
1H NMR(300MHZ,CDCl3):δ7.05(1H,dd),6.98(1H,dd),4.16(2H,q),3.62-3.73(1H,m),3.20(1H,br),2.73-2.97(2H,m),2.27-2.51(2H,m),1.92-2.14(2H,m),1.26(3H,t).
MS:m/e 270[M+H]+.
制备例4:
化合物S-3(7.1g)溶于甲醇(25ml),加入三乙胺(4.5ml),(Boc)2O(6.5g),待反应完全后蒸干甲醇,残留物用乙酸乙酯溶解,依次用KHSO4溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析,得9.0g化合物S-4。
1H NMR(300MHZ,CDCl3):δ7.05(1H,dd),6.98(1H,dd),4.14(2H,q),3.30-3.41(1H,m),2.87-3.00(1H,br),2.70-2.83(1H,m),2.45-2.50(2H,m),2.14-2.27(1H,m),1.84-1.96(1H,m),1.39(9H,s),1.26(3H,t).
制备例5:
化合物S-4(9.0g)溶于甲醇(20ml),氢氧化钠(2.9g)溶于水(10ml)后缓慢加至反应液,室温搅拌,反应完全后蒸干甲醇,于冰水浴中加KHSO4溶液调至pH约为2,用乙酸乙酯萃取,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,得8.74g化合物S-5。
1H NMR(300MHZ,CDCl3):δ7.07(1H,dd),6.97(1H,dd),4.19-4.30(1H,m),3.39(1H,br),2.86-3.01(1H,m),2.71-2.85(1H,m),2.55(2H,d),2.14-2.28(1H,m),1.84-2.01(1H,m),1.40(9H,s).
MS:m/e 340[M+H]-.
制备例6:
将化合物S-5采用HPLC手性制备液相仪(色谱柱型号为AD-H)进行手性拆分,分别得到单一手性异构体S-5a和S-5b。色谱保留时间分别为tR=13.5min,tR=20.0min。
S-5a:比旋光度-21°(C=0.5)。S-5b:比旋光度+21°(C=0.5)。
制备例7:1-(3,5-二硝基苯甲酰基)-哌嗪(S-18)的制备
N-Boc哌嗪(290mg),3.5-二硝基苯甲酸苯甲酸(300mg),HOBT(191mg),N-甲基吗啉(0.17ml)溶于DMF(5ml)中,加入EDCI(407mg),室温搅拌,反应完全,加水,EA萃取,EA层依次用饱和NaHCO3溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得化合物S-18-1(203mg)。
化合物S-18-1(203mg)溶于CH2Cl2,加入CF3COOH(0.5ml),1h反应完全,加入CH2Cl2稀释,依次用饱和NaHCO3溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,浓缩得167mg 1-(3,5-二硝基苯甲酰基)-哌嗪(S-18)。MS:m/e 281[M+H]+.
制备例8:1-(2-乙氧基苯甲酰基)哌嗪(S-19)的制备
N-Boc哌嗪(393mg),邻乙氧基苯甲酰氯(0.25ml),三乙胺溶(0.56ml)于二氯甲烷(5ml),室温搅拌,反应完全后,加入CH2Cl2稀释,依次用1M HCl溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩得372mg化合物S-19-1。
化合物I-2(372mg)溶于CH2Cl2,加入CF3COOH(1.5ml),1h反应完全,加入CH2Cl2稀释,依次用饱和NaHCO3溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩得333mg 1-(2-乙氧基苯甲酰基)哌嗪(S-19)。MS:m/e 235[M+H]+.
制备例9:1-(2-硝基苯甲酰基)哌嗪(S-20)的制备
按照与制备例7相同的方法,以2-硝基苯甲酸为试剂合成1-(2-硝基苯甲酰基)哌嗪(S-20)。MS:m/e 236[M+H]+.
制备例10:1-(3-氯苯甲酰基)哌嗪(S-21)的制备
按照与制备例7相同的方法,以间氯苯甲酸为试剂合成1-(3-氯苯甲酰基)哌嗪(S-21)。
MS:m/e 225[M+H]+.
制备例11:1-(吡啶-2-基-酰基)哌嗪(S-22)的制备
按照与制备例7相同的方法,以2-吡啶甲酸为试剂合成1-(吡啶-2-基-酰基)哌嗪(S-22)。
MS:m/e 192[M+H]+.
制备例12:1-(吡嗪-2-基-酰基)哌嗪(S-23)的制备
按照与制备例7相同的方法,以吡嗪单羧酸为试剂合成1-(吡嗪-2-基-酰基)哌嗪(S-23)。
MS:m/e 193[M+H]+.
制备例13:3-腈基-2-(((S)-吡咯-2-基)甲氧基)吡啶(S-24)的制备
化合物S-24-1(1.5g)溶于CH2Cl2,加入三乙胺(2.5ml),加入Boc2O(3g),反应过夜,加CH2Cl2稀释,有机层依次用1M HCl溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,短柱层析得1.39g化合物S-24-2。
化合物S-24-2(1.38g)溶于THF(10ml),冰浴下滴加BH3-THF(7ml)溶液,反应完全后,冰浴下加入甲醇淬灭,蒸干,EA溶解,EA层依次用饱和NaHCO3溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩得1.28g化合物S-24-3。
NaH(180mg)悬浮于DMF(5ml)中,冰浴下加入化合物S-24-3(250mg)的DMF溶液(3ml),10min后,加入2-氯-3-氰基吡啶(166mg)的DMF溶液(3ml),反应完全,加入NH4Cl溶液淬灭,EA萃取,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得308mg化合物S-24-4。
化合物S-24-34(308mg)溶于CH2Cl2,滴加CF3COOH(1ml),30min反应完全,蒸干,CH2Cl2溶解,依次用饱和NaHCO3溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,短柱层析得184mg 3-腈基-2-(((S)-吡咯-2-基)甲氧基)吡啶(S-24)。MS:m/e 204[M+H]+.
制备例14:3-(甲磺酰基)-N-(((S)-吡咯-2-基)甲基)苯甲酰胺(S-25)的制备
化合物S-25-1(207mg)溶于DMF,依次加入DIPEA(0.9ml),HOBT(210mg),EDCI(298mg),3-甲砜基苯甲酸(207mg),室温搅拌,反应完全后,加入1M HCl溶液,EA萃取,EA层依次用饱和NaHCO3溶液、饱和食盐水洗涤EA层,干燥浓缩,柱层析得141mg化合物S-25-2。
化合物S-25-12(141mg)溶于CH2Cl2,加入CF3COOH(0.2ml),30min反应完全,蒸干,CH2Cl2溶解,有机层依次用饱和NaHCO3溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,短柱层析得104mg 3-(甲磺酰基)-N-(((S)-吡咯-2-基)甲基)苯甲酰胺(S-25)。
MS:m/e 283[M+H]+.
制备例15:N-(((S)-吡咯-2-基)甲基)苯磺酰胺(S-26)的制备
化合物S-26-1(200mg)溶于CH2Cl2,加入三乙胺(0.14ml),冰浴下滴加苯甲磺酰氯(176mg)的CH2Cl2溶液,滴加完毕,撤冰浴,1h反应完全,CH2Cl2稀释,有机层依次用1M HCl溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得310mg化合物S-26-2。
化合物S-26-2(310mg)溶于CH2Cl2,滴加CF3COOH(0.5ml),30min反应完全,蒸干,CH2Cl2溶解,有机层依次用NaHCO3溶液、饱和食盐水洗涤,干燥浓缩,短柱层析得180mg N-(((S)-吡咯-2-基)甲基)苯磺酰胺(S-26)。MS:m/e 241[M+H]+
制备例16:3-氯-N-(((S)-吡咯-2-基)甲基)苯甲酰胺(S-27)的制备
按照与制备例14相同的方法,以间氯苯甲酸为试剂合成3-氯-N-(((S)-吡咯-2-基)甲基)苯甲酰胺(S-27)。MS:m/e 239[M+H]+.
制备例17:化合物S-49的制备
3-甲砜基苯甲酸(60mg)溶于DMF,加入NEt3(60ul),HATU(100mg),反应完全后,加入化合物S-49-1(56mg),反应完全,加入1M HCl溶液,EA萃取,EA层依次用NaHCO3溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得50mg化合物S-49-2。
化合物S-49-2(50mg)溶于CH2Cl2,加入CF3COOH(0.3ml),反应完全后,蒸干得化合物S-49。MS:m/e 269[M+H]+.
制备例18:化合物S-50的制备
按照与制备例18相同的方法,以S-50-1为试剂合成化合物S-50。
MS:m/e 327[M+H]+.
制备例19:化合物S-57的制备
化合物S-57-1(500mg)溶于CH2Cl2,加入NEt3(1.68ml),加入Boc2O(884mg),过夜,反应完全,加入1M HCl溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,浓缩得1.1g化合物S-57-1。
NaH(26mg)悬浮于干燥THF中,冰浴下加入化合物S-57-1(100mg)的THF溶液,10min后,加入2-氯-3-氰基吡啶(74mg)的THF溶液,5h反应完全,加入饱和氯化铵溶液淬灭,蒸干THF,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩得化合物S-57-3。
化合物S-57-3溶于CH2Cl2,加入CF3COOH,反应完全后,蒸干,柱层析得化合物S-57。
MS:m/e 190[M+H]+.
制备例20:化合物S-58的制备
2-哌啶甲酸(1g)溶于甲醇中,加入三乙胺(1.42ml),Boc2O(1.85g),反应过夜,反应完全后蒸干,CH2Cl2溶解,1M HCl溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,浓缩得白色固体,石油醚洗涤得1.59g化合物S-58-1。
化合物S-58-1(500mg)溶于干燥THF,冰浴下加入硼烷四氢呋喃溶液(1ml),反应完全,加入甲醇淬灭,蒸干,柱层析得250mg化合物S-58-2。
化合物S-58-2(40mg)溶于CH2Cl2,加入CF3COOH(0.2ml),1h反应完全,蒸干得化合物S-58。MS:m/e 116[M+H]+.
制备例21:化合物S-62的制备
化合物S-62-1(300mg)溶于甲醇,加入NEt3(0.15ml),Boc2O(229mg),反应完全,蒸干溶剂,EA溶解,EA层依次用1M HCl溶液,饱和氯化钠溶液洗涤,无水硫酸钠干燥,浓缩得330mg化合物S-62-2。
化合物S-62-2(330mg)溶于干燥THF,冰浴下加入硼烷四氢呋喃溶液(2ml),反应完全,加入甲醇淬灭,蒸干,柱层析得150mg化合物S-62-3。
NaH(45mg)悬浮于干燥THF中,冰浴下加入化合物S-62-3(110mg)的THF溶液,10min后,加入2-氯-3-氰基吡啶(52mg)的THF溶液,室温搅拌,18h后反应完全,饱和氯化铵溶液淬灭,蒸干THF,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得40mg化合物S-62-4。
化合物S-62-4(40mg)溶于CH2Cl2,加入CF3COOH(0.2ml),1h反应完全,蒸干得化合物S-62。MS:m/e 294[M+H]+.
制备例22:化合物S-63的制备
化合物S-63-1(150mg)溶于DMF,加入NH4Cl(218mg),DIPEA(0.37ml),冰浴下加入HATU(293mg),反应完全后,加入1M HCl溶液,EA萃取,EA层依次用NaHCO3溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得40mg化合物S-63-2。
化合物S-63-2(40mg)溶于CH2Cl2,加入CF3COOH(0.2ml),反应完全后,蒸干得化合物S-63。MS:m/e 129[M+H]+.
制备例23:化合物S-64的制备
按照与制备例24相同的方法,以S-64-1为试剂合成化合物S-64。
MS:m/e 205[M+H]+.
制备例24:化合物S-65的制备
化合物S-65-1(300mg)溶于丙酮,加入K2CO3(385mg),CH3I(0.6ml),过夜,反应完全,蒸干溶剂,EA萃取,饱和氯化钠溶液洗涤EA层,无水硫酸钠干燥,浓缩,短柱层析得190mg化合物S-65-2。
化合物S-65-2(190mg)溶于二氯甲烷,-78℃冷却,滴加DAST(0.17ml)试剂,室温搅拌,反应完全后,加冰水淬灭,分液,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得150mg化合物S-65-3。
化合物S-65-3(28mg)溶于CH2Cl2,加入CF3COOH(0.2ml),1h反应完全,蒸干得化合物S-65。MS:m/e 166[M+H]+.
制备例25:化合物S-68的制备
按照与制备例7相同的方法,以对甲氧基苯甲酸为试剂合成化合物S-68。
MS:m/e 221[M+H]+.
制备例26:化合物S-69的制备
按照与制备例7相同的方法,以对甲氧基苯甲酸为试剂合成化合物S-69。
MS:m/e 235[M+H]+.
制备例27:化合物S-70的制备
按照与制备例7相同的方法,以3.4-二氟苯甲酸为试剂合成化合物S-70。
MS:m/e 227[M+H]+.
制备例28:化合物S-71的制备
按照与制备例7相同的方法,以间甲基苯甲酸为试剂合成化合物S-71。
MS:m/e 205[M+H]+.
制备例29:化合物S-72的制备
按照与制备例7相同的方法,以S-72-1为试剂合成化合物S-72。
MS:m/e 245[M+H]+.
制备例30:化合物S-73的制备
按照与制备例7相同的方法,以S-73-1为试剂合成化合物S-73。
MS:m/e 246[M+H]+.
制备例31:化合物S-74的制备
按照与制备例7相同的方法,以S-74-1为试剂合成化合物S-74。
MS:m/e 244[M+H]+.
制备例32:化合物S-75的制备
按照与制备例7相同的方法,以S-75-1为试剂合成化合物S-75。
MS:m/e 301[M+H]+.
制备例33:化合物S-76的制备
按照与制备例7相同的方法,以S-76-1试剂合成化合物S-76。
MS:m/e 208[M+H]+.
制备例34:化合物S-77的制备
按照与制备例7相同的方法,以S-77-1为试剂合成化合物S-77。
MS:m/e 390[M+H]+.
制备例35:化合物S-78的制备
按照与制备例7相同的方法,以S-78-1为试剂合成化合物S-78。
MS:m/e 249[M+H]+.
制备例36:化合物S-79的制备
按照与制备例7相同的方法,以S-79-1为试剂合成化合物S-79。MS m/e 323[M+H]+。
制备例37:化合物S-80的制备
按照与制备例7相同的方法,以S-80-1为试剂合成化合物S-80。MS m/e 337[M+H]+。
制备例38:化合物S-81的制备
按照与制备例7相同的方法,以S-81-1为试剂合成化合物S-81。MS m/e 235[M+H]+。
制备例39:化合物S-82的制备
按照与制备例14相同方法,以3-吡啶甲酸为试剂合成化合物S-82。MS m/e 206[M+H]+。
制备例40:化合物S-83的制备
按照与制备例14相同方法,以2,4-二氟苯甲酸为试剂合成化合物S-83。
MS m/e 241[M+H]+。
制备例41:化合物S-84的制备
按照与制备例14相同的方法,以化合物S-84-2为试剂合成化合物S-84。
MS m/e 284[M+H]+。
制备例42:化合物S-85的制备
按照与制备例14相同的方法,以化合物S-85-2为试剂合成化合物S-85。
MS m/e 340[M+H]+。
制备例43:化合物S-86的制备
按照与制备例14相同的方法,以化合物S-86-2为试剂合成化合物S-86。
MS m/e 302[M+H]+。
制备例44:化合物S-87的制备
按照与制备例14相同的方法,以化合物S-87-2为试剂合成化合物S-87。
MS m/e 358[M+H]+。
制备例45:化合物S-88的制备
按照与制备例14相同的方法,以化合物S-88-2为试剂合成化合物S-88。
MS m/e 320[M+H]+。
制备例46:化合物S-89的制备
按照与制备例14相同的方法,以化合物S-89-2为试剂合成化合物S-89。
MS m/e 376[M+H]+。
制备例47:化合物S-90的制备
按照与制备例14相同的方法,以化合物S-90-2为试剂合成化合物S-90。
MS m/e 362[M+H]+。
制备例48:化合物S-91的制备
按照与制备例14相同的方法,以化合物S-91-2为试剂合成化合物S-91。
MS m/e 344[M+H]+。
制备例49:化合物S-92的制备
按照与制备例14相同的方法,以化合物S-92-2为试剂合成化合物S-92。
MS m/e 367[M+H]+。
制备例50:化合物S-93的制备
按照与制备例14相同的方法,以化合物S-93-2为试剂合成化合物S-93。
MS m/e 385[M+H]+。
制备例51:化合物S-94的制备
化合物S-94-1(30.45g)溶于的无水THF(300ml),加入NaBH4(17.1g),搅拌降温到0℃,滴加三氟化硼乙醚溶液(72mL),0.3h滴加完毕,自然升至室温,3h反应完全,慢慢滴入NaOH水溶液淬灭反应,无气泡产生后加快速度,调PH值中性,乙酸乙酯提取,饱和食盐水水洗,无水硫酸钠干燥,旋干,得26g化合物S-94-2。
化合物S-94-2(28g),加入甲苯(250mL)和的氯化亚砜(40mL),室温开始迅速反应,搅拌40min,气体产生速度减慢后升温至60℃,每小时升温10℃,温度达到90℃时,反应完全,降温,水洗三次,无水硫酸钠干燥,活性炭脱色,旋干,得30g化合物S-94-3。
化合物S-94-3(30g)溶于DMF(200mL),加入甘氨酸甲酯盐酸盐(22g),0℃下滴加三乙胺(60Ml)到反应瓶中,完毕后室温搅拌30min,升温到60℃,过夜反应,反应结束后降温,加水,乙酸乙酯提取,合并有机相,无水硫酸钠干燥,活性炭脱色,旋干,过柱,得8g化合物S-94-4
化合物S-94-4(260mg)溶于2.5ml的1,4-二氧六烷,NaHCO3(178mg)加入水中溶解,加入到反应瓶中,搅拌降温到0℃,加入CBZ-Cl(0.25Ml),反应结束后,减压蒸出二氧六环,乙酸乙酯提取,合并有机相,饱和食盐水洗涤,无水硫酸钠干燥,旋干,得400mg黄色油状液体,过柱分离,得300mg化合物S-94-5
化合物S-94-5(8.2g),Fe粉(6.4g)中加入甲醇(50ml),醋酸(5ml),升温至70℃,加入氯化铵(12g)水溶液,反应完全后蒸干溶剂,加入二氯甲烷溶解,过滤,浓缩,柱层析得6.7g化合物S-94-6。
氢氧化锂(1.4g)溶于水中,加入化合物S-94-6(2g)的THF溶液,1h反应完全,蒸干THF,加4M HCl溶液调PH<4,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩得2g化合物S-94-7。
化合物S-94-7(2g)溶于二氯甲烷,冰浴下,加入HOBT(1.3g),EDCI(1.6g),5min后加入DIPEA(2.6ml),撤冰浴,30min反应完全,加二氯甲烷稀释,反应也依次用1M HCl溶液,饱和碳酸氢钠溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得1.37g化合物S-94-8。
化合物S-94-8(500mg)溶于甲醇,加入Pd/C(100mg),通入氢气,1h反应完全,过滤,浓缩得400mg化合物S-94。
制备例52:化合物S-95的制备
NaH(7.7g)悬浮于干燥DMF(200ml)中,加入2-氯-3-硝基吡啶(30g),缓慢滴加丙二酸二甲酯(21ml),搅拌过夜,加水淬灭,EA萃取,饱和食盐水洗涤EA层,浓缩,柱层析得20g化合物S-95-1。
化合物S-95-1(13g)溶于6N盐酸溶液中,100℃加热,TLC监测至反应完全,加入6N
NaOH溶液中和,CH2Cl2萃取,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩得11g化合物S-95-2。
化合物S-95-2(5.5g),NBS(9.9g)悬浮于CCl4(100ml),加入AIBN(1.32g),回流1d,停止反应,过滤,洗涤滤渣,蒸干溶剂,柱层析得8g化合物S-95-2与化合物S-95-3混合物。
化合物S-95-3(8g)与化合物BNO-Br混合物溶于DMF,加入甘氨酸甲酯盐酸盐(5g),0℃下,滴加三乙胺(15ml),室温搅拌至反应完全,加入H2O,EA萃取,饱和食盐水洗涤洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得1.63g化合物S-95-4。
化合物S-95-4(1.6g)溶于1.4-二氧六烷,加入NaHCO3(1g)的水溶液,冰浴下,滴加CBZ-Cl(1.2ml),室温搅拌至反应完全,蒸干溶剂,加入H2O,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得2g化合物S-95-5。
化合物S-95-5(2.3g)溶于甲醇(50ml),加入醋酸(1ml),加入Fe粉(2g),升温至70℃,加入氯化铵(3g)的水溶液,反应完全,蒸干溶剂,EA溶解,过滤,浓缩,柱层析得2g化合物S-95-6。
化合物S-95-6(1.8g)溶于AcOH(20ml),120℃加热回流,TLC监测至反应完全,蒸干溶剂,EA溶解,EA层依次用饱和碳酸氢钠溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得1.2g化合物S-95-7。
化合物S-95-7(470mg)溶于甲醇,加入Pd/C(70mg),通入H2,室温搅拌至反应完全,过滤,浓缩得420mg化合物S-95。
制备例53:化合物S-96的制备
氯磺酸(10ml)滴加至2.4-二氟苯甲酸(5g)中,升至150℃,2h后反应完全,冷至室温,反应液缓慢滴加至冰中,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩得4.8g产物S-96-1。
冰浴下,浓氨水(6ml)中分批加入化合物S-96-1(400mg),撤冰浴,1h反应完全,蒸除部分溶剂,加浓盐酸调PH=1,过滤,水洗,蒸干得340mg化合物S-96-2。
N-Boc-1.2-乙二胺(200mg)溶于DMF,依次加入DIPEA(0.53ml)、化合物S-96-2(350mg)、HOBT(254mg)、EDCI(360mg),室温搅拌过夜,次日,反应液中加1M HCl溶液,EA萃取,EA层依次用饱和碳酸氢钠溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,短柱层析得化合物S-96-3。
化合物S-96-3(70mg)中加入2ml HCl乙醇溶液,搅拌至反应完全,蒸干得化合物S-96。
制备例54:化合物S-97的制备
3-氨基吡嗪-2-羧酸(15g)溶于硫酸甲醇溶液中(CH3OH∶H2SO4=10∶1),加热回流过夜,次日蒸干甲醇,EA溶解,EA层依次用饱和碳酸氢钠溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩得8g化合物S-97-1。
四氢铝锂(5g)悬浮于干燥THF(150ml)中,冰浴,分批加入化合物S-97-1(8g),加完后,反应液移至室温,5h反应完全,滴加水(10ml)淬灭,加入1M NaOH(10ml)溶液,加入硫酸钠,过滤,EA洗涤滤渣多次,浓缩,柱层析得3.5g化合物S-97-2。
氯化亚砜(2ml)溶于THF(100ml),冰浴下滴加化合物S-97-2(2.9g)的THF溶液,滴加完毕,移至室温,1h反应完全,蒸干,柱层析得2.7g化合物S-97-3。
化合物S-97-3(2.5g)溶于DMF,加入甘氨酸甲酯盐酸盐(2.6g),冰浴下,滴加三乙胺(8ml),滴加完毕,移至室温,8h反应完全,加水,EA萃取,浓缩,柱层析得570mg化合物-S-97-4。
化合物S-97-4(540mg)溶于1.4-二氧六烷,加入NaHCO3(460mg)的水溶液,冰浴下,滴加CBZ-Cl(0.42ml),室温搅拌至反应完全,蒸干溶剂,加入H2O,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得化合物S-97-5。
化合物S-97-5(1.2g)溶于AcOH,加入DMAP(80mg),120℃加热回流,3d反应完全,蒸干AcOH,EA溶解,EA层依次用饱和碳酸氢钠溶液,饱和食盐水洗涤,浓缩,柱层析得370mg化合物S-97-6。
化合物S-97-6(370mg)溶于甲醇,加入Pd/C(50mg),通入氢气,反应完全后,过滤,浓缩得170mg化合物S-97。
制备例55:化合物S-100的制备
化合物S-32(450mg)溶于CH2Cl2,加入三乙胺(0.5ml),冰浴下,滴加氯甲酸苄酯(0.4ml),反应完全,加CH2Cl2稀释,有机层依次用1M HCl溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩得700mg化合物S-100-1。
NaH(70mg)悬浮于干燥DMF中,冰浴下,滴加化合物S-100-1(450mg)的DMF溶液,室温搅拌1h,冰浴,滴加碘甲烷(80ul),室温搅拌1h,反应完全,冰浴,滴加饱和氯化铵溶液淬灭,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得350mg化合物S-100-2。
化合物S-100-2(350mg)溶于甲醇,加入Pd/C(40mg),通入H2,反应完全,过滤,浓缩得110mg化合物S-100。
制备例56:化合物S-101的制备
2-硝基-4-氟甲苯(5.5g)溶于四氯化碳,加入NBS(7.7g),AIBN(1g),76℃加热,次日,停止反应,冷至室温,过滤,浓缩,柱层析得4.6g化合物S-101-1.
化合物S-101-1(4.6g)溶于DMF,加入2.7g甘氨酸甲酯盐酸盐,冰浴下,滴加三乙胺(8.3ml),室温搅拌过夜,次日反应完全,加入水,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得2.6g化合物S-101-2.
化合物S-101-2(2.6g)溶于CH2Cl2,滴加Boc2O(1.83g),室温搅拌至反应完全,加CH2Cl2稀释,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,短柱层析得化合物S-101-3.
化合物S-101-3(2.83g)溶于甲醇,加Pd/C(300mg),通入H2,反应完全,过滤浓缩得2.7g化合物S-101-4。
氢氧化锂(2g)溶于水中,加入化合物S-101-4(2.7g)的THF溶液,1h反应完全,蒸干THF,加4M HCl溶液调PH<4,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩得化合物S-101-5。
化合物S-101-5溶于二氯甲烷,冰浴下,加入HOBT(1.5g),EDCI(2.1g),5min后加入DIPEA(1.3ml),撤冰浴,30min反应完全,加二氯甲烷稀释,反应液依次用1M HCl溶液,饱和碳酸氢钠溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得1g化合物S-101-6。
化合物S-101-6(70mg)溶于CH2Cl2,加入三氟醋酸(0.2ml),反应完全,蒸干得化合物S-101。
制备例57:化合物S-102的制备
对硝基苯甲酸(5.1g)悬浮于干燥CH2Cl2(50ml)中,加入DMF(2滴),滴加草酰氯(8ml),反应完全,蒸干。40%甲胺水溶液(5ml),加入三乙胺,冰浴下,滴加酰氯的THF溶液,反应完全,蒸干THF,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩得化合物S-102-1。
化合物S-102-1(1g)溶于甲醇,加入Pd/C(100mg),通入H2,反应完全,过滤,浓缩得化合物化合物S-102。
制备例58:化合物S-103的制备
2-甲基-3-硝基苯甲酸(5g)溶于甲醇(50ml),加入浓硫酸(5ml),加热回流过夜,次日,停止反应,蒸干甲醇,EA溶解,EA层依次用饱和碳酸氢钠溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩得4g化合物S-103-1。
化合物S-103-1(3.5g)溶于CCl4,加入NBS(3.5g),AIBN(600mg),加热回流过夜,次日停止反应,冷至室温,过滤,滤液加CH2Cl2稀释,饱和食盐水洗涤,无水硫酸钠干燥,浓缩得化合物S-103-2。
化合物S-103-2溶于甲醇溶液,加入氨甲醇溶液,加热回流,2h反应完全,过滤得产物,滤液浓缩,柱层析,合并得3.6g化合物化合物S-103-3。
化合物化合物S-103-3(1.5g)溶于甲醇,加入Pd/C(200mg),通入H2,反应完全,过滤,浓缩得1g化合物化合物S-103。
制备例59:化合物S-104的制备
按照与制备例58相同的方法,以2-甲基-4-硝基苯甲酸为试剂合成化合物S-104。
MS m/e 149[M+H]+
制备例60:化合物S-105的制备
按照与制备例14相同的方法,以2-噻唑甲酸为试剂合成化合物S-105。
MS m/e 212[M+H]+
制备例61:化合物S-106的制备
按照与制备例14相同的方法,以3-氟苯甲酸为试剂合成化合物S-106。
MS m/e 223[M+H]+
制备例62:化合物S-107的制备
钠氢(96mg)悬浮于干燥DMF(10ml)中,冰浴下,滴加化合物S-101-6(500mg)的DMF溶液,室温1h,冰浴,滴加碘甲烷(0.1ml),移至室温,反应完全,冰浴,滴加氯化铵溶液淬灭,EA萃取,浓缩,柱层析得550mg化合物S-107-1。
化合物S-107-1(100mg)溶于二氯甲烷中,加入三氟醋酸,反应完全,过滤,浓缩得化合物S-107。
制备例63:化合物S-108的制备
钠氢(96mg)悬浮于干燥DMF(10ml)中,冰浴下,滴加化合物S-94-8(500mg)的DMF溶液,室温1h,冰浴,滴加碘甲烷(0.1ml),移至室温,反应完全,冰浴,滴加氯化铵溶液淬灭,EA萃取,浓缩,柱层析得570mg化合物S-108-1。
化合物S-108-1(570mg)溶于甲醇中,加入Pd/C(60mg),通入氢气,反应完全,过滤,浓缩得280mg化合物S-108。
制备例64:化合物S-109的制备
按照与制备例14相同的方法,以化合物S-109-2为试剂合成化合物S-109。
MS m/e 388[M+H]+
制备例65:化合物S-110的制备
按照与制备例14相同的方法,以化合物S-110-2为试剂合成化合物S-110。
MS m/e 390[M+H]+
制备例66:化合物S-111的制备
间氨基苯甲酸(2g)溶于甲醇,冰浴,滴加氯化亚砜(0.93ml),回流过夜,次日反应完全,蒸干,EA溶解,依次用饱和碳酸氢钠溶液,饱和食盐水不洗涤,无水硫酸钠干燥,浓缩得化合物S-111-1。
化合物S-111-1(1g)溶于CH2Cl2,冰浴,加入吡啶(1.43ml),甲磺酰氯(0.54ml),1h后移至室温,反应完全,加入CH2Cl2稀释,依次用1M HCl溶液,饱和食盐水洗涤,干燥,浓缩得化合物S-111-2。
化合物S-111-2(1.3g)溶于甲醇,加入氢氧化锂(0.45g)的水溶液,搅拌至反应完全,EA萃除杂质,水层用浓盐酸调PH-2,EA萃取,饱和食盐水洗涤EA层,干燥浓缩得化合物S-111-3。
化合物S-111-3(300mg)溶于DMF,依次加入三乙胺(0.54ml),HBOT(261mg),EDCI(370mg),N-Boc乙二胺(227mg),室温搅拌过夜,次日,加入1M HCl溶液,EA萃取,EA层用饱和碳酸氢钠溶液,饱和食盐水不洗涤,无水硫酸钠干燥,浓缩,柱层析得化合物S-111-4。
化合物S-111-4(66mg)溶于CH2Cl2,加入三氟醋酸(0.3ml),反应完全,蒸干得化合物S-111
制备例67:化合物S-112的制备
按照与制备例66相同的方法,以化合物2-氟-5-氨基苯甲酸为试剂合成化合物S-112。
制备例68:化合物S-113的制备
按照与制备例66相同的方法,以化合物3-氨基-4-氯-苯甲酸为试剂合成化合物S-113。
制备例69:化合物S-114的制备
按照与制备例14相同的方法,以化合物S-114-2为试剂合成化合物S-114。
MS m/e 360[M+H]+
制备例70:化合物S-115的制备
按照与制备例14相同的方法,以化合物S-115-2为试剂合成化合物S-115。
MS m/e 388[M+H]+
制备例71:化合物S-116的制备
化合物S-116-1(10g)溶于甲醇,加入浓盐酸(5.1ml),加入Pd/C(1g),通入氢气,2h反应完全,过滤,浓缩得6g化合物S-116-2。
化合物S-116-2(1g)溶于CH2Cl2,加入三乙胺(1.5ml),冰浴下,滴加三氟乙酸酐(0.68ml),反应不完全,补加三乙胺与三氟乙酸酐,反应完全,蒸干,加入CH2Cl2稀释,加水分层,饱和食盐水洗涤有机层,干燥,浓缩,短柱层析得1.2g化合物S-116-3。
化合物S-116-3(1.2g)溶于醋酸(5ml),冰浴下,加入浓硫酸(2ml),10min后,加入多聚甲醛(0.2g),室温2h不反应,60℃加热反应,反应完全,反应液倒入冰水中,EA萃取,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得化合物S-116-4。
化合物S-116-4(800mg)溶于甲醇,加入碳酸钾的水溶液,反应完全,蒸干甲醇,EA萃取,饱和食盐水洗涤,无水硫酸钠干燥,浓缩得化合物S-116。
制备例72:化合物S-117的制备
LDA的THF溶液(2M,25ml),冷至-78℃,滴加1-N-Boc-3-哌啶酮(10g)的THF溶液,滴加完毕,搅拌20min,滴加三氟乙酸乙酯(6ml),移至室温,反应2h,加水淬灭,稀盐酸中和反应液,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩得化合物S-117-1。
三氟乙脒(200mg)中加入化合物S-117-1(296mg)的吡啶溶液,80℃反应,2h后反应完全,蒸干溶剂,EA溶解,EA层依次用1M HCl溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得280mg化合物S-117-2.
化合物S-117-2(280mg)中加入氯化氢乙酸乙酯溶液(10ml),室温搅拌,反应完全,蒸干得化合物S-117。
制备例73:化合物S-118的制备
化合物S-118-1(0.10g)溶解到无水四氢呋喃(5ml)中,氮气保护,冰水下加入BH3·THF(1.2ml),再在冰水下搅拌15分钟,然后加热回流12小时。反应液中慢慢加入甲醇,淬灭未反应完的硼烷,旋蒸去甲醇与四氢呋喃,剩余物中加入甲醇和盐酸,再回流3小时。旋蒸去溶剂后,剩余物加水,DCM提取3次,水相调节PH=12,再用DCM提起3次,合并有机相,水洗,盐水洗,干燥,浓缩,柱层析(DCM∶MeOH∶TEA=100∶2∶0.2)得化合物S-118(35mg)。
1H NMR(400MHz,CDCl3):δ7.16-7.08(m,2H),6.86(td,1H),6.80(dd,1H),3.94(s,2H),3.18-3.06(m,4H).
MS m/e 149[M+H]+,297[2M+H]+
制备例74:化合物S-119的制备
化合物S-119-1(0.78g),甘氨酸甲酯盐酸盐(0.70g)和HOBT(0.82g)溶解到无水二氯甲烷(10ml)中,再加入三乙胺(2.1ml),冰水冷却下加入EDCI(1.16g),自然升温,搅拌过夜。TLC反应完全。反应液中加水淬灭,二氯甲烷提取3次,合并有机相,PH=1的盐酸水溶液洗,饱和NaHCO3洗,水洗,盐水洗,干燥,浓缩得粗产品。固体用乙醚洗,过滤得化合物S-119-2。
1H NMR(400MHz,CDCl3):δ7.47-7.37(m,1H),6.49(bs,1H),6.42-6.33(m,2H),5.74(bs,2H),4.21(d,J=5.05Hz,2H),3.83(s,3H).。
MS m/e 227[M+H]+,249[M+Na]+,193[M-H]-
化合物S-119-2(93mg)溶于醋酸(5ml)中,加热至120度,搅拌过夜。TLC反应完全。旋蒸去醋酸后,加入乙醚搅拌,过滤得化合物S-119-3。
1H NMR(400MHz,DMSO-d6):δ10.48(s,1H),8.56(t,J=5.97Hz,1H),7.82(dd,J=6.64,8.83Hz,1H),7.08(td,J=2.57,8.47Hz,1H),6.90(dd,J=2.54,10.40Hz,1H),3.63(d,J=5.77Hz,2H).
MS m/e 195[M+H]+,193[M-H]-
化合物S-119-3(0.17g)溶解到无水四氢呋喃(5ml)中,冰水下加入BH3·THF(4.4ml),再在冰水下搅拌15分钟,然后加热回流12小时。TLC反应完全。反应液中慢慢加入甲醇,淬灭未反应完的硼烷,旋蒸去甲醇与四氢呋喃,剩余物中加入甲醇和盐酸,再回流3小时。TLC反应完全。旋蒸去溶剂后,剩余物加水,DCM提取3次,水相调节PH=12,再用DCM提起3次,合并有机相,水洗,盐水洗,干燥,浓缩,柱层析得化合物S-119。
1H NMR(400MHz,CDCl3):δ7.11-7.03(m,1H),6.58-6.45(m,2H),3.98(bs,1H),3.89(s,2H),3.18-3.11(m,2H),3.12-3.05(m,2H),1.72(bs,1H).
MS m/e 167[M+H]+
制备例75:化合物S-120的制备
按照与制备例74相同的方法,以S-120-1为原料,合成化合物S-120。
S-120-2
1H NMR(400MHz,CDCl3):δ7.52(d,J=8.15Hz,1H),6.93(s,1H),6.90(d,J=8.92Hz,1H),6.65(bs,1H),5.71(bs,2H),4.23(d,J=5.06Hz,2H),3.83(s,3H).
MS m/e 277[M+H]+,275[M-H]-
S-120-3
1H NMR(400MHz,DMSO-d6):δ10.58(s,1H),8.77(t,J=5.87Hz,1H),7.96(d,J=8.21Hz,1H),7.61-7.51(m,1H),7.49-7.42(m,1H),3.67(d,J=5.77Hz,2H).
MS m/e 243[M-H]-
S-120
1H NMR(400MHz,CDCl3):δ7.22(d,J=7.74Hz,1H),7.08(d,J=7.23Hz,1H),7.03(s,1H),4.10(bs,1H),3.96(s,2H),3.19-3.13(m,2H),3.13-3.06(m,2H).
MS m/e 217[M+H]+,215[M-H]-
制备例76:化合物S-121的制备
按照与制备例74相同的方法,以S-121-1为原料,合成化合物S-121。
S-121-2
1H NMR(400MHz,CDCl3):δ7.34(d,J=8.44Hz,1H),6.69(d,J=2.01Hz,1H),6.63(dd,J=2.02,8.44Hz,1H),6.59(bs,1H),5.67(bs,2H),4.20(d,J=5.09Hz,2H),3.82(s,3H).
MS m/e 243[M+H]+,241[M-H]-
S-121-3
1H NMR(400MHz,DMSO-d6):δ10.47(s,1H),8.62(t,J=6.04Hz,1H),7.77(d,J=8.48Hz,1H),7.28(dd,J=2.06,8.48Hz,1H),7.16(d,J=2.05Hz,1H),3.63(d,J=5.78Hz,2H).
MS m/e 209[M-H]-
S-121
1H NMR(400MHz,CDCl3):δ7.04(d,J=7.76Hz,1H),6.84-6.76(m,2H),3.97(bs,1H),3.89(s,2H),3.17-3.04(m,4H).
MS m/e 183[M+H]+
制备例77:化合物S-122的制备
按照与制备例74相同的方法,以S-122-1为原料,合成化合物S-122。
S-122-2
1H NMR(400MHz,CDCl3):δ7.27(d,J=8.47Hz,1H),6.87(d,J=1.89Hz,1H),6.79(dd,J=1.90,8.40Hz,1H),6.55(bs,1H),5.64(bs,2H),4.20(d,J=5.05Hz,2H),3.82(s,3H).
MS m/e 287,289[M+H]+,309,311[M+Na]+,285,287[M-H]-
S-122-3
1H NMR(400MHz,DMSO-d6):δ10.45(s,1H),8.62(t,J=5.81Hz,1H),7.68(d,J=8.41Hz,1H),7.41(dd,J=1.85,8.44Hz,1H),7.31(d,J=1.87Hz,1H),3.62(d,J=5.79Hz,2H).
MS m/e 253,255[M-H]-
S-122
1H NMR(400MHz,CDCl3):δ7.02-6.89(m,3H),3.96(bs,1H),3.87(s,2H),3.15-3.10(m,2H),3.09-3.05(m,2H).
MS m/e 227,229[M+H]+
制备例78:化合物S-123的制备
按照与制备例74相同的方法,以S-123-1为原料,合成化合物S-123。
S-123-2
MS m/e 239[M+H]+.
S-123-3
1H NMR(400MHz,DMSO-d6):δ10.29(s,1H),8.37(t,J=5.68Hz,1H),7.71(d,J=8.77Hz,1H),6.82(dd,J=2.48,8.79Hz,1H),6.63(d,J=2.45Hz,1H),3.79(s,3H),3.58(d,J=5.68Hz,2H).
MS m/e 207[M+H]+.
S-123
1H NMR(400MHz,CDCl3):δ7.04(d,J=8.23Hz,1H),6.41(dd,J=2.51,8.18Hz,1H),6.36(d,J=2.44Hz,1H),3.93(bs,1H),3.87(s,2H),3.79(s,3H),3.12(m,2H),3.09-3.03(m,2H).
MS m/e 179[M+H]+.
制备例79:化合物S-124的制备
按照与制备例74相同的方法,以S-124-1为原料,合成化合物S-124。
S-124-2
1H NMR(400MHz,CDCl3):δ7.52(d,J=2.24Hz,1H),7.30(dd,J=2.15,8.57Hz,1H),6.59(d,J=8.65Hz,1H),5.54(bs,2H),4.20(d,J=5.13Hz,2H),3.82(s,3H).
MS m/e 287,289[M+H]+,309,311[M+Na]+,285,287[M-H]-
S-124-3
1H NMR(400MHz,DMSO-d6):δ10.48(s,1H),8.68(t,J=5.83Hz,1H),7.83(d,J=2.44Hz,1H),7.70(dd,J=2.47,8.62Hz,1H),7.07(d,J=8.65Hz,1H),3.62(d,J=5.78Hz,2H).
MS m/e 253,255[M-H]-.
S-124
1H NMR(400MHz,CDCl3):δ7.24(d,J=2.36Hz,1H),7.18(dd,J=2.34,8.29Hz,1H),6.67(d,J=8.30Hz,1H),3.94(bs,1H),3.87(s,2H),3.15-3.04(m,4H).
MS m/e 227,229[M+H]+.
制备例80:化合物S-125的制备
化合物S-125(1.15g,5.0mmol),溶解到无水N-甲基吡咯烷酮(18ml)中,氮气保护下加入CuCN(1.35g,15.0mmol),加热到200度反应3.5小时。TLC反应完全。反应液冷却后慢慢加入到乙二胺水溶液(15%)中,搅拌1小时后,乙酸乙酯提取3次,合并有机相,氨水(10%)洗两次,盐水洗,干燥,浓缩,过柱得化合物S-125(150mg)。
1H NMR(400MHz,CDCl3):δ7.38(d,J=1.89Hz,1H),7.35(dd,J=1.96,8.16Hz,1H),6.76(d,J=8.15Hz,1H),4.35(bs,1H),3.92(s,2H),3.25(m,2H),3.14-3.03(m,2H).
EIMS m/e 173[M]+.
制备例81:化合物S-126的制备
化合物S-121(1.2g,6.6mmol)溶于二氯甲烷(15ml)中,冰水下冷却,加入三乙胺(2.74ml,0.2mol),再加入Boc2O,自然升温,搅拌过夜。TLC显示反应完全。反应液倒入水中,二氯甲烷提取3次,合并有机相,PH=1的盐酸洗,饱和碳酸氢钠洗,水洗,盐水洗,干燥,浓缩得化合物S-126-1。
1H NMR(400MHz,CDCl3):δ7.14(m,1H),6.84(dd,J=1.98,7.96Hz,1H),6.78(d,J=6.67Hz,1H),4.35(d,2H),3.95(bs,1H),3.64(dd,J=3.52,6.00Hz,2H),3.16(s,2H),1.43(s,9H).
MS m/e 281[M-H]-.
化合物S-126-1(0.5g,1.77mmol)溶于DMF(10ml)中,再加入碳酸钾(0.73g,5.3mmol),冰水冷却下加入碘甲烷(0.13ml,2.1mmol),自然升温,搅拌过夜,补加碘甲烷(0.13ml,2.1mmol),加热到60度,反应10小时,TLC显示有部分原料未反应。反应液倒入水中,二氯甲烷提取3次,合并有机相,水洗,盐水洗,干燥,浓缩,柱层析得化合物S-126-2(0.3g)。
化合物S-126-2(0.3g)溶于二氯甲烷(10ml)中,加入三氟乙酸(1ml),室温搅拌6小时,TLC检测反应完全。直接旋干二氯甲烷和过量的三氟乙酸,得到化合物S-126的三氟乙酸盐。
1H NMR(400MHz,DMSO-d6):δ9.00(bs,2H),7.36(d,1H),7.01-6.99(m,2H),4.18(bs,2H),3.31-3.16(m,4H),2.89(s,3H).
MS m/e 197[M+H]+.
制备例82:化合物S-127的制备
化合物S-126-1(0.1g,0.35mmol)溶解到无水吡啶(3ml)中,再加入醋酸酐(80μL,0.84mmol,2.4eq)加热到100度3小时,TLC反应完全。反应液冰水中冷却,用盐酸缓慢的调节至PH=3,二氯甲烷提取3次,合并有机相,饱和碳酸氢钠洗,水洗,盐水洗,干燥,浓缩,过柱得化合物S-127-2(100mg)
1H NMR(400MHz,CDCl3):δ7.30(m,2H),7.25(m,1H),4.92-4.58(m,2H),4.30-3.80(m,2H),3.41-3.10(m,1H),2.75(m,1H),1.97(s,3H),1.65-1.35(m,9H).
MS m/e 347[M+Na]+.
化合物S-127-2(100mg)溶于二氯甲烷(10ml)中,再加入三氟乙酸(1ml),室温搅拌过夜。TLC显示反应完全。旋蒸去二氯甲烷和过量的三氟乙酸,固体用乙醚洗,过滤,烘干,得化合物S-127。
1H NMR(400MHz,DMSO-d6):δ7.71(d,J=2.12Hz,1H),7.62(d,J=8.23Hz,1H),7.51(dd,J=2.11,8.22Hz,1H),4.67(d,J=14.88Hz,1H),4.34(s,2H),3.38(d,J=13.50Hz,1H),3.20(t,J=12.47Hz,1H),2.91(t,J=13.32Hz,1H),1.90(s,3H).
MS m/e 225[M+H]+.
制备例83:化合物S-128的制备
按照与制备例51相同的方法,以化合物2-硝基-4-三氟甲基苯甲酸为试剂合成化合物S-128。
制备例84:化合物S-129的制备
按照与制备例56相同的方法,以化合物2-硝基-4-溴苯甲酸为试剂合成化合物S-129-6。
化合物S-129-6(300mg)溶于乙腈,加入碘化钠(800mg),滴加三甲基氯硅烷(0.8ml),反应完全,加水,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得150mg化合物S-129。
制备例85:化合物S-130的制备
按照与制备例14相同的方法,以化合物S-130-2为试剂合成化合物S-130。
MS m/e 385[M+H]+.
制备例86:化合物S-131的制备
化合物S-129-6(30mg)溶于DMF,加入氰化锌(150mg),四三苯基膦钯(100mg),氮气保护,80℃,反应过夜,次日加水,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得化合物S-131-1。化合物S-131-1溶于甲醇,加入Pd/C,通入H2,反应12h,过滤,浓缩,柱层析得化合物S-131。
以下化合物由市场采购或由上海特化医药科技有限公司提供:
实施例1:
制备例2的化合物S-2(42g)溶于甲苯(250ml),加入DMAP(5g),3-(三氟甲基)-5,6,7,8-四氢-[1,2,4]三唑并[4,3-a]吡嗪盐酸盐(39g),三乙胺(36ml),氮气保护,120℃回流5h后,蒸干溶剂,残留物用乙酸乙酯溶解,乙酸乙酯相依次用1M HCl溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得35g产物1-1。
上述产物(20g)溶于甲醇(50ml),加入氨甲醇溶液(30ml),加入乙酸铵(16g),65℃下反应,2h反应完全,冷至室温,加入氰基硼氢化钠(9g),加入醋酸(3ml)调pH=5,反应过夜,次日蒸干溶剂,残留物用二氯甲烷溶解,有机层依次用饱和NaHCO3溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得实施例1标题化合物(16.5g)。
1H NMR(300MHZ,CD3OD):δ7.14(1H,dd),7.05(1H,dd),4.18-5.14(2H,m),4.27-4.36(2H,m),4.00-4.14(2H,m),3.69-3.78(1H,m),2.77-3.00(2H,m),2.53-2.75(2H,m),2.03-2.27(2H,m).
MS m/e 416[M+H]+.
实施例2~3:
将实施例1的化合物经硅胶柱层析得一对对映体化合物2和化合物3的混合物;以及另一对对映体化合物4和化合物5的混合物。化合物2、3与4、5为非对映异构体。
实施例4~5:
将实施例1的化合物采用HPLC手性制备液相仪(色谱柱型号为AD-H)进行手性拆分,分别得到单一手性异构体实施例4化合物和实施例5化合物。色谱保留时间分别为tR=48.0min,tR=35.0min。
实施例4化合物:e.e.值>98%。1H NMR(300MHZ,CD3OD):δ7.07(1H,dd),7.00(1H,dd),4.89-5.16(2H,m),3.90-4.31(4H,m),3.81(1H,br),3.25(1H,br),2.78-2.96(2H,m),2.50(2H,d),2.03-2.22(2H,m).MS:m/e 416[M+H]+.比旋光度+25°(C=0.5)。
实施例5化合物:e.e.值>98%。1H NMR(300MHZ,CD3OD):δ7.06(1H,dd),6.99(1H,dd),4.89-5.14(2H,m),3.86-4.31(4H,m),3.80(1H,br),3.25(1H,br),2.77-3.00(2H,m),2.50(2H,d),2.03-2.19(2H,m).MS:m/e 416[M+H]+.比旋光度-25°(C=0.5)。
实施例6:
制备例6的化合物S-5a(100mg)溶于DMF,加入NEt3(0.1ml),HATU(123mg),5min反应完全,加入3-(三氟甲基)-5,6,7,8-四氢-[1,2,4]三唑并[4,3-a]吡嗪盐酸盐(68mg),室温搅拌过夜,反应完全,加入1M HCl溶液,EA萃取,EA层依次用NaHCO3溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得化合物5-1(77mg)。
化合物5-1(77mg)溶于CH2Cl2,加入CF3COOH(0.3ml),1h反应完全,加入二氯甲烷稀释,饱和碳酸氢钠溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,柱层析得化合物5(50mg)。e.e.值>98%。
实施例7:
化合物7-1(11g)悬浮于CH2Cl2(150ml)中,加入1,2-乙二硫醇(6.6ml),加入BF3·Et2O溶液(2.1ml),室温搅拌,次日反应完全,加入CH2Cl2稀释,依次用水,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,用CH2Cl2/PE重结晶,得10.8g化合物7-2。
化合物7-2(10.8g)溶于CH2Cl2(100ml)中,加入DMAP(6.8g),米氏酸(5.6g),冰浴下滴加DCC(8.4g)的CH2Cl2溶液(50ml),自然升至常温,反应完全后,过滤,滤液依次用1M HCl洗涤,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,用石油醚-乙酸乙酯结晶得9.2g化合物7-3。
化合物7-3(9.2g),TsOH(2g),EtOH(50ml),80℃加热,溶液逐渐澄清,1h后反应完全,蒸干溶剂,柱层析得8.8g产物7-4。
化合物7-4(8.8g)溶于甲苯(100ml)中,加入DMAP(0.9g),3-(三氟甲基)-5,6,7,8-四氢-[1,2,4]三唑并[4,3-a]吡嗪盐酸盐(7.1g),三乙胺(5.2ml),N2保护,120℃加热,6h后,蒸干溶剂,乙酸乙酯溶解,有机层依次用1M HCl溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得9.3g产物7-5。
化合物7-5(9.2g)溶于氨甲醇溶液(30ml)中,加入甲醇(50ml),加入醋酸铵(5.8g),N2保护,65℃下反应,1h后反应完全,冷至室温,加入NaBH3CN(3.5g),用醋酸调pH=5,室温搅拌,次日反应完全,浓缩反应液,用饱和NaHCO3溶液中和醋酸,加入二氯甲烷,分层,有机相依次用水、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得7.5g目标物7。
1H NMR(300MHZ,CD3OD):δ7.43(1H,dd),7.37(1H,dd),5.04(2H,s),4.25(1H,br),4.13(1H,br),4.01(2H,br),3.72(1H,br),3.52-3.67(4H,m),3.07-3.18(1H,m),3.39-3.47(1H,m),2.91-3.01(2H,m),2.58-2.67(1H,m).MS:m/e 506[M+H]+.
实施例8:
化合物7(720mg)溶于甲醇(10ml)中,加入HgCl2(550mg),30min反应完全,过滤,浓缩滤液,柱层析,得实施例8的标题化合物450mg。
1H NMR(300MHZ,CD3OD):δ7.74(1H,dd),7.63(1H,dd),5.04(2H,s),4.34(2H,br),4.24(1H,t),4.06(1H,t),3.90(1H,br),3.15-3.21(1H,m),3.12(1H,t),2.87-3.05(2H,m),2.69(1H,dt).MS:m/e 430[M+H]+.
实施例9:
化合物8(260mg)溶于甲醇(5ml)中,冰浴下加入硼氢化钠(40mg),30min反应完全,浓缩反应液,加入CH2Cl2溶解,有机相依次用水、饱和食盐水洗涤,无水硫酸钠干燥,浓缩得目标物230mg。
1H NMR(300MHZ,CD3OD):δ7.18-7.30(2H,m),5.04(2H,br),4.99(1H,br),4.34(1H,br),4.24(1H,r),4.06(2H,br),3.76(1H,br),3.34(1H,m),2.78(1H,dd),2.62(1H,dd),2.45-2.57(1H,m),1.84-1.95(1H,m).MS:m/e 432[M+H]+.
实施例10:
化合物10-1(100mg),苄胺(75mg),对甲苯磺酸(20mg),甲苯(5ml),110℃回流反应,5h反应完全,冷却,过滤,蒸干溶剂,残留物用甲醇溶解,冰浴下加入硼氢化钠(60mg),反应完全后,蒸干溶剂,用CH2Cl2溶解,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得20mg化合物10-2。
化合物10-2(20mg)溶于CH2Cl2(1ml),加入三氟醋酸(0.2ml),1h反应完全,蒸干溶剂,用甲基叔丁基醚结晶,得化合物10.CF3COOH(15mg)。
1H NMR(300MHZ,CD3OD):δ7.42-7.64(7H,m),5.04(2H,br),4.99(1H,br),4.34(1H,br),4.24(1H,r),4.06(4H,br),3.76(1H,br),3.34(1H,m),2.78(1H,dd),2.62(1H,dd),2.45-2.57(1H,m),1.84-1.95(1H,m).MS:m/e 521[M+H]+.
化合物10.CF3COOH用饱和碳酸氢钠游离,得碱式化合物10。
实施例11:
化合物11-1(330mg)溶于CH2Cl2(10ml),冰浴下滴加DAST试剂(0.1ml),30min反应完全,加水淬灭,CH2Cl2稀释,分层,饱和食盐水洗涤CH2Cl2层,无水硫酸钠干燥,浓缩,柱层析得60mg化合物11-2。
化合物11-2(60mg)溶于CH2Cl2,加入三氟醋酸(0.3ml),反应完全后,加入CH2Cl2稀释,分层,CH2Cl2层依次用饱和碳酸氢钠溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩得34mg化合物11。
1H NMR(300MHZ,CD3OD):δ7.56(1H,t),7.35(1H,t),7.02(1H,d),6.7(1H,dd),5.04(2H,br),4.34(1H,br),4.24(1H,r),4.06(2H,br),3.76(1H,br),3.34(1H,m),2.78(1H,dd),2.62(1H,dd).
MS:m/e 414[M+H]+.
实施例12:
NaHMDS(19ml)溶于干燥THF(50ml)中,氮气置换,-78℃下冷却,滴加化合物12-1(4.1g)的THF溶液,搅拌45min,滴加苄溴(3ml)的THF溶液,30min后自然升温,反应完全后,加入氯化铵溶液淬灭,蒸干THF,用乙酸乙酯萃取,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得4.5g化合物12-2。
化合物12-2(4.5g)溶于甲醇(20ml),水(20ml)中,加入氢氧化钠(1.3g),回流,反应完全后,蒸干甲醇,用1M HCl溶液调pH=2,用乙酸乙酯萃取,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩得4g化合物12-3。
丙二酸单乙酯钾盐(1.62g)悬浮于乙腈(5ml)中,加入三乙胺(2.1ml),氯化镁(1.13g),室温搅拌2h。化合物12-3(1.3g)悬浮于乙腈(10ml)中,加入CDI(0.9g),室温搅拌至反应完全,加至上述反应液中。搅拌过夜,次日滴加13%HCl溶液至澄清,分层,浓缩有机层,残留物用EA溶解;EA萃取水层,合并EA层,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得1.3g化合物12-4。
化合物12-4(1g)溶于甲苯(20ml),加入DMAP(94mg),3-(三氟甲基)-5,6,7,8-四氢-[1,2,4]三唑并[4,3-a]吡嗪盐酸盐(738mg),三乙胺(0.5ml),氮气保护,120℃回流,5h后,蒸干溶剂,残留物用乙酸乙酯溶解,依次用1M HCl溶液、饱和食盐水洗涤,干燥,浓缩,柱层析得915mg化合物12-5。
化合物12-5(550mg)溶于氨甲醇溶液(10ml),加入乙酸铵(600mg),65℃下回流,24h反应完全,冷至室温,加入氰基硼氢化钠(198mg),乙酸调pH=5,室温搅拌,次日蒸干溶剂,残留物用二氯甲烷溶解,依次用饱和碳酸氢钠溶液、饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得目标物。
1H NMR(300MHZ,CD3OD):δ7.16-7.30(4H,m),6.87-7.08(3H,t),4.89-5.14(2H,m),4.13-4.22(2H,m),3.96-4.16(2H,m),3.68(1H,br),3.18-3.24(1H,m),2.75-3.00(2H,m),2.26-2.74(4H,m),2.03-2.30(2H,m).MS:m/e 506[M+H]+.
实施例13:
NaHMDS(19ml)溶于干燥THF(50ml)中,氮气置换,-78℃下,滴加化合物12-1(3.9g)的THF溶液,搅拌45min,滴加邻氯氯苄(2.5ml)的THF溶液,搅拌30min,反应完全后,加入氯化铵溶液淬灭,蒸干THF,EA萃取,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得产物4.5g化合物13-1。
化合物13-1(4.5g)溶于甲醇(20ml),水(20ml)中,加入氢氧化钠(1.3g),回流,反应完全后,蒸干甲醇,1M HCl溶液调PH=2,EA萃取,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩得4g化合物13-2。
丙二酸单乙酯钾盐(1.62g)悬浮于乙腈(5ml)中,加入三乙胺(2.1ml),氯化镁(1.13g),室温搅拌2h。化合物13-2(1.3g)悬浮于乙腈(10ml)中,加入CDI(0.9g),室温搅拌至反应完全。加至上述反应液中。搅拌过夜,次日滴加13%HCl溶液至澄清,分层:蒸干上层,EA溶解;EA萃取下层,合并EA层,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得1.3g化合物13-3。
化合物13-3(1g)溶于20ml甲苯,加入DMAP(94mg),3-(三氟甲基)-5,6,7,8-四氢-[1,2,4]三唑并[4,3-a]吡嗪盐酸盐(738mg),三乙胺(0.5ml),氮气保护,120℃回流,5h后,蒸干溶剂,EA溶解,EA层依次用1M HCl溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得915mg化合物13-4。
化合物13-4(550mg)溶于氨甲醇溶液(10ml),加入乙酸铵(600mg),65℃下回流,24h反应完全,冷至室温,加入氰基硼氢化钠(198mg),乙酸调PH=5,室温搅拌,次日蒸干溶剂,二氯甲烷溶解,饱和碳酸氢钠溶液洗涤有机层,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得化合物13。
1H NMR(300MHZ,CD3OD):δ7.92(1H,br),7.16-7.30(2H,m),6.87-7.08(3H,t),4.89-5.14(2H,m),4.13-4.22(2H,m),3.96-4.16(2H,m),3.68(1H,br),3.18-3.24(1H,m),2.75-3.00(2H,m),2.26-2.74(4H,m),2.03-2.30(2H,m).MS:m/e 540[M+H]+.
实施例14:
NaHMDS(60ml)溶于干燥THF(50ml),-78℃冷却,滴加化合物12-1(12g)的50ml THF溶液,滴加完毕,搅拌45min,滴加2-苄氧基溴乙烷(13.4g)的THF(50ml)溶液,滴加完毕,搅拌半小时后自然升温,反应完全后,饱和氯化铵溶液淬灭,蒸干THF,EA溶解,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得9.4g化合物14-1。
化合物14-1(9.4g)溶于甲醇(40ml),水(40ml)中,加入NaOH(3g),79℃回流,1h反应完全,蒸干溶剂,1M调PH=2-3,EA萃取,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩得8.5g化合物14-2。
丙二酸单乙酯钾盐(10.9g)悬浮于乙腈(30ml)中,加入11ml三乙胺,6.1g氯化镁,室温搅拌2h。化合物14-2(8.5g)悬浮于乙腈(30ml)中,加入CDI(4.98g),室温搅拌至反应完全,加至上述反应液中。搅拌过夜,次日滴加1M HCl溶液至澄清,分层:蒸干上层,EA溶解;EA萃取下层,合并EA层,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得7.6g化合物14-3。
化合物14-3(7.5g)溶于甲苯(100ml),加入DMAP(0.7g),3-(三氟甲基)-5,6,7,8-四氢-[1,2,4]三唑并[4,3-a]吡嗪盐酸盐(10g),三乙胺(7ml),氮气保护,120℃回流,5h后,蒸干溶剂,EA溶解,EA层依次用1M HCl溶液、饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得10g化合物14-4。
化合物14-4(10g)溶于甲醇(50ml),加入氨甲醇溶液(50ml),乙酸铵(7.1g),N2保护,65℃加热至反应完全,冷至室温,加入氰基硼氢化钠(3.2g),加入醋酸调PH=5,反应完全,蒸干溶剂,1M NaOH溶液调PH至碱性,EA萃取,饱和食盐水洗涤EA层,无水硫酸钠干燥,浓缩,柱层析得3.4g化合物14。
1H NMR(300MHZ,CD3OD):δ7.14-7.31(5H,m),7.03-7.12(2H,m),4.98(2H,d),4.37(2H,s),4.16-4.28(2H,m),4.04-4.14(1H,m),3.95-4.01(1H,m),3.66(1H,dd),3.34-3.43(2H,m),2.83-2.92(3H,m),2.29-2.39(2H,m),1.95-2.05(3H,m).MS:m/e 550[M+H]+.
实施例15:
14(16.8g)溶于甲醇(20ml),加入三乙胺(5.1ml),Boc2O(7.3g),室温搅拌,1h反应完全,蒸干溶剂,EA溶解,1M HCl溶液洗涤有机层,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,短柱层析得11.5g化合物15-1。
化合物15-1(11.5g)溶于甲醇(50ml),加入Pd/C(1.2g),醋酸(1ml),通入氢气,40℃加热,搅拌30h后反应完全,过滤,蒸干溶剂得10g化合物15-2。
化合物15-2(100mg)溶于氯化氢甲醇溶液,2h后反应完全,蒸干溶剂,二氯甲烷溶解,碳酸氢钠溶液洗涤,饱和食盐水洗涤,干燥浓缩,柱层析得60mg化合物15。
1H NMR(300MHZ,CD3OD):δ7.24(1H,dd),7.16(1H,dd),5.07(2H,d),4.37(1H,br),4.24(1H,br),4.04-4.17(2H,m),3.67(1H,d),3.50-3.59(1H,m),3.38-3.47(1H,m),2.84-3.02(3H,m),2.33-2.58(2H,m),1.96-2.13(2H,m),1.81-1.93(1H,m).MS:m/e 460[M+H]+.
实施例16:
NaH(30mg)溶于THF(4ml),冰浴下加入化合物15-2(220mg)的THF(3ml)溶液,滴加2-氯氯苄(0.1ml),移至室温,后40℃加热,反应完全后,饱和氯化铵溶液淬灭,蒸干THF,二氯甲烷萃取,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得120mg化合物16-1。
化合物16-1(120mg)溶于二氯甲烷(3ml),滴加三氟醋酸(0.3ml),2h反应完全,加入二氯甲烷稀释,饱和碳酸氢钠溶液洗涤,饱和食盐水洗涤,干燥浓缩,短柱层析得46mg化合物16。
1H NMR(300MHZ,CD3OD):δ7.24(1H,dd),7.16(1H,dd),5.07(2H,d),4.37(1H,br),4.24(1H,br),4.04-4.17(2H,m),3.67(1H,d),3.50-3.59(1H,m),3.38-3.47(1H,m),2.84-3.02(3H,m),2.33-2.58(2H,m),1.96-2.13(2H,m),1.81-1.93(1H,m).MS:m/e 584[M+H]+.
实施例17:
NaH(36mg)溶于THF(4ml),冰浴下加入化合物15-2(250mg)的THF(3ml)溶液,滴加4,6-二氯嘧啶(74mg)的THF(2ml)溶液,30min反应完全,冰浴下,饱和氯化铵溶液淬灭,蒸干THF,二氯甲烷萃取,饱和食盐水洗涤有机层,无水硫酸钠干燥,浓缩,柱层析得170mg化合物17-1。
化合物17-1(170mg)溶于二氯甲烷(5ml),滴加三氟醋酸(0.3ml),2h反应完全,加入二氯甲烷稀释,饱和碳酸氢钠溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,柱层析得57mg化合物17。
1H NMR(300MHZ,CD3OD):δ8.32(1H,d),7.30(1H,t),7.16(1H,t),6.63(1H,d),5.07(1H,d),3.95-4.40(6H,m),3.38-3.47(1H,m),2.84-3.02(3H,m),2.33-2.58(2H,m),1.96-2.13(2H,m),1.81-1.93(1H,m).
MS:m/e 572[M+H]+.
实施例18:
1-(3,5-二硝基苯甲酰基)-哌嗪(S-18)(52mg)溶于DMF(3ml),依次加入HOBT(38mg),DIPEA(0.16ml),EDCI(54mg),制备例5的化合物S-5(64mg),室温搅拌,反应完全后,加入1M HCl溶液,EA萃取三次,EA层依次用饱和NaHCO3溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得52mg化合物18-1。
化合物18-1(52mg)溶于二氯甲烷(3ml),滴入CF3COOH(0.3ml),30min反应完全,加入二氯甲烷稀释,饱和碳酸氢钠溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,柱层析得40mg化合物18。
1H NMR(300MHZ,CD3OD):δ9.07(1H,t),8.70(2H,d),7.26(1H,t),7.17(1H,t),3.42-3.91(8H,m),3.20(1H,s),2.62-3.07(4H,m),2.36(1H,br),1.93-2.10(2H,m).
MS:m/e 504[M+H]+.
实施例19:
按照与实施例18相同的方法,以制备例5的化合物S-5为原料,以1-(2-乙氧基苯甲酰基)哌嗪(S-19)为试剂合成化合物19。
1H NMR(300MHZ,CD3OD):δ7.41(1H,t),7.22(2H,t),6.98-7.16(3H,m),4.04-4.18(2H,m),3.42-3.91(8H,m),3.39(1H,br),2.53-3.07(5H,m),2.17-2.33(1H,m),1.98-2.12(1H,m),1.28(3H,t).
MS:m/e 458[M+H]+.
实施例20:
按照与实施例18相同的方法,以制备例5的化合物S-5为原料,以1-(2-硝基苯甲酰基)哌嗪(S-20)为试剂合成化合物20。
1H NMR(300MHZ,CD3OD):δ8.25(1H,dd),7.84(1H,td),7.71(1H,td),7.53(1H,dd),7.20(1H,q),7.10(1H,q),3.50-3.98(8H,m),3.35(1H,br),2.48-3.01(5H,m),2.14-2.28(1H,m),1.98-2.12(1H,m).
MS:m/e 459[M+H]+.
实施例21:
按照与实施例18相同的方法,以制备例5的化合物S-5为原料,以1-(3-氯苯甲酰基)哌嗪(S-21)为试剂合成化合物21。
1H NMR(300MHZ,CD3OD):δ7.42-7.54(2H,m)7.37(1H,d),7.23(1H,t),7.13(1H,t),3.91(1H,br),3.38-3.84(7H,m),2.56-3.07(5H,m),2.18-2.36(1H,m),1.96-2.13(1H,m).
MS:m/e 448[M+H]+.
实施例22:
制备例5的化合物S-5(45mg)溶于DMF,加入NEt3(0.1ml),HATU(53mg),5min反应完全,加入1-(吡啶-2-基-酰基)哌嗪(S-22)(50mg),18℃搅拌过夜,反应完全,加入1M HCl溶液,EA萃取,EA层依次用NaHCO3溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得37mg化合物22-1。
化合物22-1(37mg)溶于CH2Cl2,加入CF3COOH(0.3ml),1h反应完全,加入二氯甲烷稀释,饱和碳酸氢钠溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,柱层析得30mg化合物22。
1H NMR(300MHZ,CD3OD):δ8.86(1H,br),8.48(1H,br),8.09(1H,br),7.99(1H,br),7.29(1H,t),7.18(1H,t),4.08(1H,br),3.47-3.95(7H,m),2.75-3.09(5H,m),2.29-2.45(1H,m),1.95-2.10(2H,m).
MS:m/e 415[M+H]+.
实施例23:
按照与实施例22相同的方法,以制备例5的化合物S-5为原料,以1-(吡嗪-2-基-酰基)哌嗪(S-23)为试剂合成化合物23。
1H NMR(300MHZ,CD3OD):δ8.89(1H,br),8.71(1H,br),8.65(1H,br),7.28(1H,t),7.17(1H,t),4.06(1H,br),3.47-3.95(7H,m),2.68-3.07(5H,m),2.29-2.45(1H,m),1.95-2.10(2H,m).
MS:m/e 416[M+H]+.
实施例24:
按照与实施例22相同的方法,以制备例5的化合物S-5为原料,以3-腈基-2-(((S)-吡咯-2-基)甲氧基)吡啶(S-24)为试剂合成化合物24。
1H NMR(300MHZ,CD3OD):δ8.32-8.42(1H,m),8.02-8.11(1H,m),7.17-7.27(1H,m),7.05-7.17(2H,m),4.68(1H,td),4.45-4.51(1H,m),3.92-4.01(1H,m),3.53-3.70(2H,m),3.41-3.53(1H,m),2.92-3.04(1H,m),2.80-2.92(2H,m),2.61-2.73(1H,m),2.22-2.38(2H,m),1.95-2.18(5H,m).
MS:m/e 427[M+H]+.
实施例25:
按照与实施例22相同的方法,以制备例5的化合物S-5为原料,以3-(甲磺酰基)-N-(((S)-吡咯-2-基)甲基)苯甲酰胺(S-25)为试剂合成化合物25。
1H NMR(300MHZ,CD3OD):δ8.39(1H,br),8.07-8.21(2H,m),7.68-7.80(1H,m),7.27(1H,t),7.10(1H,t),4.42(1H,d),4.02-4.25(1H,m),3.41-3.70(5H,m),3.20(1H,s),3.16(3H,s),2.79-3.09(3H,m),2.60-2.76(1H,m),2.26-2.43(1H,m),1.88-2.22(5H,m).
MS:m/e 506[M+H]+.
实施例26:
按照与实施例22相同的方法,以制备例5的化合物S-5为原料,以N-(((S)-吡咯-2-基)甲基)苯磺酰胺(S-26)为试剂合成化合物26。
1H NMR(300MHZ,CD3OD):δ7.74(2H,br),7.42-7.58(3H,m),7.19(1H,br),7.09(1H,br),3.88-4.07(2H,m),3.33-3.54(3H,m),3.12(1H,s),3.20(1H,s),2.75-2.97(4H,m),2.49-2.62(1H,m),2.20-2.36(1H,m),1.79-2.05(5H,m).
MS:m/e 464[M+H]+.
实施例27:
按照与实施例22相同的方法,以制备例5的化合物S-5为原料,以3-氯-N-(((S)-吡咯-2-基)甲基)苯甲酰胺(S-27)为试剂合成化合物27。
1H NMR(300MHZ,CD3OD):δ7.77(1H,s),7.70(1H,d),7.54(1H,d),7.45(1H,dd),7.24(1H,t),6.98(1H,t),4.11-4.31(2H,m),3.46-3.60(5H,m),2.79-3.09(4H,m),2.63-2.77(1H,m),2.25-2.44(1H,m),1.92-2.07(5H,m).
MS:m/e 462[M+H]+.
实施例28:
按照与实施例22相同的方法,以制备例5的化合物S-5为原料,以4-氮杂环庚酮(S-28)为试剂合成化合物28。
1H NMR(300MHZ,CD3OD):δ7.07(1H,t),7.00(1H,t),3.81-3.89(1H,m),3.71-3.80(1H,m),3.58-3.71(2H,m),3.41-3.58(2H,m),2.86-3.00(2H,m),2.42-2.85(6H,m),2.11-2.35(2H,m),1.65-1.93(2H,m).
MS:m/e 337[M+H]+.
实施例29:
按照与实施例22相同的方法,以制备例5的化合物S-5为原料,以2,3,6,7-四氢-1H-氮杂卓(S-29)为试剂合成化合物29。
1H NMR(300MHZ,CD3OD):δ7.24(1H,t),7.18(1H,t),5.72-5.84(2H,m),3.96-4.12(2H,m),3.49-3.71(4H,m),2.86-3.05(3H,m),2.63-2.77(1H,m),2.29-2.42(4H,m),1.95-2.07(1H,m),1.84-1.93(1H,m).
MS:m/e 321[M+H]+
实施例30:
按照与实施例22相同的方法,以制备例5的化合物S-5为原料,以4,5,6,7-四氢噻吩并[2,3-c]吡啶(S-30)为试剂合成化合物30。
1H NMR(300MHZ,CD3OD):δ7.21-7.29(2H,m),7.13-7.20(1H,m),6.81-6.87(1H,m),4.59-4.74(2H,m),4.08(1H,br),3.84-4.01(1H,m),3.80(1H,q),3.56(1H,br),2.72-3.08(6H,m),2.32-2.43(1H,m),1.95-2.06(1H,m).
MS:m/e 363[M+H]+.
实施例31:
制备例5的化合物S-5(120mg)溶于DMF,加入NEt3(0.15ml),HATU(150mg),5min反应完全,加入1-(2,3-二氯苯基)哌嗪盐酸(S-31,104mg),18℃搅拌至反应完全,加入1M HCl溶液,EA萃取,EA层依次用NaHCO3溶液,饱和食盐水洗涤,无水硫酸钠干燥,浓缩,柱层析得70mg化合物31-1。
化合物31-1(70mg)溶于CH2Cl2,加入CF3COOH(0.3ml),1h反应完全,蒸干,甲基叔丁基醚结晶得化合物31的三氟乙酸盐(46mg)。
1H NMR(300MHZ,CD3OD):δ7.21-7.31(3H,m),7.17(1H,t),7.08(1H,t),4.03-4.12(1H,m),3.79(2H,br),3.69(2H,br),2.89-3.11(7H,m),2.70-2.80(1H,m),2.31-2.43(1H,m),1.96-2.09(2H,m).
MS:m/e 454[M+H]+.
1H NMR(300MHZ,d6-DMSO):δ7.85(3H,br),7.46(1H,dd),7.28-7.37(3H,m),7.14(1H,t),3.92(1H,br),3.54-3.69(4H,m),3.42-3.52(1H,m),2.64-3.05(8H,m),2.16-2.28(1H,m),1.96-2.09(1H,m).
MS:m/e 454[M+H]+.
将化合物31的三氟乙酸盐溶于CH2Cl2,饱和碳酸氢钠溶液洗涤,饱和食盐水洗涤,将有机相干燥、浓缩,得化合物31。
1H NMR(300MHZ,d6-DMSO):δ7.28-7.40(3H,m),7.23(1H,t),7.14(1H,t),3.58-3.72(4H,m),3.54(1H,br),3.34(2H,m),3.17(1H,br),2.64-3.05(6H,m),2.30-2.48(2H,m),1.96-2.09(2H,m).
MS:m/e 454[M+H]+.
实施例32:
按照与实施例31相同的方法,以制备例5的化合物S-5和4,5-二氢-1H-苯并[1,4]二氮杂-2(3H)-酮(S-32)为原料合成化合物32的三氟乙酸盐。
1H NMR(300MHZ,CD3OD):δ7.31(2H,br),7.04-7.26(4H,m),7.08(1H,t),4.70(2H,d),4.51(1H,s),4.24(1H,s),3.52(1H,br),2.84-3.06(3H,m),2.80(2H,br),2.20-2.42(1H,m),1.89-2.05(1H,m).
MS:m/e 386[M+H]+.
将化合物32的三氟乙酸盐溶于CH2Cl2,饱和碳酸氢钠溶液洗涤,饱和食盐水洗涤,将有机相干燥、浓缩,得化合物32。
实施例33:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以7-羟基-1,2,3,4-四氢喹啉(S-33)为试剂合成化合物33。
1H NMR(300MHZ,CD3OD):δ7.34-7.39(1H,m),7.31(1H,dd),7.20(1H,dd),7.11-7.15(2H,m),4.15(1H,br),3.62(1H,br),3.45-3.51(2H,m),2.97-3.17(3H,m),2.88-2.95(3H,m),2.33-2.46(1H,m),2.09-2.15(2H,m),1.98-2.07(1H,m).
MS:m/e 373[M+H]+.
实施例34:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-34为试剂合成化合物34。
1H NMR(300MHZ,CD3OD):δ8.85(2H,d),8.09(2H,s),7.11-7.25(2H,m),3.70-4.20(11H,m),3.09-3.23(3H,m),2.75-3.05(4H,m),2.21-2.38(2H,m),1.93-2.08(2H,m).
MS:m/e 445[M+H]+.
实施例35:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-35为试剂合成化合物35。
1H NMR(300MHZ,CD3OD):δ8.64(1H,s),7.32(1H,t),7.18(1H,t),4.81(2H,s),4.14(1H,br),3.62(1H,br),3.20(2H,q),2.77-3.07(4H,m),2.30-2.47(1H,m),2.00-2.17(1H,m).
MS:m/e 360[M+H]+.
实施例36:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以间氯苯胺(S-36)为试剂合成化合物36。
1H NMR(300MHZ,CD3OD):δ7.80(1H,s),7.41(1H,d),7.22-7.33(2H,m),7.16(1H,t),7.09(1H,d),4.01-4.11(1H,m),3.57(1H,br),2.68-3.11(4H,m),2.31-2.46(1H,m),2.01-3.14(1H,m).
MS:m/e 351[M+H]+.
实施例37:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-37为试剂合成化合物37。
1H NMR(300MHZ,CD3OD):δ7.26-7.43(1H,m),7.18(1H,t),6.82-7.09(2H,m),4.04-4.38(2H,m),3.75-3.94(6H,m),3.40-3.70(4H,m),3.20(6H,q),2.81-3.13(4H,m),2.28-2.40(1H,m),2.02-2.23(2H,m).
MS:m/e 472[M+H]+.
实施例38:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-38为试剂合成化合物38。
1H NMR(300MHZ,CD3OD):δ7.28(1H,t),7.18(1H,t),4.44(1H,d),4.03(1H,br),3.36-3.68(5H,m),2.60-3.10(4H,m),2.27-2.44(1H,m),1.86-2.14(3H,m).
MS:m/e 311[M+H]+.
实施例39:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-39为试剂合成化合物39。
1H NMR(300MHZ,CD3OD):δ7.27(1H,t),7.16(1H,t),4.52(1H,t),3.88-4.09(2H,m),3.58(1H,br),3.33-3.51(4H,m),2.61-3.08(6H,m),2.44-2.58(1H,m),2.26-2.42(1H,m),1.95-2.07(1H,m).
MS:m/e 429[M+H]+.
实施例40:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-40为试剂合成化合物40。
1H NMR(300MHZ,CD3OD):δ7.26(1H,t),7.16(1H,t),4.46-4.58(2H,t),3.87-4.08(1H,m),3.64-3.78(4H,m),3.50-3.61(2H,m),2.56-3.06(4H,m),2.23-2.45(2H,m),1.96-2.11(2H,m).
MS:m/e 369[M+H]+.
实施例41:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-41为试剂合成化合物41。
1H NMR(300MHZ,CD3OD):δ7.99(1H,d),7.71(2H,s),7.28(1H,t),7.16(1H,t),5.44(1H,td),3.92-4.14(2H,m),3.67-3.80(1H,m),3.59(1H,br),2.82-3.12(4H,m),2.50-2.69(1H,m),2.32-2.48(1H,m),2.14-2.30(3H,m),1.95-2.12(1H,m).
MS:m/e 489[M+H]+.
实施例42:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-42为试剂合成化合物42。
1H NMR(300MHZ,CD3OD):δ7.46(2H,d),7.28(1H,t),7.18(1H,t),5.32(1H,td),4.04(1H,br),3.85(1H,br),3.61-3.72(1H,m),3.56(1H,br),2.77-3.08(4H,m),2.27-2.54(2H,m),1.96-2.24(4H,m).
MS:m/e 361[M+H]+.
实施例43:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-43为试剂合成化合物43。
1H NMR(300MHZ,CD3OD):δ7.92(2H,dd),7.72(2H,dd),7.29(1H,m),7.18(1H,t),4.70(1H,dd),4.61(1H,dd),4.05(1H,br),3.54-3.76(3H,m),2.67-3.10(5H,m),1.93-2.50(6H,m).
MS:m/e 534[M+H]+.
实施例44:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-44为试剂合成化合物44。
1H NMR(300MHZ,CD3OD):δ7.28(1H,t),7.17(1H,t),4.00(1H,br),3.79(1H,d),3.56(1H,br),2.83-3.07(3H,m),2.67-2.80(2H,m),2.28-2.44(2H,m),1.99-2.09(1H,m),1.45-1.79(6H,m).
MS:m/e 353[M+H]+.
实施例45:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-45为试剂合成化合物45。
1H NMR(300MHZ,CD3OD):δ7.49(3H,br),7.37(2H,d),7.10-7.27(2H,m),4.17(1H,br),3.97(1H,br),3.79(3H,s),3.65-3.75(1H,m),3.43-3.57(2H,m),2.79-3.14(4H,m),2.57-2.74(1H,m),2.25-2.52(2H,m),2.20(1H,d),1.96-2.07(1H,m),1.91(2H,q),1.56-1.75(1H,m),1.38-1.54(1H,m),0.92(3H,t).
MS:m/e 514[M+H]+.
实施例46:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-46为试剂合成化合物46。
1H NMR(300MHZ,CD3OD):δ7.34(1H,t),7.20(1H,t),4.04-4.32(2H,m),3.90(2H,br),3.55-3.85(8H,m),3.43-3.55(3H,m),2.79-3.29(7H,m),2.33-2.48(1H,m),1.98-2.15(1H,m).
MS:m/e 398[M+H]+.
实施例47:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-47为试剂合成化合物47。
1H NMR(300MHZ,CD3OD):δ7.33(1H,t),7.19(1H,t),3.73-4.18(11H,m),3.53-3.66(3H,m),3.44(2H,br),3.10-3.21(3H,m),2.85-3.09(3H,m),2.33-2.48(1H,m),1.98-2.11(1H,m).
MS:m/e 398[M+H]+.
实施例48:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-48为试剂合成化合物48。
1H NMR(300MHZ,CD3OD):δ7.33(1H,t),7.19(1H,t),3.73-4.18(11H,m),3.53-3.66(3H,m),3.44(2H,br),3.10-3.21(3H,m),2.85-3.09(3H,m),2.33-2.48(1H,m),1.98-2.11(1H,m).
MS:m/e 429[M+H]+.
实施例49:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-49为试剂合成化合物49。
1H NMR(300MHZ,CD3OD):δ8.40(1H,br),8.14-8.20(1H,m),8.12(1H,d),7.74(1H,td),7.26(1H,t),7.16(1H,t),4.54-4.66(1H,m),4.04(1H,br),3.79-3.95(1H,m),3.46-3.77(4H,m),3.16(3H,s),2.95-3.06(1H,m),2.80-2.95(2H,m),2.61-2.74(1H,m),2.25-2.43(2H,m),2.13-2.22(1H,m),1.97-2.08(1H,m).
MS:m/e 492[M+H]+.
实施例50:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-50为试剂合成化合物50。
1H NMR(300MHZ,CD3OD):δ8.41(1H,br),8.17(1H,d),8.13(1H,d),7.74(1H,td),7.26(1H,t),7.16(1H,t),4.73(1H,t),4.68(1H,dd),4.01-4.10(1H,m),3.92-4.00(1H,m),3.76(3H,t),3.60-3.67(1H,m),3.52-3.60(1H,m),3.16(3H,s),2.82-3.06(3H,m),2.67--2.79(1H,m),2.42-2.52(1H,m),2.28-2.40(2H,m),1.97-2.08(1H,m).
MS:m/e 550[M+H]+.
实施例51:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-51为试剂合成化合物51。
1H NMR(300MHZ,CD3OD):δ7.30(1H,dt),7.15(1H,t),4.76(1H,dd),3.83-4.00(1H,m),3.48-3.62(2H,m),2.80-3.07(3H,m),2.58-2.72(1H,m),2.26-2.42(1H,m),1.95-2.15(3H,m),1.70-1.81(1H,m),1.00-1.13(1H,m),0.79-0.92(1H,m).
MS:m/e 350[M+H]+.
实施例52:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-52为试剂合成化合物52。
1H NMR(300MHZ,CD3OD):δ7.61(1H,d),7.28(1H,t),7.15(1H,t),6.94(1H,d),4.66(2H,br),4.09(1H,br),3.84(3H,s),3.82(3H,s),3.60(1H,br),2.95-3.08(3H,q),2.81-2.93(3H,m),2.80(1H,m),2.38(1H,br),2.04-2.09(2H,m).
MS:m/e 445[M+H]+.
实施例53:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-53为试剂合成化合物53。
1H NMR(300MHZ,CD3OD):δ7.25(1H,dt),7.17(1H,t),4.19(1H,dt),3.99(2H,br),3.63-3.69(3H,m),3.52(1H,br),2.79-3.08(4H,m),2.42-2.75(4H,m),2.28-2.39(1H,m),1.94-2.07(2H,m).
MS:m/e 381[M+H]+.
实施例54:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-54为试剂合成化合物54。
1H NMR(300MHZ,CD3OD):δ7.28(1H,dt),7.18(1H,t),4.49-4.62(1H,m),3.88-4.21(2H,m),3.67-3.80(3H,m),3.44-3.67(2H,m),2.79-3.12(3H,m),2.56-2.75(1H,m),2.28-2.52(2H,m),2.12-2.25(1H,m),1.94-2.11(1H,m).
MS:m/e 367[M+H]+.
实施例55:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-55为试剂合成化合物55。
MS:m/e 483[M+H]+.
实施例56:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-56为试剂合成化合物56。
1H NMR(300MHZ,CD3OD):δ7.24(1H,dt),7.16(1H,t),3.95-4.06(1H,m),3.67-3.75(1H,m),3.50-3.60(2H,m),3.45(2H,dd),2.73-3.06(3H,m),2.56-2.69(1H,m),2.28-2.42(1H,m),1.97-2.09(1H,m),1.41-1.57(2H,m),1.05(3H,s),0.93(3H,d).
MS:m/e 335[M+H]+.
实施例57:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-57为试剂合成化合物57。
1H NMR(300MHZ,CD3OD):δ8.41(1H,br),8.09(1H,d),7.27(1H,br),7.09-7.21(2H,m),5.78(1H,d),4.06(1H,br),3.78(3H,br),3.57(1H,br),2.60-3.50(4H,m),2.17-2.42(3H,m),1.97-2.12(2H,m).
MS:m/e 413[M+H]+.
实施例58:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-58为试剂合成化合物58。
1H NMR(300MHZ,CD3OD):δ8.09(1H,dd),7.74(1H,dd),7.37(1H,t),7.19(1H,t),6.46(1H,t),4.40-4.54(1H,m),4.23-4.35(2H,m),3.68(1H,br),3.50-3.61(1H,m),3.36-3.44(1H,m),2.84-3.10(3H,m),2.32-2.48(1H,m),1.69-2.11(9H,m).
MS:m/e 441[M+H]+.
实施例59:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-59为试剂合成化合物59。
1H NMR(300MHZ,CD3OD):δ7.29(1H,t),7.17(1H,t),7.07(1H,t),6.79(2H,d),4.07(1H,br),3.65-3.84(4H,m),3.58(1H,br),3.16-3.26(3H,m),2.72-3.08(5H,m),2.29-2.44(1H,m),1.98-2.14(1H,m).
MS:m/e 466[M+H]+.
实施例60:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-60为试剂合成化合物60。
1H NMR(300MHZ,CD3OD):δ7.27(1H,t),7.17(1H,t),4.56(1H,d),3.97-4.17(2H,m),3.54(1H,br),2.14-3.08(9H,m),1.92-2.07(2H,m).
MS:m/e 366[M+H]+.
实施例61:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-61为试剂合成化合物61。
1H NMR(300MHZ,CD3OD):δ7.29(1H,t),7.17(1H,t),4.18(1H,br),3.84-4.10(3H,m),3.71(1H,d),3.50-3.67(2H,m),3.32-3.49(4H,m),2.82-3.07(3H,m),2.43-2.74(3H,m),2.25-2.42(1H,m),1.94-2.10(1H,m).
MS:m/e 415[M+H]+.
实施例62:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-62为试剂合成化合物62。
1H NMR(300MHZ,CD3OD):δ8.35(1H,dd),8.06(1H,dd),7.20-7.28(1H,m),7.06-7.17(2H,m)4.48-4,.58(2H,m),3.96-4.07(2H,m),3.90(1H,dd),3.35-3.47(6H,m),2.82-3.02(4H,m),2.77-2.81(1H,m),2.61-2.67(2H,m),2.27-2.41(1H,m),1.96-2.05(1H,m).
MS:m/e 517[M+H]+.
实施例63:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-63为试剂合成化合物63。
1H NMR(300MHZ,CD3OD):δ7.27(1H,t),7.16(1H,t),4.36-4.52(1H,m),3.94-4.17(2H,m),3.62-3.76(1H,m),3.48-3.61(1H,m),2.78-3.10(4H,m),2.47-2.77(2H,m),2.29-2.44(1H,m),1.96-2.13(1H,m).
MS:m/e 352[M+H]+.
实施例64:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-64为试剂合成化合物64。
1H NMR(300MHZ,CD3OD):δ7.29(1H,t),7.17(1H,t),4.49(1H,t),4.01(1H,d),3.90(1H,d),3.47-3.58(1H,m),3.41(4H,br),3.20(1H,q),2.63-3.07(5H,m),2.39-2.49(1H,m),2.27-2.38(1H,m),1.96-2.10(1H,m).
MS:m/e 428[M+H]+
实施例65:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-65为试剂合成化合物65。
1H NMR(300MHZ,CD3OD):δ7.29(1H,t),7.16(1H,t),3.91-4.12(3H,m),3.71-3.78(3H,m),3.57(1H,br),2.47-3.10(7H,m),2.28-2.45(1H,m),1.93-2.08(1H,m).
MS:m/e 389[M+H]+.
实施例66:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-66为试剂合成化合物66。
1H NMR(300MHZ,CD3OD):δ7.27(1H,t),7.18(1H,t),5.20(1H,d),3.99(1H,br),3.79(1H,d),3.53(1H,br),2.82-3.08(3H,m),2.63-2.81(1H,m),2.22-2.45(2H,m),1.94-2.07(1H,m),1.39-1.82(6H,m).
MS:m/e 352[M+H]+.
实施例67:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-67为试剂合成化合物67。
1H NMR(300MHZ,CD3OD):δ7.29(1H,t),7.16(1H,t),4.08(1H,br),3.96(1H,br),3.70(3H,s),3.59(1H,br),2.71-3.09(5H,br),2.26-2.57(3H,m),1.94-2.12(2H,m),1.82-1.93(1H,m),1.69-1.81(2H,m).
MS:m/e 383[M+H]+.
实施例68:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-68为试剂合成化合物68。
1H NMR(300MHZ,DMSO-d6):δ7.8(3H,br),7.26-7.48(4H,m),6.99(2H,d),3.91(1H,br),3.79(3H,s),3.51(8H,br),2.58-2.97(5H,m),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 444[M+H]+.
实施例69:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-69为试剂合成化合物69。
1H NMR(300MHZ,DMSO-d6):δ7.77(3H,br),7.44(1H,dd),7.31(1H,dd),7.14(2H,d),6.86(2H,d)3.89(1H,br),3.72(3H,s),3.67(2H,d),3.30-3.56(8H,m),2.58-2.97(5H,m),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 458[M+H]+.
实施例70:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-70为试剂合成化合物70。
1H NMR(300MHZ,DMSO-d6):δ7.8(3H,br),7.26-7.57(4H,m),7.21(1H,t),3.91(1H,br),3.37-3.73(8H,m),3.19-3.33(2H,m),2.58-2.97(5H,m),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 450[M+H]+.
实施例71:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-71为试剂合成化合物71。
1H NMR(300MHZ,DMSO-d6):δ7.84(3H,br),7.44(1H,t),7.25-7.35(3H,m),7.16-7.24(2H,m),3.91(1H,br),3.27-3.73(8H,m),2.58-2.97(5H,m),2.34(3H,s),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 428[M+H]+.
实施例72:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-72为试剂合成化合物72。
1H NMR(300MHZ,DMSO-d6):δ7.80(3H,br),7.67(2H,dd),7.45(1H,t),7.32(2H,t),7.19(1H,t),4.19(3H,s),3.92(1H,br),3.38-3.79(8H,m),2.58-2.97(5H,m),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 468[M+H]+.
实施例73:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-73为试剂合成化合物73。
1H NMR(300MHZ,DMSO-d6):δ7.80(3H,br),7.72(1H,d),7.65(1H,t),7.45(1H,t),7.38(2H,t),7.32(1H,t),3.92(1H,br),3.41-3.68(10H,m),2.58-2.97(5H,m),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 469[M+H]+.
实施例74:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-74为试剂合成化合物74。
1H NMR(300MHZ,DMSO-d6):δ7.68-7.89(5H,m),7.39-7.55(2H,m),7.32(1H,t),7.23(1H,t),7.15(1H,t),3.93(1H,br),3.83(3H,s),3.38-3.79(8H,m),2.58-2.97(5H,m),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 467[M+H]+.
实施例75:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-75为试剂合成化合物75。
1H NMR(300MHZ,DMSO-d6):δ7.78(3H,br),7.35-7.48(3H,m),7.30(1H,t),7.17-7.25(3H,m),7.02-7.12(2H,m),6.87(1H,t),3.91(1H,br),3.38-3.79(8H,m),2.58-2.97(5H,m),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 524[M+H]+.
实施例76:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-76为试剂合成化合物76。
1H NMR(300MHZ,DMSO-d6):δ10.9(1H,br),7.83(3H,br),7.56(1H,t),7.44(1H,t),7.30(1H,t),6.53(2H,d),3.91(1H,br),3.27-3.72(8H,m),2.57-2.97(5H,m),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 431[M+H]+.
实施例77:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-77为试剂合成化合物77。
1H NMR(300MHZ,DMSO-d6):δ7.87(1H,br),7.82(3H,br),7.72(1H,br),7.44(1H,dd),7.42(1H,d),7.30(1H,dd),3.91(1H,br),3.38-3.77(8H,m),2.67-2.97(5H,m),2.4(3H,s),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 613[M+H]+.
实施例78:
按照与实施例31相同的方法,以制备例5的化合物S-5为原料,以S-78为试剂合成化合物78。
1H NMR(300MHZ,DMSO-d6):δ7.85(3H,br),7.46(1H,t),7.31(1H,t),6.85(4H,br),5.27(1H,br),4.39(1H,br),4.20(1H,br),3.91(1H,br),3.34-3.79(8H,m),2.58-2.97(5H,m),2.12-2.29(1H,m),1.93-2.07(1H,m).
MS:m/e 472[M+H]+.
实施例79~124:
以制备例6的手性化合物S-5a为原料,与不同的含N化合物(试剂S)反应,参照实施例18制备消旋化合物的制备方法,制备以下单一手性化合物,具体试剂S及对应合成的实施例化合物详见下表:
实施例125~154:
以制备例6的手性化合物S-5a为原料,与不同的含N化合物(试剂S)反应,参照实施例31的制备方法,制备以下单一手性化合物,具体试剂S及对应合成的化合物详见下表:
实施例155:
以制备例6的手性化合物S-5a和化合物155-1为原料合成化合物155-2。
化合物155-2(150mg)溶于甲醇,加入Pd/C(20mg),通入H2,反应完全,过滤,浓缩,柱层析得23mg化合物155-3。
化合物155-3(23mg)溶于CH2Cl2,加入三氟醋酸(0.2ml),反应完全,蒸干,EA溶解,EA层依次用饱和碳酸氢钠溶液,饱和食盐水洗涤,干燥浓缩,溶于甲醇,加入草酸(4mg),搅拌10min,浓缩得化合物155。
1H NMR(300MHZ,DMSO-d6):δ9.03(1H,d),8.16-8.31(2H,m),7.56-7.69(1H,m),7.21-7.45(2H,m),4.24(1H,br),3.76(1H,br),3.37-3.57(4H,m),3.06(4H,br),2.69-2.93(3H,m),2.53-2.61(1H,m),2.34(4H,br),1.75-2.11(7H,m).MS m/e 612[M+H]+.
实施例156~162:
以制备例6的手性化合物S-5a为原料,与不同的含N化合物(试剂S)反应,参照实施例31的制备方法,制备以下单一手性化合物,具体试剂S及对应合成的化合物详见下表:
实施例163:
参照实施例31的制备方法,以制备例6的手性化合物S-5a和S-116为原料合成化合物163。1H NMR(300MHZ,CD3OD-d4):δ7.88(1H,dd),7.11-7.47(4H,m),4.72-5.25(2H,m),3.89(3H,s),3.71-3.82(2H,m),3.54(1H,br),2.71-3.07(6H,m),2.31-2.42(1H,m),1.97-2.09(2H,m).
MS m/e 415[M+H]+.
实施例164:
化合物163-1溶于甲醇,加入氢氧化锂的水溶液,反应完全,加入1M HCl溶液调pH至酸性,EA萃取,饱和食盐水洗涤,干燥浓缩164-1。
化合物164-1溶于CH2Cl2,加入三氟醋酸(0.2ml),反应完全,蒸干,EA溶解,饱和碳酸氢钠溶液洗涤,饱和食盐水洗涤,干燥,浓缩得化合物164。
1H NMR(300MHZ,CD3OD-d4):δ7.92(1H,dd),7.11-7.47(4H,m),5.05-5.25(2H,m),3.71-3.86(2H,m),3.58(1H,br),2.71-3.10(6H,m),2.32-2.45(1H,m),1.97-2.09(2H,m).
MS m/e 401[M+H]+.
实施例165:
参照实施例31的制备方法,以制备例6的手性化合物S-5a和S-117为原料合成化合物165。
1H NMR(300MHZ,DMSO-d6):δ7.91(3H,br),7.48(1H,t),7.32(1H,t),4.92(2H,d),3.81-3.97(2H,m),3.14(1H,br),2.66-3.03(5H,m),1.92-2.26(4H,m).
MS m/e 495[M+H]+.
实施例166:
制备例6的手性化合物S-5a(50mg,0.147mmol),化合物S-119(26mg,0.176mmol,1.2eq)和HOBt(25mg,1.25eq)溶解到无水二氯甲烷(5ml)中,再加入二异丙基乙胺(72μl,3eq),冰水冷却下加入EDCI(35mg,1.25eq),自然升温,搅拌过夜。TLC反应完全。反应液中加水淬灭,二氯甲烷提取3次,合并有机相,pH=1的盐酸水溶液洗,饱和NaHCO3洗,水洗,盐水洗,干燥,浓缩,柱层析得化合物166-1(58mg)。
MS m/e 494[M+Na]+.
化合物166-1溶于二氯甲烷(10ml)中,加入浓盐酸(1ml),搅拌过夜。TLC显示反应完全。旋蒸去二氯甲烷和过量的盐酸,加水溶解后再次旋干,残余物中再加入乙醚分散,搅拌,离心,得化合物166。
1H NMR(400MHz,DMSO-d6):δ7.36-7.17(m,1H),7.10-6.81(m,4H),4.64-4.45(m,2H),4.01-3.69(m,3H),3.49-3.24(m,3H),2.95-2.62(m,4H),2.28-2.10(m,1H),1.91-1.77(m,1H).
MS m/e 390[M+H]+.
实施例167~185:
以制备例6的手性化合物S-5a为原料,与不同的含N化合物(试剂S)反应,参照实施例31或者实施例166的制备方法,制备以下单一手性化合物,具体试剂S及对应合成的化合物详见下表:
实施例186-246:
以制备例5化合物S-5为原料,与不同的含N化合物(试剂S)反应,参照实施例18或实施例31或实施例166的制备方法,制备以下化合物,具体试剂S及对应合成的化合物详见下表:
分子对接技术评估化合物活性
计算机辅助药物设计是合理药物设计的主要方法和工具。本发明通过反复尝试各种对接程序、确定了分子对接方法,优化了分子对接参数,获得了DPP-4抑制剂的构效关系,可用于设计符合通式I所示的新型DPP-4抑制剂。优选的对接用计算程序为Schrodinger 2010版中的glide(LLC,New York,NY)。对接靶点选用与sitagliptin共结晶的DPP-4蛋白结构(PDB ID:1X70)。对接的范围设置为一个包括DPP-4催化结合位点中的S1、P1和P2口袋的立方体。所有设计的化合物结构在软件中构建,并利用Ligprep模块在保持手性不变的前提下在PH=7+2范围内进行结构优化。对关键的氨基手动指定其质子化状态为带1各单位的正电荷。
对接计算采用XP精度。在对接中,每个化合物分子产生8000个构象,将前1000个优势构象进行能量优化并重新评估。将非极性氢原子的半径缩小为标准值的80%以获得更多的输出构象类型。综合考虑分子对接所提供的信息,包括化合物与DPP-4活性口袋中关键氨基酸残基的作用、与口袋形状契合程度以及疏水基团伸出口袋外部的特征等,选择了部分化合物分子进行化学合成和生物学检测。新合成化合物分子的生物活性测试结果表明,当计算打分函数Gsocre优于-10kcal/mol时,化合物将具有抑制DPP-4活性能力。下表中列出了计算打分函数Gsocre优于-10kcal/mol的化合物,但本申请不限于这些化合物分子。
生物学评价
1.本发明中部分化合物对DPP-4的抑制活性测定
本发明使用人结肠癌细胞株Caco-2的细胞裂解液作为DPP-4酶的来源(Thomas,L.,M.Eckardt,et al,The Journal of Pharmacology and Experimental Therapeutics325(1):175-182,2008)。在96孔板100μL/孔的筛药体系中,H-Gly-Pro-AMC底物(AnaSpec)的终浓度为0.1mg/ml,加入不同浓度的待测化合物37℃孵育30min后,以激发波长380nm/发射波长460nm检测荧光信号强度。根据检测获得的荧光值计算受试样品对DPP-4的酶活抑制率(%),并将酶活性抑制率达到50%时的浓度定为该化合物作用的IC50值。抑制率(%)根据下式进行:
抑制率%=(RFU空白-RFU化合物)/(RFU空白-RFU阴性对照)X100%
RFU化合物、RFU空白和RFU阴性对照分别表示化合物孔、空白孔和不加酶的阴性对照孔30min与0min的荧光值之差
经过以上方法检测DPP-4酶活,结果显示多个化合物对DPP-4有不同程度的抑制活性,其中实施例5化合物的活性较好,对DPP-4的抑制活性的IC50值为19.9nM;以上市DPP-4抑制剂Sitagliptin作为阳性对照,在该平台上测得的阳性药IC50为34.1nM,与文献值接近(Kim,D.,L.Wang,et al.J.Med.Chem 48(1):141-151.2005)。
本发明的化合物对DPP-4的抑制活性的测试结果列在表1中。
表1:化合物各浓度对DPP-4抑制率(%)a
a实验结果(抑制率)用(平均值±标准差)表示(n≥2)
2.实施例化合物对DPP-8和DPP-9的选择性测定
DPP-8、DPP-9与DPP-4同属于丝氨酸蛋白酶家族,DPP-8和DPP-9的抑制会引起多器官毒性和严重的免疫毒性(Lankas,G.R.,B.Leiting,et al.Diabetes 54:2988-2994.2005),所以DPP-4抑制剂的选择性非常重要。人重组DPP-8酶购自abcam,人重组DPP-9酶购自R&D Systems。在96孔板100μL/孔的筛药体系中,H-Gly-Pro-AMC底物的终浓度为0.1mg/ml,加入不同浓度的待测化合物37℃孵育30min后,以激发波长(EX)380nm/发射波长(EM)460nm检测荧光信号。根据体系的荧光值计算受试样品对DPP-8和DPP-9的抑制率(%),并将酶活性抑制率达到50%时的浓度定为该化合物作用的IC50值。抑制率(%)根据下式进行:
抑制率%=(RFU空白-RFU化合物)/(RFU空白-RFU阴性对照)X100%
RFU化合物、RFU空白和RFU阴性对照分别表示化合物孔、空白孔和不加酶的阴性对照孔30min与0min的荧光值之差。
以Sitagliptin作为阳性对照,比较化合物对DPP-8/9的选择性。
实验结果见表2、表3和表4,表2为实施例5化合物和Sitagliptin对DPP-8和DPP-9的抑制活性的IC50,如表3所示,实施例5化合物对于DPP-8的抑制活性的IC50与DPP-4的IC50之比约为3296倍,对于DPP-9的抑制活性的IC50与DPP-4的IC50之比大于5000倍而阳性药Sitagliptin相应的分别仅有约1139倍和大于2900倍,说明实施例5化合物比阳性药Sitagliptin具有更好的选择性。表4为其他实施例化合物对DDP8和DPP-9的抑制率。
表2:小分子抑制剂对DDP8和DPP-9的抑制率(IC50:单位:μM)
表3:小分子抑制剂对DDP8和DPP-9的选择性倍数
表4:小分子抑制剂对DDP8和DPP-9的抑制率
3.实施例化合物改善C57BLKS/J小鼠口服糖耐量水平
6-8周龄雄性C57BLKS/J小鼠按上海药物研究所SPF级动物饲养标准操作规程饲养。小鼠随机分组,每组6-8只,测量体重,禁食12h后,尾静脉取血,利用罗氏血糖仪及血糖试纸测空腹血糖水平。
受试化合物按不同剂量灌胃给药,给药后60分钟,各组小鼠进行口服糖耐量实验(Oral glucose tolerance test,OGTT)。具体步骤为:化合物灌胃给药后60分钟,再次测定各组小鼠的血糖水平,同时灌胃给予5g/kg体重葡萄糖溶液,并计为0时间点,然后分别在20、40和80分钟,尾静脉取血测血糖水平,绘制OGTT曲线,计算曲线下面积(AUC),利用单因素方差分析计算各组差异。
对实施例5化合物(代号TPN6573)进行详细的浓度梯度实验,以Sitagliptin为阳性对照,得到实验结果如图1(a)和图1(b)所示,实施例5化合物(代号TPN6573)能够显著改善小鼠的葡萄糖耐受,在较低剂量下(1mg/kg)仍然有很强的体内活性。
对其他实施例化合物,给药剂量10mg/kg,检测其在小鼠模型上对急性糖耐量的作用(表5),其中AUC抑制百分比=(对照组AUC-化合物组AUC)/对照组AUC*100%。
表5实施例化合物对血糖的抑制作用
由上表可见,实施例化合物显著改善了小鼠糖耐量,显示了较强的体内降糖活性。
4.实施例5化合物(代号TPN6573)单剂量C57BLKS/J小鼠急性毒性实验
6-8周龄雄性C57BLKS/J小鼠按上海药物研究所SPF级动物饲养标准操作规程饲养。小鼠随机分为2组,每组10只,测量体重,过夜禁食14h后,口服灌胃给药2000mg/kg的实施例5化合物(代号TPN6573),和同等剂量的阳性药sitagliptin作为对照。观察两组小鼠的健康状况;两周之后摘眼球取血,检测丙氨酸转移酶(ALT)和天门冬氨酸转移酶(AST)活性。
两周内两组小鼠并无死亡,进食和饮水都没有明显的异常。测量ALT和AST的结果如图2(a)和图2(b)所示:实验结果表明,与阳性药sitagliptin相比,实施例5化合物(代号TPN6573)并没有明显的毒性。
- 还没有人留言评论。精彩留言会获得点赞!