一种基于RAFT聚合法提高7,8‑二羟基黄酮水溶性的方法与流程
一种基于RAFT聚合法提高7,8-二羟基黄酮水溶性的方法技术领域:本发明属于RAFT聚合、PEG-A单体接枝和药物毒性测试技术领域,涉及一种基于RAFT聚合方法提高7,8-二羟基黄酮水溶性的方法,将PEG-A通过RAFT聚合接枝到药物上从而提高药物的水溶性的方法。
背景技术:
:7,8-二羟基黄酮(7,8-DHF)是一种可以模仿脑源性神经营养因子(BDNF)效应的药物,它可以通过血脑屏障进入大脑细胞组织,对神经系统起到了保护的作用,从而可以用于改善多种脑功能异常的疾病,如帕金森病。但是由于7,8-二羟基黄酮的水溶性较差,影响了它的药物作用时间和效果,因此,考虑通过对7,8-二羟基黄酮进行改性以增加它的水溶性,因为PEG-A结构上的亲水性基团羟基可以大大的提高药物的水溶性,所以寻求设计一种通过RAFT聚合反应在7,8-二羟基黄酮上接枝PEG-A,以达到增加其水溶性目的方法,为治愈帕金森等多种神经退行性疾病提供可行性方案。帕金森病(Parkinson’disease,PD)早期被称为“震颤麻痹”,它是一种常见的缓慢进行性神经系统病变疾病,多发于中老年人,平均发病年龄基本上都在在60岁左右,40岁以下的青年型帕金森患者很少,我国65岁以上人群的帕金森病(PD)患病率更是到了1.7%左右。而且帕金森病(PD)的患病率和发病率还会随着年龄的增长而逐渐的增加,这说明衰老也能增加发病的几率。另外,大多数的帕金森病患者是没有家族史的,只有极少数的病变患者会有家族史。帕金森病的症状在刚开始时可能不太明显,但以后病情会逐渐的加重,一般会先出现肢体的一侧不灵活,然后就会波及到了肢体的另一侧,主要体现在手脚等部位有静止性震颤、运动动作艰难、肌肉僵硬发直、姿势出现平衡性障碍等,但是他们的四肢肌肉力量并没有完全丧失,仍然可以做常人的事情,只不过会比较艰辛。另外,帕金森病患者除了会出现上述的症状外,可能还会伴随着其他非运动的症状,如情绪异常的低落消沉、恐慌焦虑、失眠、认知有障碍、身体会感到疲惫及疼痛等等。帕金森疾病的这一系列症状已经给患者和他们的家人带来了严重的不便,更是惊醒人们要深刻的认识他们的危害,积极的了解帕金森疾病的相关知识。虽然随着研究学者不断的探讨研究,对帕金森病(PD)的了解也是逐步的深入,但是由于帕金森病理的这个谜团至今也尚未解开,抗帕金森(PD)药物的反应机理更是复杂多变,所以即使目前治疗帕金森(PD)疾病的方法和路径如雨后春笋般层出不穷,PD的治疗仍然是以药物疗法为主。现在,药物治疗的原理主要是及时补充人体内缺失的多巴胺,市面上的药品主要有抗胆碱类、多巴类(左旋多巴)、多巴胺受体激动剂和促动剂等等,这些药品虽然可以在一定时期内可以保护和修复一些神经,缓解患者的帕金森症状,提高他们的生活质量,但是如果长期的服用这些药物,大多数的患者可能会出现治疗效果减弱、症状波荡起伏不定、精神异常、机体运动障碍等副作用,甚至一些药物产生的代谢物会与细胞内的某些物质发生有毒反应,加重了患者的症状。所以需要寻找更加持续高效且健康的药品,在近期的研究中,科学家发现7,8-二羟基黄酮不仅可以减少细胞的死亡和神经细胞元的丧失来保护神经系统,还可以穿过血脑屏障进入大脑,仿照脑源性神经保护因子(BDNF)的表达,继而增加了基底内胆碱神经元的数目,从而提高了神经元细胞群的抗氧化能力,达到保护神经系统的目的。
技术实现要素:
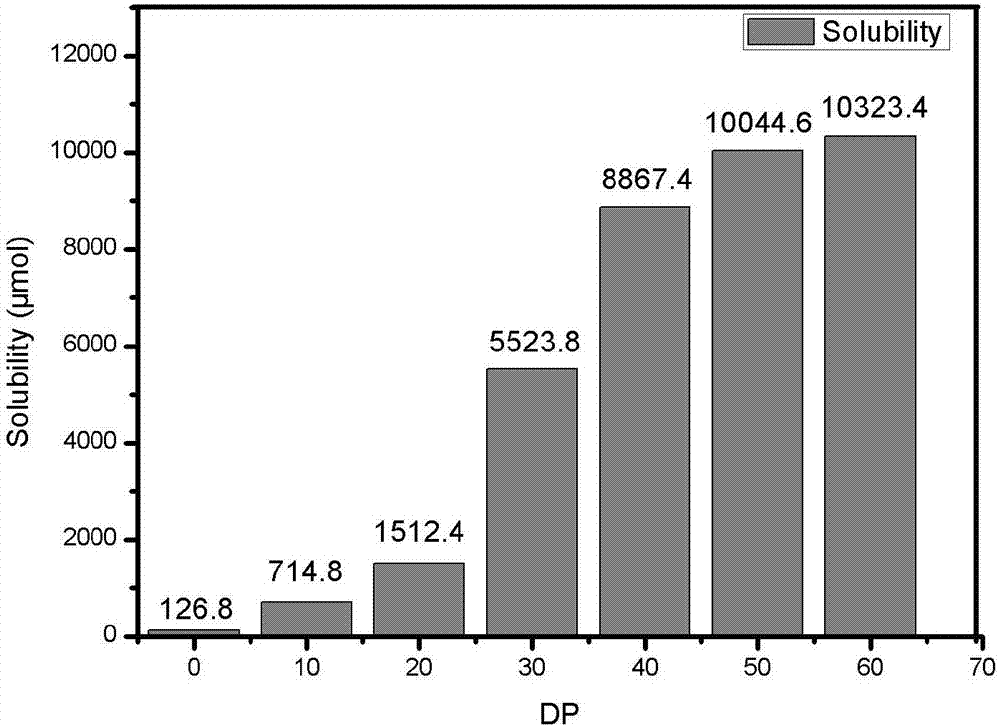
:本发明的目的在于克服现有技术存在的缺点,寻求设计提供一种通过RAFT聚合法提高7,8-二羟基黄酮水溶性的方法,通过RAFT聚合反应在7,8-DHF上接枝PEG-A,以达到增加其水溶性的目的。为了实现上述目的,本发明具体包括以下步骤:1、将RAFT试剂进行酰氯化反应:(1)分别各取25mL二氯甲烷、四氢呋喃、正己烷、甲苯于容量瓶,并分别置于无水硫酸钠中干燥;(2)称取RAFT试剂1.50g于25mL圆底烧瓶用6mL二氯甲烷溶解,将10mL二氯亚砜用等体积二氯甲烷稀释,逐滴加入到圆底烧瓶,在75℃下回流;(3)将所得产物在40℃下旋蒸至只剩固体,加入5mL甲苯,再次旋蒸,如此重复进行三次;(4)用重量百分比浓度大于98.0%正己烷洗涤沉淀,并超声处理,重复进行三次,得到沉淀;2、将RAFT试剂接枝到7,8-DHF上:(1)取步骤1制备的0.17g沉淀溶于5mL四氢呋喃得到溶解后的沉淀,取0.05g黄酮溶于3mL四氢呋喃并进行超声处理得到溶解后的黄酮冰浴;(2)在溶解后的黄酮冰浴中加入1mL三乙胺,再将溶解后的沉淀逐滴加入到黄酮冰浴中,在30摄氏度温度条件下反应24h;(3)配制1mol/L的稀盐酸溶液100mL;(4)将步骤(2)反应得到的产物50℃下旋蒸,直至只剩下固体沉淀;(5)用步骤(3)配制的稀盐酸洗涤固体沉淀后再用有机膜抽滤,洗去三乙胺盐酸盐等盐类;(6)将剩下的物质溶于二氯甲烷,超声处理后用普通滤纸抽滤,收集滤液;(7)将滤液静止析出固体,抽滤得到固体产物;3、RAFT聚合反应将PEG-A接枝到7,8-DHF上:取5mg固体产物、0.31g单体聚(乙二醇)甲基醚丙烯酸酯(PEG-A)、0.0007gAIBN依次止于25mL圆底烧瓶,通入氮气30分钟,70℃下进行聚合反应24h得到聚合产物。本发明所述RAFT试剂为具有羧基的RAFT试剂。本发明所述步骤3所述单体聚(乙二醇)甲基醚丙烯酸酯(PEG-A)是有双键的PEG单体。本发明步骤3中通过控制单体与RAFT试剂的比例来控制改性后药物(聚合产物)的聚合度,聚合产物的分散度(PDI)<1.3。本发明与现有技术相比,其工艺简单,操作方便,7,8-DHF水溶性的提高效果明显,易于控制分子量,成本低,毒性低,可通过RAFT聚合较为精确控制聚合度,从而合成具有不同分子量,不同聚合度的7,8-DHF。附图说明:图1为本发明的工艺流程原理示意图。图2为本发明实施例1中7,8-DHF溶解度测定图。图3为本发明实施例2中7,8-DHF药物药效测定曲线图,其中(a)7,8-DHF以及改性后的7,8-DHF的绝对药效的测定,(b)为改性后7,8-DHF相对于7,8-DHF药效(100%)的相对药效的测定。具体实施方式:下面通过实例并结合附图对本发明作进一步说明。实施例1:7,8-DHF溶解度的测定本实施例对改性后7,8-DHF(7个样本是通过控制RAFT试剂与单体的比例分别得到,样本1为纯7,8-DHF;样本2比例为1:10;样本3比例为1:20;样本4比例为1:30;样本5比例为1:40;样本6比例为1:50;样本7比例为1:60)的溶解度进行了测定,测定结果如图2所示,从图2中可以看出7,8-DHF的溶解度在10044μmol/L左右,相对于改性前只有126.8μmol/L溶解度的7,8-DHF,改性后的7,8-DHF(聚合度为60时)的溶解度提高了78倍。实施例2:改性后药物药效的测定本实施例对改性后的7,8-DHF药物药效进行测定,结果如图3所示,从图3(a)可以看出,这7个聚合度的样本的血管舒张度分别是88.6±6.2%,84.3±4.3%,80.2±6.2%,79.6±3.3%,77.2±4.9%,75.9±3.8%and70.2±1.8%;图3(b)表明改性后的7,8-DHF的药效随着聚合度的增加而减小.当聚合度为60时,改性后的7,8-DHF的药效为原药物水平的79.2%。实施例3:改性后细胞毒性的测定(DT为细胞毒性等级)本实施例对改性后7,8-DHF药物对细胞毒性进行测定,结果如表1所示,由表1可得改性后的药物对细胞的毒性等级为一,与原来药物的毒性为同一等级,其药效只有小幅度降低,药物的毒性与原来为同一等级。表1:
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1