鉴定埃及伊蚊抗药性状的成套试剂及其应用的制作方法
本发明涉及生物技术领域中鉴定埃及伊蚊抗药性状的成套试剂及其应用。
背景技术:
埃及伊蚊(Aedes aegypti)是热带地区的重要吸血蚊虫种类,是登革热、登革出血热、黄热病、基孔肯亚热等多种传染病的主要传播媒介。近年来,广东、云南等地相继发生登革热疫情,报告病例数持续上升,疫情形势相当严峻。登革热是世界上分布最广、发病人数最多、危害最大的重要媒虫病之一。鉴于该病迄今为止没有疫苗预防和特效药治疗,所以媒介控制措施成为该病防治最有效的途径。而媒介防治中,化学防治是杀灭蚊虫最重要的方法,尤以高效的拟除虫菊酯为主。拟除虫菊酯是一类化学合成杀虫剂,因其具有快速击倒、杀虫效能高、对人畜等非靶生物低毒、在环境低滞留等特点,自20世纪70年代起就开始广泛用于农业和卫生害虫的防治。然而,拟除虫菊酯的连续过度使用引起了蚊虫抗药性的快速提升,药效不断下降。研究表明埃及伊蚊对氯氰菊酯、溴氰菊酯、氯菊酯和三氟氯氰菊酯等多种拟除虫菊酯均产生了不同程度的抗药性。
拟除虫菊酯主要作用于蚊虫的钠离子通道,钠离子通道结构基因上的点突变是造成蚊虫神经系统对拟除虫菊酯敏感性下降的主要原因,由此产生的抗药性称之为击倒抗性(knockdown resistance,kdr)。已在多种蚊虫体内发现了钠离子通道基因上的点突变导致蚊虫对多种拟除虫菊酯产生抗药性。目前,关于我国埃及伊蚊的kdr抗性机制还没有相关报道,通过我们的前期实验,发现在我国的埃及伊蚊kdr基因上广泛存在三个点突变(S989P、V1016G和F1534C),其中S989P和V1016G与埃及伊蚊对拟除虫菊酯的抗性显著正相关关系,并且发现V1016G突变是我国埃及伊蚊中起主导作用的点突变,其中V1016G突变是kdr基因的第3047位的T突变为G引发的kdr基因编码的蛋白质突变。在对墨西哥、拉丁美洲马提尼克岛和越南的埃及伊蚊的研究中,V1016G点突变也显示出与埃及伊蚊对拟除虫菊酯的抗性相关。目前我国还没有成型的针对埃及伊蚊抗拟除虫菊酯性分子检测方法和试剂盒。
技术实现要素:
本发明所要解决的技术问题是如何鉴定埃及伊蚊的抗药性状。
为解决上述技术问题,本发明首先提供了鉴定或辅助鉴定埃及伊蚊抗药性状的成套试剂。
本发明所提供的鉴定或辅助鉴定埃及伊蚊抗药性状的成套试剂,由名称为分别为A和B的引物组组成;
所述A包括CD2和CD3,所述CD2为SEQ ID No.2所示的单链DNA,所述CD3为SEQ ID No.3所示的单链DNA;所述B包括所述CD2和CD4,所述CD4为SEQ ID No.4所示的单链DNA。
上述成套试剂中,所述A可由所述CD2和所述CD3组成,也可由所述CD2、所述CD3和CD1组成,所述CD1为SEQ ID No.1所示的单链DNA;所述B可由所述CD2和所述CD4组成,也可由所述CD2、所述CD4和所述CD1组成。
上述成套试剂中,所述A和所述B可独立包装。所述A中的所述CD2和所述CD3以及所述CD1均可独立包装。所述B中的所述CD2和所述CD4以及所述CD1均可独立包装。
上述成套试剂中,所述A和所述B仪器使用时,所述A与所述B的摩尔比可为1:1。所述A的所述CD2和所述CD3一起使用时,其质量比可为1:1;所述CD1、所述CD2和所述CD3一起使用时,其质量比可为3:4:4。所述B的所述CD2和所述CD4一起使用时,其质量比可为1:1;所述CD1、所述CD2和所述CD4一起使用时,其质量比可为3:4:4。
为解决上述技术问题,本发明还提供了鉴定或辅助鉴定埃及伊蚊抗药性状的引物组。
本发明所提供的鉴定或辅助鉴定埃及伊蚊抗药性状的引物组,为所述B或所述A。
为解决上述技术问题,本发明还提供了鉴定或辅助鉴定埃及伊蚊抗药性状的系统。
本发明所提供的鉴定或辅助鉴定埃及伊蚊抗药性状的系统,由X1和X2组成;所述X1为所述成套试剂、所述A或所述B,所述X2为进行PCR扩增所需的试剂和/或仪器。所述鉴定或辅助鉴定埃及伊蚊抗药性状的系统可为鉴定或辅助鉴定埃及伊蚊抗药性状的试剂或试剂盒。
为解决上述技术问题,本发明还提供了非疾病诊断和治疗的鉴定或辅助鉴定埃及伊蚊抗药性状的方法。
本发明所提供的非疾病诊断和治疗的鉴定或辅助鉴定埃及伊蚊抗药性状的方法,包括如下Ⅰ或Ⅱ:
Ⅰ、如下J和K:
J、以待测埃及伊蚊基因组DNA为模板,采用所述A和所述B分别进行PCR扩增得到A的PCR产物和B的PCR产物;
K、检测步骤J得到的PCR产物,按照K1)、K2)或K3)确定埃及伊蚊抗药性状:
K1)所述A的PCR产物在250-500bp间为一条带,所述B的PCR产物在250-500bp间无条带,所述待测埃及伊蚊不抗药或候选不抗药;所述A的PCR产物和所述B的PCR产物在250-500bp间均为一条带,所述待测埃及伊蚊抗药或候选抗药;所述A的PCR产物在250-500bp间无条带,所述B的PCR产物在250-500bp间为一条带,所述待测埃及伊蚊抗药或候选抗药;
K2)所述A的PCR产物为344bp的一条带或587bp和344bp的两条带,所述B的PCR产物无条带或为587bp的一条带,所述待测埃及伊蚊不抗药或候选不抗药;所述A的PCR产物和所述B的PCR产物均为344bp的一条带或587bp和344bp的两条带,所述待测埃及伊蚊抗药或候选抗药;所述A的PCR产物无条带或587bp的一条带,所述B的PCR产物为344bp的一条带或587bp和344bp的两条带,所述待测埃及伊蚊抗药或候选抗药;
K3)所述A的PCR产物为SEQ ID No.6和SEQ ID No.5所示的两个DNA片段或SEQ ID No.6所示的DNA片段,所述B的PCR产物为SEQ ID No.5所示的DNA片段或无DNA片段,所述待测埃及伊蚊不抗药或候选不抗药;所述A的PCR产物为SEQ ID No.6和SEQ ID No.5所示的两个DNA片段或SEQ ID No.6所示的DNA片段,所述B的PCR产物为SEQ ID No.7和SEQ ID No.5所示的两个DNA片段或SEQ ID No.7所示的DNA片段,所述待测埃及伊蚊抗药或候选抗药;所述A的PCR产物为SEQ ID No.5所示的DNA片段或无DNA片段,所述B的PCR产物为SEQ ID No.7和SEQ ID No.5所示的两个DNA片段或SEQ ID No.7所示的DNA片段,所述待测埃及伊蚊抗药或候选抗药;
Ⅱ、如下L和M:
L、以待测埃及伊蚊基因组DNA为模板,采用所述B进行PCR扩增得到B的PCR产物;
M、检测步骤L得到的PCR产物,按照M1)、M2)或M3)确定埃及伊蚊抗药性状:
M1)所述B的PCR产物在250-500bp间无条带,所述待测埃及伊蚊不抗药或候选不抗药;所述B的PCR产物在250-500bp间为一条带,所述待测埃及伊蚊抗药或候选抗药;
M2)所述B的PCR产物无条带或为587bp的一条带,所述待测埃及伊蚊不抗药或候选不抗药;所述B的PCR产物为344bp的一条带或587bp和344bp的两条带,所述待测埃及伊蚊抗药或候选抗药;
M3)所述B的PCR产物为SEQ ID No.5所示的DNA片段或无DNA片段,所述待测埃及伊蚊不抗药或候选不抗药;所述B的PCR产物为SEQ ID No.7和SEQ ID No.5所示的两个DNA片段或SEQ ID No.7所示的DNA片段,所述待测埃及伊蚊抗药或候选抗药。
上述非疾病诊断和治疗的鉴定或辅助鉴定埃及伊蚊抗药性状的方法中,所述A和所述B在两个体系中分别进行PCR扩增。所述A的PCR扩增体系可含有待测埃及伊蚊基因组DNA,所述CD1、所述CD2、所述CD3,DNA聚合酶,dNTPs,去离子水,Mg2+。25μL的A的PCR扩增体系可含有100ng待测埃及伊蚊基因组DNA,所述CD1、所述CD2和所述CD3的浓度可分别为0.08μM、0.12μM和0.16μM。PCR扩增条件可为:
所述B的PCR扩增体系可含有待测埃及伊蚊基因组DNA,所述CD1、所述CD2、所述CD4,DNA聚合酶,dNTPs,去离子水,Mg2+。25μL的B的PCR扩增体系可含有100ng待测埃及伊蚊基因组DNA,所述CD1、所述CD2和所述CD4的浓度可分别为0.08μM、0.12μM和0.16μM。PCR扩增条件可为:
所述DNA聚合酶和所述dNTPs均可为宝生物工程有限公司产品。
为解决上述技术问题,本发明还提供了鉴定或辅助鉴定埃及伊蚊基因型的方法。
本发明所提供的鉴定或辅助鉴定埃及伊蚊基因型的方法,所述基因型为RR基因型、RS基因型和SS基因型,所述方法包括如下O和P:
O、以待测埃及伊蚊基因组DNA为模板,采用所述A和所述B分别进行PCR扩增得到A的PCR产物和B的PCR产物;
P、检测步骤O得到的PCR产物,按照P1)、P2)或P3)确定埃及伊蚊基因型:
P1)所述A的PCR产物在250-500bp间为一条带,所述B的PCR产物在250-500bp间无条带,所述待测埃及伊蚊的基因型为SS基因型;所述A的PCR产物和所述B的PCR产物在250-500bp间均为一条带,所述待测埃及伊蚊的基因型为RS基因型;所述A的PCR产物在250-500bp间无条带,所述B的PCR产物在250-500bp间为一条带,所述待测埃及伊蚊的基因型为RR基因型;
P2)所述A的PCR产物为344bp的一条带或587bp和344bp的两条带,所述B的PCR产物无条带或为587bp的一条带,所述待测埃及伊蚊的基因型为SS基因型;所述A的PCR产物和所述B的PCR产物均为344bp的一条带或587bp和344bp的两条带,所述待测埃及伊蚊的基因型为RS基因型;所述A的PCR产物无条带或587bp的一条带,所述B的PCR产物为344bp的一条带或587bp和344bp的两条带,所述待测埃及伊蚊的基因型为RR基因型;
P3)所述A的PCR产物为SEQ ID No.6和SEQ ID No.5所示的两个DNA片段或SEQ ID No.6所示的DNA片段,所述B的PCR产物为SEQ ID No.5所示的DNA片段或无DNA片段,所述待测埃及伊蚊的基因型为SS基因型;所述A的PCR产物为SEQ ID No.6和SEQ ID No.5所示的两个DNA片段或SEQ ID No.6所示的DNA片段,所述B的PCR产物为SEQ ID No.7和SEQ ID No.5所示的两个DNA片段或SEQ ID No.7所示的DNA片段,所述待测埃及伊蚊的基因型为RS基因型;所述A的PCR产物为SEQ ID No.5所示的DNA片段或无DNA片段,所述B的PCR产物为SEQ ID No.7和SEQ ID No.5所示的两个DNA片段或SEQ ID No.7所示的DNA片段,所述待测埃及伊蚊的基因型为RR基因型。
其中,所述采用所述A和所述B分别进行PCR扩增可利用上述非疾病诊断和治疗的鉴定或辅助鉴定埃及伊蚊抗药性状的方法中的反应体系和反应条件进行。
上述鉴定或辅助鉴定埃及伊蚊基因型的方法中,所述SS基因型为埃及伊蚊的两条染色体中kdr基因的第3047位均为T;所述RS基因型为埃及伊蚊的两条染色体中一条染色体kdr基因的第3047位为T,另一条染色体kdr基因的第3047位为G;所述RR基因型为埃及伊蚊的两条染色体中kdr基因的第3047位均为G。所述SS基因型的埃及伊蚊为不抗药埃及伊蚊,所述RS基因型和所述RR基因型的埃及伊蚊均为抗药埃及伊蚊。
为解决上述技术问题,本发明还提供了下述任一应用:
H1、所述成套试剂、所述A、所述B或所述系统在制备鉴定或辅助鉴定埃及伊蚊抗药性状的试剂或试剂盒中的应用;
H2、所述成套试剂、所述A、所述B或所述系统在非疾病诊断和治疗的鉴定或辅助鉴定埃及伊蚊抗药性状中的应用;
H3、所述鉴定或辅助鉴定埃及伊蚊基因型的方法在鉴定或辅助鉴定埃及伊蚊抗药性状中的应用。
为解决上述技术问题,本发明还提供了所述成套试剂的制备方法。
本发明所提供的所述成套试剂的制备方法,包括1)或2):
1)将所述A和所述B单独包装;
2)将所述A和所述B的各单链DNA单独包装。
本发明中,所述抗药为抗拟除虫菊酯,如抗氯氰菊酯、溴氰菊酯、氯菊酯和/或三氟氯氰菊酯。
本发明提供的鉴定或辅助鉴定埃及伊蚊的成套试剂,可用来鉴定埃及伊蚊对拟除虫菊酯的抗药性状况,快捷、简便、灵敏。采用本发明的鉴定或辅助鉴定埃及伊蚊的成套试剂,只需提取单只埃及伊蚊的基因组DNA进行PCR鉴定,因此对待测埃及伊蚊的数量没有特殊的要求,另外还无需埃及伊蚊的饲养场所和设施,也不需要投入长时间的人力物力来观察。独立1人2小时内即可完成50份样本的检验,被检样本能够准确、有效、直接地检测出点突变,能够区分抗性个体和敏感个体,鉴定准确率达100%。比针对kdr基因的其它引物对检测埃及伊蚊对拟除虫菊酯抗药性的灵敏度和特异性显著增加。
附图说明
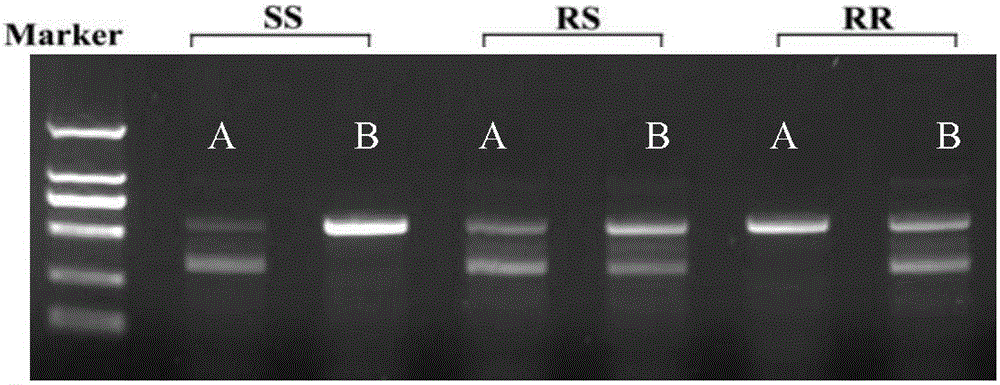
图1为三种基因型的电泳结果。
图2为鉴定埃及伊蚊抗药性状的成套试剂的检测条件的探索。
图3为鉴定埃及伊蚊抗药性状的成套试剂的检测条件的探索。
图4为鉴定埃及伊蚊抗药性状的成套试剂的检测条件的探索。
图5为鉴定埃及伊蚊抗药性状的成套试剂的检测条件的探索。
图6为鉴定埃及伊蚊抗药性状的成套试剂的检测条件的探索。
图7为鉴定埃及伊蚊抗药性状的其它引物的检测结果。
图1-图7中,A表示A管的PCR产物;B表示B管的PCR产物,SS表示SS基因型,RS表示RS基因型;RR表示RR基因型。
具体实施方式
下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。
下述实施例中的实验方法,如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例1、鉴定埃及伊蚊抗药性状的成套试剂的制备
鉴定埃及伊蚊抗药性状的成套试剂,由名称为分别为A和B的引物组组成;
A由CD1、CD2和CD3组成,B由CD1、CD2和CD4组成,CD1为SEQ ID No.1所示的单链DNA,CD2为SEQ ID No.2所示的单链DNA,CD3为SEQ ID No.3所示的单链DNA,CD4为SEQ ID No.4所示的单链DNA。
CD1和CD2可从野生型的埃及伊蚊基因组或含有V1016G突变的伊蚊基因组中扩增出序列5所示的587bp的DNA片段,CD2和CD3可从野生型的埃及伊蚊基因组中扩增出序列6所示的344bp的DNA片段,CD2和CD4可从含有V1016G突变的埃及伊蚊基因组中扩增出序列7所示的344bp的DNA片段。
实施例2、埃及伊蚊抗药性检测
分别提取野外捕获的编号为AA001-AA100的100只埃及伊蚊的基因组DNA。
将每只埃及伊蚊的基因组DNA分别按照如下方法进行PCR扩增(扩增体系如表1):
(1)取试剂T(宝生物工程有限公司,产品号DR011,试剂T的组分如表2所示)分别加入到2个PCR管中,标记为A管和B管,每管12.5μL。
(2)向A管中加入1.1μL试剂P1,向B管中加入1.1μL试剂P2。试剂P1为实施例1的CD1、CD2和CD3与水组成的溶液,试剂P1中CD1、CD2和CD3的摩尔比为3:4:4;试剂P1为实施例1的CD1、CD2和CD4与水组成的溶液,试剂P1中CD1、CD2和CD4的摩尔比为3:4:4。
(3)分别向A管和B管中加入9.9μL去离子水。
(4)分别向A管和B管中加入1.5μL埃及伊蚊的基因组DNA,每管埃及伊蚊的基因组DNA约为100ng。
(5)将以上的A管和B管中所有成分混合均匀后,放入PCR仪中,按以下PCR扩增条件设置反应条件。A管的体系中CD1、CD2和CD3的浓度分别为0.12μM、0.16μM和0.16μM;B管的体系中CD1、CD2和CD4的浓度分别为0.12μM、0.16μM和0.16μM。
表1、PCR扩增体系
表2、T试剂的配方
PCR扩增条件:
每只埃及伊蚊分别得到两种PCR产物,A管的PCR产物为A的PCR产物,B管的PCR产物为B的PCR产物。用1.5%的琼脂糖凝胶电泳对所有的PCR产物进行检测。根据每只埃及伊蚊基因组的两种PCR产物判断其基因型,结果如表3所示。基因型的判断方法为:如果A的PCR产物在250-500bp间为一条带,B的PCR产物在250-500bp间无条带,埃及伊蚊的基因型为SS基因型;如果A的PCR产物和B的PCR产物在250-500bp间均为一条带,埃及伊蚊的基因型为RS基因型;如果A的PCR产物在250-500bp间无条带,B的PCR产物在250-500bp间为一条带,埃及伊蚊的基因型为RR基因型。SS基因型的埃及伊蚊不抗药,RS基因型和RR基因型的埃及伊蚊均抗药。三种基因型的电泳结果如图1所示。
表3、埃及伊蚊基因组鉴定结果及抗药性
表3中,+表示含有一条带,-表示无条带。
将A的PCR产物和B的PCR产物的250-500bp间的DNA片段进行测序,A的PCR产物的250-500bp间的DNA片段均为序列6所示的DNA片段,相应的埃及伊蚊的基因组DNA均无V1016G突变;B的PCR产物的250-500bp间的DNA片段均为序列7所示的DNA片段,相应的埃及伊蚊的基因组DNA均含有V1016G突变。表明B的PCR产物250-500bp间的DNA片段为序列7所示的DNA片段的埃及伊蚊抗药,而B的PCR产物250-500bp间无DNA片段、A的PCR产物的250-500bp间的DNA片段为序列6所示的DNA片段的埃及伊蚊不抗药。测序结果表明利用鉴定埃及伊蚊抗药性状的成套试剂鉴定埃及伊蚊的抗药性的方法是可行的,并且鉴定埃及伊蚊抗药性状的准确率达100%。
对比例1、鉴定埃及伊蚊抗药性状的成套试剂的检测条件的探索
1、检测条件1
将实施例2中表1的PCR扩增体系替换为表4的体系,退火温度替换为61℃,分别对三种基因型的埃及伊蚊进行检测。
表4、PCR扩增体系A
其中,试剂A1为实施例1的CD1、CD2和CD3与水组成的溶液,试剂A1中CD1、CD2和CD3的摩尔比为1:2:1,A管的体系中CD1、CD2和CD3的浓度分别为0.12μM、0.24μM和0.12μM;试剂A2为实施例1的CD1、CD2和CD4与水组成的溶液,试剂A2中CD1、CD2和CD4的摩尔比为1:2:1,B管的体系中CD1、CD2和CD4的浓度分别为0.12μM、0.24μM和0.12μM。
在使用上述引物和PCR方法条件下,电泳结果如图2,目的条带有的清晰有的较弱,仍然有较明显的杂带,影响结果判断。
2、检测条件2
将实施例2中表1的PCR扩增体系替换为表5的体系,退火温度替换为61℃,分别对三种基因型的埃及伊蚊进行检测。
表5、PCR扩增体系B
其中,试剂B1为实施例1的CD1、CD2和CD3与水组成的溶液,试剂B1中CD1、CD2和CD3的摩尔比为4:6:3,A管的体系中CD1、CD2和CD3的浓度分别为0.16μM、0.24μM和0.12μM;试剂B2为实施例1的CD1、CD2和CD4与水组成的溶液,试剂B2中CD1、CD2和CD4的摩尔比为4:6:3,B管的体系中CD1、CD2和CD4的浓度分别为0.16μM、0.24μM和0.12μM。
在使用上述引物和PCR方法条件下,电泳结果如图3,目的条带不清晰,影响结果判断。
3、检测条件3
将实施例2中表1的PCR扩增体系替换为表6的体系,退火温度替换为61℃,分别对三种基因型的埃及伊蚊进行检测。
表6、PCR扩增体系C
其中,试剂C1为实施例1的CD1、CD2和CD3与水组成的溶液,试剂C1中CD1、CD2和CD3的摩尔比为2:5:2,A管的体系中CD1、CD2和CD3的浓度分别为0.08μM、0.20μM和0.08μM;试剂C2为实施例1的CD1、CD2和CD4与水组成的溶液,试剂C2中CD1、CD2和CD4的摩尔比为2:5:2,B管的体系中CD1、CD2和CD4的浓度分别为0.08μM、0.20μM和0.08μM。
在使用上述引物和PCR方法条件下,电泳结果如图4,目的条带不清晰,而且有较弱杂带,影响结果判断。
4、检测条件4
将实施例2中表1的PCR扩增体系替换为上表6的体系,退火温度替换为62℃,分别对三种基因型的埃及伊蚊进行检测。
在使用上述引物和PCR方法条件下,电泳结果如图5,目的条带不清晰,而且有多条杂带,影响结果判断。
5、检测条件5
将实施例2中表1的PCR扩增体系替换为表7的体系,退火温度替换为61℃,分别对三种基因型的埃及伊蚊进行检测。
表7、PCR扩增体系D
其中,试剂D1为实施例1的CD1、CD2和CD3与水组成的溶液,试剂D1中CD1、CD2和CD3的摩尔比为3:2:4,A管的体系中CD1、CD2和CD3的浓度分别为0.12μM、0.08μM和0.16μM;试剂D2为实施例1的CD1、CD2和CD4与水组成的溶液,试剂D2中CD1、CD2和CD4的摩尔比为3:2:4,B管的体系中CD1、CD2和CD4的浓度分别为0.12μM、0.08μM和0.16μM。
在使用上述引物和PCR方法条件下,电泳结果如图6,目的条带不清晰,影响结果判断。
对比例2、鉴定埃及伊蚊抗药性状的其它引物
将实施例2中的CD1、CD2、CD3和CD4分别替换为CD1′(GCCACCGTAGTGATAGGAAATC)、CD2′(CGGGTTAAGTTTCGTTTAGTAGC)、CD3′(TGTTTCCCACTCGCACAGGT)和CD4′(TGTTTCCCACTCGCACAGGG),CD1′、CD2′、CD3′和CD4′均为单链DNA,按照表8的扩增体系分别对三种基因型的埃及伊蚊进行检测。
表8、PCR扩增体系E
其中,试剂E1为CD1′、CD2′和CD3′与水组成的溶液,试剂E1中CD1′、CD2′和CD3′的摩尔比为1:2:1,A管的体系中CD1′、CD2′和CD3′的浓度分别为0.12μM、0.24μM和0.12μM;试剂E2为实施例1的CD1′、CD2′和CD4′与水组成的溶液,试剂E2中CD1′、CD2′和CD4′的摩尔比为1:2:1,B管的体系中CD1′、CD2′和CD4′的浓度分别为0.12μM、0.24μM和0.12μM。
PCR扩增条件:
在使用上述引物和PCR方法条件下,电泳结果如图7,虽然目的条带清晰可见,但是有明显杂带,影响结果判断。
<110> 中国人民解放军军事医学科学院微生物流行病研究所
<120> 鉴定埃及伊蚊抗药性状的成套试剂及其应用
<160> 7
<170> PatentIn version 3.5
<210> 1
<211> 25
<212> DNA
<213> 人工序列
<220>
<223>
<400> 1
caccgtagtg ataggaaatc tagta 25
<210> 2
<211> 25
<212> DNA
<213> 人工序列
<220>
<223>
<400> 2
gttaagtttc gtttagtagc ggtag 25
<210> 3
<211> 18
<212> DNA
<213> 人工序列
<220>
<223>
<400> 3
tttcccactc gcacaggt 18
<210> 4
<211> 18
<212> DNA
<213> 人工序列
<220>
<223>
<400> 4
tttcccactc gcacaggg 18
<210> 5
<211> 587
<212> DNA
<213> 埃及伊蚊(Aedes aegypti)
<400> 5
caccgtagtg ataggaaatc tagtagtaag tattccgttt ggaagttcat ctgtaaggct 60
gactgaaagt aaattggagc gcacaacaga cctattatgc tgtaattcgt gattcaacta 120
gttacaaaag accgttgatc ttgatagcat caatattaga ggcgtgctag cagcgagcga 180
ggggcgtacc aatttacttt tagtcagtct ttcttgcatt ctttcgtgct aaccgacaaa 240
ttgtttccca ctcgcacagg tacttaacct tttcttagcc ttgcttttgt ccaatttcgg 300
ttcatcctcg ctgtcggcac cgacggccga caacgaaacg aacaagatcg cggaggcgtt 360
caatcggata tcgcgcttct ccaactggat caagtcgaac atcgccaacg cgctcaagtt 420
cgtgaaaaac aagttaacaa gccagattgc gtccgtgcag cccgcaggtg agcagcacaa 480
tcatctcagt tggatatgga acgaaggtta ttatccactt gcgttttcta acactaaact 540
aaataactat ctgttactac tactaccgct actaaacgaa acttaac 587
<210> 6
<211> 344
<212> DNA
<213> 埃及伊蚊(Aedes aegypti)
<400> 6
tttcccactc gcacaggtac ttaacctttt cttagccttg cttttgtcca atttcggttc 60
atcctcgctg tcggcaccga cggccgacaa cgaaacgaac aagatcgcgg aggcgttcaa 120
tcggatatcg cgcttctcca actggatcaa gtcgaacatc gccaacgcgc tcaagttcgt 180
gaaaaacaag ttaacaagcc agattgcgtc cgtgcagccc gcaggtgagc agcacaatca 240
tctcagttgg atatggaacg aaggttatta tccacttgcg ttttctaaca ctaaactaaa 300
taactatctg ttactactac taccgctact aaacgaaact taac 344
<210> 7
<211> 344
<212> DNA
<213> 埃及伊蚊(Aedes aegypti)
<400> 7
tttcccactc gcacagggac ttaacctttt cttagccttg cttttgtcca atttcggttc 60
atcctcgctg tcggcaccga cggccgacaa cgaaacgaac aagatcgcgg aggcgttcaa 120
tcggatatcg cgcttctcca actggatcaa gtcgaacatc gccaacgcgc tcaagttcgt 180
gaaaaacaag ttaacaagcc agattgcgtc cgtgcagccc gcaggtgagc agcacaatca 240
tctcagttgg atatggaacg aaggttatta tccacttgcg ttttctaaca ctaaactaaa 300
taactatctg ttactactac taccgctact aaacgaaact taac 344
- 还没有人留言评论。精彩留言会获得点赞!