一种交联菊糖的制备方法与流程
本发明涉及菊糖生产技术领域,特别是涉及一种交联菊糖的制备方法。
背景技术:
菊糖(inulin),又称菊粉、土木香粉,多存在于菊科植物中,如菊芋、大丽菊等的块茎和菊苣、牛蒡等的根。菊糖是一种天然果糖聚合物,由d-呋喃果糖分子以β-(2,1)糖苷键连接而成,每个菊糖分子末尾以α-(1,2)糖苷键连接一个葡萄糖残基,聚合度通常为2~60,平均聚合度为10。菊糖作为一种生物多糖,具有肠道益生菌、促进矿物质吸收、抗氧化、降血糖、降血脂等多种生理功能。同时,菊糖具有良好的溶解性、凝胶特性、保湿性和较高粘度,能够改善食品质构、提高食品的流变学特性和营养学特性,因而,菊糖成为近几年研究热点之一。
然而,现在研究菊糖大多采用直接提取的天然菊糖,天然菊糖的分子量跨度很大,平均聚合度较低,导致其性质不稳定,例如形成凝胶状态不稳定。
技术实现要素:
鉴于以上所述现有技术的缺点,本发明的目的在于提供一种交联菊糖的制备方法,用于解决现有技术中菊糖性质不稳定等问题。
为实现上述目的及其他相关目的,本发明提供一种交联菊糖的制备方法,配制含有菊糖和交联剂的水溶液,调节体系ph在7-11,在15-75℃下反应,得到交联菊糖。
在本发明的一些实施例中,配制含有菊糖和交联剂的水溶液时,菊糖在水溶液中的质量浓度为2.5-12.5%。
在本发明的一些实施例中,配制含有菊糖和交联剂的水溶液时,菊糖在水溶液中的质量浓度为2.5-7.5%。
在本发明的一些实施例中,配制含有菊糖和交联剂的水溶液时,菊糖在水溶液中的质量浓度为2.5-5%。
在本发明的一些实施例中,交联剂选自六偏磷酸钠、三偏磷酸钠中的至少一种。
在本发明的一些实施例中,加入交联剂的质量为菊糖干重的2-14%。
在本发明的一些实施例中,加入交联剂的质量为菊糖干重的8-14%。
在本发明的一些实施例中,加入交联剂的质量为菊糖干重的10-14%。
在本发明的一些实施例中,配制含有菊糖和交联剂的水溶液时,用于调节体系ph的试剂选自na2co3水溶液、naoh水溶液中的至少一种。
在本发明的一些实施例中,配制含有菊糖和交联剂的水溶液时,调节体系ph在9.5-11。
在本发明的一些实施例中,反应温度为30-60℃。
在本发明的一些实施例中,调节体系ph后,反应时间为0.5-4.5h。
在本发明的一些实施例中,调节体系ph后,反应时间为2.5-4.5h。
在本发明的一些实施例中,反应结束后,调节体系ph至中性,向体系中加入有机溶剂,交联菊糖沉淀后,固液分离,得到的固体即为交联菊糖。
在本发明的一些实施例中,反应结束后,采用盐酸调节体系ph。
在本发明的一些实施例中,反应结束后,调节体系ph至7.0±0.2。
在本发明的一些实施例中,有机溶剂选自无水乙醇、体积浓度为95%的乙醇水溶液中的至少一种。
在本发明的一些实施例中,对得到的固体进行真空冷冻干燥,得到交联菊糖。
在本发明的一些实施例中,真空冷冻干燥的压力≤60pa。
在本发明的一些实施例中,真空冷冻干燥的温度为-60~-40℃。
在本发明的一些实施例中,真空冷冻干燥的时间为8~12h。
本发明第二方面提供上述方法制得的交联菊糖。
本发明第三方面提供上述交联菊糖在食品生产中的用途,可作为食品添加剂,如食品中脂肪替代品、质构改良剂、稳定剂、抗老化剂、防冻剂、辅助乳化剂等。
如上所述,本发明的一种交联菊糖的制备方法,具有以下有益效果:本发明对菊糖分子进行磷酸基交联,制备菊糖磷酸酯,明显提高其平均聚合度,使其具备更高粘度和凝胶特性。
附图说明
图1显示为本发明实施例的磷含量标准曲线图。
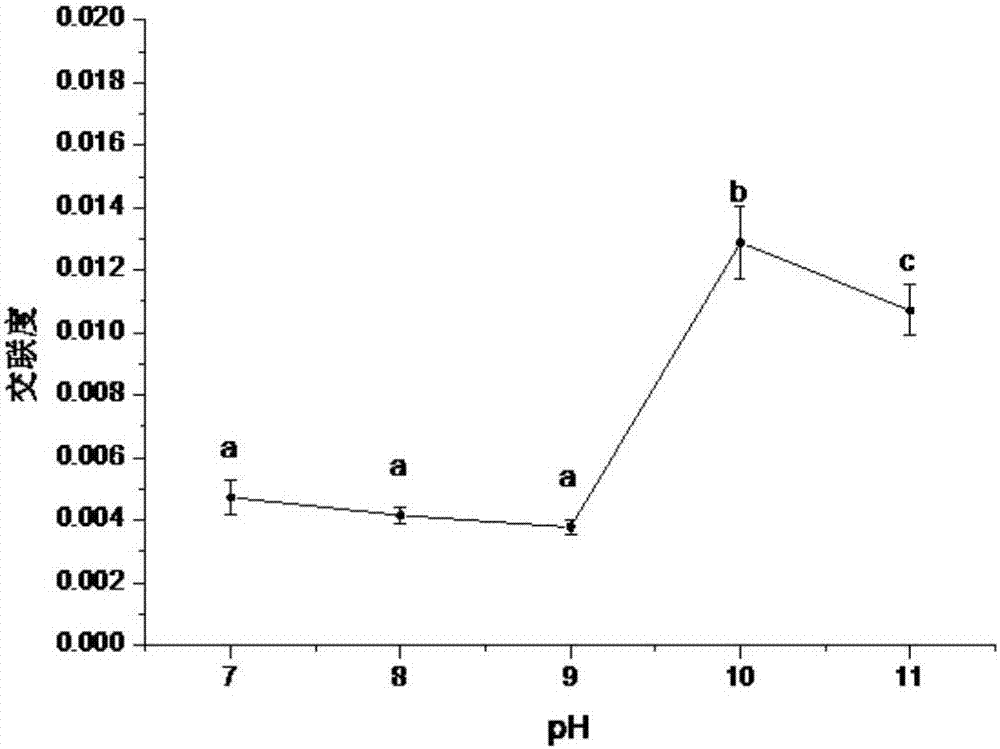
图2显示为本发明实施例中ph对交联度的影响曲线图。
图3显示为本发明实施例中菊糖质量浓度对交联度的影响曲线图。
图4显示为本发明实施例中反应时间对交联度的影响曲线图。
图5显示为本发明实施例中交联剂用量对交联度的影响曲线图。
图6显示为本发明实施例中温度对交联度的影响曲线图。
图7-1显示为本发明实施例中ph和交联剂用量对交联菊糖交联度影响的响应面。
图7-2显示为本发明实施例中ph和交联剂用量对交联菊糖交联度影响的等高线。
图8-1显示为本发明实施例中反应时间和ph对交联菊糖交联度影响的响应面。
图8-2显示为本发明实施例中反应时间和ph对交联菊糖交联度影响的等高线。
图9-1显示为本发明实施例中菊糖质量浓度和交联剂用量对交联菊糖交联度影响的响应面。
图9-2显示为本发明实施例中菊糖质量浓度和交联剂用量对交联菊糖交联度影响的等高线。
图10-1显示为本发明实施例中反应时间和菊糖质量浓度对交联菊糖交联度影响的响应面。
图10-2显示为本发明实施例中反应时间和菊糖质量浓度对交联菊糖交联度影响的等高线。
具体实施方式
以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
文中所提及的交联剂用量是指加入的交联剂质量占菊糖干重的百分比,以下实施例以六偏磷酸钠为交联剂进行实验,当然,本发明也可以采用三偏磷酸钠等其他物质作为交联剂。
1材料与方法
1.1材料与试剂
菊糖,食品级,购于西安瑞林生物科技有限公司;六偏磷酸钠、无水碳酸钠、无水磷酸二氢钠、盐酸、硫酸、硝酸、高氯酸、亚硫酸钠、对苯二酚等均为分析纯,购于成都市科龙化工试剂厂。
1.2仪器与设备
hh-6d数显恒温水浴磁力搅拌器:惠州市宏业仪器有限公司;phs-3型精密酸度计:上海大普仪器有限公司;lgj-10真空冷冻干燥机:北京松源华兴科技发展有限公司;fa2004a电子天平:上海精天电子仪器有限公司;centrifuge5810型台式高速离心机:德国eppendorf公司。
1.3交联菊糖的制备
取一定质量的菊糖原料,配成一定浓度的菊糖溶液,加入一定量的六偏磷酸钠,充分搅拌使其溶解,再向体系中逐滴加入na2co3水溶液,调节体系ph,然后将整个体系置于恒温水浴磁力搅拌装置中,在一定温度和一定搅拌转速下反应一段时间。反应结束后,用一定浓度的hcl水溶液中和至ph为7.0±0.2,加入95%(体积浓度)的乙醇后,在4℃下沉淀过夜,离心,再用95%(体积浓度)的乙醇水溶液洗涤沉淀,然后在压力20pa、温度-55℃条件下真空冷冻干燥12h,得到交联菊糖。
1.4取代度的测定
1.4.1结合磷含量测定
精密称取在105℃下干燥的磷酸二氢钾0.4394g,置于1000ml容量瓶中,加水溶解并稀释至刻度,得到磷标准储备液(100μg/ml),准确吸取10ml磷标准储备液,置于100ml容量瓶中,加水稀释至刻度,混匀,得到磷标准使用液。准确吸取磷标准使用液0ml、0.5ml、1.0ml、2.0ml、3.0ml、4.0ml、5.0ml,分别置于20ml具塞试管中,依次加入2ml0.5%的钼酸铵溶液摇匀,静置几秒钟,加入1ml20%的亚硫酸钠溶液,1ml0.5%对苯二酚溶液,摇匀。加水至刻度,混匀。静置0.5h以后,在分光光度计660nm波长处测定吸光度。以测出的吸光度对磷含量绘制标准曲线。
称取交联菊糖样品0.1g于凯氏烧瓶,加入3ml硫酸、3ml高氯酸-硝酸(1:4,v/v)消化液,置于消化炉上使其消化完全,待溶液放冷后,加20ml水,赶酸。冷却,转移至100ml凯氏烧瓶,合并洗液并倒入容量瓶,加水至刻度,混匀。此溶液为试样测定液。取0.1g菊糖样品按同一方法做空白溶液。准确吸取试样测定液2ml及同量的空白溶液,分别置于20ml具塞试管,后续测定步骤同标准曲线。以测出的吸光度在标准曲线上查得试样液中的磷含量。结果计算见式(1)。
式中:
p——试样中磷含量,单位为毫克每克(mg/g);
m1——由标准曲线查得试样测定液中磷的质量,单位为毫克(mg);
v1——试样消化液定容总体积,单位为毫升(ml);
v2——测定用试样消化液的体积,单位为毫升(ml);
m——试样的质量,单位为克(g)。
计算结果保留两位有效数字。
1.4.2交联度(dlc)的计算
交联度是指每个菊糖分子中葡萄糖残基环上的羟基被磷酸基团取代的平均值,交联菊糖的反应交联度的计算公式如下所示:
式中:
dlc——试样交联度;
δp——试样与空白组磷含量差值,单位为毫克每克(mg/g)。
1.5实验设计
1.5.1单因素试验
选定菊糖质量浓度、交联剂用量、体系ph值、反应温度和反应时间5个因素作单因素试验,考察各单因素对交联度的影响。
1.5.2响应面优化试验
利用分析软件design-expert8.06进行试验设计及数据分析。以交联度为响应指标,利用中心组合设计(ccd)对单因素筛选到的关键因子做进一步的分析,通过实验数据拟合得到二阶响应面模型,最终确定最优实验条件,并进行验证。
1.6数据统计与分析
利用spass17.0软件对试验结果进行差异显著性分析(p<0.05),试验结果以平均值±标准差表示,图中a、d、c、d等不同字母表示p=0.05水平下各试验点具有显著差异。
2结果与讨论
2.1磷含量标准曲线
磷含量标准曲线如图1所示。
2.2单因素试验结果
2.2.1ph值对交联菊糖交联度的影响
以固定菊糖质量浓度5%、交联剂用量11%、反应温度45℃、在不同ph(7、8、9、10、11)条件下反应2.5h,考察不同ph对交联菊糖交联度的影响,结果见图2。
从图2可以看出,碱性条件有利于菊糖的交联,交联度随反应体系ph增加而升高,当反应体系ph超过10时,交联度呈现下降趋势。这是因为,体系ph由na2co3调节,na2co3的作用一方面是活化菊糖分子上的羟基,失去氢原子变成氧负离子形式,产生可以发生交联反应的菊糖-ona活化分子,更容易与六偏磷酸钠发生亲核取代反应,从而增强了交联剂对菊糖分子的渗透能力,交联剂与菊糖分子中羟基的作用机会增加,提高了交联反应的活性和六偏磷酸钠的利用率;另一方面,保证反应体系维持在碱性环境下。ph升高代表反应体系中na2co3浓度增大,na2co3分子渗透到菊糖分子的速度随之加快,生成更多的菊糖钠盐;但ph超过10时,菊糖容易发生碱解从而导致交联度下降。因此,适宜的体系ph为10。
2.2.2菊糖质量浓度对交联菊糖的影响
以固定交联剂用量11%、反应温度45℃、ph值为10,在不同菊糖质量浓度(2.5%、5%、7.5%、10%、12.5%)条件下反应2.5h,考察不同菊糖质量浓度对交联菊糖交联度的影响,结果见图3。
由图3可以看出,当菊糖质量浓度为5%时,交联菊糖的交联度最大。当菊糖质量浓度小于5%时,交联度随菊糖质量浓度的增加而增大;当菊糖质量浓度大于5%时,交联度随菊糖质量浓度的增加而减小。这可能是因为,菊糖质量浓度较低时,交联剂与菊糖分子的接触几率减小,反应效率低,交联度较低,随着菊糖质量浓度的升高,交联剂与菊糖分子的接触几率增加,菊糖分子与交联剂发生亲核取代反应的发生率增强。但是,菊糖质量浓度过高时,反应体系太过粘稠,菊糖分子不能与交联剂充分结合,降低交联程度。因此,适宜的菊糖质量浓度为5%。
2.2.3反应时间对交联菊糖交联度的影响
以固定菊糖质量浓度5%、交联剂用量11%、反应温度45℃、ph值为10的条件下反应不同时间(0.5h、1.5h、2.5h、3.5h、4.5h),考察不同反应时间对交联菊糖交联度的影响,结果见图4。
由图4可以看出,当反应时间为3.5h时,交联菊糖的交联度最大。当反应时间小于3.5h时,交联度随反应时间的延长而增大;当菊糖反应时间超过3.5h后,交联度随反应时间的延长而下降。这是因为,随着反应时间的延长,交联剂与菊糖分子充分接触,反应程度增强,交联度上升,当反应时间达到3.5h时,反应已基本接近终点,交联度达到最大,继续延长反应时间,反应很慢,不仅浪费能源,而且长时间的搅拌导致菊糖分子碱化降解,使得交联度不增反降。因此,适宜的反应时间为3.5h。
2.2.4交联剂用量对交联菊糖交联度的影响
以固定菊糖质量浓度5%、反应温度45℃、ph值为10、不同交联剂用量(2%、5%、8%、11%、14%)的条件下反应2.5h,考察不同交联剂用量对交联菊糖交联度的影响,结果见图5。
由图5可以看出,当交联剂用量为11%时,交联菊糖的交联度最大。当交联剂用量小于11%时,交联度随交联剂的增加而增大;当交联剂用量超过14%后,交联度随交联剂增加略有下降。这是因为随着六偏磷酸钠量的增加,菊糖分子与交联剂接触机会增大,反应效率提高,从而使交联度呈增高趋势。但是,当六偏磷酸钠的用量增加到11%以后,已达到反应所需的用量,菊糖反应完全,交联菊糖交联度变化趋于平稳。并且,若体系中交联剂浓度过高,逆向反应增强,使菊糖交联程度略有下降。因此,适宜的六偏磷酸钠用量为11%。
2.2.5温度对交联菊糖交联度的影响
以固定菊糖质量浓度5%、ph值为10、交联剂用量11%,不同反应温度(15℃、30℃、45℃、60℃、75℃)的条件下反应2.5h,考察不同反应温度对交联菊糖交联度的影响,结果见图6。
由图6可以看出,温度对交联菊糖的交联度影响不显著,当反应温度为45℃时,交联菊糖的交联度最大;当反应温度低于45℃时,交联度随反应温度的升高略有增大;当反应温度超过45℃后,交联度随反应温度的升高略有下降。这是因为当反应温度升高时,分子运动加速,反应物分子间碰撞几率增加,增加了交联剂向菊糖分子内部的扩散速率,有利于交联反应,交联度增大。但是随着反应温度继续升高,六偏磷酸钠的分解程度增大,导致菊糖分子进行交联反应的六偏磷酸钠量随之减少,不利于交联反应的进行。因此,适宜的反应温度为45℃。
2.3响应面法优化试验结果
2.3.1二次多项回归方程的拟合与方差分析
根据单因素试验结果,选取对交联度影响较显著的体系ph、交联剂用量、菊糖质量浓度、反应时间4个因素进行响应面优化,响应面试验设计因素和水平表见表1。
表1.中心组合设计因素水平表
采用design-expertv8.0.6软件对表2数据进行回归拟合,得到交联度(y)的二次多项回归方程如下:
y=+0.014+3.623e-4a+6.497e-4b-5.656e-4c+2.275e-4d+3.779e-4ab+1.406e-5ac+2.479e-4ad-1.798e-4bc+3.606e-4bd+2.717e-4cd-8.684e-4a2-6.136e-4b2-1.069e-4c2-7.588e-4d2(3)
式中:y为交联度;a、b、c、d则分别ph、交联剂用量、菊糖质量浓度和反应时间的编码值。
表2中心组合设计方案及结果
对ccd试验结果进行方差分析,结果见表3。由表3可以看出:模型总回归项p<0.0001,表明本试验所建立的数学回归模型极显著;失拟项p=0.4816,不显著,说明该回归模型选择适当;决定系数r2为0.9804,说明模型预测值与实验真实值之间的相关性可达98.04%,校正决定系数r2adj值0.9621,表明仅有3.79%的变异不能被该回归模型解释,即模型拟合度良好;cv值为3.06%,说明该回归模型所输出的数据精确度较高,误差较低;信噪比为22.959,大于4.0,说明该模型可以在这个设计空间内运行。综合各分析参数,该模型可用来预测交联菊粉的交联度。
对模型中回归系数的显著性检验表明:a、b、c、a2、b2、c2、d2对交联度有极显著影响(p<0.0001),d、ab、ad、cd对交联度影响高度显著(p<0.001),bc对交联度影响显著(p<0.05),其它项系数影响均不显著(p>0.05)。根据系数估计值a=3.623e-4,b=6.497e-4,c=-5.656e-4,d=2.275e-4可知,影响因素的主效应关系为:b>c>a>d。
表3回归模型方差分析
注:p<0.001,表示差异极显著;p<0.01,表示差异高度显著;p<0.05,表示差异显著。
2.3.2各因素交互作用分析
响应曲面图是响应值对应试验因素构成的三维空间曲面图,可以直观地反映各因素及它们之间的交互作用对响应值的影响。响应面曲线越陡,表明该因素对响应值影响越大,反之亦然。由响应面的陡峭程度可知,各因素对响应值影响效应依次为:b>c>a>d,这与方差分析结果相一致。
由方差分析可知,交互项ab、ad、cd高度显著,bc显著。由图7-1和7-2可以看出,交联度随着ph的增大先增加后减小,随交联剂用量的增加而增加并趋于平稳,两因素交互作用较强,影响高度显著。由图8-1和8-2可以看出,随ph和反应时间的增加,交联度呈上升趋势,当ph和反应时间到达某一水平时,交联度达到最大值,此后没有进一步上升而是有所下降,这可能ph较高、时间较长使交联剂和菊糖分子发生分解,两因素交互作用较强,影响高度显著。由图9-1和9-2可以看出,交联度随着菊糖质量浓度的增大先增加后减小,随交联剂用量的增加而增加并趋于平稳,反应体系中菊糖质量浓度和交联剂的用量,影响着菊糖-ona活化分子浓度,进而影响菊糖钠盐与六偏磷酸钠发生亲核反应几率,两因素交互作用较强,影响显著。由图10-1和10-2可以看出,随菊糖质量浓度和反应时间的增加,交联度呈上升趋势,当菊糖质量浓度和反应时间到达某一水平时,交联度达到最大值,此后没有进一步上升而是有所下降,两因素交互作用较强,影响高度显著。因此,在实际应用中,一定温度条件下,可以通过控制交联剂用量、ph、菊糖质量浓度和反应时间以获得较高交联度的交联菊糖。
2.3.3最佳条件的确定与验证试验
从ccd试验设计得到的最优工艺参数为:ph10.19、交联剂用量12.04%、菊粉质量浓度4.63%、反应时间3.59h。此条件下制得交联菊糖的取代度预测值为0.013939。
验证实验结果证实:在响应面优化的最佳工艺条件下,交联度的实测值为0.013663±0.001162,预测精度高达98.02%,证明该模型可用于交联菊粉交联度的预测。
3结论
本实验通过单因素实验筛选对交联菊糖交联度影响显著的因子并对其进行响应面分析,建立了一个以交联度为目标值,以ph、交联剂用量、反应时间、菊糖质量浓度为因子的数学模型,方差分析表明其拟合较好。确定交联菊糖最优制备工艺为ph10.19、交联剂用量12.04%、菊粉浓度4.63%、反应时间3.59h。在此工艺条件下交联菊糖交联度为0.013663±0.001162,平均聚合度超过13,特性粘度可达5.9176±0.234ml/g,40%质量浓度凝胶指数为100。4个试验因素对交联度影响的主次顺位为交联剂用量>菊糖质量浓度>ph>反应时间。
综上所述,本发明对菊糖分子进行磷酸基交联,制备菊糖磷酸酯,明显提高其平均聚合度,使其具备更高粘度和更佳凝胶特性。
上述实施例仅例示性说明本发明的原理及其功效,而非用于限制本发明。任何熟悉此技术的人士皆可在不违背本发明的精神及范畴下,对上述实施例进行修饰或改变。因此,举凡所属技术领域中具有通常知识者在未脱离本发明所揭示的精神与技术思想下所完成的一切等效修饰或改变,仍应由本发明的权利要求所涵盖。
- 还没有人留言评论。精彩留言会获得点赞!