一种软刀素肽的制备方法与流程
本发明属于多肽药物领域,具体涉及一种软刀素肽的制备方法。
背景技术:
软刀素肽(urumin),是一种从青蛙皮肤提取分离的抗流感病毒防御肽,有望用于杀灭h1型流感病毒。软刀素肽的的氨基酸序列如下:iplrgafingrwdsqchrfsngaiaca,其相对分子量为2961.38,它能够靶向h1型季节性流感病毒,物理性地破坏病毒粒子,从而保护幼年小鼠免于h1流感病毒的感染。由于目前的抗病毒药物靶点为na和m2蛋白,本研究的软刀素肽的作用靶点为ha蛋白的茎状结构域。因此,软刀素肽对大多数耐药的h1型流感病毒是有效的。软刀素肽的ic50值(半数有效量)是
但是目前只能从青蛙皮肤中分离,其提取的效率太低。需要提供一种高效、简便、高纯度、高产率的全合成软刀素肽的方法。
技术实现要素:
本发明的目的在于提供一种高效地制备软刀素肽的方法。
一种高效合成软刀素肽(urumin)的制备方法,包括如下步骤:
一种软刀素肽的固相合成方法,其特征在于:
所述软刀素肽的序列如下:iplrgafingrwdsqchrfsngaiaca
所述方法它包括如下步骤:
(1)取树脂固相载体和n端fmoc保护的氨基酸,通过固相合成法,按软刀素肽主链肽序依次偶联具有n端fmoc保护的氨基酸,得到全肽树脂,当偶联上一个具有n端fmoc保护的氨基酸后,采用脱保护剂脱除fmoc基团,再偶联下一个具有n端fmoc保护的氨基酸;
(2)采用tfa/tips/edt/水的切割试剂,将肽链从肽树脂上脱下,经过纯化即得软刀素肽。
步骤(1)所述的树脂固相载体为wang树脂。
步骤(1)中,所述固相合成时,树脂的载样量为0.33mmol/g。
步骤(1)中,所述固相合成时,采用dic—hobt氨基酸缩合体系,采用的活化剂为hobt、dmap和dic。其中,fmoc-ala-oh、hobt、dmap、dic的比例为(5-8):(4-6):(2-4):(5-10)。优选地,所述fmoc-ala-oh、hobt、dmap、dic的比例为5:5:3:8。
步骤(3)中,tfa:tips:edt:水的比例为(90-95):(2-4):(2-4):(1-2)。
步骤(3)中tfa:tips:edt:水的比例为95:2:2:1(v/v/v/v)。
步骤(3)中,所述纯化的方法为反向高效液相色谱法,条件如下:色谱柱:odsc18柱;流动相:流动相b为0.1%tfa/水,流动相a为0.1%tfa/乙腈;梯度洗脱程序:90%流动相b、10%流动相a洗3min,30%流动相b、70%流动相a洗30min,0%流动相b、100%流动相a洗40min,检测波长214nm和254nm。
其中,所述高效液相色谱法的流速10ml/min,进样量2ml。
本发明的优点在于通过固相合成制备软刀素肽(urumin),本发明制备的直链肽,合成过程简单,具有很高的纯度和产率,本能满足目标化合物的生物活性测试,本发明方法可大规模工业制造,应用前景良好。
术语解释:
fmoc:芴甲氧羰基
dcm:二氯甲烷
dmf:n,n-二甲基甲酰胺
hobt:1-羟基苯并三唑
dmap:4-二甲氨基吡啶
dic:n,n-二异丙基碳二亚胺
nmp:n-甲基吡咯烷酮
tfa:三氟乙酸
tips:三异丙基硅烷
edt:1,2-乙二硫醇
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
图1合成路线图,其中,a:dcm,dmf,fmoc-ala-oh,hobt,dmap,dic,2h;b:20%的哌啶/dmf溶液,10min;c:fmoc-氨基酸,hobt,dic的nmp溶液;d:tfa/tips/edt/水=95:2:2:1(v/v/v/v),2h;
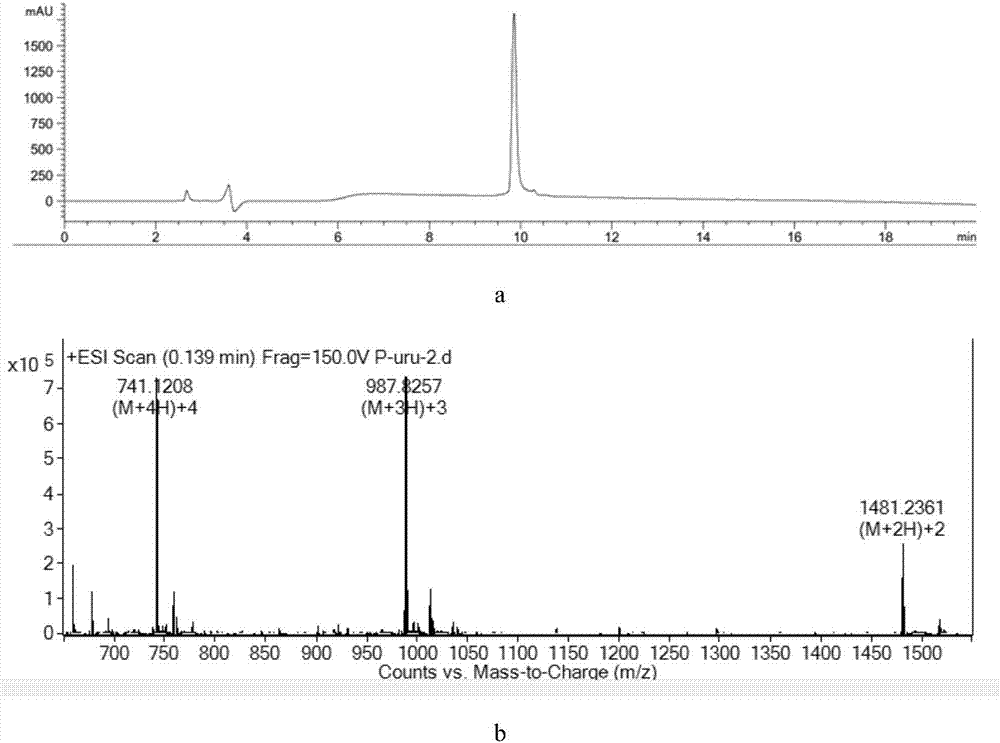
图2为纯化后的目标化合物高效液相色谱图(a)和质谱图(b)。
具体实施方式
实验材料:
氨基酸;wang树脂购自上海吉尔生化有限公司;
n-甲基吡咯烷酮(nmp)、n,n-二异丙基碳二亚胺(dic)、1-羟基苯并三唑(hobt)、三氟乙酸(tfa)、乙腈,三异丙基硅烷(tips)、1,2-乙二硫醇(edt)购自北京百灵威科技有限公司;
茚三酮、n,n-二甲基甲酰胺(dmf)、二氯甲烷(dcm)、哌啶、苯酚、甲醇均为分析纯(国药集团化学试剂北京有限公司)。
实施例1本发明制备软刀素肽(urumin)的方法
一、制备
1、合成策略
软刀素肽(urumin)是一种含丰富种类氨基酸的多肽。我们通过前期试验探索,优化选择以wang树脂为载体树脂与肽链c端的氨基酸以共价键结合。在dic—hobt氨基酸缩合体系中,以异亮氨酸为直链肽的氨基端,丙氨酸为直链肽的羧基端,通过固相合成制备软刀素肽(urumin)。粗肽产物用高效液相色谱(qp-hplc)进行纯化,获得目标化合物软刀素肽(urumin)。
2、直链肽的固相合成过程
采用如图1所示的合成路线制备软刀素肽(urumin),其中,步骤1中化合物2与fmoc-ala-oh的比例为300mg:156mg,所述步骤2中化合物3置于20%的哌啶/dmf溶液中脱除fmoc保护基;化合物5表示wang树脂与合成完成后直链肽的结合物。
具体步骤如下:
(1)称取wang树脂300mg(载样量为0.33mmol/g)置于固相合成反应管中,加入5mldcm浸泡溶胀15min,用dmf冲洗三次抽干;
(2)向树脂中加入含有fmoc-ala-oh(156mg,5倍当量),hobt(81mg,5倍当量),dmap(182.5mg,3倍当量),dic(100ul,8倍当量)的5mldmf溶液,置于气浴恒温振荡器中在常温下反应2h,反应结束后抽干反应液用dcm、dmf洗涤wang树脂各三次,取少量树脂用乙醇茚三酮溶液检测显无色;
(3)向树脂中加入5毫升20%的哌啶/dmf溶液反应10分钟脱去丙氨酸上n端的fmoc保护,用dcm、dmf洗涤wang树脂各三次,取少量树脂用乙醇茚三酮溶液检测显色;
(4)重复步骤(2)(3)的做法,依次将fmoc-cys(trt)-oh、fmoc-ala-oh、fmoc-ile-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-ser(otbu)-oh、fmoc-phe-oh、fmoc-arg(pdf)-oh、fmoc-his(trt)-oh、fmoc-cys-oh、fmoc-gln(trt)-oh、fmoc-ser(otbu)-oh、fmoc-asp(otbu)-oh、fmoc-trp-oh(boc)、fmoc-arg(pdf)-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-arg-oh、fmoc-leu-oh、fmoc-pro-oh、fmoc-ile-oh。偶联到树脂上,脱保护基,得到化合5;
(5)将树脂置于tfa/tips/edt/水=95:2:2:1(v/v/v/v)的切割试剂中反应2小时,过滤收集滤液,用氩气鼓泡至原有体积的一半,用冰乙醚反复洗涤离心三次,常温低压干燥得目标化合物1。粗品收率52.8%。
收率的计算方法:实际产量/理论产率*100%。本发明中,理论产量为295.9mg。
3、产物直链肽的纯化
将所得的目标产物用乙腈和水溶解,通过反向高效液相色(qp-hplc)分离纯化。分离条件如下:
仪器:lc-6a制备液相色谱仪,色谱柱:odsc18柱(20mm×250mm,
流动相:乙腈、水
步骤与参数:流动相b为0.1%tfa/水,流动相a为0.1%tfa/乙腈,梯度洗脱:90%b(3min)一30%b(30min)一0%b(40min),流速10ml/min,检测波长214nm和254nm,进样量2ml。
经测定与粗品主峰出峰时间一致,且本法所制备软刀素肽的纯度>98%(图2a),纯收率5.3%。
收率的计算方法:实际产量/理论产率*100%。本发明中,理论产量为295.9mg。
二、产物的鉴别与结构分析
将步骤3所得产物通过hplc进行鉴别以及hr-q-tof-ms(高分辨基质辅助激光解析电离飞行时间质谱)进行结构分析,色谱流动相为乙腈和水。
通过hr-esi-ms质谱仪分析,质谱图中741.1263对应[m+4h]+峰,987.8257对应[m+3h]+峰,1481.2327对应[m+2h]+峰(图2b),与软刀素肽理论分子量2961.38,在误差范围之内,显示主峰物质分子量与软刀素肽相符,说明本发明制备得到了软刀素肽。
实验结果说明,本发明方法可以制备得到软刀素肽,而且纯度大于98%,本发明方法的产率高,应用前景良好。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
序列表
<110>成都医学院
<120>一种软刀素肽的制备方法
<130>gy044-17p1531
<160>1
<170>siposequencelisting1.0
<210>1
<211>27
<212>prt
<213>软刀素肽(rananigromaculata)
<400>1
ileproleuargglyalapheileasnglyargtrpaspserglncys
151015
hisargpheserasnglyalailealacysala
2025
- 还没有人留言评论。精彩留言会获得点赞!