荧光定量PCR法检测外周血CA242mRNA的试剂盒的制作方法
本发明属生物技术领域,为一种通过逆转录(rt)mrna样品得到cdna,再结合实时荧光定量pcr检测技术,可以精确定量检测标本中人外周血ca242mrna的表达量的试剂盒。
背景技术:
本发明属生物技术领域,为一种通过逆转录(rt)mrna样品得到cdna,再结合实时荧光定量pcr检测技术,可以精确定量检测标本中人外周血ca242mrna的表达量的试剂盒。
胰腺癌是一种恶性程度很高,诊断和治疗都很困难的消化道恶性肿瘤,约90%为起源于腺管上皮的导管腺癌。其发病率和死亡率近年来明显上升。5年生存率<1%,是预后最差的恶性肿瘤之一。许多患者确诊时即已为晚期,失去了最佳的手术时机。即使早期胰腺癌患者,有很大一部分患者5年内死于复发和转移。其原因可能是在术前或术时已有非常少量肿瘤细胞,转移到血液、淋巴结、骨髓、或其它远处器官,形成肿瘤微转移,而普通的检测方法不能发现。
早期发现、早期诊断是胰腺癌早期治疗的基础和前提,也是有效提高胰腺癌患者生存率、改善其预后的重要保证。由于癌瘤早期体积微小,采用b超、ct扫描等手段均难以早期发现。血液转移是肿瘤扩散的主要途径之一,因此在患者外周血进行肿瘤细胞基因表达检测、肿瘤特异性标记产物检测是了解肿瘤转移情况的一个有效的方式,因而肿瘤标记物的检测对肿瘤形成及转移的诊断具有极大的帮助。但是在肿瘤转移发生的早期,外周血中的肿瘤细胞很少,无法完全依赖病理形态检查,同时肿瘤特异性抗原的含量也很少,也很难通过常用的elisa或ria等方法检测到,因此对循环血中的微量肿瘤细胞基因表达和一些特异产物检测的研究,引起了人们的广泛关注。
聚合酶链式反应(pcr)是一种用于放大扩增特定的dna片段的分子生物技术,是位于体外的特殊dna复制,能将微量的dna大幅增加。taqman荧光定量pcr技术及相应检测仪器的推出使得人们可以在利用pcr高灵敏性的情况下,对pcr产物进行实时精确定量检测,不仅解决了pcr的定量问题,而且还大大提高了检测的特异性。因此我们通过荧光定量pcr技术检测外周血中微量肿瘤细胞,荧光定量pcr技术有着病理学或elisa/ria等方法无法比拟的高灵敏度和相对的高特异性,为外周血中微量肿瘤细胞的检测带来了希望。
ca242是目前发现的胰腺癌最具特异性肿瘤标志物之一,其特异性高表达于胰腺癌,正常成人外周血中均不表达,因此ca242的阳性表达可作为胰腺癌的标志物之一。因而检测外周血中ca242mrna的表达能为胰腺癌的确定及预后的判断提供重要的参考依据。
技术实现要素:
本发明试剂盒包含:红细胞裂解液、总rna抽提试剂、无rna酶的水、反转录缓冲液、dntp混合物、逆转录酶储存液、pcr反应液、探针、标准品、对照品;除标准品用te溶解外,其他各种溶液所用溶剂均为纯化水;
检测用引物分检测用上游引物和检测用下游引物:
上游引物序列为:p1:5'-aattaaagtgagggtctcggagaa-3';
下游引物序列为:p2:5'-agaggtcgcaggaagaaatatca-3'
荧光探针序列为:5'-fam-tgagaggccccgctg-tamra-3'
标准品序列为:
aattaaagtgagggtctcggagaagaagcaggaactgagtttcctgagaggccccgctgaggctttgttgatatttcttcctgcgacctct
对照品分为阳性对照品与阴性对照品,阳性对照品为含有ca242cdna的样品,浓度为104copies/µ1,te溶解,阴性对照品为外周血总rna的反转录产物。
本试剂盒保存-20℃,尽量减少反复冻融。
本发明建立了利用taqman技术检测ca242mrna表达的方法,并经检测患者标本,表明该方法切实可行。由于本方法采用了pcr扩增技术,使得ca242表达的检测敏感性大大提高,而且由于荧光探针的应用,使得其特异性大大提供,降低了常规pcr的假阳性率,使得微量检测变为可能。本方法所设计的引物、探针及检测结果,可以为荧光定量pcr检测试剂盒的开发提供可靠的依据。
本检测项目采用了先进的特异性荧光探针杂交定量pcr检测技术,在实时荧光定量pcr检测技术出现之前,人们对pcr模板的定量不论是直接pcr还是竞争性pcr,采用的都是终点法,并且pcr模板的定量依赖于pcr产物电泳图或者利用elisa定量pcr产物的方式进行检测,再由此推测起始模板的量,但这些方法属于半定量水平。随着实时荧光定量pcr技术的出现,我们可以做到对pcr模板的精确定量,这种定量不仅保持了常规pcr的高灵敏性,而且由于特异性荧光探针杂交技术的应用,使得被检测基因的特异性大大提高。
本发明试剂盒使用方法:
每次检测均应设立阳性对照品和阴性对照品。
标准曲线制作:将标准品(2×106copies/ul)梯度稀释为2×105,2×104,2×103,2×102,2×101copies/ul,取10ul为模板,同待测样品一同进行pcr扩增,制作标准定量曲线。
逆转录:总体积10ul,其中5ul70℃预变性5分钟的待测rna,3.0ulrt反应液(用前将反转录缓冲液加入到反转录酶中混匀后使用),2.0ul无rna酶的水。于普通pcr仪上反应,设置反应条件为:37℃20分钟,95℃5分钟,4℃30分钟。
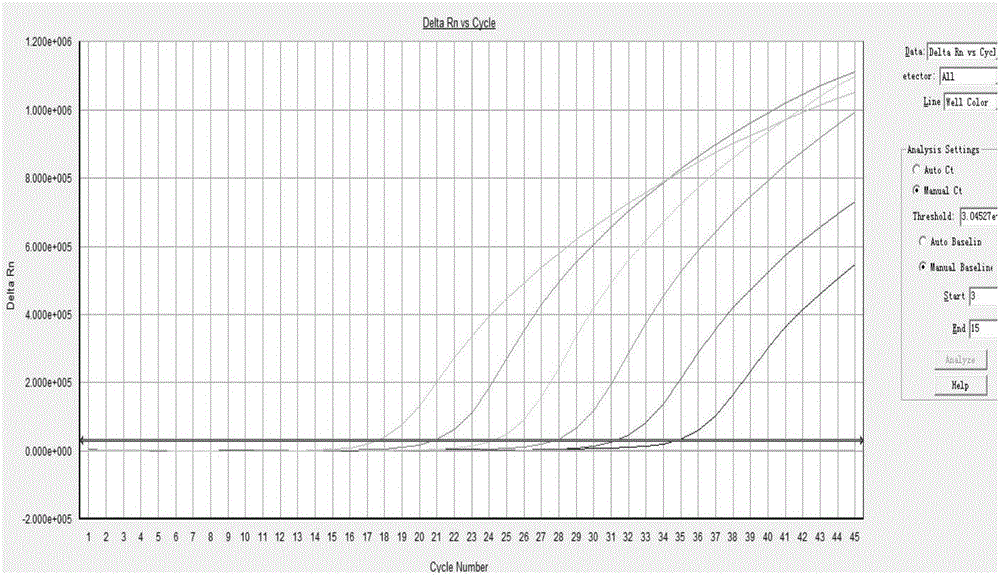
扩增检测:在荧光定量pcr仪上进行,总体积25ul,其中13.5ulpcr缓冲液(用前将pcr反应液加入到dntp混合物中混匀后使用),10ul检测样品(逆转录产物、标准品、阳性或阴性对照),1.5ul探针。反应条件:95℃预变性5分钟,95℃30秒、60℃30秒、72℃30秒共45个循环,72℃延伸10分钟后置4℃。根据所获得的标准曲线,计算得到各待测标本的拷贝数。附图说明,图1实时荧光定量rt-pcr标准品检测;图2实时荧光定量rt-pcr标准曲线。
具体实施方式
本发明结合附图和具体实施例作进一步说明,应该理解,这些实施例仅用于说明目的,而不限制本发明范围。
实施例1
荧光定量rt-pcr法检测ca242的表达
一、材料:
trizol试剂及限制性内切酶均购自invitrogen公司,pgem-t-easy克隆系统、m-mlv逆转录酶、taqdna聚合酶、oligo(dt)15-18购自美国promega公司,逆转录使用的普通pcr仪为biometrapcr仪,7300型定量pcr仪为美国appliedbiosystems公司产品。
二、引物及探针设计与合成:
以ca242全基因序列为模板,使用primerexpressv3.0软件分析taqman引物和探针位点,并同时考虑ca242基因组dna序列情况,从中选择最佳组合。
检测用pcr引物序列为:
上游引物序列为:p1:5'-aattaaagtgagggtctcggagaa-3';
下游引物序列为:p2:5'-agaggtcgcaggaagaaatatca-3',均由上海生工合成
荧光探针序列为:5'-fam-tgagaggccccgctg-tamra-3',由大连宝生物技术公司合成
三、检测标准品制备:
标准品由上海生工合成,然后用克隆系统插入pcr2.1克隆载体,并将阳性克隆经测序验证。ecorⅰ酶切后回收即为标准品,测定浓度并换算成(拷贝数/体积)。
实施例2
一、标本检测;
7例经病确诊的胰腺癌患者外周血标本,分离外周血有核细胞,离心收集细胞用trizol试剂提取细胞总rna,取5ulrna,3.0ulrt反应液(用前将反转录缓冲液加入到反转录酶中混匀后使用),2.0ul无rna酶的水,进行逆转录,得到10ulcdna。用上下游引物在abi公司7300型pcr仪上进行pcr扩增,条件为95℃5分钟变性,95℃30秒、62℃30秒、72℃30秒进行45个循环扩增,最后于72℃延伸10分钟后置4℃。同时加标准品检测作标准曲线。测定结果经仪器处理后根据标准曲线计算出检测标本的表达量。
二、结果
(一)标准品的制备:
经测序,上述设计标准品完全与预期相符,回收的标准品片段序列如下(包括两端ecorⅰ位点):
gaattc
aattaaagtgagggtctcggagaagaagcaggaactgagtttcctgagaggccccgctgaggctttgttgatatttcttcctgcgacctct
gaattc
(二)样品检测:
标准品检测结果参见图1,标准曲线参见图2:
7例患者外周血标本检测结果如下:
本发明是结合最佳实施例进行描述的,然而在预读了本发明的上述内容后,本领域技术人员可以对本发明做各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
aattaaagtgagggtctcggagaagaagcaggaactgagtttcctgagaggccccgctgaggctttgttgatatttcttcctgcgacctct
- 还没有人留言评论。精彩留言会获得点赞!