检测MLH1表达水平的试剂在制备肿瘤靶向药敏感性检测试剂盒中的用途的制作方法
本发明属于肿瘤分子生物学领域,具体涉及一种检测mlh1表达水平的试剂在制备肿瘤靶向药敏感性检测试剂盒中的用途。
背景技术:
随着分子生物学技术的发展,人们对肿瘤发病机制有了进一步认识,继而开始了针对细胞受体、关键基因和调控分子为靶点的治疗,称之为“靶向治疗targetedtherapy”,因此,肿瘤靶向药也成为治疗肿瘤的重要药物。与传统化疗药物相比,肿瘤靶向药具有特异性强、疗效明显、正常组织损伤少等优点,此类药物主要有两类,单克隆抗体和小分子化合物。现已有多靶点治疗药物—索拉非尼(2005年上市,sorafenib,bay43-9006)、舒尼替尼(2006年上市,sunitinib,su11248)上市和多个多靶点小分子化合物处于临床试验阶段。
肿瘤靶向小分子化合物药显示出广谱的抗肿瘤活性,尤其是索拉非尼、舒尼替尼上市以来显著延长肝癌、肾癌等晚期肿瘤患者的总生存,改善生活质量,而且这类药物大多具有低毒性、使用方便、可长期用药等特点,临床应用前景广阔。但仍有一部分患者对这类药物发生原发或继发耐药,导致治疗失败。如晚期肾癌患者一线接受sunitinib治疗的中位疾病无进展生存(pfs)仅为8-10个月;sorafenib治疗晚期肾癌的中位pfs只有5.8个月,阐明其耐药机制,发现耐药相关预测分子,对提高肿瘤疗效具有重要意义。
另外,这类药物价格比较昂贵,精准用药将能够大大减轻患者家庭的经济负担。但目前缺乏有效的生物标记物筛选出对靶向药如索拉非尼、舒尼替尼可能有效的亚组人群。同时,也无有效的血液学标志物监控此类药物何时出现耐药,以便及时采用其他治疗措施抑制肿瘤进展。
错配修复蛋白1(mlh1),是dna错配修复系统的1个主要基因,研究表明,mlh1与肿瘤的发生密切相关,其表达下降或缺失会引起错配修复功能的降低,从而使自发突变率增加而增加基因组的不稳定,导致细胞的异常增生进而癌变。但是,目前尚未见mlh1表达与肿瘤靶向药索拉非尼或舒尼替尼治疗肝癌、肾癌相关的报道。
技术实现要素:
发明人在肿瘤多靶点小分子抑制剂药物敏感性检测方面进行了详细研究,发现了mlh1可以作为其分子标志物。其中,mlh1的表达水平与肿瘤靶向药物sorafenib、sunitinib对肝癌、肾癌治疗的药物敏感性相关。因此,通过检测mlh1表达水平,可以预测待检肿瘤患者的药物治疗效果。
据此,本发明提供了一种肿瘤靶向药敏感性检测试剂盒,以及检测mlh1表达水平的试剂在制备肿瘤靶向药敏感性检测试剂盒中的用途,并在此基础上,提供了一种调节肿瘤靶向药敏感性的药物。
本发明提供了一种肿瘤靶向药敏感性检测试剂盒,它包括任选的用于检测mlh1表达水平的试剂。
其中,所述肿瘤靶向药是索拉非尼和/或舒尼替尼;
和/或,所述肿瘤为肝癌、肾癌。
其中,所述检测mlh1表达水平的试剂包括检测mlh1蛋白表达水平的试剂和/或特异性扩增mlh1基因mrna的pcr引物。
本发明还提供了检测mlh1表达水平的试剂在制备肿瘤靶向药敏感性检测试剂盒中的用途。
其中,所述肿瘤靶向药是索拉非尼和/或舒尼替尼;
和/或,所述肿瘤为肝癌、肾癌。
其中,所述检测mlh1表达水平的试剂包括检测mlh1蛋白表达水平的试剂和/或特异性扩增mlh1基因mrna的pcr引物。
本发明还提供了提高microrna-31-5p表达水平的试剂在制备增强肿瘤靶向药敏感性药物中的用途。
其中,所述药物为逆转肿瘤靶向药耐药性的药物。
其中,所述肿瘤靶向药是索拉非尼和/或舒尼替尼。
本发明还提供了一种增强肿瘤靶向药敏感性的药物,其特征在于:它能够提高mlh1的蛋白表达水平和/或提高其编码基因转录的mrna含量;
其中,所述肿瘤靶向药是索拉非尼和/或舒尼替尼;所述肿瘤为肝癌、肾癌。
本发明试剂盒通过检测mlh1的表达水平,可以判断不同肿瘤患者对肿瘤靶向药的敏感性,进而判断其是否适用特定的肿瘤靶向药治疗:若mlh1的表达水平低,则患者对肿瘤靶向药sorafenib、sunitinib耐药,若mlh1的表达水平高,则肿瘤靶向药sorafenib、sunitinib敏感性高,可用于预测临床肿瘤患者的药物治疗效果,为患者采取相关的治疗措施或者决策提供依据,临床应用前景良好。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
图1靶向药物耐药关键分子microrna-31-5p的靶基因为mlh1,其过表达能下调mlh1mrna水平,从而下调mlh1的蛋白表达,进而导致细胞对靶向药物耐药。
(a)应用microrna数据库寻找microrna-31-5p发挥作用的靶基因,初步明确microrna-31-5p在靶基因mlh-13’端的结合位点;
(b)荧光酶素实验表明microrna-31-5p的靶基因是mlh-1;
(c)microrna-31-5pmimics能下调mlh-1的mrna水平,microrna-31-5p抑制剂上调mlh-1的mrna水平;
(d)westernblot显示microrna-31-5pmimics能下调mlh-1的蛋白水平;
(e)westernblot显示mlh1蛋白在耐药细胞株较其对应药物敏感的细胞株下调;
(f)克隆形成实验显示过表达mlh-1能使耐药细胞对靶向药物敏感,表现为克隆形成受抑;
(g)划痕实验显示过表达mlh-1能使耐药细胞对靶向药物敏感,表现为划痕修复受抑。
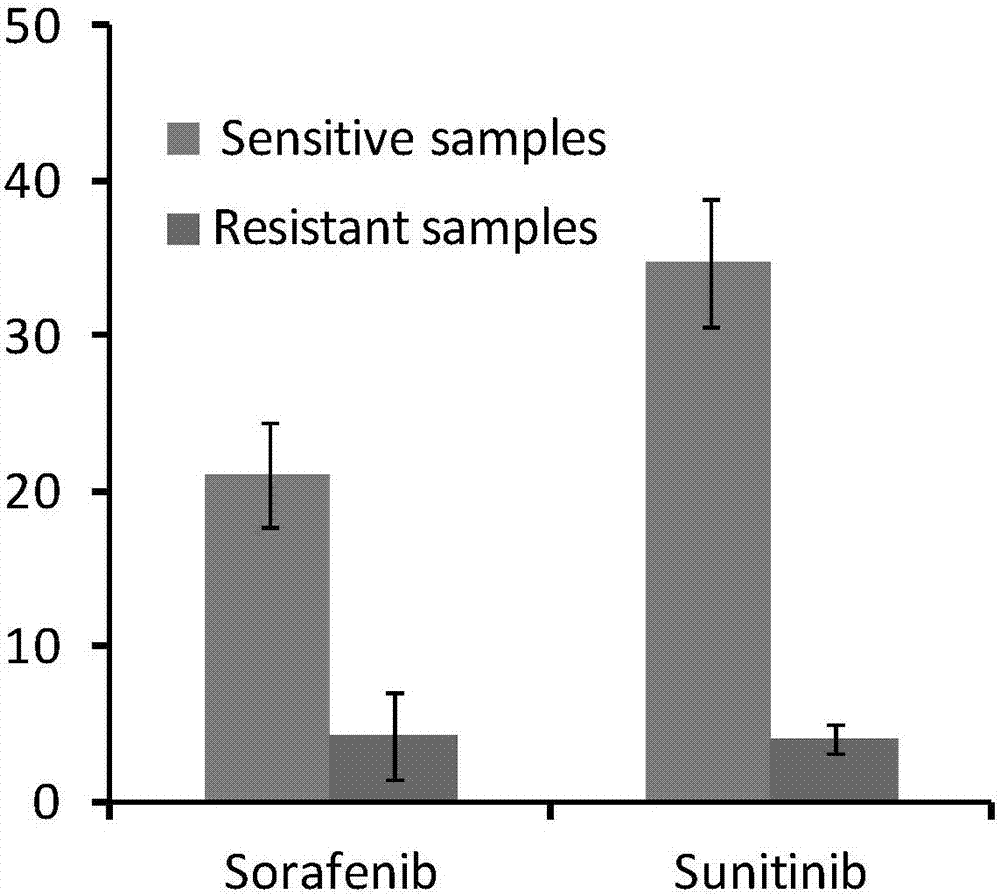
图2rt-pcr显示耐药细胞株及敏感细胞株中的mlh1表达差异。
具体实施方式
下面以实施例作进一步说明,但本发明不局限于这些实施例。
本发明具体实施方式中使用的原料、设备均为已知产品,通过购买市售产品获得。
实施例1mlh1表达与肿瘤靶向药物敏感性的关系
1、肿瘤靶向药耐药细胞株的建立
选择5种细胞株:肾癌细胞株786-0、achn;肝癌细胞株:hepg2、plc/prf/5;人脐静脉内皮细胞株:huvec,分别用dmem或1640培养基培养,mtt法检测药物sorafenib及sunitinib的ic50。
然后采用浓度梯度递增持续诱导法(最初使用各细胞的ic50处理细胞,细胞死亡后换液去掉漂浮的死亡细胞后逐步按10%-20%增加药物浓度,3-6个月后耐药细胞诱导完成)诱导sorafenib或sunitinib耐药肝癌细胞株、肾癌细胞株及人脐静脉内皮细胞株的产生。
具体结果见下表1和2:
表1亲本及建立的sorafenib耐药细胞株的ic50
sorr:对sorafenib耐药。肾癌细胞株:786-0、achn;肝癌细胞株:hepg2、plc/prf/5;人脐静脉内皮细胞株:huvec
表2亲本及建立的sunitinib耐药细胞株的ic50
sunr:对sunitinib耐药。肾癌细胞株:786-0、achn;肝癌细胞株:hepg2;人脐静脉内皮细胞株:huvec
2、westernblot检测mlh-1在靶向药物敏感与耐药细胞株中的表达水平
使用ripabuffer提取靶向药物耐药及敏感细胞的蛋白,westernblot检测mlh-1蛋白(抗体:购于abcamab92312)在耐药细胞系(786-0-sorr和achn-sorr)及其对应的药物敏感细胞株的表达水平。
结果如图1e所示,与sorafenib、sunitinib敏感细胞株相比,耐药细胞株中的mlh1蛋白表达显著下调。
此外,通过慢病毒过表达mlh-1,按照常规方法进行克隆形成实验及划痕实验,结果显示过表达mlh-1能使靶向药物耐药细胞对靶向药物再次敏感,表现为克隆形成能力减低、划痕修复能力减弱(图1-f,g),这可能与肿瘤细胞恢复敏感性相关。
3、mlh-1的调控分子机制研究
(1)首先,应用microrna数据库(如miranda,targetscan,rnahybrid,pictar等)寻找microrna-31-5p发挥作用的靶基因,初步明确microrna-31-5p在靶基因mlh-13’端的结合位点(图1-a)。
(2)其次,荧光素酶报告基因实验,结果显示microrna-31-5p类似物能降低靶基因mlh-13’utr野生型载体的荧光酶活性,而microrna-31-5p抑制剂能上调靶基因mlh-13’utr野生型载体的荧光酶活性。而对于靶基因mlh-13’utr突变型载体而言,microrna-31-5p类似物或抑制剂对靶基因无明显调控(图1-b)。
(3)然后,使用microrna-31-5p类似物或抑制剂((选择本领域常用的microrna-31-5p类似物或抑制剂,只要能够调控其表达即可))处理细胞,rt-pcr检测靶基因mlh-1mrna水平的改变。
mlh-1检测引物:
forwardprimer:tattcataggcaagatgctggc;
reverseprimer:tatggttgttctcgtctccttctc。
结果见图1-c,rt-pcr结果显示microrna-31-5p类似物能下调mlh1mrna水平,其抑制剂能上调mlh1mrna水平。
(4)使用microrna-31-5p类似物或抑制剂处理细胞,westernblot检测靶基因mlh-1蛋白水平的改变(mlh1抗体购于abcamab92312)。
结果如图1-d所示,可见microrna-31-5p类似物能下调mlh1蛋白水平。
microrna-31-5p的靶基因为mlh1,microrna-31-5p的过表达能下调mlh1mrna水平,从而下调mlh1的蛋白表达,进而导致细胞对sorafenib耐药(图2)。
实施例3临床检测mlh1在敏感与耐药肿瘤患者中的表达水平
收集临床上sorafenib或sunitinib耐药、敏感的肾透明细胞癌患者的肿瘤病理标本(其中,sorafenib敏感患者28名,患者中位年龄33岁;sorafenib耐药患者30名,患者中位年龄38岁;sunitinib敏感患者35名,患者中位年龄37岁;sunitinib耐药患者29名,患者中位年龄42岁),利用rt-pcr检测sorafenib或sunitinib原发耐药及药物敏感的肿瘤患者组织病理标本中mlh1的mrna水平。
使用的mlh-1检测引物如下:
forwardprimer:tattcataggcaagatgctggc;
reverseprimer:tatggttgttctcgtctccttctc。
结果如图2所示,其中,sorafenib敏感患者肿瘤病理标本mlh1的表达水平为21.2±3.4,sorafenib耐药患者肿瘤病理标本mlh1的表达水平为4.34±2.8;
sunitinib敏感患者肿瘤病理标本mlh1的表达水平为34.7±4.1,sunitinib耐药患者肿瘤病理标本mlh1的表达水平为3.2±0.9。
可见,与sorafenib、sunitinib敏感组相比(耐药前),耐药组患者的mlh1表达水平显著降低,差异有统计学意义。说明二种肿瘤靶向药的治疗敏感性与mlh1表达水平相关,mlh1的高表达会显著提高肿瘤患者对靶向药的敏感性。因此,检测mlh1表达水平可预测患者对二种肿瘤靶向药是否响应,从而指导患者的临床用药选择。
综上,本发明试剂盒通过检测mlh1的表达水平,可以判断不同肿瘤患者对肿瘤靶向药的敏感性,进而判断其是否适用特定的肿瘤靶向药治疗:若mlh1的表达水平低,则患者对肿瘤靶向药sorafenib、sunitinib耐药,若mlh1的表达水平高,则肿瘤靶向药sorafenib、sunitinib敏感性高,可用于预测临床肿瘤患者的药物治疗效果,为患者采取相关的治疗措施或者决策提供依据,临床应用前景良好。
- 还没有人留言评论。精彩留言会获得点赞!