一种复合启动子及其在提高肺炎克雷伯氏杆菌的3-羟基丙酸产量中的应用的制作方法
本发明属于生物化工生产领域,涉及一种复合启动子及其在提高肺炎克雷伯氏杆菌的3-羟基丙酸产量中的应用。
背景技术
3-羟基丙酸(3-hydroxypropionicacid,3-hp)是重要的平台化合物,具有广阔市场前景。化学合成3-hp难度大,分离纯化困难,而且污染环境,因此制约了其大规模的应用。生物法生产3-hp具有低成本、易操作、条件温和、环境友好等优势。肺炎克雷伯氏杆菌(klebsiellapneumoniae)具有较高的甘油耐受性、较强的甘油代谢能力,且自身可合成辅酶b12等特点,因此成为利用甘油生物法生产3-hp的优势宿主菌。k.pneumoniae利用甘油脱水酶(dhab)催化甘油生成3-羟基丙醛(3-hpa),3-hpa在醛脱氢酶(aldh)的催化下生成3-hp。
由于甘油脱水酶的活性高于醛脱氢酶,导致3-hpa的积累,3-hpa对细胞具有毒性,因此消弱细胞的生长代谢。为了高产3-hp,需要提高醛脱氢酶的活性。启动子作为重要的基因表达调控元件,其活性直接影响到外源基因能否高效表达。k.pneumoniae为非模式生物,缺少合适的强启动子使醛脱氢酶高效表达,造成3-hp的生产过程转化率较低。
技术实现要素:
为了解决上述问题,本发明的目的在于提供一种复合启动子,该启动子可高效表达醛脱氢酶,从而快速催化3-hpa生产3-hp,一方面防止3-hpa的积累对细胞生长代谢的削弱,另一方面可提高3-hp的产量。
本发明的第二个目的在于提供一种重组载体。
本发明的第三个目的在于提供一种上述重组载体的制备方法。
本发明的第四个目的在于提供一种生产3-羟基丙酸的肺炎克雷伯氏杆菌重组菌。
本发明的第五个目的在于提供一种上述生产3-羟基丙酸的肺炎克雷伯氏杆菌重组菌的制备方法。
本发明的第六个目的在于提供一种上述复合启动子或带有复合启动子的重组载体在提高肺炎克雷伯氏杆菌的3-羟基丙酸产量中的应用。
为了实现上述目的,本发明提供一种复合启动子,所述复合启动子含有2-5个tac启动子核心序列;
其中,当该复合启动子含有2个tac启动子核心序列时,序列如seqidno.2所示;
当该复合启动子含有3个tac启动子核心序列时,序列如seqidno.3所示;
当该复合启动子含有4个tac启动子核心序列时,序列如seqidno.4所示;
当该复合启动子含有5个tac启动子核心序列时,序列如seqidno.5所示。
本发明还提供一种重组载体,由上述的复合启动子、puuc醛脱氢酶基因和pet-28a载体组成,其中puuc醛脱氢酶基因序列如seqidno.6所示;该重组载体为表达载体。
本发明还提供上述重组载体的制备方法:包括如下步骤:
1)用限制性内切酶bglii/ecori分别对复合启动子序列和pet-28a载体进行双酶切;
2)电泳,琼脂糖凝胶回收酶切后的复合启动子片段和pet-28a载体片段;
3)使用连接酶将复合启动子片段和pet-28a载体片段连接,得到含有复合启动子片段的载体;
4)pcr扩增puuc基因序列;
5)用限制性内切酶saci/ecori分别对步骤3)制得的含有复合启动子片段的载体和步骤4)制得的puuc基因序列进行双酶切;
6)电泳,琼脂糖凝胶回收酶切后的含有复合启动子的载体片段和puuc基因片段;
7)使用连接酶将含有复合启动子的载体片段和puuc基因片段连接,得到重组载体。
本发明还提供一种生产3-羟基丙酸的肺炎克雷伯氏杆菌重组菌,所述肺炎克雷伯氏杆菌重组菌包含上述的复合启动子或上述的重组载体。
本发明还提供上述生产3-羟基丙酸的肺炎克雷伯氏杆菌重组菌的制备方法:包括如下步骤:
1)制感受态细胞:将野生型肺炎克雷伯氏杆菌培养活化、冰浴30min,冷冻离心,去上清,水洗两次,制成感受态细胞;
2)将重组载体与感受态细胞充分混合后放入电击杯进行电击转化;
3)将电击转化后的电转液与培养基混合后涂布到抗性固体培养基中,经筛选获得生产3-羟基丙酸的肺炎克雷伯氏杆菌重组菌。
本发明还提供一种用于培养上述肺炎克雷伯氏杆菌重组菌的发酵培养基,该发酵培养基的配方为:kh2po42.7g/l;nh4no32.4g/l;k2hpo4·3h2o4.2g/l;(nh4)2so42g/l;caco30.15g/l;mgso4·7h2o0.12g/l;nah2po41.6g/l;edtana20.001g/l;柠檬酸0.06g/l;甘油40g/l;酵母粉4g/l;微量元素1.25ml/l;微量元素溶液:na2mo4·2h2o0.045g/l;feso4·7h2o1.7g/l;cocl2·2h2o0.12g/l;zncl20.05g/l;nicl2·6h2o0.025g/l;h3bo30.16g/l;mncl2·4h2o0.1g/l;cucl2·2h2o0.06g/l;hcl(37%)3.6ml。
本发明还提供上述复合启动子或上述重组载体在提高肺炎克雷伯氏杆菌的3-羟基丙酸产量中的应用。
本发明所用tac启动子是由trp启动子和lacuv5拼接而成,tac作为较强的诱导型启动子,可在肺炎克雷伯氏杆菌(k.pneumoniae)中启动基因表达。为获得更高的转录活性,满足生产的需要,将tac启动子核心序列进行了串联,设计得到一系列复合启动子pntac(n=2~5),并用其过表达k.pneumoniae自身的aldh编码基因puuc(kpn_01018(kegg数据库中的登录号),从而构建3-hp高产工程菌。将复合启动子及aldh编码基因进行pcr扩增。测序正确后将启动子和puuc在k.pneumoniae中超表达,获得了重组k.pneumoniae(pntac-puuc),并测定其对3-羟基丙醛的催化能力。结果表明,当3段tac启动子的核心序列串联时,即重组k.pneumoniae(p3tac-puuc)的aldh活性最高,达到34.36u/mg,是k.pneumoniae野生菌(4.21u/mg)的8.16倍。在5l发酵罐中培养该工程菌,96h时3-hp产量高达99.8g/l。此时甘油转化率为87.7%,时空产率(productivity)为1.04g·l-1·h-1。
本发明的有益效果在于:
本发明提供一种复合启动子、重组载体及其构建的高产3-羟基丙酸工程菌,该复合启动子可高效表达醛脱氢酶,从而快速催化3-hpa生产3-hp,一方面防止3-hpa的积累对细胞生长代谢的削弱,另一方面可提高3-hp的产量,而利用该启动子构建的k.pneumoniae的高效表达系统,对k.pneumoniae甘油代谢途径进行改造,可实现3-hp的高产。
附图说明
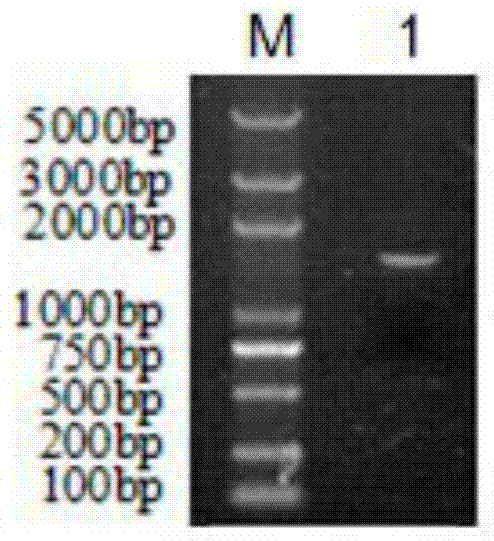
图1为本发明中puuc基因的电泳结果图。
图2a为本发明中重组菌k.p(ptac-puuc)的pcr的电泳结果图。
图2b为本发明中重组菌k.p(p2tac-puuc)的pcr的电泳结果图。
图2c为本发明中重组菌k.p(p3tac-puuc)的pcr的电泳结果图。
图2d为本发明中重组菌k.p(p4tac-puuc)的pcr的电泳结果图。
图2e为本发明中重组菌k.p(p5tac-puuc)的pcr的电泳结果图。
图3为本发明提供的重组菌的aldh酶活分析。
图4a为野生型菌株k.p-wt的96h发酵结果。
图4b为本发明提供的重组菌k.p(p2tac-puuc)的96h发酵结果。
图4c为本发明提供的重组菌k.p(p3tac-puuc)的96h发酵结果。
图4d为本发明提供的重组菌k.p(p4tac-puuc)的96h发酵结果。
图4e为本发明提供的重组菌k.p(p4tac-puuc)的96h发酵结果。
具体实施方式
下面的具体方法可以使本领域技术人员更全面地理解本发明,但不以任何方式限制本发明。
1.材料:
1)大肠杆菌感受态细胞(e.colibmtop10)购自北京博迈德生物技术有限公司。
2)野生型肺炎克雷伯氏杆菌klebsiellapneumoniaedsm2026(k.pneumoniaedsm2026)购自德国微生物菌种保藏中心(dsmz),菌种保藏编号:dsm2026,在实施例中也会简写为k.p-wt、k.pneumoniae-wt或k.pneumoniae。
3)表达载体pet-28a购自invitrogen公司。
2.培养基:
lb培养基(液体):酵母提取物5g/l,蛋白胨10g/l,nacl10g/l,ph值7.0。lb固体培养基为在液体培养基中加入1.5%的琼脂(质量体积比)。抗性培养基需加入硫酸卡那霉素至终浓度50μg/ml。
肺炎克雷伯氏杆菌的发酵培养基(基础):kh2po41.4g/l;nh4no31.7g/l;k2hpo4·3h2o3.6g/l;(nh4)2so42.9g/l;caco30.15g/l;mgso4·7h2o0.5g/l;nah2po41.6g/l;edtana20.001g/l;柠檬酸0.06g/l;甘油40g/l;酵母粉4.2g/l;微量元素1.25ml/l;
微量元素溶液:na2mo4·2h2o0.045g/l;feso4·7h2o1.7g/l;cocl2·2h2o0.12g/l;zncl20.05g/l;nicl2·6h2o0.025g/l;h3bo30.16g/l;mncl2·4h2o0.1g/l;cucl2·2h2o0.06g/l;hcl(37%)3.6ml。
3.序列合成由北京博迈德基因技术有限公司完成。
4.限制性内切酶bglii/ecori/saci、t4ligase连接酶购自newengland
biolabs(beijing,china)。
5.琼脂糖回收试剂盒购自北京博迈德基因技术有限公司。
实施例1重组载体pet-pntac的制备
根据报道的tac启动子核心序列(29bp)设计复合启动子,并进行化学合成,获得含有2-5个tac启动子核心序列的基因片段pntac(n=2~5)。由于复合启动子含有较多重复序列,且分子量较小,利用pcr进行基因扩增时条件较难控制,故在设计时引入bglii/ecori酶切位点,合成的基因直接双酶切后与载体pet-28a连接得到重组载体pet-pntac(n=2~5),其中下划线标注的部分为酶切位点,黑色加粗字体标注为tac启动子核心序列。两个核心序列之间为间隔序列(tgtggaattgtg),给予rna聚合酶足够的空间进行结合,序列参考了载体pet28a启动子之后的部分序列;最后一个tac启动子核心序列之后是间隔序列(tgtggaattgtg),再之后是lac操纵子序列(lacoperator),是诱导型启动子tac阻遏物的结合位点,操纵子序列后也包含了核糖体识别位点aaggag,之后需要预留出空间使核糖体结合,一般载体的间隔为6~15bp,其中9bp效果较好,故在酶切位点之前添加9bp序列。
当该复合启动子含有2个tac启动子核心序列时pntac(n=2),序列如seqidno.2所示;
当该复合启动子含有3个tac启动子核心序列时pntac(n=3),序列如seqidno.3所示;
当该复合启动子含有4个tac启动子核心序列时pntac(n=4),序列如seqidno.4所示;
当该复合启动子含有5个tac启动子核心序列时pntac(n=5),序列如seqidno.5所示:
为了比较含有不同tac启动子核心序列的差异,这里也设计了含有1个tac启动子核心序列pntac(n=1)的序列,序列如seqidno.1所示:
首先将含有不同tac核心序列的基因片段分别插入到pet-28a载体中。
1)酶切
用限制性内切酶bglii/ecori分别对复合启动子片段和载体pet-28a进行双酶切。酶切温度为37℃,反应时间2h。反应结束后,体系经65℃热失活15min,以终止反应。
酶切反应体系
2)电泳
将酶切产物分别按常规方法进行电泳。
选择大胶板。
称量0.60g琼脂糖,倒入80mltae缓冲液,加热溶解。
倒胶入胶板,加入2μlgoldview染液,静置凝胶20min。
小心拔下上样梳子,将胶板放入电泳槽中,补充缓冲液至完全没过胶板。
将10μl酶切后的反应液,加入2μlloadingbuffer,混合均匀,加入上样孔中。
加入10μlbm5000+dnamarker。
盖上电泳槽,接通电源,开始电泳。
待结束后,移至暗箱式紫外投射仪下观察结果。
3)琼脂糖切胶回收
使用琼脂糖回收试剂盒完成,具体步骤为:(a)将切下的电泳条带放入小体积ep管中,加入300μl的溶胶液,于65℃金属浴中温浴至胶体变为液体状;(b)过吸附柱后,高速离心丢掉废液;(c)用500μl75%乙醇对吸附柱进行漂洗,漂洗两次;(d)待乙醇干后,用30μl分子操作水洗脱吸附的片段,-20℃保存备用。
4)连接
切胶回收后获得的目的基因与质粒载体以1:1(v:v)混合均匀,利用连接酶将两者连接。连接温度65℃,反应时间1h。
连接反应体系:
5)化学法热转化
在无菌操作台中,将上述连接体系加入到大肠杆菌感受态细胞(e.colibmtop10)中并混合均匀,加入890μllb培养基(液体),37℃,200rpm复苏1h后涂布抗性平板,37℃培养15h,挑菌鉴定,分别得到重组载体pet-pntac(n=1~5)。
实施例2重组肺炎克雷伯氏杆菌的制备
依据genbank公布的puuc基因序列(如seqidno.6所示)设计引物,通过引物序列(puuc-f(seqidno.7)和puuc-r(seqidno.8))将saci及ecori酶切位点分别引入到基因的两端,以k.pneumoniaedsm2026基因组为模板,进行pcr扩增。将puuc基因连接至载体pet-pntac中,得到重组质粒(pet-pntac-puuc),转入大肠杆菌bmtop10中进行测序验证。提取测序正确的质粒电穿孔转化至野生型肺炎克雷伯氏杆菌k.pneumoniaedsm2026,培养并提取基因组dna,进行pcr,之后电泳验证puuc基因是否成功转化进去,pcr的引物为pet28a载体的通用引物,结果如图2a~图2e所示。分别保存连接正确的重组菌k.pneumoniae(pntac-puuc)(n=1~5)。
具体方法如下:
1)pcr扩增
pcr引物为:下划线标注的为酶切位点
pcr反应体系:
pcr反应条件:
将pcr产物进行电泳,通过片段大小确认pcr产物是否为puuc基因,结果如图1所示,其中m为dnamarkerdl2000plus;1为puuc基因,从电泳大小上看确实为puuc基因(1488bp)。
琼脂糖凝胶回收,通过酶切位点ecori/saci将基因puuc分别连接至载体pet-pntac(n=1~5)中,得到重组质粒(pet-pntac-puuc(n=1~5)),转入大肠杆菌e.colibmtop10中进行测序验证。提取测序正确的质粒电穿孔转化至肺炎克雷伯氏杆菌并进行验证。分别保存连接正确的重组菌k.pneumoniae(pntac-puuc)(n=1~5)。此外,将没有连接puuc基因的载体pet-ptac也进行电转化,得到一株重组菌k.pneumoniae(ptac)作为含有空载体的对照菌株,用于酶活测定。
载体电穿孔转化k.pneumoniae具体步骤如下:
(a)将野生型k.pneumoniae在4mllb培养基中,于37℃,200rpm的摇床中恒温震荡培养12h用于菌株的活化;(b)将活化的菌液以1%(v/v)的量,无菌操作,接至10mllb中,于37℃恒温,200rpm震荡,培养90min;(c)将菌液冰浴30min;(d)用冷冻离心机对菌体进行高速冷冻离心,去上清并用无菌双蒸水清洗感受态细胞,重复两次;(e)将重组质粒与制备好的感受态细胞充分混合后置于电转杯进行电击转化;(f)将电转液与890μllb培养基充分混合,放入小体积离心管中,37℃,200rpm,培养1h,涂布于lb抗性固体培养基中,37℃倒置,约培养12h,进行pcr验证携带puuc基因的载体是否成功转化进入宿主菌。
采用前述方法进行pcr,电泳,结果如图2a-图2e所示分别为对转化菌落中的载体中puuc片段进行pcr,图2a-图2e中m均为dnamarkerdl2000plus,图2a中1提取自k.p(ptac-puuc),图2b中1提取自k.p(p2tac-puuc);图2c中1提取自k.p(p3tac-puuc);图2d中1提取自k.p(p4tac-puuc);图2e中1提取自k.p(p5tac-puuc)。从上述结果可以看出,均出现了正确条带,说明载体成功转化进了克雷伯菌。
实施例3醛脱氢酶的活力测定
将重组菌分别进行摇瓶发酵,培养基采用肺炎克雷伯氏杆菌的发酵培养基(基础):250ml锥形瓶装发酵培养基100ml,棉塞封口,接种量为1%(体积分数),37℃150r/min震荡培养重组菌。取24h时的发酵液10ml,12000r/min离心收集菌体,用5mlpbs缓冲液(ph7.0)重悬菌体,超声破碎细胞,工作条件为80w,工作3s,间隔2s,循环80次,即得粗酶液。酶活反应体系为2ml,包括150mm正丙醛200μl,20mmnad+200μl,粗酶液200μl,pbs缓冲液(ph7.0)1.4ml。37℃水浴5min,通过检测340nm处吸光值的增量来确定反应体系中nadh的生成量。酶活单位定义:37℃下,每分钟催化生成1μmolnadh的酶量即为一个酶活力单位。之后用5ml考马斯亮蓝g250试剂标定200μl粗酶液中的总蛋白含量,得到重组酶的比活力。
试验结果如图3所示,其中,k.p-wt为肺炎克雷伯氏杆菌野生型;k.p(ptac)为含有空载体的对照菌株;k.p(pntac-puuc)(n=1~5)为复合启动子重组菌,从图3中可以看出,重组菌相较于对照菌,酶活性有了不同程度的提升,证明aldh在重组菌中实现了较高效率的表达,且具有生物催化活性,并且其中n=3时的重组菌k.pneumoniae(p3tac-puuc)酶活最高。
实施例4最佳培养条件的确定
肺炎克雷伯氏杆菌的发酵培养基(基础):kh2po41.4g/l;nh4no31.7g/l;k2hpo4·3h2o3.6g/l;(nh4)2so42.9g/l;caco30.15g/l;mgso4·7h2o0.5g/l;nah2po41.6g/l;edtana20.001g/l;柠檬酸0.06g/l;甘油40g/l;酵母粉4.2g/l;微量元素1.25ml/l。
微量元素溶液:na2mo4·2h2o0.045g/l;feso4·7h2o1.7g/l;cocl2·2h2o0.12g/l;zncl20.05g/l;nicl2·6h2o0.025g/l;h3bo30.16g/l;mncl2·4h2o0.1g/l;cucl2·2h2o0.06g/l;hcl(37%)3.6ml。
由于上述培养基为现有技术中肺炎克雷伯氏杆菌发酵的常用的培养基,而在培养肺炎克雷伯氏杆菌重组菌生产3-hp时,会对碳源、氮源产生的消耗与基础培养基会有所不同,因此,在上述配方技术上进行优化。
根据摇瓶发酵中不同培养基成分添加量的变化确定重组菌产3-hp的最佳培养条件(以aldh酶活最高的k.pneumoniae(p3tac-puuc)为培养对象)。
250ml锥形瓶装发酵培养基100ml,棉塞封口,接种量为1%(体积分数),37℃150r/min震荡培养重组菌。每隔3h取样,高效液相色谱测定3-羟基丙酸产量。具体分析方法如下:色谱柱为c18反向柱,柱温25℃,流动相为超纯水并添加0.05%磷酸,工作流速为0.8ml/min,采用紫外检测器。取2ml发酵液12000rpm离心5min,取上清液经0.22μm微孔滤膜过滤后留存,用于高效液相色谱检测。
其中所用发酵培养基的浓度如表1所示。当其中一个成分含量发生变化时,其他成分含量按照基础培养基的成分含量保持不变。
表1不同浓度培养基成分对3-hp产量的影响
根据以上摇瓶发酵结果,得到最佳培养基成分配方如表2所示:
表2最佳培养基成分
进一步优化后的培养条件:
肺炎克雷伯氏杆菌的发酵培养基:kh2po42.7g/l;nh4no32.4g/l;k2hpo4·3h2o4.2g/l;(nh4)2so42g/l;caco30.15g/l;mgso4·7h2o0.12g/l;nah2po41.6g/l;edtana20.001g/l;柠檬酸0.06g/l;甘油40g/l;酵母粉4g/l;微量元素1.25ml/l。
微量元素溶液:na2mo4·2h2o0.045g/l;feso4·7h2o1.7g/l;cocl2·2h2o0.12g/l;zncl20.05g/l;nicl2·6h2o0.025g/l;h3bo30.16g/l;mncl2·4h2o0.1g/l;cucl2·2h2o0.06g/l;hcl(37%)3.6ml。
利用优化后的培养条件,进行上罐发酵的ph值优化,ph值分别恒定在6、7和8的状态下进行36h的发酵,测定3-hp及相关代谢产物的产量,以aldh酶活最高的k.pneumoniae(p3tac-puuc)为对象,结果见表3。
表3不同ph值下甘油的碳硫分布
其中,gcr为甘油转化率;3-hp为3-羟基丙酸;la为乳酸;ac为乙酸;1,3-pd为1,3-丙二醇;2,3-bd为2,3-丁二醇;gly为甘油。
由于发酵培养基中甘油作为培养基中的唯一碳源,为菌体生长提供必要的底物。而3-hp是克雷伯菌中甘油代谢的主要产物,在生产3-hp的过程中,乳酸、乙酸、1,3-丙二醇,2,3-丁二醇成为竞争甘油资源的副产物。
由表3可以看出,在ph值为7的状态下,k.pneumoniae(p3tac-puuc)的3-hp产量最高,因此确定ph7为最优发酵培养ph值。
实施例5重组菌的上罐发酵
在5l发酵罐(上海保兴)中分别对野生型及包含复合启动子(pntac-puuc(n=2~5))的不同重组工程菌进行96h的上罐发酵,装液量为3l,保持温度在37℃,自动流加酸碱使ph维持在7.0,通气量为1.5vvm,搅拌转速为400rpm,每3h取样测定生物量、甘油剩余量、3-羟基丙酸及相关代谢产物产量,使甘油浓度维持在20g/l以上。分析方法同摇瓶发酵。
所用培养基配方如下:
肺炎克雷伯氏杆菌的发酵培养基:kh2po42.7g/l;nh4no32.4g/l;k2hpo4·3h2o4.2g/l;(nh4)2so42g/l;caco30.15g/l;mgso4·7h2o0.12g/l;nah2po41.6g/l;edtana20.001g/l;柠檬酸0.06g/l;甘油40g/l;酵母粉4g/l;微量元素1.25ml/l。
微量元素溶液:na2mo4·2h2o0.045g/l;feso4·7h2o1.7g/l;cocl2·2h2o0.12g/l;zncl20.05g/l;nicl2·6h2o0.025g/l;h3bo30.16g/l;mncl2·4h2o0.1g/l;cucl2·2h2o0.06g/l;hcl(37%)3.6ml。
实验结果如图4a-图4e所示,从图4a中可以看出,野生型k.pwt的3-hp的产率非常低,从图4b、图4d、图4e中可以看出,当n=2,4,5时重组菌k.pneumoniae(p2tac-puuc)、重组菌k.pneumoniae(p4tac-puuc)、重组菌k.pneumoniae(p5tac-puuc)在54h后3-hp的产量趋于平稳,而从图4c中可以看出,当n=3时,重组菌k.pneumoniae(p3tac-puuc)在54h后3-hp的产量继续持续上升,最高产量出现在发酵96h时,产量为99.8g/l。此时的甘油转化率及时空产率分别为87.7%,1.04g·l-1·h-1。
具体3-hp产量和甘油转化率如表4所示:
从上述结果可以看出,重组菌均比野生型的3-hp产量有大幅提高,其中重组菌k.pneumoniae(p3tac-puuc)的产量最高,其他重组菌的3-hp产量最低也在野生型菌的10倍以上。
从上述实施例中摇瓶发酵和上罐发酵的结果表明,复合启动子pntac(n=2~5)保证了醛脱氢酶基因puuc在肺炎克雷伯菌体内的高效表达,提高了3-羟基丙酸的产量,因此本发明成功构建了一系列3-羟基丙酸的高产菌k.pneumoniae(pntac-puuc)(n=2~5)。
sequencelisting
<110>北京化工大学
<120>一种复合启动子及其在提高肺炎克雷伯氏杆菌的3-羟基丙酸产量中的应用
<160>8
<170>patentinversion3.3
<210>1
<211>111
<212>dna
<213>人工序列
<400>1
agatctttgacaattaatcatcggctcgtataatgtgtggaattgtgagcggataacaat60
tcccctctagaaataattttgtttaactttaaggagaaggatatagaattc111
<210>2
<211>152
<212>dna
<213>人工序列
<400>2
agatctttgacaattaatcatcggctcgtataatgtgtggaattgtgttgacaattaatc60
atcggctcgtataatgtgtggaattgtgagcggataacaattcccctctagaaataattt120
tgtttaactttaaggagaaggatatagaattc152
<210>3
<211>193
<212>dna
<213>人工序列
<400>3
agatctttgacaattaatcatcggctcgtataatgtgtggaattgtgttgacaattaatc60
atcggctcgtataatgtgtggaattgtgttgacaattaatcatcggctcgtataatgtgt120
ggaattgtgagcggataacaattcccctctagaaataattttgtttaactttaaggagaa180
ggatatagaattc193
<210>4
<211>234
<212>dna
<213>人工序列
<400>4
agatctttgacaattaatcatcggctcgtataatgtgtggaattgtgttgacaattaatc60
atcggctcgtataatgtgtggaattgtgttgacaattaatcatcggctcgtataatgtgt120
ggaattgtgttgacaattaatcatcggctcgtataatgtgtggaattgtgagcggataac180
aattcccctctagaaataattttgtttaactttaaggagaaggatatagaattc234
<210>5
<211>275
<212>dna
<213>人工序列
<400>5
agatctttgacaattaatcatcggctcgtataatgtgtggaattgtgttgacaattaatc60
atcggctcgtataatgtgtggaattgtgttgacaattaatcatcggctcgtataatgtgt120
ggaattgtgttgacaattaatcatcggctcgtataatgtgtggaattgtgttgacaatta180
atcatcggctcgtataatgtgtggaattgtgagcggataacaattcccctctagaaataa240
ttttgtttaactttaaggagaaggatatagaattc275
<210>6
<211>1488
<212>dna
<213>klebsiellapneumoniae
<400>6
atgaattttcagcacctggcttactggcaggaaaaagcgaaaaacctggccattgaaacg60
cgcttatttattaacggcgaatattgcgccgcggccgataataccacctttgagactatc120
gaccccgccgcgcagcagacattagcccaggtcgcccgcggtaaaaaagccgacgtcgaa180
cgggcggtgaaagccgcgcgccaggcttttgataacggcgactggtcgcaggcctccccc240
gcacagcgtaaagcgatcctcactcgctttgctaatctgatggaggcccatcgtgaagag300
ctggcgctgctggaaacgctggataccggcaagccgattcgccacagcctgcgcgacgat360
attcccggcgccgcccgcgccattcgctggtatgccgaagcgctggataaagtctatggc420
gaagtggcccccaccggcagcaacgagctggcgatgatcgttcgcgaaccaattggcgtg480
atcgccgcggtggtgccgtggaacttcccgctgctgctggcctgctggaaactcggcccg540
gcgctggcggcaggcaatagcgtaatcctcaaaccctcggaaaaatcgccgcttaccgcc600
ctgcgtctggccgggctggcgaaagaggccggcctgccggacggcgtgttgaacgtggtc660
agcggctttggccacgaggccgggcaggcgctggccctgcatcctgatgttgaagtcatc720
accttcaccggctccacccgcaccggcaagcagctgctgaaagacgccggcgacagcaat780
atgaagcgcgtgtggctggaagcgggcggcaagagcgccaacattgtcttcgccgattgc840
ccggatctgcaacaagcggttcgcgccaccgccggcggcatcttctacaaccagggacag900
gtgtgcatcgccgggacccgtctgctgctcgaggagagcatcgctgacgagttcctggcg960
cggctgaaagctgaggcgcaacactggcagccgggcaacccgctcgatccggacaccacc1020
atgggcatgctgattgacaatacccatgccgacaacgtgcatagctttattcgcggcggc1080
gaaagccaaagcaccctgttcctcgacggacggaaaaacccgtggcctgccgccgttggc1140
ccgaccattttcgttgacgtcgacccggcatcaaccctcagccgggaagagatcttcggc1200
ccggtgctggtggtgacccgcttcaaaagcgaagaagaggcgctaaagctcgccaatgac1260
agcgactacggcttgggcgccgcggtgtggacccgcgatctctcccgcgcccaccgcatg1320
agccgccgcctgaaggccggctcggtcttcgtcaacaactataacgatggtgatatgacc1380
gttccgttcggcggctacaagcagagcggcaacgggcgcgataaatcgctgcacgcgctg1440
gaaaaattcaccgaactgaaaaccatctggattgccctggagtcttga1488
<210>7
<211>30
<212>dna
<213>人工序列
<400>7
ccggaattcatgatgaattttcagcacctg30
<210>8
<211>27
<212>dna
<213>人工序列
<400>8
tccgagctctcaagactccagggcaat27
- 还没有人留言评论。精彩留言会获得点赞!