托伐普坦纳米晶体的制备方法和含有托伐普坦纳米晶体的口服固体制剂与流程
本发明属于医药制剂
技术领域:
,具体涉及一种托伐普坦纳米晶体的制备方法和含有托伐普坦纳米晶体的口服固体制剂。
背景技术:
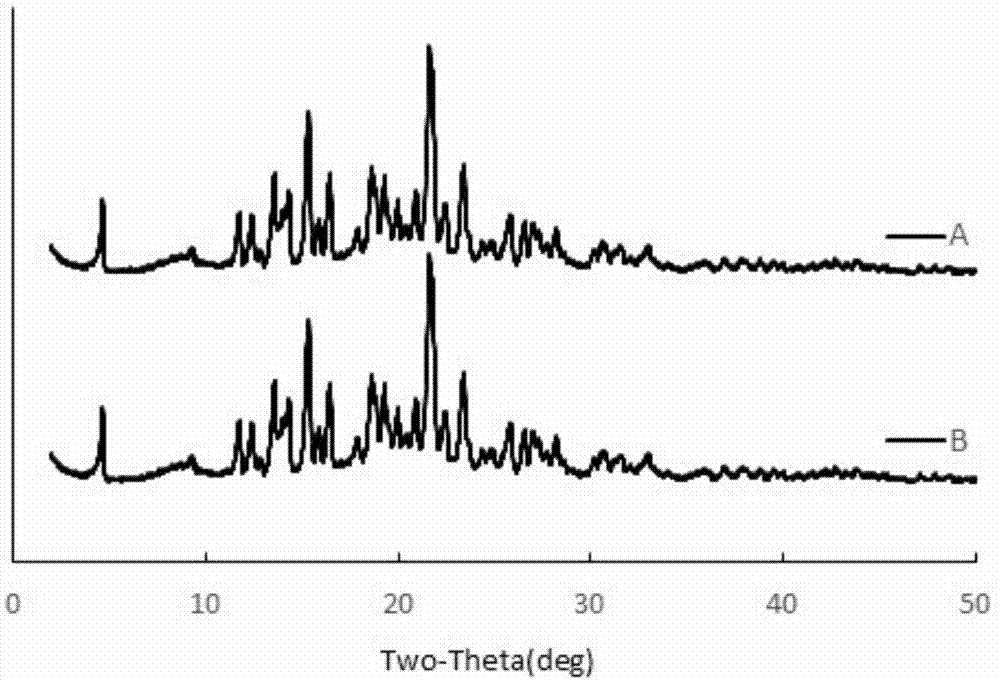
:托伐普坦是由日本大冢制药公司(otsukapharmaceuticalco.)研制开发,2009年分别在美国和欧洲上市,2010年在日本上市,商品名:samsca®。托伐普坦为特异性拮抗精氨酸加压素,用于治疗高容或等容性低钠血症伴心力衰竭、肝硬化、抗利尿激素分泌异常综合征。其化学名称为:n-[4-[(5r)-7-氯-5-羟基-2,3,4,5-四氢-1-苯并氮杂卓-1-甲酰基]-3-甲基苯基]-2-甲基苯甲酰胺,其结构式如下:。托伐普坦属于bcs分类第ⅳ类药物,低溶解,低渗透。虽然托伐普坦具有良好的药理活性,但是其较差的溶解性导致其在胃肠道吸收少,使得生物利用度较低,因此,提高托伐普坦的溶解性能是本领域面对的主要问题,目前,现有技术主要有以下几种技术手段:(1)将托伐普坦制成无定形药物,参见中国专利文献cn101686941a、cn102020609a、cn102366412a、cn102406622a、cn102512393a、cn103880747、cn107963991a等。市售商品samsca®采用的正是这种技术手段【原研专利cn101686941a】。无定形药物虽然能够有效提高托伐普坦的溶解性能和生物利用度,但是无定形药物稳定性较差,在储存过程中容易发生转晶,导致杂质甚至于有害物质大大增加。(2)将托伐普坦制成固体分散体,参见中国专利文献cn102293734a、cn102512393a、cn107432867a、cn107898759a等。由于固体分散体大多也是无定形的,因此,仍然存在稳定性较差、在储存过程中容易发生转晶、杂质指标增长较快等不足。(3)微粉化处理,参见中国专利文献cn101919864a、cn102114001a、cn102512393a、cn102552278a、cn107737110a等。现有的微粉化处理基本都是采用的气流粉碎技术,粉碎后的粒径一般大于10微米,对于托伐普坦的溶解性能和生物利用度提高有限。而cn101919864a公开的方法工艺生产过程复杂,成本较高,不适合工业化大生产。技术实现要素:本发明的目的之一在于解决上述问题,提供一种不仅能够有效提高托伐普坦的溶解性能和生物利用度,而且稳定性较好的托伐普坦纳米晶体的制备方法。本发明的目的之二在于解决上述问题,提供一种含有托伐普坦纳米晶体的口服固体制剂。实现本发明目的之一的第一种技术方案是:一种托伐普坦纳米晶体的制备方法,它是将托伐普坦置于行星式球磨机中,然后加入研磨球进行干法研磨,得到平均粒径小于1000nm的托伐普坦纳米晶体。实现本发明目的之一的第二种技术方案是:一种托伐普坦纳米晶体的制备方法,它是将托伐普坦与水置于行星式球磨机中,混合均匀后加入研磨球进行湿法研磨,再过滤、干燥,得到平均粒径小于800nm的托伐普坦纳米晶体。其中,托伐普坦与水的重量比为1∶1.5~1∶4,优选1∶2。实现本发明目的之一的第三种技术方案是:一种托伐普坦纳米晶体的制备方法,它是将托伐普坦与羟丙基纤维素以及水置于行星式球磨机中,混合均匀后加入研磨球进行湿法研磨,再过滤、干燥,得到平均粒径小于800nm的托伐普坦纳米晶体。其中,托伐普坦、羟丙基纤维素以及水的重量百分比为(20%~40%)∶(10%~20%)∶(40%~70%),优选25%∶12.5%∶62.5%。其中,羟丙基纤维素选自nissohpc-ssl、nissohpc-sl、nissohpc-l中的一种或者两种以上(含两种)。实现本发明目的之二的技术方案是:含有上述任意方法制得的托伐普坦纳米晶体的口服固体制剂。该口服固体制剂由上述任意方法制得的托伐普坦纳米晶体和药学上可接受的辅料制成。该口服固体制剂为片剂、颗粒剂或者胶囊剂。所述药学上可接受的辅料包括但不限于填充剂、粘合剂、崩解剂、润滑剂、着色剂。所述填充剂为乳糖、微晶纤维素、玉米淀粉、部分预胶化淀粉、淀粉、蔗糖、磷酸氢钙、磷酸二氢钙中的一种或者两种以上(含两种);优选为乳糖、微晶纤维素、玉米淀粉、部分预胶化淀粉中的一种或者两种以上(含两种)。所述粘合剂为聚维酮、共聚维酮、羟丙基纤维素、羟乙基纤维素、羟甲基纤维素、羟丙甲纤维素、羟乙甲纤维素、甲基纤维素、马铃薯淀粉、淀粉糖浆中的一种或者两种以上(含两种);优选为聚维酮、共聚维酮、羟丙基纤维素中的一种或者两种以上(含两种)。所述崩解剂为低取代羟丙基纤维素、交联聚维酮、交联羧甲基纤维素钠中的一种或者两种以上(含两种)。所述润滑剂为滑石粉、硬脂酸镁、胶态二氧化硅中的一种或者两种以上(含两种)。所述着色剂为fd&cblueno.2色淀。本发明具有的积极效果:(1)本发明将托伐普坦通过行星式球磨机制成纳米晶体,该纳米晶体晶型稳定,相比于无定形药物稳定性更好,而溶解性能和生物利用度又明显由于现有微粉化处理得到的微米级药物。(2)本发明的方法操作简单,生产成本较低,尤其是干法制备可以实现规模化生产。附图说明图1为实例1制得的托伐普坦纳米晶体的xrd图。图2为实例1制得的托伐普坦纳米晶体的sem图。具体实施方式(实例1)本实例的托伐普坦纳米晶体的制备方法如下:分别在行星式球磨机(型号:pulverisette5,公司:fritsch)两个研磨罐中各放置100g托伐普坦原料药,然后再分别放置5mm的玛瑙研磨球,充入氮气,设定球磨机的主盘转速为800rpm,每研磨1min后暂停1min,共研磨45min,得到托伐普坦纳米晶体。(实施例1)采用实例1制得的托伐普坦纳米晶体制成片剂,配方见表1。表1成分单剂量mg/片规格型号重量百分比实例1制得的托伐普坦纳米晶体30平均粒径<1000nm17.1%乳糖70200目40.0%微晶纤维素25ph10114.3%部分预胶化淀粉23starch150013.1%聚维酮15k308.6%低取代羟丙基纤维素10lh-215.7%硬脂酸镁2/1.1%总重175//制备方法如下:按处方量称取实例1制得的托伐普坦纳米晶体、乳糖、微晶纤维素、部分预胶化淀粉、聚维酮以及低取代羟丙基纤维素,混合均匀后加入适量纯化水作为润湿剂制软材,24目筛制粒,置烘箱中60±5℃烘干,过24目筛整粒,然后加入硬脂酸镁,混合均匀,得到颗粒物,压片,每片约重175mg。(实例2)本实例的托伐普坦纳米晶体的制备方法如下:分别在行星式球磨机(型号:pulverisette5,公司:fritsch)的两个研磨罐中各放置50g托伐普坦原料药和100g纯化水,混合均匀后,再分别放置5mm的玛瑙研磨球,充入氮气,设定球磨机的主盘转速为800rpm,每研磨1min后暂停1min,共研磨60min,研磨完成后,过滤,干燥,得到托伐普坦纳米晶体。(实施例2)采用实例2制得的托伐普坦纳米晶体制成分散片,配方见表2。表2成分单剂量mg/片规格型号重量百分比实例2制得的托伐普坦纳米晶体30平均粒径<800nm17.1%乳糖70.83200目40.5%微晶纤维素20ph10111.4%玉米淀粉20200目11.4%羟丙基纤维素20nissohpc-ssl11.4%低取代羟丙基纤维素12lh-216.9%硬脂酸镁2/1.1%fd&cblueno.2色淀0.17/0.1%总重175//制备方法如下:按处方量称取实例2制得的托伐普坦纳米晶体、乳糖、微晶纤维素、玉米淀粉以及羟丙基纤维素,混合均匀后加入适量纯化水作为润湿剂制软材,24目筛制粒,置烘箱中60±5℃烘干,过24目筛整粒,然后加入低取代羟丙基纤维素、硬脂酸镁以及fd&cblueno.2色淀,混合均匀,得到颗粒物,φ8mm平冲压片,每片约重175mg。(实例3)本实例的托伐普坦纳米晶体的制备方法如下:分别在行星式球磨机(型号:pulverisette5,公司:fritsch)的两个研磨罐中各放置50g托伐普坦原料药、25g羟丙基纤维素以及125g纯化水,混合均匀后,再分别放置5mm的玛瑙研磨球,充入氮气,设定球磨机的主盘转速为600rpm,每研磨1min后暂停1min,共研磨60min,研磨完成后,过滤,干燥,得到托伐普坦纳米晶体。(实施例3)采用实例3制得的托伐普坦纳米晶体制成包衣片剂,配方见表3。表3成分单剂量mg/片规格型号重量百分比实例3制得的托伐普坦纳米晶体45平均粒径<800nm25.7%乳糖40200目22.9%微晶纤维素40ph10122.9%部分预胶化淀粉31starch150017.7%共聚维酮6s6303.4%交联羧甲基纤维素钠10/5.7%滑石粉1200目0.6%硬脂酸镁2/1.1%总重175//制备方法如下:按处方量称取实例3制得的托伐普坦纳米晶体、乳糖、微晶纤维素、部分预胶化淀粉、共聚维酮以及交联羧甲基纤维素钠,混合均匀后,再加入滑石粉和硬脂酸镁,混合均匀,得到粉末,φ8mm浅凹冲压片,每片约重175mg。包衣:配制浓度为12%的包衣液,将片芯放入包衣锅内,启动包衣机,鼓风加热,采用喷枪喷入配制好的薄膜包衣液,直至增重2.5%,进风温度控制在60±5℃,片床温度控制在40±5℃。(对比例1~对比例3)各对比例与实施例1基本相同,不同之处在于采用的托伐普坦,具体见表4。表4托伐普坦粒径实施例1实例1制得的托伐普坦纳米晶体平均粒径<1000nm对比例1托伐普坦原料药平均粒径100~300μm对比例2微粉化处理后的托伐普坦d90为30~40μm对比例3微粉化处理后的托伐普坦d90为10~20μm(测试例1)分别对托伐普坦原料药和实例1制得的托伐普坦纳米晶体进行xrd扫描,结果见图1。其中,a曲线为托伐普坦原料药,b曲线为实例1制得的托伐普坦纳米晶体。由图1可以看出:行星式球磨后的托伐普坦依然以晶体的形式存在。(测试例2)对实例1制得的托伐普坦纳米晶体进行扫描电子显微镜观察,结果见图2。由图2可以看出:行星式球磨后的托伐普坦晶体为纳米级。(测试例3)对实例1~实例3制得的托伐普坦纳米晶体进行粒度测定,实验设备为malvernzetasizernanozs90纳米粒径电位分析仪,分散介质为水。每个实例平行测定三份样品,结果见表5。表5样品1样品2样品3实例1726±161nm832±141nm788±139nm实例2510±98nm601±123nm588±112nm实例3489±101nm509±88nm535±129nm由表5可以看出,所有样品粒径均小于1000nm,尤其是实例2和3的湿法研磨粒径更是小于800nm。(测试例4)对实施例1~实施例3、对比例1~对比例3制得的口服固体制剂以及市售商品samsca®(7h76tb1us1sa,美国)进行溶出度测定。测定方法参照《中国药典》2015年版四部通则0931溶出度测定法中的第二法,溶出介质为0.22%的sds水溶液,转速为50r/min,取样时间点为10、20、30、45、60min,结果见表6。表610min20min30min45min60min实施例147%69%82%88%89%实施例264%87%94%95%94%实施例352%84%92%92%91%对比例17%18%27%41%52%对比例218%33%55%68%75%对比例324%42%61%70%81%市售商品samsca®67%87%93%94%93%由表6可以看出,本发明制得的托伐普坦纳米晶体可以有效提高药物的体外溶出速率和溶出度,从而提高药物的生物利用度,具有商业化的可行性。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1