酞嗪酮类化合物晶型A及其制备方法与流程
本发明属于医药化学领域,具体涉及具有肿瘤作用的化合物[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐一种新晶型、其制备方法、包含所述晶型的组合物,以及所述晶型或包含所述晶型的组合物在药物制备中的用途。
背景技术:
布鲁顿氨酸激酶(bruton'styrosinekinase,btk)属于tec家族的成员。它由独特的n-端结构域即ph(pleckstrinhomology)结构域、th(techomology)同源区、sh3(srchomology3)结构域、sh2(srchomology2)结构域和催化结构域,也称sh1/tk(srchomologyl/tyrosinekinase)结构域或者激酶结构域组成(akinleyeetal:ibrutinibandnovelbtkinhibitorsinclinicaldevelopment.journalofhematology&oncology2013,6:59)。在b淋巴细胞正常发育过程中,btk基因不同蛋白区域的正确表达在b细胞的功能及多种转导途径中具有关键性作用。
基于btk信号传导通路开发小分子靶向药物为b细胞类肿瘤如白血病、发性骨髓瘤及b细胞类免疫疾病的治疗提供一条全新的途径。btk在自身免疫疾病中的作用的证据已经由btk-缺失型小鼠和btk-充足型小鼠模型试验提供(killp,etal:bruton'styrosinekinasemediatedsignalingenhancesleukemogenesisinamousemodelforchroniclymphocyticleukemia.amjbloodres2013,3(1):71-83.)。在慢性淋巴细胞白血病(cll)小鼠模型中,btk-缺失型小鼠完全废止慢性淋巴细胞白血病,btk过度表达会加速白血病发病,增加死亡率。
目前已有数种btk抑制剂得到了开发,化合物[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐,具有下式结构:
该化合物对激酶btk具有良好的抑制作用,ic50可达1nm级别,体外romas细胞活性评价也显示出良好的抑制活性,可用于治疗和/或预防肿瘤。
本领域知道,药物晶型的不同,会造成各种理化性质的差异,如溶解度、溶出速率、熔点、密度、硬度、光电学性质、蒸汽压力等。这些差异可反映在热力学稳定性上,如稳定型、亚稳定型和不稳定型;也可反映在物理化学稳定性上,如吸湿性、晶型转变、样品降解等。这些差异直接影响药物的处方制剂工艺、储存方法、体内药代动表现,进而影响到药物的安全性和有效性。
因此,研究[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐的多晶型现象并选择出在临床治疗上有意义且稳定可控的晶型具有着十分重要的意义。
技术实现要素:
在对[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐的晶型研究中,本发明的发明人共发现了几十种晶型,实验表明,在得到的众多晶型中,其中a晶型具有良好的物理化学稳定性、溶解度和生物利用度,适合制剂开发。
本发明的一个目的在于提供化合物[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐的一种命名为a晶型的晶型,所述晶型具有良好的物理化学稳定性、溶解度和生物利用度。
本发明的另一个目的是提供所述a晶型的制备方法,该方法操作简便,便于工业化大生产。
本发明的再一个目的是提供含有所述a晶型与至少一种药学上可接受的载体的药用组合物。
本发明的第四个目的在于提供一种所述a晶型在制备预防和/或治疗肿瘤的药物中的应用。
针对上述发明目的,第一方面,本发明提供[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐的a晶型,使用cu-ka辐射,其x-射线粉末衍射在衍射角2θ为4.3±0.2°、19.0±0.2°、19.3±0.2°、20.3±0.2°、20.6±0.2°、24.6±0.2°和24.9±0.2°处显示特征峰。
本领域知道,用x射线衍射测定化合物的结晶时,由于测定的仪器或测定的条件等的影响,对于所测得的峰会存在一定的测量误差,特别是x-射线衍射图的相对强度随试验条件的变化而变化。例如,2θ值的测定误差可为约±0.2°,相对强度的测定误差可为±20%。因此,在确定每种结晶结构时,应该将此误差考虑在内。可以理解为任何与本申请的a晶型具有基本相同或相似的x-射线衍射图的晶型均属于本申请的范围之内。
具体地,本发明提供的[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型,使用cu-ka辐射,其x-射线粉末衍射在衍射角2θ为4.3±0.2°、8.8±0.2°、9.4±0.2°、14.5±0.2°、15.1±0.2°、15.6±0.2°、19.0±0.2°、19.3±0.2°、20.3±0.2°、20.6±0.2°、23.1±0.2°、24.1±0.2°、24.6±0.2°、24.9±0.2°处显示特征峰。
更具体地,本发明提供的[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型,使用cu-ka辐射,其x-射线粉末衍射在衍射角2θ为4.3±0.2°、8.8±0.2°、9.4±0.2°、14.5±0.2°、15.1±0.2°、15.6±0.2°、19.0±0.2°、19.3±0.2°、20.3±0.2°、20.6±0.2°、23.1±0.2°、24.1±0.2°、24.6±0.2°、24.9±0.2°、30.1±0.2°和30.9±0.2°处显示特征峰。
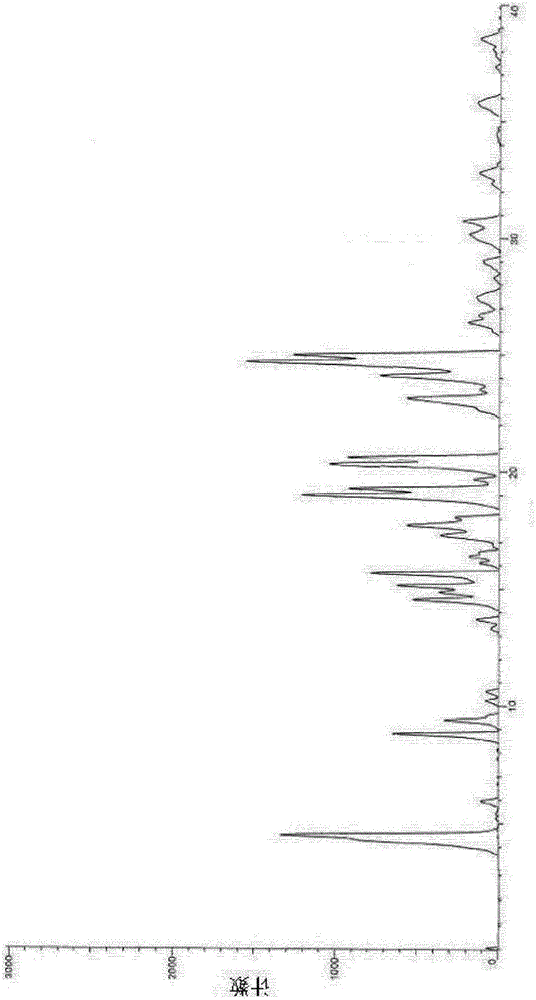
本发明提供的[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型具有如图1所述x-衍射图。
第二方面,本发明提供本发明的[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型的制备方法,所述的方法包括如下步骤:
步骤a:式(1)的化合物与式(2)的化合物缩合得到式(3)的化合物;
步骤b:式(3)的化合物与式(4)的化合物反应得到式(5)的化合物;
步骤c:式(5)的化合物脱去保护基得到式(6)的化合物;
步骤d:式(6)的化合物与丙烯酰氯反应得到式i化合物;
步骤e:式(i)化合物与甲磺酸反应制得式(i)化合物甲磺酸盐,反应路线如下:
步骤f:将步骤e所得式(i)化合物甲磺酸盐加入甲醇-丙酮-水混合溶剂中,回流,0-5℃析晶,即得[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型。
根据所述制备方法,步骤f中所述的甲醇-丙酮-水混合溶剂中甲醇、丙酮和水的体积比为(10~15):2:2;优选地,步骤f中所述的甲醇-丙酮-水混合溶剂中甲醇、丙酮和水的体积比为6:1:1。
根据所述制备方法,步骤f中所述的甲醇-丙酮-水混合溶剂的使用量为每克[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐使用甲醇-丙酮-水混合溶剂5-15ml;优选地,步骤f中所述的甲醇-丙酮-水混合溶剂的使用量为每克[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐使用甲醇-丙酮-水混合溶剂5-10ml。
第三方面,本发明提供药物组合物,其包含本发明的[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型和药学上可接受的载体。将[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型与药学上可接受的载体混合制备成药物制剂,以适合于经口或胃肠外给药。给药方法包括,但不限于皮内、肌内、腹膜内、静脉内、皮下、鼻内和经口途径。所述制剂可以通过任何途径施用,例如通过输注或推注,通过经上皮或皮肤粘膜(例如口腔粘膜或直肠等)吸收的途径施用。给药可以是全身的或局部的。经口施用制剂的实例包括固体或液体剂型,具体而言,包括片剂、丸剂、粒剂、粉剂、胶囊剂、糖浆、乳剂、混悬剂等。所述制剂可通过本领域已知的方法制备,且包含药物制剂领域常规使用的载体。
第四方面,本发明提供[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型或[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型的药物组合物在制备预防和/或治疗肿瘤的药物中的应用,包括向肿瘤易发人群或肿瘤患者施用治疗有效量的本发明的[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型或[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型的药物组合物,以有效降低肿瘤发生率、延长肿瘤患者生命。
本发明的[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型具有良好的稳定性、溶解度和生物利用度,适合用于制成药物制剂。
附图说明
图1是[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型的x-射线衍射图。
具体实施方式
以下结合实施例更详细的解释本发明,本发明的实施例仅用于说明本发明的技术方案,并非限定本发明的范围。
实施例1[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯的制备
步骤1:称取5-氨基-3,4-二氢异喹啉-2(1h)-甲酸叔丁酯(50mmol)和dipea(100mmol)于反应瓶中,加入二氯甲烷300ml,室温搅拌下缓慢滴加氯甲酸对氯苄酯(51mmol),滴毕,室温下继续搅拌1h,停止反应,浓缩反应混合物,加入乙酸乙酯70ml,稀盐酸水溶液(0.2-0.3n)和饱和食盐水洗涤,无水硫酸钠干燥,过滤,浓缩得(3,4-二氢异喹啉-2(1h)-甲酸叔丁酯-5-基)-氨基甲酸对氯苄酯,直接用于下一步,esi–ms:[m+h]+m/z417。
步骤2:称取3-氟-1-二甲氧基甲基苯(500mmol)于反应瓶中,加入四氢呋喃(800ml)溶解,60℃、氮气保护下,加入s-buli(565mmol),将反应液在-60℃下搅拌1h;称取干冰(50mmol)于另一反应瓶中,加入四氢呋喃(200ml),加入n-buli(5ml),氮气保护下搅拌2h后,加入上述混合物,继续搅拌30min,停止反应,加入水1000ml,用浓盐酸调节ph至2,分离有机相,水相用乙酸乙酯萃取,合并有机相,饱和食盐水洗涤,无水硫酸钠干燥,重结晶得到6-氟-2-二甲氧基甲基苯甲酸;称取6-氟-2-二甲氧基甲基苯甲酸(400mmol)、乙酸(93mmol)、肼(600mmol)于反应瓶中,加入异丙醇300ml,氮气保护下,100℃回流反应2h,停止反应,加入乙酸乙酯300ml,水500ml,萃取,合并有机相,无水硫酸钠干燥,悬干,柱层析纯化得8-氟-2h-酞嗪-1-酮,esi–ms:[m+h]+m/z165。
步骤3:称取8-氟-2h-酞嗪-1-酮(150mmol)、(3,4-二氢异喹啉-2(1h)-甲酸叔丁酯-5-基)-氨基甲酸对氯苄酯(195mmol)于反应瓶中,加入dmf100ml,55℃下反应过夜,停止反应,加入水100ml,二氯甲烷200ml,萃取,分离有机相,水相继续用二氯甲烷萃取(3*50ml),合并有机相,无水硫酸钠干燥,柱层析纯化得(3,4-二氢异喹啉-2(1h)-甲酸叔丁酯-5-基)-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯。
步骤4:称取(3,4-二氢异喹啉-2(1h)-甲酸叔丁酯-5-基)-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯(50mmol)于反应瓶中,加入三氟乙酸20ml,室温下搅拌1h,减压浓缩至干,加入乙酸乙酯80ml,依次用1.5m磷酸氢二钠水溶液和饱和食盐水洗涤,无水硫酸钠干燥,过滤,减压浓缩得中间体(1,2,3,4-四氢异喹啉-5-基)氨基甲酸-8-氟-2-(2h)-酞嗪-1-酮基苄酯;称取所得中间体(1,2,3,4-四氢异喹啉-5-基)氨基甲酸-8-氟-2-(2h)-酞嗪-1-酮基苄酯(20mmol)于反应瓶中,加入二氯甲烷100ml溶解,0℃下加入diea(40mmol),搅拌30min后,继续在0℃下滴加丙烯酰氯(20mmol),滴毕,室温搅拌3h,停止反应,加水100ml,二氯甲烷萃取(3*50ml),合并有机相,无水硫酸钠干燥,柱层析纯化得[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯。
1hnmr(600mhz,cdcl3)(δ,ppm):9.50(s,1h),8.10(s,1h),7.88~7.85(m,1h),7.77~7.75(m,1h),7.54~7.52(m,3h),7.34~7.32(m,2h),7.21~7.18(m,3h),6.57~6.55(m,1h),6.41~6.39(m,1h),4.65(s,2h),4.22(s,2h),3.61~3.59(m,2h),3.13~3.11(m,2h),2.05~2.03(m,3h).
esi–ms:[m+h]+m/z513。
实施例2:[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐的制备
称取实施例1化合物(0.5mmol)于反应瓶中,加丙酮5ml室温下搅拌0.5h,滴加甲磺酸丙酮溶液(含甲磺酸0.55mmol)1ml,滴毕,室温下继续搅拌1h,加压蒸除溶剂,室温下真空干燥获得标题化合物。
1hnmr(600mhz,cdcl3)(δ,ppm):9.50(s,1h,重水交换后消失),8.10(s,1h),7.88~7.85(m,1h),7.77~7.75(m,1h),7.54~7.52(m,3h),7.34~7.32(m,2h),7.21~7.18(m,3h),6.57~6.55(m,1h),6.41~6.39(m,1h),5.17(s,2h),4.22(s,2h),3.61~3.59(m,2h),3.13~3.11(m,2h),2.84~2.81(s,3h),2.05~2.03(m,3h).
实施例3:[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型的制备
称取1.0g[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐于反应瓶中,加入12ml体积比为5:1:1的甲醇-丙酮-水混合溶液,回流10min,自然冷却至室温,0-5℃析晶12h,得到[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型。
实施例4:[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型的制备
称取1.0g[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐于反应瓶中,加入10ml体积比为6:1:1的甲醇-丙酮-水混合溶液,回流10min,自然冷却至室温,0-5℃析晶12h,得到[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型。
实施例5:[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型的制备
称取1.0g[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐于反应瓶中,加入7ml体积比为6:1:1的甲醇-丙酮-水混合溶液,回流10min,自然冷却至室温,0-5℃析晶12h,得到[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型。
实施例6:[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型的制备
称取1.0g[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐于反应瓶中,加入5ml体积比为15:2:2的甲醇-丙酮-水混合溶液,回流10min,自然冷却至室温,0-5℃析晶12h,得到[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型。
以上实施例3-6制备的[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型,经测量具有基本相同的x射线衍射图谱,见图1。
实施例7[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型的稳定性测试
称取3份[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型1.0g,分别平铺于培养皿中,1份开口置于光照照度为4500lx±500lx条件下放置10天,1份开口置于室温75%相对湿度(rh)条件下放置10天,1份开口置于室温92.5%相对湿度(rh)条件下放置10天,于第0、5、10天取样,考查最大单杂、总杂质、晶型和外观的变化,实验结果见表1。
表1
上述实验结果均表明,本发明的[2(1h)-丁-2-烯酰基-3,4-二氢异喹啉-5-基]-氨基甲酸-4-[8-氟-(2h)-酞嗪-1-酮基]苄酯甲磺酸盐a晶型具有良好的化学稳定性和物理稳定性。
- 还没有人留言评论。精彩留言会获得点赞!