一种针对KRAS基因突变检测的试剂盒的制作方法
本发明涉及分子生物学技术领域,具体涉及一种针对kras基因突变进行检测的试剂盒。
背景技术:
kras属于ras基因家族主要成员之一,位于egfr信号通路的下游。kras编码p21蛋白,在mapk信号通路中起作用,是一种致癌基因,能够与gdp/gtp结合并促进gtp酶活性。当kras发生突变时不能被水解酶水解失活,并处于持续激活状态,可以引起raf/mapk的上调,传递多种生存通路信号,从而使细胞过度生长、增殖,抑制egfr-tkis的作用。17%到25%人类肿瘤中存在kras基因的突变,其突变可以导致多种恶性肿瘤,包括胰腺(95%),甲状腺(55%),大肠癌(35%),肺癌(35%)等。kras基因被激活最常见的方式是点突变,多发生在n端的第12、13和61、146密码子,其中以第12密码子突变最常见。ras家族基因在癌症中没有可用的药物直接拮抗此靶点,主要影响信号通路上下游靶点药物的使用效果,突变主要导致egfr靶向药,braf靶向药的耐药性等。
全球结直肠癌每年新发病例数约120万,年病死人数超过60万,发病率居第4位。近些年,结直肠癌的发病率呈明显上升趋势。早在2009年,美国临床肿瘤学会(asco)即建议对于转移性结直肠癌患者,在选择抗egfr的单抗药物(西妥昔单抗或帕尼单抗)治疗前应检测kras基因状态。多个大样本、多中心iii期临床研究结果提示,kras基因第2号外显子第12、13位密码子的突变状态与阻断egfr的单克隆抗体——西妥昔单抗、帕尼单抗的疗效明确相关,kras野生型的患者可以从西妥昔单抗和帕尼单抗的治疗中获得最大化的生存效益。
kras基因突变发生在大约30%的肺腺癌中。肺癌kras突变主要定位在第12和13号密码子。同时,肺癌中的kras突变似乎与egfr和alk易位互不相容,众多研究显示,kras基因突变是影响tki药物疗效的不利因素。此外,也有研究表明,kras突变患者通常都有吸烟史。虽然kras的发现比egfr早二十多年,但由于研发难度大,目前针对kras的靶向药物少之又少。2013年《nccn非小细胞肺癌临床实践指南》明确指出:肿瘤患者接受egfr靶向药物治疗之前,必须进行ras基因突变检测,根据检测结果决定是否使用egfrtki靶向药物作为临床治疗措施。新的指南规定,ras基因如果发生了突变,则不建议病人使用egfrtki进行分子靶向治疗。在携带kras突变的肺癌临床研究显示,kras突变与肺癌患者对吉非替尼和厄洛替尼原发耐药相关,携带kras突变的患者在厄洛替尼治疗中显示出较差的疗效。
体细胞突变目前最常用的方法是arms-pcr法,即扩增受阻突变系统荧光pcr法,该方法主要用来检测点突变,尤其是检测突变含量很低的体细胞突变。
荧光pcr的优点是反应灵敏、特异性高:具有模板序列特异的taqman探针在引物特异的基础上进一步提高了pcr的专一性;每扩增一个特异产物只释放一个分子的荧光染料,仪器检测的是特异扩增的结果,非特异产物对检测信号没有影响,有效提高检测的专一性。有多种不同波长的荧光基团对可供选择,使得taqman探针法可以实现在同一管内检测多重pcr,降低成本也提高效率和准确性避免了荧光染料对pcr反应的影响。
rnaseh2是一种广泛存在于真核生物和原核生物中核糖核酸酶,可以通过断裂磷酸二酯键,有效地移除rna/dna杂交链中的rna链,在dna复制起始、转录过程中r-loop的移除、dna的错配修复、冈崎片段中rna引物的降解等过程发挥重要的作用。rnaseh2可以水解各种类型的rna/dna杂交链,甚至包括仅含单个核糖核甘酸的杂交链。
rnaseh2是一种专一识别rna-dna杂合体的酶,并能特异识别单个rna碱基与dna模板互补的位点。本专利利用rnaseh2和pcr技术相结合开发一种新型的针对kras基因突变的检测,目前还没有查到将该方法运用到kras基因突变检测中的相关技术。
技术实现要素:
有鉴于此,本发明运用了双相酶系统rnaseh2和dna聚合酶技术,自主设计相关基因检测的引物和探针序列,进一步提供了一种针对kras基因突变进行检测的试剂盒,可以更灵敏方便地对样本进行检测。
本发明的技术方案是这样实现的:本发明第一方面提供了一组针对kras基因突变检测的引物组合,所述引物组合包括引物序列seqidno.1~seqidno.8。其中,小写字母a、c、t代表核糖核酸碱基,大写字母a、t、g、c代表脱氧核糖核酸碱基,所述引物序列seqidno.1~seqidno.7的3'端连接有间隔臂x,这样使引物能够特异地与模板序列结合,并在rnaseh2剪切后能特异扩增。
本发明第二方面提供了一种针对kras基因突变检测的探针,该探针分别位于相应靶核酸序列区域中的一段寡核苷酸单链序列,能特异地和靶核酸序列碱基配对,所述探针包括针对kras基因突变对应的探针序列seqidno.9,序列seqidno.9的5’端标记有荧光基团,3’端标记有淬灭基团。
在以上技术方案的基础上,优选的,所述seqidno.9探针5’端标记有fam荧光基团,3’端标记有淬灭基团bhq1。
本发明第三方面提供了一种针对kras基因突变检测的酶混合液,包括rnaseh2和taqdna聚合酶,所述rnaseh2酶与taqdna聚合酶酶活性浓度比为1:50~1:400,优选酶活性浓度比为1:300。
本发明第四方面提供了一种针对kras基因突变检测的试剂盒,包括上述引物序列seqidno.1~seqidno.8,上述探针序列seqidno.9,上述酶混合液,pcr缓冲液和4种dntps。
在以上技术方案的基础上,优选的,所述针对kras基因突变检测的试剂盒由以下试剂组成:
(1)pcr反应预混液:成分包括pcr缓冲液、4种dntps、探针seqidno.9和通用人源性内标探针、引物由seqidno.1~seqidno.8及通用内标引物混合而成;
(2)酶混合液:成分包括rnaseh2和taqdna聚合酶,所述rnaseh2与taqdna聚合酶酶活性浓度比为1:50~1:400;
(3)阴性质控品:构建的kras基因突变为阴性的质粒模板;
(4)阳性质控品:构建的kras基因突变为阳性的质粒模板;
更进一步优选的,所述酶混合液中,rnaseh2与taqdna聚合酶酶活性浓度比为1:300。
本发明第五方面提供了一种针对kras基因突变检测的方法,包括以下步骤:
(1)设计相关基因分型的引物和探针序列,所述如引物seqidno.1~seqidno.8所示,所述探针如seqidno.9所示;
(2)用dna提取液提取组织dna模板;
(3)pcr扩增检测:以步骤(2)提取的组织dna为模板,利用本发明提供的试剂盒进行相应的扩增检测,将pcr反应预混液和酶混合液按照36:0.5的体积比配成混合液后,加入到相应的反应孔中,然后加入提取的组织dna模板4μl,同时做一个阴性对照孔和一个阳性对照孔,pcr反应条件为95℃预变性5分钟,然后95℃变性10秒,58℃退火延伸45秒,共40次循环,在退火延伸阶段收集荧光;
(4)结果判定:根据各荧光通道的信号值来判断是否有扩增,有扩增就代表该荧光通道对应的检测位点为阳性,即有突变存在;没有扩增,就说明该通道对应的检测位点突变低于本试剂盒检测限。
本发明的试剂盒相对于现有技术具有以下有益效果:
(1)本发明开发了一种新的针对kras基因突变检测的方法及试剂盒,运用了双相酶系统rnaseh2和dna聚合酶技术,由于采用的是双酶系统扩增法,在普通引物的基础上有所改变,即在引物序列seqidno.1~seqidno.7的3'端连接有间隔臂x,这样使引物能够特异地与模板序列结合,并在rnaseh2剪切后能特异扩增;
(2)充分利用了taqman探针技术的优点,结合rnaseh2的特点,采用双酶系统针对kras基因第12、13位密码子突变设计特异性探针和引物,来检测低含量体细胞突变的目的;
(3)设计了针对kras基因突变检测的引物和探针,采用荧光pcr,封闭式检测,减少了后期污染的可能性;
(4)本发明提供的试剂盒的敏感度高,检测快速,稳定性好,封闭式检测,减少了后期污染的可能性。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
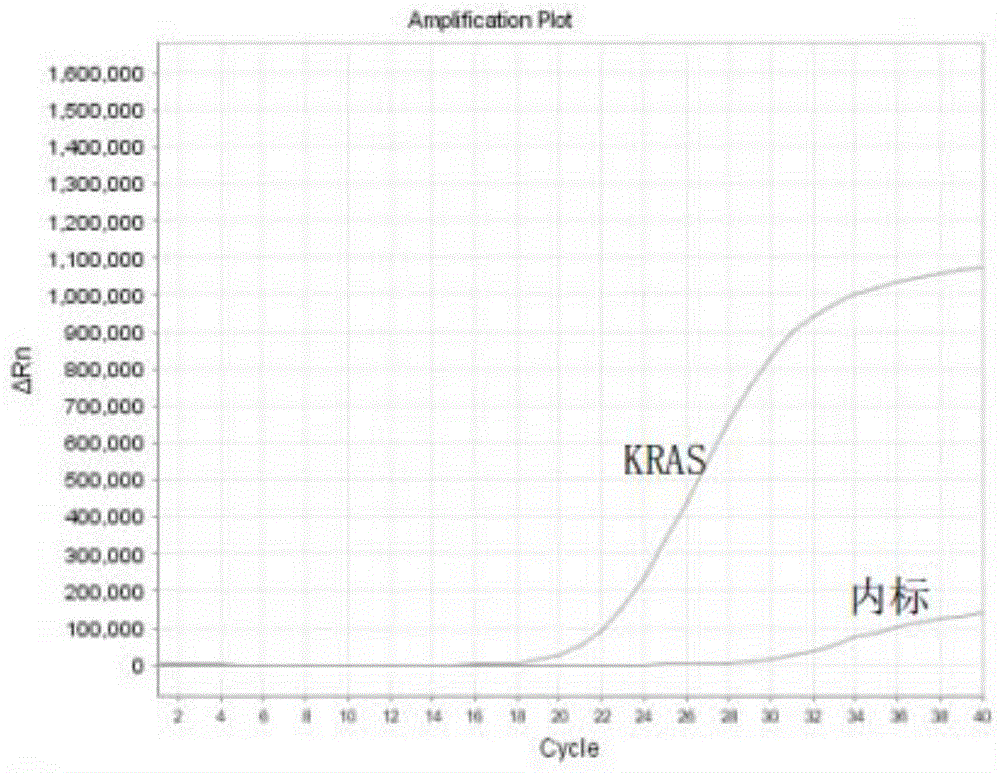
图1为本发明的kras基因突变检测为阳性时的扩增曲线;
图2为本发明的kras基因突变检测为阳性时的扩增曲线。
具体实施方式
下面将结合本发明实施方式,对本发明实施方式中的技术方案进行清楚、完整地描述,显然,所描述的实施方式仅仅是本发明一部分实施方式,而不是全部的实施方式。基于本发明中的实施方式,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施方式,都属于本发明保护的范围。
实施例一
本实施例设计了针对kras基因突变检测的引物和探针序列,设计针对kras基因突变检测的引物序列seqidno.1~seqidno.8,设计针对kras基因突变对应的探针序列seqidno.9,具体序列如下:
5'-gtggtagttggagctgatgg-x,序列如seqidno.1所示;
5'-gtggtagttggagctgctgg-x,序列如seqidno.2所示;
5'-gtggtagttggagctgttgg-x,序列如seqidno.3所示;
5'-gtggtagttggagctagtgg-x,序列如seqidno.4所示;
5'-gtggtagttggagctcgtg-x,序列如seqidno.5所示;
5'-gtggtagttggagcttgtgg-x,序列如seqidno.6所示;
5'-gtagttggagctggtgacgta-x,序列如seqidno.7所示;
5'-atcaaagaatggtcctgcac-3',序列如seqidno.8所示;
fam-tagctgtatcgtcaaggcactc-bhq1,序列如seqidno.9所示。
上述引物与普通引物不同的是,本发明专利由于采用的是双酶系统扩增法,即rnaseh2和taqdna聚合酶双酶系统,因此,在普通引物的基础上有所改变,引物序列seqidno.1~seqidno.7的3'端连接有间隔臂x,这样使引物能够特异地与模板序列结合,并在rnaseh2剪切后能特异扩增;本发明专利经过对序列的分析和引物探针的优化设计,最终筛选出了本发明专利所示的能够对针对kras基因突变位点检测的引物和探针序列。
实施例二
本实施例制备了一种针对kras基因突变检测的试剂盒,为了保证检测系统的可靠性,本发明专利还引入了阳性和阴性质控品。
试剂盒具体设计如下:
(1)pcr反应预混液:成分包括pcr缓冲液、4种dntps、探针seqidno.9和通用人源性内标探针、引物由seqidno.1~seqidno.8及通用内标引物混合而成;
(2)酶混合液:成分包括rnaseh2和taqdna聚合酶,所述rnaseh2与taqdna聚合酶酶活性浓度比为1:50;
(3)阴性质控品:构建的kras基因突变为阴性的质粒模板;
(4)阳性质控品:构建的kras基因突变为阳性的质粒模板;
更加优选的,所述酶混合液中,rnaseh2酶与taqdna聚合酶酶活性浓度比为1:300。
由上述四种试剂按照不同规格包装成不同大小的试剂盒。
实施例三
本实施例制备了一种针对kras基因突变检测的试剂盒,为了保证检测系统的可靠性,本发明专利还引入了阳性和阴性质控品。
试剂盒具体设计如下:
(1)pcr反应预混液:成分包括pcr缓冲液、4种dntps、探针seqidno.9和通用人源性内标探针、引物由seqidno.1~seqidno.8及通用内标引物混合而成;
(2)酶混合液:成分包括rnaseh2和taqdna聚合酶,所述rnaseh2与taqdna聚合酶酶活性浓度比为1:300;
(3)阴性质控品:构建的kras基因突变为阴性的质粒模板;
(4)阳性质控品:构建的kras基因突变为阳性的质粒模板;
由上述四种试剂按照不同规格包装成不同大小的试剂盒。
实施例四
本实施例制备了一种针对kras基因突变检测的试剂盒,为了保证检测系统的可靠性,本发明专利还引入了阳性和阴性质控品。
试剂盒具体设计如下:
(1)pcr反应预混液:成分包括pcr缓冲液、4种dntps、探针seqidno.9和通用人源性内标探针、引物由seqidno.1~seqidno.8及通用内标引物混合而成;
(2)酶混合液:成分包括rnaseh2和taqdna聚合酶,所述rnaseh2与taqdna聚合酶酶活性浓度比为1:400;
(3)阴性质控品:构建的kras基因突变为阴性的质粒模板;
(4)阳性质控品:构建的kras基因突变为阳性的质粒模板;
由上述四种试剂按照不同规格包装成不同大小的试剂盒。
实施例五
本实施例采用实施例三制备得到的针对kras基因突变检测的试剂盒检测样本,具体检测步骤如下:
(1)设计相关基因分型的引物和探针序列,所述如引物seqidno.1~seqidno.8所示,所述探针如seqidno.9所示;
(2)用dna提取液提取组织dna模板;
(3)pcr扩增检测:以步骤(2)提取的组织dna为模板,利用本发明提供的试剂盒进行相应的扩增检测,将pcr反应预混液和酶混合液按照36:0.5的体积比配成混合液后,加入到相应的反应孔中,然后加入提取的组织dna模板4μl,同时做一个阴性对照孔和一个阳性对照孔,pcr反应条件为95℃预变性5分钟,然后95℃变性10秒,58℃退火延伸45秒,共40次循环,在退火延伸阶段收集荧光;
(4)结果判定:根据各荧光通道的信号值来判断是否有扩增,有扩增就代表该荧光通道对应的检测位点为阳性,即有突变存在;没有扩增,就说明该通道对应的检测位点突变低于本试剂盒检测限。
按实施例五方法测定的kras基因突变阳性样本的扩增曲线如附图1所示;测定的kras基因突变阴性样本的扩增曲线如附图2所示。
将针对kras基因突变检测的试剂盒用于某组织样本的检测,采用dna提取液提取组织样本中的dna模板,按实施例五方法步骤进行检测,检测所得扩增曲线如附图1所示,图1显示该样本kras基因突变为阳性,试剂盒检测结果与测序结果一致。
以上所述仅为本发明的较佳实施方式而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
序列表
<110>武汉千麦医学检验所有限公司
<120>一种针对kras基因7种突变检测的试剂盒
<130>2018-11-1
<141>2018-11-13
<160>9
<170>siposequencelisting1.0
<210>1
<211>20
<212>dna
<213>(人工合成)
<400>1
gtggtagttggagctgatgg20
<210>2
<211>20
<212>dna
<213>(人工合成)
<400>2
gtggtagttggagctgctgg20
<210>3
<211>20
<212>dna
<213>(人工合成)
<400>3
gtggtagttggagctgttgg20
<210>4
<211>20
<212>dna
<213>(人工合成)
<400>4
gtggtagttggagctagtgg20
<210>5
<211>19
<212>dna
<213>(人工合成)
<400>5
gtggtagttggagctcgtg19
<210>6
<211>20
<212>dna
<213>(人工合成)
<400>6
gtggtagttggagcttgtgg20
<210>7
<211>21
<212>dna
<213>(人工合成)
<400>7
gtagttggagctggtgacgta21
<210>8
<211>20
<212>dna
<213>(人工合成)
<400>8
atcaaagaatggtcctgcac20
<210>9
<211>22
<212>dna
<213>(人工合成)
<400>9
tagctgtatcgtcaaggcactc22
- 还没有人留言评论。精彩留言会获得点赞!