一种血中循环肿瘤细胞金属多槽俘获装置的制作方法
本实用新型涉及医疗技术领域,特别是一种血中循环肿瘤细胞金属多槽俘获装置。
背景技术:
血中循环肿瘤细胞(Circulating tumor cells, CTC)是指从肿瘤原发灶脱落到脉管并在血流中循环的细胞。CTC是肿瘤转移的基础也是患者使用化疗的依据。因此,CTC是从血中观察肿瘤预后和治疗效果的重要生物标记物。目前,众多的研究表明直肠癌、肺癌、乳腺癌、前列腺癌、肝癌、胰腺癌等肿瘤病人血中CTC数目的多少与肿瘤病人的预后及复发相关。肿瘤病人血中CTC数目越多,病人的预后越差。
由于相对于血中的白细胞CTC数目太少,所以,CTC的俘获和富集显得尤其的重要。目前,主要有基于肿瘤细胞表面特定抗原表达的检测技术如CellSearch和基于肿瘤细胞形态大小的CTC检测技术(Isolation by Size of Epithelial Tumor Cells, ISET)。
美国FDA批准的CellSearch主要是基于CTC表面能表达一些上皮细胞特定的抗原如EpCAM、 Cytokeratin (CK) 8、18、19 。针对这些抗原的抗体包被在微柱上,通过抗原-抗体的相互作用而把CTC从其它的血细胞中分离出来。由于主要依赖CTC表面表达的特定抗原,CellSearch对EpCAM/CK 阴性的CTC和EMT(上皮细胞向间质细胞的转化细胞,不表达EpCAM 和 CK,肿瘤远处转移的元凶)均不能俘获,并且在操作过程中易引起CTC的死亡,从而导致低的CTC俘获率。低的CTC俘获率不能真实的反映肿瘤患者体内肿瘤的负载状态。正是基于它的这些缺点,CellSearch目前仅适用于批准使用的特定临床情况。
ISET利用大多数的肿瘤细胞的体积比血中红、白细胞大的特点,不能通过滤过膜上的孔而留在过滤膜上。与CellSearch相比,ISET能够显著的提高CTC的俘获率。ISET不但能俘获EpCAM和CK阳性的CTC而且对EpCAM和CK阴性的CTC以及EMT均能俘获。但ISET的过滤膜并不是特异性的用于CTC的俘获,并且该膜上的孔径大小不一,分布不均匀,孔径的密度偏低,易被非CTC污染,这些缺点又限制了CTC俘获率的提高。
ISET过滤膜上的滤过孔径是圆型的,为了降低血液过滤过程中,液体剪切应力和压力对CTC膜的损伤,血液预先要使用1%左右的甲醛来处理,用于固定CTC,保持CTC膜的完整。但是,甲醛处理过的CTC就没有活性了,不能进行后续的肿瘤细胞的培养,也不能对肿瘤细胞作进一步的功能学上的分析。对CTC的离体培养可以实时监测抗肿瘤药物的疗效,并能协助新的抗肿瘤药物的研发。槽状孔径则能降低液体剪切应力对CTC形态的破坏,从而避免使用甲醛。俘获后的CTC通过与过滤膜的静电作用而留在膜上,当需要收获这些细胞时,需用酶的消化,而不能保持细胞结构的完整性。有效的方法是在过滤膜上涂有一层疏水的多聚化合物,通过消除细胞与过滤膜之间的静电作用,从而避免使用酶的消化。但疏水化合物涂层会影响孔径的大小,影响CTC的俘获。
技术实现要素:
为了克服现有的CTC检测技术所导致的CTC俘获率较低、检测中没有活的CTC、部分肿瘤患者CTC被漏检、CTC检测可靠性差的缺点,本实用新型的目的在于提供一种血中循环肿瘤细胞金属多槽俘获装置,提高CTC俘获率和CTC检测的可靠性。
为实现上述目的,本实用新型采用了以下技术方案:
一种血中循环肿瘤细胞金属多槽俘获装置,包括血液储存装置和蠕动负压泵,还包括:
金属多槽阵列芯片,该金属多槽阵列芯片包括金属片,以及均布于金属片表面的若干个矩形槽孔;所述矩形槽孔的长度和宽度分别为 20-100μm和4-10μm;
芯片储存盒,该芯片储存盒包括空心的盒体,所述盒体的内部通过所述的金属多槽阵列芯片分隔为上盒体和下盒体;
入口管,该入口管与所述的上盒体连通,且入口管连接血液储存装置;
出口管,该出口管与所述的下盒体连通,且出口管连接蠕动负压泵;
第一导管,该第一导管与所述的上盒体连通,用于输送CTC荧光染色抗体或CTC清洗液;
第二导管,该第二导管与所述的上盒体连通,用于收集俘获的CTC。
优选的,所述芯片储存盒的材质为聚二甲基硅氧烷、丙烯酸树脂或其它有机硅的多聚化合物。
优选的,所述芯片储存盒为正方体或长方体结构。
优选的,所述上盒体和下盒体为分体式结构,上盒体与下盒体之间通过金属多槽阵列芯片固定在一起。
优选的,所述金属片为镍金属材质。
本实用新型具有的有益效果如下:本实用新型在现有ISET技术之上的改进,利用金属片取代过滤膜,避免使用消化酶和疏水化合物涂层;金属片上的矩形槽孔取代传统过滤膜上的圆孔,以降低血流的剪切应力并停用甲醛,可以保证俘获到结构完整的活的CTC,用于肿瘤细胞的培养、离体抗肿瘤药物的疗效评估和肿瘤细胞的功能学研究。本实用新型的整套装置能提高CTC俘获率和CTC检测的可靠性,可广泛应用于肿瘤的早期诊断,肿瘤的个性化治疗和新的肿瘤药物的开发。
附图说明
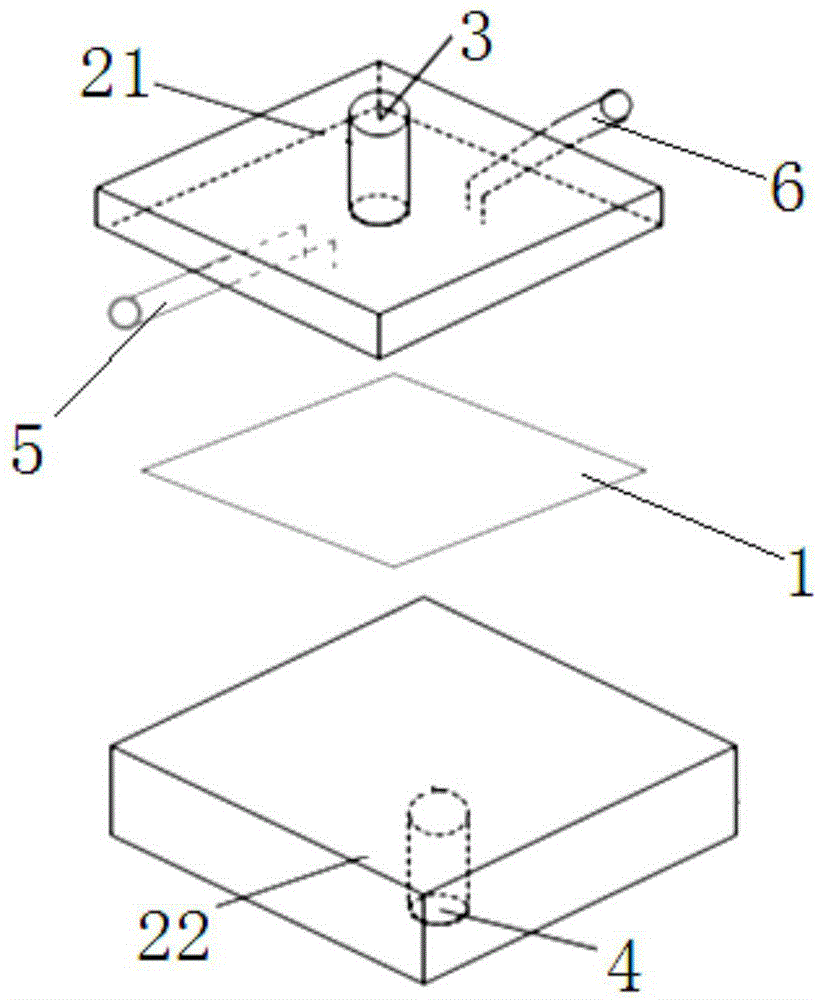
图1是本实用新型的分解结构示意图;
图2是金属多槽阵列芯片的结构示意图;
图中:1-金属多槽阵列芯片、10-金属片、11-矩形槽孔、21-上盒体、22-下盒体、3-入口管、4-出口管、5-第一导管、6-第二导管。
具体实施方式
下面结合附图对本实用新型做进一步说明:
参照图1所示的一种血中循环肿瘤细胞金属多槽俘获装置,包括血液储存装置和蠕动负压泵(血液储存装置和蠕动负压泵可参考现有技术,本实施例中不再详述),还包括:金属多槽阵列芯片1,芯片储存盒,入口管3,出口管4,第一导管5和第二导管6。
参照图2所示,该金属多槽阵列芯片1包括金属片10,以及均布于金属片10表面的若干个矩形槽孔11。
金属片10可以是长方形、正方形或者不规则形态,金属片10可以优选采用镍金属或其它金属材质,金属片10上的矩形槽孔11的长为20~100um,宽为4~10μm。
矩形槽孔11可通过电铸刻而形成;矩形槽孔11的宽度决定了CTC的俘获率,如矩形槽孔11的宽度过宽,则部分CTC通过槽孔而过滤掉;如矩形槽孔11的宽度过窄,则有大量的白细胞与CTC一起留在金属片10上而阻塞矩形槽孔11,影响CTC的俘获率。本实施例的矩形槽孔11的尺寸为经过大量试验得出的最适宜尺寸。
矩形槽孔11的均匀分布可以避免白细胞的对矩形槽孔11的阻塞和污染。高的矩形槽孔11密度有助于提高CTC的俘获率,但过高的矩形槽孔11密度则反而影响CTC的俘获,本实施例中相邻两个矩形槽孔11之间的间隔为40~100μm,可以保证较高的CTC俘获率。
所述芯片储存盒包括空心的盒体,所述盒体的内部通过所述的金属多槽阵列芯片1分隔为上盒体21和下盒体22。
芯片储存盒是血液滤过和CTC俘获的场所,理想的材料是光学透明、无毒、不容易燃烧、电绝缘性和疏水性都好,并具有很高的抗剪切能力。本实施例中,通过聚二甲基硅氧烷(PDMS)、丙烯酸树脂 (Acrylic)或其它的有机硅化合物来建构芯片储存盒。
作为本实施例的优选实施方式,芯片储存盒整体为正方体或长方体结构,上盒体21和下盒体22设计为分体式结构,上盒体21与下盒体22之间通过金属多槽阵列芯片1固定在一起。固定方式可以是通过具有粘性的胶布、固定用的夹子或螺丝,将上盒体21、金属多槽阵列芯片1和下盒体22固定在一起。
所述入口管3与所述的上盒体21连通,且入口管3连接血液储存装置;所述出口管4与所述的下盒体22连通,且出口管4连接蠕动负压泵;所述第一导管5与所述的上盒体21连通,用于输送CTC荧光染色抗体或CTC清洗液;所述第二导管6与所述的上盒体21连通,用于收集俘获的CTC。
入口管3和出口管4在上盒体21和下盒体22上的位置是可以选择的,可以在盒体的正中间,也可以在中间的某一位置或盒体的周边某一位置,只要保证血液能够全部通畅的通过入口管3进入到金属多槽阵列芯片1上,再从金属多槽阵列芯片1下方的出口管4流出。
第一导管5和第二导管6必须在上盒体21上,可以在正中间、中间某一位置或上盒体21的周边某一位置,两个导管要有足够的长度能接近金属多槽阵列芯片1,保证抗体混合液能完全的金属多槽阵列芯片1和满足CTC的收集。
入口管3,出口管4,第一导管5和第二导管6均可以采用软管或硬管,可以是塑料或其它材料。各管的直径取决于血液储存装置的输出口径的大小和血液流动引起的压力改变情况。
本实用新型的操作方法如下:
将血液储存装置中经过抗凝处理的血液,通过入口管3输送入芯片储存盒的上盒体21中, 在出口管4连接的蠕动负压泵的作用下,血液通过金属多槽阵列芯片1,大部分的红细胞和白细胞通过金属片10上的矩形槽孔11,再通过出口管4流出。而CTC则会被截留在金属多槽阵列芯片1上,由于利用金属片10取代过滤膜,避免使用消化酶和疏水化合物涂层;金属片10上的矩形槽孔11取代传统过滤膜上的圆孔,以降低血流的剪切应力并停用甲醛,可以保证俘获到结构完整的活的CTC;同时作为过滤器的芯片储存盒2在蠕动负压泵的作用下保持低的压力梯度,能保持CTC细胞结构的完整性。
当CTC俘获在金属多槽阵列芯片上后,可根据需要除对俘获的肿瘤细胞作形态观察外,如尚要进一步的观察肿瘤细胞表面某些特殊抗原/标记物的表达。则混合的抗体溶液通过第一导管5进入上盒体21而到达金属多槽阵列芯片上的CTC。调节出口管4蠕动负压泵压力的大小而决定混合抗体溶液与细胞作用的时间长短的流出速度。对细胞的清洗也是通过第一导管5输送CTC清洗液来进行的。抗体反应结束后,取出芯片用于图像观察。
当CTC俘获在金属多槽阵列芯片1上后,可根据需要收集CTC用于肿瘤细胞的培养。将细胞培养液可以通过第一导管5输送入上盒体21,从而到达金属多槽阵列芯片1上的CTC。CTC的收集通过第二导管6来进行的,同样可以通过将第二导管6连接蠕动负压泵来进行。培养液的流速和负压的大小可决定CTC收集。
以上所述的实施例仅仅是对本实用新型的优选实施方式进行描述,并非对本实用新型的范围进行限定,在不脱离本实用新型设计精神的前提下,本领域普通技术人员对本实用新型的技术方案作出的各种变形和改进,均应落入本实用新型权利要求书确定的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!